Abstract
Se describen los procedimientos para la cría masiva de Telenomus alsophilae como parásito de huevos del medidor gigante del ciprés Oxydia trychiata, una plaga importante de coníferas en Colombia. Se concluye que la técnica sugerida es sencilla, de fácil manejo, muy barata y de grandes beneficios en el control de esta plaga.
Introduccion
Los parásitos de huevos constituyen uno de los grupos de insectos benéficos más importantes en programas de control biológico e integrado de plagas, debido a que destruyen el huevo del insecto plaga antes de que emerja la larva y ocasione el daño. Por otra parte, son por lo general de ciclo corto y se pueden producir masivamente en el laboratorio.
Durante 1975 se importó el parásito de huevos, Telenomus alsophilae Viereck, para evaluarlo en el control del medidor gigante, Oxydia trychiata (Guenée) (Lepidoptera:Geometridae), plaga de importancia económica en las reforestaciones de coníferas que se adelantan en los departamentos de Antioquia y Caldas.
Pimentel (1963) discutió un método poco común de usar parásitos que normalmente atacan un género específico de insectos para controlar insectos de otros géneros. El caso registrado con T. alsophilae y O. trychiata es un ejemplo de este enfoque ya que la introducción y establecimiento del parásito fue exitosa, lográndose controlar un brote severo del medidor. El parásito, cuyo huésped natural en los Estados Unidos es un defoliador de hoja ancha, provenía de 39° de latitud norte y fue transferido a un defoliador que se alimenta de coníferas a una latitud de 6°N (Bustillo, 1976; Drooz et al 1977; Bustillo y Drooz 1977).
En este informe se presentan los detalles de la técnica empleada en la multiplicación masiva del T. alsophilae, con el fin de que sea de utilidad o sirva de guía para otros programas de multiplicación de parásitos de huevos en Colombia. La metodología descrita es sencilla y no requiere de materiales muy costosos. Se presentan además algunos de los aspectos de su biología sobre este nuevo huésped e información necesaria para el programa de cría y liberación en el campo.
Revision De Literatura
El efecto de los parásitos de huevos sobre defoliadores forestales ha sido revisado recientemente por Anderson (1976). La mayoría de los casos se refieren al efecto de parásitos nativos sobre sus huéspedes.
Uno de los casos más documentados registrado recientemente es el de Ooencyrtus ennomophagus Yoshimoto, que ocasionó el colapso del Ennomos subsignarius (Hübner) en Connecticut (Kaya y Anderson 1974). Una especie no descrita de Telenomus sp., fue importante para el control del mismo insecto en el sur de los montes Apalaches en los Estados Unidos (Ciesla 1964; Drooz et al 1974).
Telenomus alsophilae es un parásito común del Alsophila pometaria Harris (Fedde, et al 1973) y Phigalia titea Cramer (Talerico, 1968), geométridos que afectan árboles de hoja ancha en los Estados Unidos. Este parásito se introdujo a Colombia con el fin de ensayarlo contra el medidor gigante, Oxydia trychiata (Guenée) lográndose su establecimiento y control del brote de ésta plaga (Bustillo 1976; Bustillo y Drooz, 1977; Drozz et al, 1977).
Mucho se ha escrito acerca de crías de insectos parásitos, pero la información pertinente a parásitos de huevos de defoliadores forestales es limitada. Varios autores han registrado crías en gran escala de Trichogramma en varios países; esta información ha sido revisada por Finney y Fisher (1964). Estas especies las crían a menudo sobre huéspedes artificiales o sea no naturales.
Crossman (1917) describió las crías masivas de Ooencyrtus kuwanai (Howard), usando huevos colectados del campo de Lymantria dispar L., como huésped. Anastatus disparis Ruschka ha sido criado también en grandes números aunque no se produjeron generaciones consecutivas en el laboratorio (Burgess y Crossman, 1929). El procedimiento usual fue colectar huevos de L. dispar en el campo, donde el parásito era abundante, separar los huevos parasitados en el laboratorio y luego redistribuir los huevos parasitados en el campo.
Procedimientos de cría se han descrito también para Telenomus phalaenarum Nees sobre huevos de Nygmia phaeorrhoea (Donov). y O. ennomophagus sobre huevos de E. subsignarius (Howard y Fiske, 1911; Anderson y Kaya, 1974).
Materiales Y Metodos
Los parásitos T. alsophilae se recibieron desde los Estados Unidos en masas de huevos parasitadas de A. pometaria. Este material se mantuvo en cuarentena en desecadores, en cuya base se colocó una capa de cloruro de sodio saturada de agua para proveer una humedad constante del 76%, a una temperatura promedia de 22°C (rango 16-30°C). Este material se mantuvo así hasta cuando las larvas provenientes de huevos no parasitados cesaran de emerger.
Los huevos de O. trychiata se obtuvieron colectando polillas en el campo y colocándolas en jaulas de marcos de madera y paredes de anjeo de 40 centímetros de lado. Las polillas ovipositaron sobre tiras de papel encerado que eran sacadas y reemplazadas diariamente para la colección de las masas de huevos.
La cría masiva del T. alsophilae se llevó a cabo en un insectario de campo localizado en la Estación Experimental "Tulio Ospina" del Instituto Colombiano Agropecuario, ICA, en Bello, (Antioquia) a 1450 m de altura y una temperatura media de 22°C (rango 16-30°C). Las observaciones sobre ciclo de vida, desarrollo, comportamiento y las pruebas sobre susceptibilidad del parásito a huevos de diferentes edades se llevaron a cabo tanto en Bello como bajo condiciones de campo. Los estudios de campo se llevaron a cabo en plantaciones comerciales de pino pátula en San Félix, Hacienda La García (2340 m de altura y 16°C de temperatura media, rango 6-26°C) y El Retiro, Hacienda Horizontes (2300 m de altura y 17°C de temperatura media, rango 10-22°C).
Resultados
La cría masiva del parásito de huevos Telenomus alsophilae se llevó a cabo en la siguiente forma. Las polillas traidas del campo se colocaron en jaulas de marcos de madera y paredes de anjeo de 40 cm de lado para que ovipositaran sobre tiras de papel encerado (Fig. 1). Estas se retiraban diariamente y con una tijera se cortaba alrededor de las masas de huevos para luego colocarlas en confinamiento con los T. alsophilae (Fig. 2).
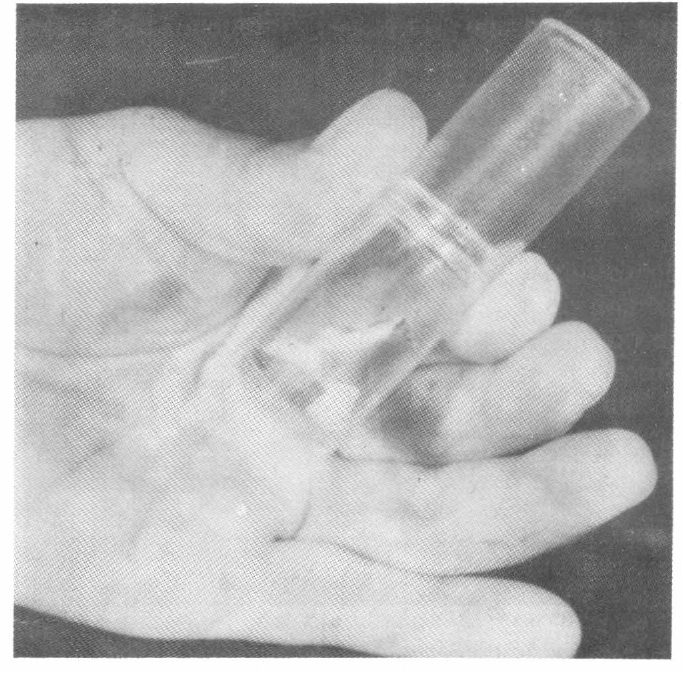
El recipiente utilizado para este fin fue de plástico transparente de 2,0 cm de diámetro por 3,5 cm de alto; a la tapa del recipiente se le hizo un orificio de 1,0 cm de diámetro el cual se cubrió con tela de nylon muy fina, pra evitar el escape de los parásitos y proveer aireación (Fig. 3). Para pasar las avispitas de un recipiente a otro se aprovecha su fototropismo positivo a la luz colocando el recipiente vacío hacia una fuente luminosa (Fig. 4). Después de que los parásitos están en el recipiente se introduce la masa de huevos del O. trychiata para que sea parasitada (Fig. 5). Seguidamente se coloca una motica de algodón de dentistería (Fig. 6) impregnada de una solución de miel de abeja, para alimentar los parásitos, y por último se cierra el recipiente.
La solución de miel de abeja se prepara en una concentración del 40% de miel pura en agua destilada (Fig. 7). Con una jeringa desechable, se succiona la miel y se aplica lentamente a un pedacito de algodón dental, procurando que quede saturado pero que no escurra, ya que esto puede causar la muerte de los parásitos al quedar pegados en la miel (Fig. 8).
El algodón de dentistería se usa debido a que no permite que los parásitos se enreden en el. Al algodón se le puede adicionar más miel al cabo de unos 3 o 4 días si se encuentra muy seco. Para la manipulación de los parásitos es conveniente usar un pincel No. 5. En la Figura 9 aparecen los principales instrumentos usados en este proceso.
Los recipientes de plástico con los parásitos y los huevos se guardaron en desecadoras a una temperatura promedia ambiente de 22°C y humedad constante del 76%. Esta humedad se logró colocando en la base del desecador una capa de cloruro de sodio saturada de agua (Fig. 10).
Una vez que la incubación de los huevos parasitados terminaba y ocurría la emergencia de los parásitos (Fig. 11), éstos se trasladaron a frascos dulceros de vidrio de boca ancha. A estos frascos se hizo necesario introducir tiras delgadas y retorcidas de papel para que las avispistas se posaran sobre ellas. Se observó que en esta forma se mantienen mejor y la mortalidad es muy baja comparada cuando no se colocan las tiras en el recipiente. Estos frascos se taparon con una tela de nylon y se usaron para llevar fácilmente un mayor número de parásitos y liberarlos en el campo (Fig. 12).
El T. alsophilae en su estado adulto tiene una gran longevidad, siempre y cuando se lo alimente con la solución de miel del 40% y se mantenga a 22°C y humedad del 76%. Se ha registrado una duración hasta de 13 meses para las hembras y de 8 meses para los machos. Las altas temperaturas io afectan mucho y causan un alto porcentaje de mortalidad en el laboratorio.
El ciclo de vida varía de acuerdo con la temperatura como se puede apreciar en el Cuadro 1. A la temperatura promedia de 26.1°C en el laboratorio, el ciclo de huevo a adulto demoró 21 días, tomando menos de un día para la eclosión del huevo, 12 días en el estado larvario, un día en prepupa y 7 días en pupa. En cambio a 14,6°C de temperatura promedia en el campo, el ciclo duró 51 días de los cuales, el huevo demoró un día en eclosionar, el estado larvario 19 días, en prepupa 2 días y en pupa 39 días. El estado larvario se reconoce porque se alcanza a observar a través del corion el cuerpo blanco cremoso; el estado pupal se caracteriza porque el insecto toma un color negro. El efecto de la temperatura en el desarrollo del parásito es muy importante porque permite acelerar o retardar la emergencia de éste en un momento dado con el fin de sincronizar las liberaciones en el campo.
La copulación ocurre tan pronto emergen del huevo y sólo dura unos pocos segundos; los machos pueden copular varias veces. El número de días que se debe dejar una masa de huevos expuesta a los parásitos depende del número de huevos de la masa y del número de hembras que se introduzcan en el recipiente. Como regla general, una masa que contenga 200 huevos se puede dejar un día con 30 parásitos en que 20 de los cuales sean hembras, con lo cual se asegura un 100% de parasitismo.
Para parasitar los huevos de O. trychiata el T. alsophilae observa el siguiente comportamiento. Camina sobre los huevos y los palpa con sus antenas. Una vez que selecciona el punto de oviposición el parásito raspa el corion con el ovipositor antes de la inserción. Una vez que completa la oviposición "raya" el huevo con movimientos circulares del ovipositor, aparentemente segregando alguna sustancia química que "marca" el huevo y evita el superparasitimos por otros individuos. El proceso total toma 7 minutos.
Ciclo de vida hasta emergencia del adulto del Telenomus alsophilae en huevos de Oxydia trychiata sometidos a diferentes temperaturas ambientales.
La edad del huevo del huésped es crítica para un parasitismo exitoso (Cuadro 2). A 25°C, huevos de 0-1 día de edad fueron 100% parasitados, mientras que huevos de 2 días de edad sólo un 51% fueron parasitados. A 17°C que son las condiciones de campo donde se liberó el parásito, huevos hasta de 3 días de edad son parasitados en un 82%. En ambos casos el parasitismo declina progresivamente a medida que aumenta la edad del huevo, pero a 25°C todos los huevos de 5 días de edad mueren a pesar que el parásito no complete su desarrollo exitósamente, sin embargo, a 17°C el porcentaje de emergencia de larvas es del 31%. La observación hecha sobre la relación de sexos a ésta temperatura indica una mayor proporción de hembras sobre machos, con excepción de los huevos de 6 y 9 días de edad. Esta situación es favorable si se tiene en cuenta que un macho puede copular varias veces.
El T. alsophilae también se reproduce en huevos infértiles. En una prueba de 91 huevos infértiles de O. trychiata, 64% produjeron parásitos. Los huevos infértiles permanecen atractivos al parásito por 15 días; una masa de huevos de esta edad con 118 huevos produjo 64 parásitos (54%). Esta capacidad es muy útil en los programas de producción masiva.
La multiplicación de este parásito bajo condiciones de campo ha sido muy exitosa hasta el presente y sólo ha estado limitada por el suministro de huevos de O. trychiata. En 1975, en dos meses se multiplicaron alrededor de 57.000 avispitas; en 1977, en el lapso de tres meses cuando se logró obtener un buen suministro de polillas del campo el número de T. alsophilae obtenidos se elevó hasta casi 400.000 individuos, los cuales se han venido liberando en plantaciones forestales en las cuales se ha observado alguna población de O. trychiata. La multiplicación del T. alsophilae bajo este procedimiento ha resultado barata, se estima que producir 1500 parásitos no cuesta más de $2.00 a los precios actuales.

Jaula usada para la obtención de los huevos de O. trychiata, observe las tiras de papel sobre las que ovipositan las polillas.
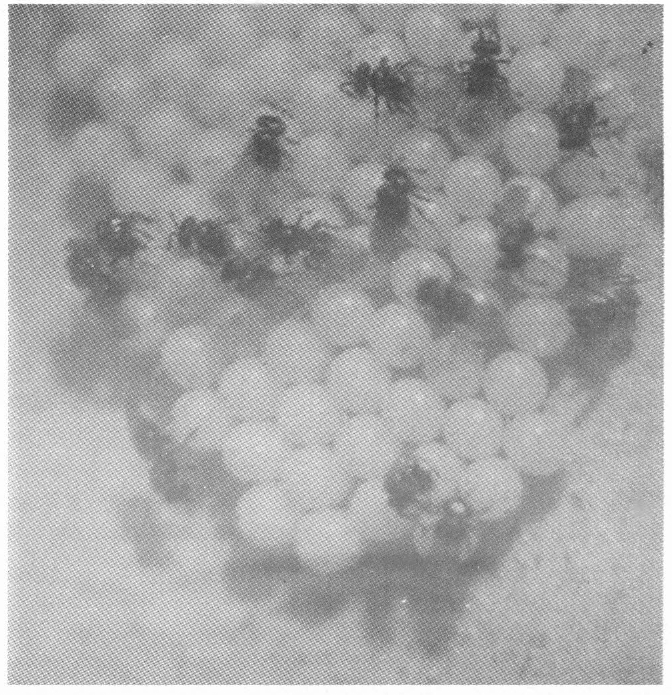
Microfotografía de las avispitas parasitando los huevos de O. trychiata.
Edad de los huevos de Oxydia trychiata en relación con el parasitismo del Telenomus alsophilae. Huevos incubados a 25°C y 17°C de temperatura media ambiental.
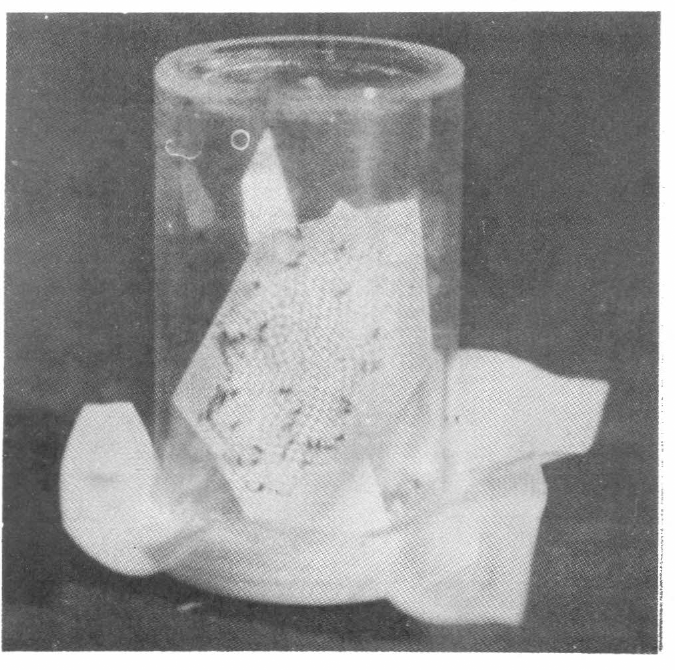
Apariencia del recipiente de plástico tapado; la tela y un orificio en la tapa permiten la aireación de las avispitas.
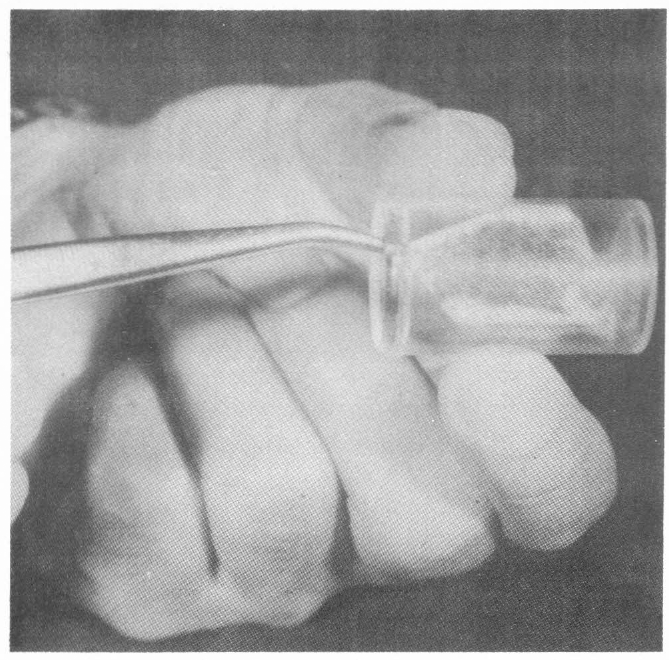
Los parásitos se traspasan de un recipiente a otro vacío aprovechando su respuesta al fototropismo positivo.
Luego se introduce una masa de huevos para que sea parasitada.
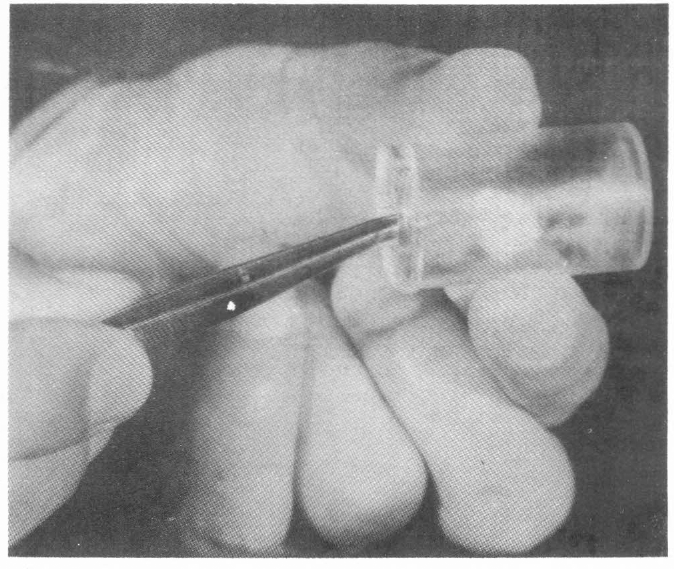
Con ayuda de una pinza se coloca también el algodón impregnado de miel de abeja para la alimentación del T. alsophilae.
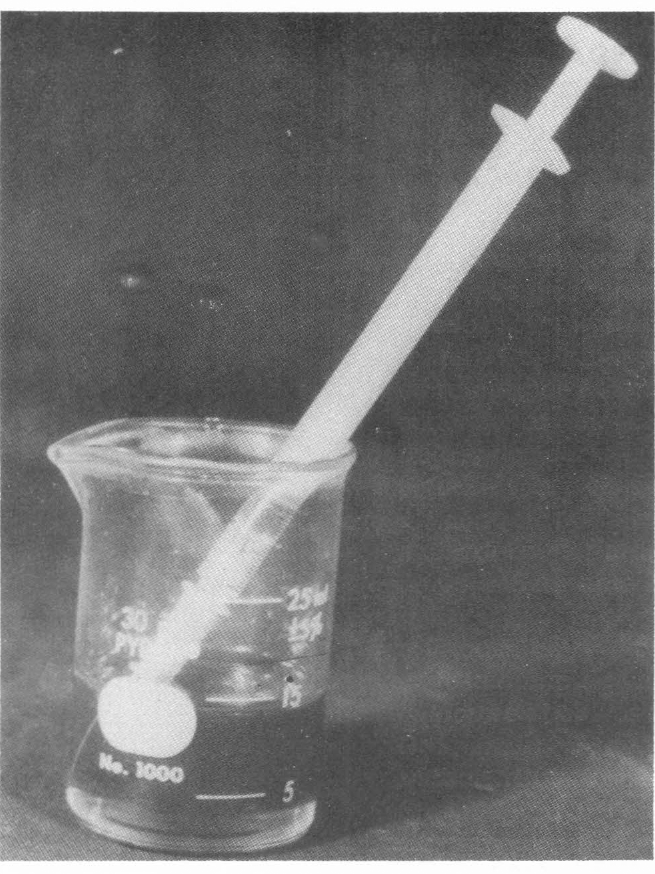
Jeringa y solución de miel de abeja usada para la alimentación de los parásitos.
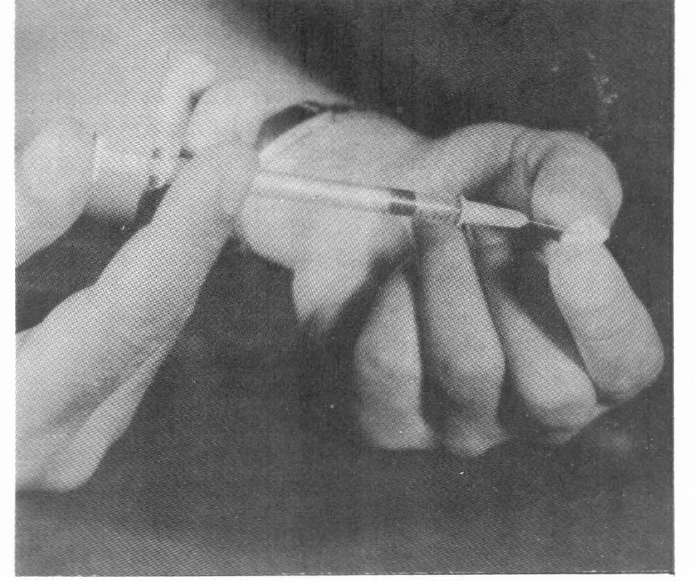
La jeringa se usa para inyectar la miel en los algodoncitos de dentistería.

Instrumentos usados para la cría del Telenomus alsophilae: tijera, pincel, pinza suave, jeringa, alfiler y algodón de dentistería.

Desecador usado para incubar los huevos parasitados hasta la emergencia de las avispitas.

Apariencia de los huevos parasitados por T. alsophilae próximos a emerger.
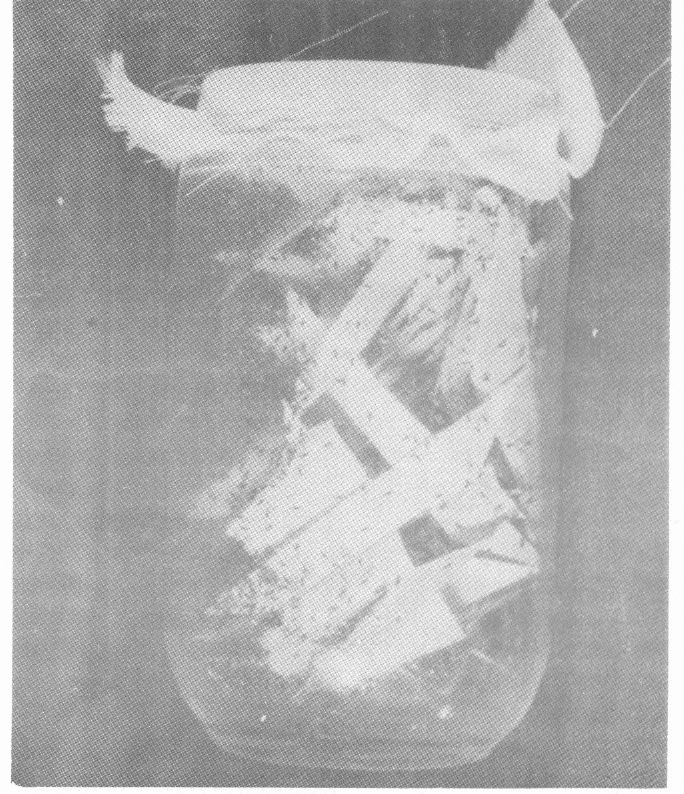
Frasco usado para almacenar los adultos que están listos para la liberación en el campo.
Conclusiones
Los procedimientos de cría masiva del parásito de huevos Telenomus alsophilae aquí expuestos pueden ser usados en escala comercial por una asociación de reforestadores o alguna otra entidad particular o estatal para la supresión del O. trychiata en plantaciones de coníferas en Antioquia. La técnica es sencilla, de fácil manejo, muy barata y de grandes beneficios en el control de la plaga.
Se debe ensayar el T. alsophilae contra otros lepidópteros plagas especialmente geométridos como son las especies Oxydia vesulia Cramer, O. hispata Cramer, O. brundata Guenée y O. noctuitaria Walker que afectan los cultivos de cafeto en Colombia.
Esta metodología de cría puede servir de guía para la cría masiva de otros parásitos de huevos que afectan otras plagas en nuestro medio.
Los resultados con este parásito insinúan que se debe dar un mayor apoyo a este tipo de investigaciones empezando con un reconocimiento detallado de nuestra fauna para luego estudiar las possi bilidades de cría masiva de aquellos parásitos de mayor importancia.
En estos estudios no se debe descartar la posibilidad de usar parásitos introducidos de otras partes del mundo.
Footnotes
Agradecimientos
El autor expresa sus más sinceros agradecimientos al Dr. Arnold T. Drooz quien suministró la colonia del parásito en estudio. A los señores Juan A. Olaya y Roberto Gómez por la valiosa ayuda en las labores de cría del parásito.
