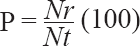Abstract
Epilachna difficilis was reported for the first time on Bonplandia geminiflora (Polemoniaceae). To study the biological and ecological aspects of this species, samples were taken weekly in 2011 in "La Gloria" Canyon, Sahuayo, Michoacán, México, and complementary studies were conducted in the laboratory. The first occurrence of E. difficilis was observed in mid-August and the last in early December. Defoliation to B. geminiflora ranged from 38.0-98.5%. Six species of predators, viz., Podisus congrex, Podisus brevispinus, Oplomus dichrous, Oplomus pulcher (Hemiptera: Pentatomidae: Asopinae), Pselliopus nigropictus, and Rocconota sp. (Hemiptera: Reduviidae), were recorded. Temperature and precipitation were positively correlated (r = 0.8 and 0.6, respectively) with higher population peaks. However, E. difficilis showed a wide range of adaptability in different regions and climates where its host plants grow. Under laboratory conditions, five instars were recorded during 25.95 days of larval development; the entire lifecycle was completed in 37.8 ± 1.7 days. Of the five crops species evaluated, only cucumber suffered damage (30.0%) by adult insects, although all insects died thereafter. This is the first bio-ecological study of E. difficilis. Results may be useful in the biological control of related pests such as E. varivestis.
Introducción
La familia Coccinellidae es uno de los grupos más importantes de insectos que se alimentan de pulgones, cochinillas, psílidos, moscas blancas y arañas rojas (Hoffmann y Frodsham 1993; Giorgi et al. 2009). Por esa razón, se han utilizado en importantes programas de control biológico en todo el mundo (DeBach 1964; Arredondo y Rodríguez del Bosque 2008). La familia también incluye especies fitófagas, en particular dentro de la subfamilia Epilachninae, cuyos adultos y larvas consumen diversas especies de plantas, en las que raspan los tejidos blandos y succionan la savia, dejando solo las nervaduras de la lámina foliar; las plantas dañadas dan una apariencia de "encaje" (Gordon 1975; Giorgi et al. 2009). Unas pocas especies de epilacninos son plagas agrícolas importantes (Li y Cook 1961; Richards 1983; King y Saunders 1984; Li 1993; Beyene et al. 2007); por ejemplo, el escarabajo mexicano del frijol, Epilachna varivestis Mulsant, 1850 (Coleoptera: Coccinelidae) que se alimenta de frijol y soya (King y Saunders 1984; Sánchez-Arroyo 1997).
Basados en el conocimiento de que diversas especies de epilacninos se alimentan en plantas silvestres y algunos son muy específicos (Hirano 1985; Sawada y Ohgushi 1994; Koizumi et al. 1999; Fujiyama et al. 2008), esas especies pudieran ser consideradas no dañinas a la agricultura.
Estudios de insectos fitófagos no plaga de cultivos pueden tener una importancia en manejo integrado de plagas, dado que ellos actúan como reguladores de plantas que, eventualmente, pudieran convertirse en malezas (Hoffmann y Frodsham 1993; Van Driessche et al. 2007). También, insectos fitófagos con daño económico insignificante o nulo pueden ser útiles como hospederos alternos de enemigos naturales de plagas, estrategia ampliamente recomendada en control biológico de insectos (Ehler 1998; Landis 2000; Kapadia 2001; Wyckhuys et al. 2013; Cortez-Madrigal et al. 2014). Además, algunas especies de epilacninos producen metabolitos secundarios que son potencialmente útiles en manejo de plagas (Camarano et al. 2012).
En 2008 se registraron poblaciones de Epilachna difficilis Mulsant, 1850 (Coleoptera: Coccinellidae: Epilachninae; Fig. 1) alimentándose en la planta Bonplandia geminiflora Cav. (Polemoniaceae) en la Barranca "La Gloria", Sahuayo, Michoacán, México. Inicialmente se asumió que se trataba de E. varivestis, pero observaciones detalladas indicaron que la especie correspondía a E. difficilis. Esta especie pudiera ser un importante hospedero alterno de enemigos naturales de epilacninos plaga. Aunque algunos epilacninos tienen hospederos específicos (King y Saunders 1984; Hirano 1985; Sawada y Ohgushi 1994), antes de evaluar cualquier insecto fitófago como hospedero alterno de enemigos naturales, deben dirigirse estudios para entender aspectos biológicos y ecológicos. El objetivo de este estudio fue conocer la biología, preferencias alimenticias, dinámica poblacional y factores de regulación de E. difficilis en la barranca "La Gloria", Sahuayo, Michoacán.

Morfología de Epilachna difficilis colectada en Bonplandia geminiflora de la barranca"La Gloria", Sahuayo, Michoacán, México. A. Adulto. B. Huevos. C. Larva. D. Pupa. E-F. Genitalia del macho: E. Falobase. F. Sifo.
Materiales y métodos
Identificación de la especie.
Los adultos del coleóptero se observaron y recolectaron primero en agosto del 2008, se conservaron en alcohol al 75 % y enviaron al Laboratorio de Entomología del Campo Agrícola Experimental del INIFAP en Celaya, Guanajuato, México, donde fueron identificados con base en observaciones morfológicas de la genitalia del macho (Fig. 1D) y claves dicotómicas (Gordon 1975).
Muestreos.
Para estudiar aspectos ecológicos y de distribución temporal y regional de E. difficilis, de julio-diciembre del 2011, semanalmente se muestrearon 200 plantas de B. geminiflora en la barranca "La Gloria" de Sahuayo, Michoacán, México. Se registraron: las masas de huevos, larvas, adultos y enemigos naturales. Además, se evaluó la incidencia y niveles de defoliación (hojas dañadas) del insecto en B. geminiflora. "Incidencia" fue definida como el número de plantas con presencia de epilacninos en sus cuatro estados de desarrollo, expresado en porcentaje del total de plantas; "el nivel de defoliación" por otro lado, se definió como el número de hojas dañadas por planta y expresada como porcentaje del total de hojas.
El estudio se complementó con exploraciones regionales en el Occidente de Michoacán, que incluyó las localidades de "Los Chorros" del Varal, municipio de Los Reyes; Jalapa, municipio de Zináparo; Tacámbaro; y "cerro" de Emiliano Zapata, municipio de Villamar. La primera con altitudes de 900-1.000 msnm, clima semicálido subhúmedo, con lluvias en verano, con una temperatura media de 22,2 °C; Jalapa, a una altitud de 1.840-1.880 msnm, clima templado con lluvias en verano y temperatura entre 14-30 °C. Tacámbaro se ubica a 1.640 msnm, con clima tropical y templado, con lluvias en verano y temperatura que oscila entre 8,8 a 26,9 °C; y Finalmente, el cerro de Emiliano Zapata ubicado a 1.540 msnm, con clima templado, lluvias en verano y temperatura entre 10,4 a 25,4 °C (INAFED 2009).
Para observar posible emergencia de parasitoides y depredadores, muestras de huevos, larvas y adultos se llevaron al laboratorio. Allí, los depredadores potenciales registrados en campo (con base al grupo taxonómico y depredación en E. difficilis) se confrontaron con huevos, larvas, pupas y adultos del coccinélido; los que resultaron positivos, se preservaron en alcohol al 75% para su identificación a orden y familia. Los depredadores efectivos fueron identificados por el Dr. Harry Urad Brailovsky Alperowitz, especialista en Hemiptera, Departamento de Zoología, Instituto de Biología, UNAM, México, D. F.
De la estación climatológica más cercana (CONAGUA, Sahuayo, Mich.) se obtuvieron datos de temperatura y precipitación. Se exploró gráficamente la dinámica poblacional del insecto. Para investigar la posible relación entre los principales picos poblacionales vs temperatura, precipitación y depredadores, se evaluaron correlaciones lineales (Programa Microsoft Excel, 2010) entre los principales picos poblacionales de E. difficilis y los depredadores; y para la precipitación y temperatura, mediante datos de fechas previas al pico poblacional (tres para precipitación y una para temperatura).
Biología.
En el momento de la cópula, se transfirió una pareja de adultos a cajas Petri (15,0 x 2,5 cm) con hojas de B. geminiflora como alimento y renovadas cada 48 h. Las masas de huevos se colocaron inmediatamente en cajas Petri de plástico (10,0 x 1,5 cm), etiquetadas y rotuladas con el número de huevos y fecha de oviposición. Una vez que emergieron las larvas, éstas se separaron individualmente en cajas Petri (10,0 x 1,5 cm) con hojas de B. geminiflora como alimento. Las larvas se criaron en condiciones de laboratorio (16,9-25,8 °C, 12:12 h luz: obscuridad) y diariamente se revisaron en busca de cambio de instar (con base a mudas); esto, hasta la emergencia de los adultos. El tiempo de desarrollo (días) de cada instar y estado biológico se estimó con base a tres repeticiones en el tiempo, con 10 individuos por repetición. Para identificar posible dimorfismo sexual y determinar la proporción sexual, se removió y examinó la genitalia (n = 30); también, mediante una micro-reglilla® con 0,1 mm de precisión (BioQuip, EEUU) se tomaron medidas de longitud de huevos, larvas, pupas y adultos (n = 15).
Especificidad de adultos.
Se utilizaron: frijol, Phaseolus vulgaris L.; alfalfa, Medicago sativa L.; garbanzo, Cicer arietinum L. (Fabaceae); calabaza, Cucurbita sp.; y pepino, Cucumis sativus L. (Cucurbitaceae), cultivos de gran importancia en la región de estudio. De acuerdo con el método propuesto por Richardson y Whittaker (1982), Kokko et al. (1995) y Zvereva et al. (1995), de hojas frescas recién cortadas, se obtuvieron discos de 2 cm de diámetro. Las pruebas se establecieron en cajas Petri (15,0 x 2,5 cm) con un disco de hoja y cinco adultos. Previo a los bioensayos, los insectos se alimentaron durante una semana con plantas de B. geminiflora; y después, sujetos a 12 h de ayuno. Se incluyeron tres repeticiones y B. gemeniflora se incluyó como control. Una prueba apareada consistió en colocar dos discos de hoja en cajas Petri; uno del cultivo seleccionado y el otro de B. geminiflora. La preferencia de las especies se estimó con base a la siguiente ecuación:
donde: P, es la preferencia de los insectos registrada en porcentaje; Nr, es el número de insectos registrados diariamente por disco de hoja; Nt, es el número total de insectos liberados en la prueba. Se incluyó un testigo sin insectos. Los discos de hoja fueron pesados antes y después de la exposición a los coccinélidos mediante una balanza analítica (Mettler®, EEUU). La pérdida de biomasa se determinó por la diferencia en el peso final del disco. La prueba concluyó cuando todos los insectos murieron en los tratamientos.
Resultados
Morfología y biología de E. difficilis.
Los huevos (Fig. 1B) son de color amarillo, oval-alargado y 1,73 ± 0,13 mm de largo, colocados en grupos de 17-45 huevos en el envés de las hojas. El período de incubación fue de 5,0 ± 0,1 días. Las larvas (Fig. 1C) son de color amarillo claro a marrón. El dorso está cubierto con seis filas longitudinales de espinas ramificadas. Las larvas pasan por cinco estadios. Los tiempos de desarrollo promedio y las mediciones de longitud de cada estadio se presentan en la Tabla 1. La larva completó su desarrollo en 21 días. En algunos casos, se observó canibalismo de larvas.
Tiempo medio de desarrollo (días) y medidas (mm) por etapa de desarrollo de la especie Epilachna difficilis bajo condiciones de laboratorio (16,9-25,8 °C, 12:12 h luz: obscuridad).
Media desviación estándar.
Media + desviación estándar basada en tres repeticiones. H =Huevo, L = Larva, PP = Prepupa, P = Pupa.
La pre-pupa es similar a la larva pero sésil. La longitud media es de 5,45 ± 0,28 mm y transcurre en 4,9 ± 0,77 días. Las pupas (Fig. 1D) son amarillas, ovoides, con unos pocos pelos en la región anterior, y 4,45 ± 0,3 mm de largo. Esta etapa dura 6,9 ± 0,9 días. El ciclo de vida de huevo a adulto fue de 37,8 ± 1,7 días. Con base a esta información y a la dinámica poblacional de campo, se estima que E. difficilis podría tener alrededor de tres generaciones anuales en el área de estudio.
Los adultos son ovalados, redondos, convexos, de color amarillo-oro o bronce, con nueve puntos negros dispuestos en tres filas de bandas transversales y manchas en cada élitro (Fig. 1A). Cuando son jóvenes presentan una pubescencia grisácea en el pronoto y élitros. La longitud media de machos y hembras es 4,49 ± 0,23 y 5,02 ± 0,24 mm, respectivamente. La proporción de sexos en condiciones de laboratorio fue de 1:1.
Incidencia de E. difficilis en B. geminiflora.
La incidencia de E. difficilis (plantas con huevos, larvas, adultos o daños) en las poblaciones de B. geminiflora fue bien sincronizado con los niveles de abundancia de su hospedero. La incidencia osciló entre el 15,0% el 18 de agosto, al 100,0 % el 11 de noviembre. Después del pico más alto, se observó una reducción gradual en la incidencia del insecto antes de desaparecer en diciembre (Fig. 2), a pesar de que se observaron plantas de B. geminiflora en la región.
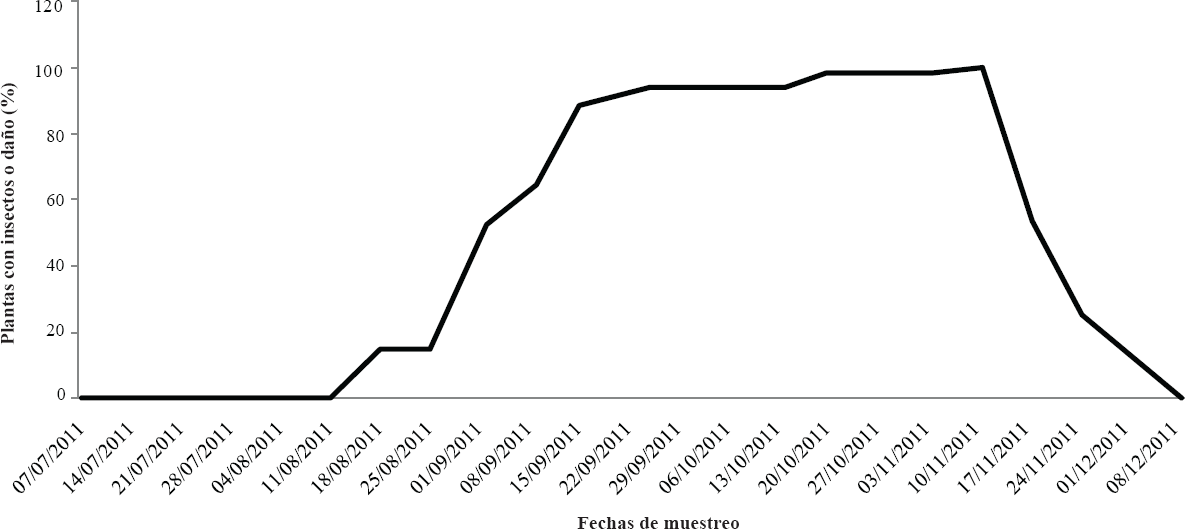
Incidencia de E. difficilis en poblaciones de B. geminiflora. Barranca "La Gloria," Sahuayo, Michoacán.
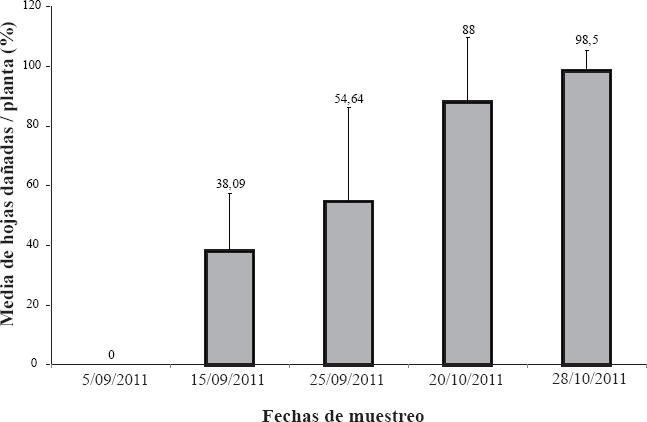
Porcentaje de hojas dañadas (severidad) por larvas y adultos de E. difficilis en plantas de B. geminiflora. Barranca "La Gloria", Sahuayo, Michoacán, México.
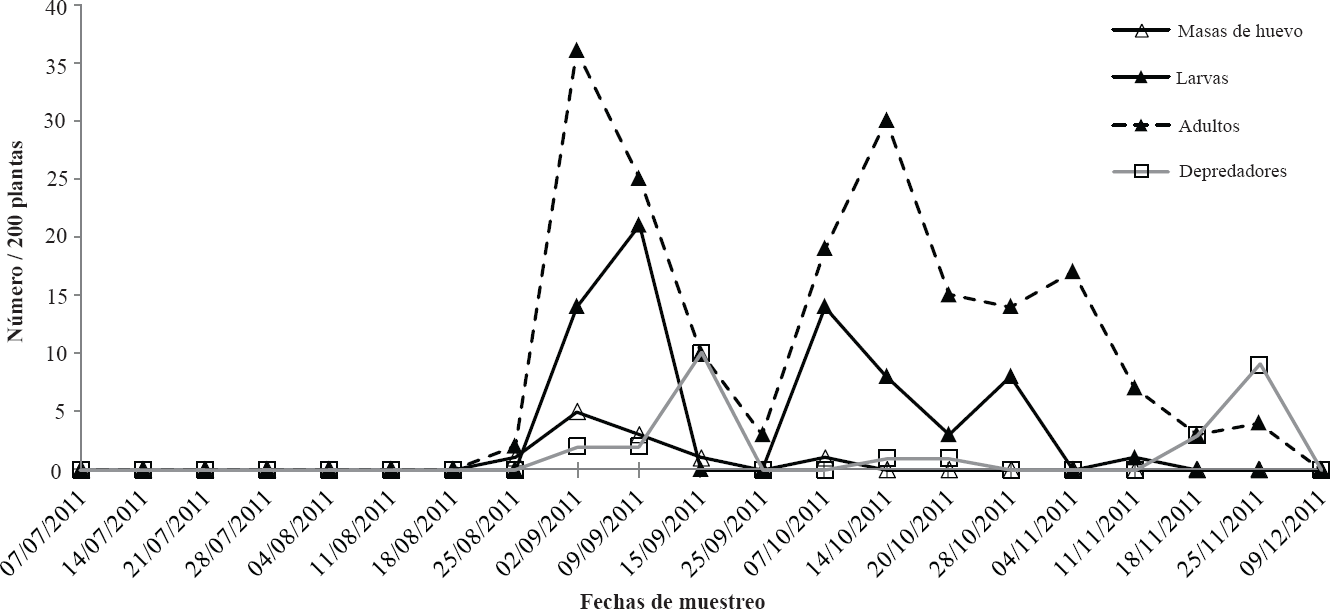
Dinámica poblacional de Epilachna difficilis sobre Bonplandia geminiflora en la barranca "La Gloria", Sahuayo, Michoacán, México.
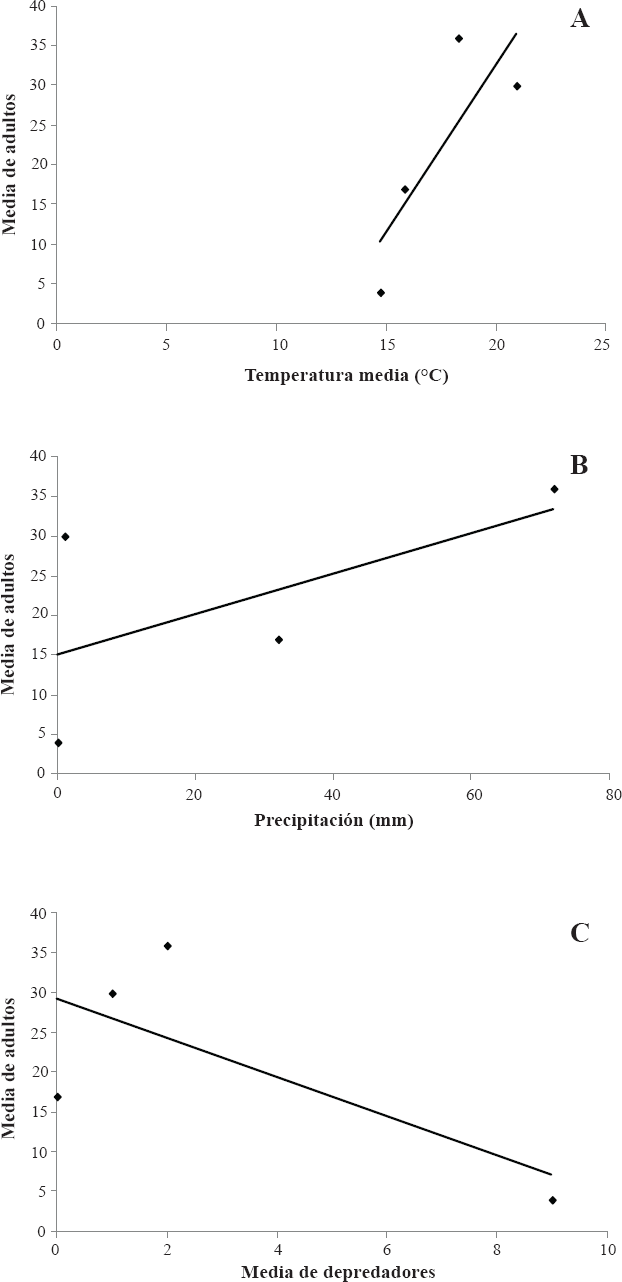
Índices de correlación entre los principales picos poblacionales de E. difficilis con los factores bióticos y abióticos de regulación bajo las condiciones de la barranca "La Gloria", Sahuayo, Michoacán, México. A. Temperatura. B. Precipitación. C. Depredadores.
Las larvas y adultos de E. difficilis se alimentaron en el envés de las hojas de B. geminiflora, dejando sólo las nervaduras y parte de la epidermis. Finalmente, los tejidos restantes adquieren un color marrón. A veces, los adultos se alimentaron en los tallos tiernos. Con base en los niveles de defoliación (hojas dañadas), el daño de E. difficilis en B. geminiflora varió desde 38,0 % hasta 98,5%, con el pico más alto, el 28 de octubre (Fig. 3).
Enemigos naturales de E. difficilis.
Aunque se observaron varios grupos de depredadores cercanos a individuos de E. difficilis o en la misma planta donde estaba presente, sólo siete especies de hemipteros se confirmaron como depredadores del insecto en condiciones de campo y laboratorio.
Podisus congrex (Stal, 1862) (Hemiptera: Pentatomidae) se colectó el 13 de septiembre en la comunidad de Jalapa, Michoacán. Se registró como ninfa alimentándose de una masa de huevos de E. difficilis en B. geminiflora. En condiciones de laboratorio, sólo se alimentó de huevos y larvas, dejando a los adultos.
Podisus brevispinus Phillips, 1982 (Hemiptera: Pentatomidae) se registró frecuentemente en la barranca La Gloria, alimentándose de pupas de E. difficilis. En el laboratorio, el depredador completó su ciclo de vida con el consumo de larvas y pupas del coccinélido. Podisus sp. (Hemiptera: Pentatomidae) se registró en la etapa de ninfa en el campo depredando una larva de lepidóptero en B. geminiflora. Las ninfas son de color amarillo con manchas negras en el mesonoto y el abdomen. Los adultos son de color marrón oscuro, con manchas de color marrón claro distribuidos al azar y una espina bífida en cada lado del pronoto, en laboratorio se alimentaron sólo de pupas.
Oplomus dichrous Herrich-Schaeffer, 1839 (Hemiptera: Pentatomidae) se registró como ninfa depredando en larvas de E. difficilis en B. geminiflora. En condiciones de laboratorio, larvas y pupas de E. difficilis fueron aceptados como presa, pero no el adulto.
Oplomus pulcher Dallas, 1851 (Hemiptera: Pentatomidae) se registró en estado adulto depredando larvas de lepidópteros en un hospedero diferente a B. gemeniflora, pero cercano a la planta. En laboratorio, la especie se alimentó de pupas de E. difficilis.
Huevos de Pselliopus nigropictus Champion, 1899 (Hemiptera: Reduviidae) fueron colectados de follaje de B. geminiflora en campo. En laboratorio, las ninfas recién nacidas se alimentaron del primer instar de larvas de E. difficilis. Esta especie es un depredador voraz, y cuando E. difficilis no fue disponible, se alimentó de otras ninfas de su misma especie. En varias ocasiones se observaron adultos de esta especie depredando adultos de E. difficilis en el campo. Lo anterior sugiere que esta especie fue un frecuente depredador del coccinélido.
Adultos de la especie Rocconota sp. fueron colectados en B. geminiflora. En condiciones de laboratorio se alimentó de larvas y pupas de E. difficilis. De acuerdo con observaciones en laboratorio, tanto P. nigropictus y Rocconota sp. sobrevivieron hasta cuatro meses sin comer.
Otras especies de depredadores generalistas se registraron en plantas de Bonplandia incluyendo: larvas de Chrysopidae (Neuroptera) y adultos de Cleridae y Carabidae (Coleoptera) y otros cuatro morfoespecies de la familia Pentatomidae. Sin embargo, las pruebas de depredación, en todos los casos, fueron negativas y los insectos murieron antes de alimentarse de E. difficilis.
Dinámica poblacional.
Los primeros adultos de E. difficilis se registraron a finales de agosto y desde entonces, el crecimiento de la población mantuvo altos niveles; cuatro picos se registraron durante el año: septiembre, octubre y dos en noviembre de alta a baja magnitud, respectivamente (Fig. 4). El análisis gráfico muestra una estrecha relación entre las masas de huevos, larvas y adultos. A medida que la temperatura y la precipitación disminuyeron, los niveles poblacionales de E. difficilis también disminuyeron, desapareciendo en diciembre, aunque en las zonas bajas del cañón existían poblaciones de su planta hospedera. Un análisis de correlación mostró una estrecha relación de las poblaciones de E. difficilis vs. temperatura y precipitación. Por ejemplo, una correlación positiva (r = 0,8 P < 0,05) se registró entre la población del pico principal de E. difficilis y la temperatura media de una fecha anterior al pico de población (Fig. 5A). Del mismo modo, la precipitación del tercer día anterior al pico de población mostró una correlación positiva (r = 0,6; P < 0,05) entre las dos variables (Fig. 5B).
No obstante los bajos niveles poblacionales de depredadores, se obtuvo una correlación negativa (r = - 0,70, P < 0,05) entre los picos poblacionales de E. difficilis y sus depredadores (Fig. 5C), lo que junto con su distribución temporal (Fig. 4) sugiere que los depredadores registrados fueron un factor importante en la regulación de E. difficilis.
Distribución regional.
Bonplandia geminiflora y su herbívoro E. difficilis se registraron en las cuatro regiones exploradas del Occidente de Michoacán. Las regiones contrastan en características climáticas; por ejemplo, Los "Chorros del Varal" en el municipio de Los Reyes, Michoacán, se encuentra a una altitud de 900 msnm; por el contrario, Jalapa, Tacámbaro y el "cerro" de Emiliano Zapata tienen altitudes superiores (> 1.500 msnm). Del mismo modo, de acuerdo con observaciones previas, se han registrado ejemplares de E. difficilis en B. geminiflora en Tlalnepantla, Morelos, con altitudes de 2.060 msnm, con clima templado-húmedo y temperatura media anual de 17 °C (INAFED 2009).
Especificidad de E. difficilis.
Los resultados de los bioensayos sobre la especificidad de E. difficilis, mostraron que este insecto es especializado en sus hábitos alimenticios. De las cinco especies de cultivos expuestos (frijol, chicharo, alfalfa, calabaza y pepino), solo el pepino sufrió 30,0 % de daño, que consistió en pequeños mordiscos, registrados en todos los discos de hojas expuestas; Sin embargo, los adultos murieron dos días después de la alimentación. Con excepción de las nervaduras, las hojas de B. geminiflora fueron completamente consumidas, y los insectos sobrevivieron por más tiempo que los expuestos a los cultivos.
Discusión
Aunque Gordon (1975) informó de la existencia de E. difficilis en su revisión de la subfamilia Epilachninae de América, no existen sinonimias anteriores o información sobre su biología y ecología, por lo que este es el primer estudio bioecológico de E. difficilis; su morfología general y la biología es similar a otras especies de Epilachna. Sin embargo, las larvas de otras especies registradas tienen cuatro mudas (Sánchez-Arroyo 1997; Araujo-Siqueira y Massutti de Almeida 2004), mientras que las larvas de E. difficilis mudan cinco veces durante su desarrollo.
La presencia de E. difficilis en el área de estudio fue determinada por factores bióticos y abióticos, incluyendo la temperatura, precipitación y enemigos naturales. Una exploración gráfica de la dinámica poblacional y las correlaciones de los principales picos poblacionales con la temperatura y la precipitación, sugieren que estas variables climáticas fueron los factores clave en la fluctuación de E. difficilis, similar a lo indicado para otras especies de epilacninos (Sweetman 1932; Sawada y Ohgushi, 1994). Shirai y Yara (2001) registraron que las larvas y adultos de E. varivestis fueron fuertemente inhibidos cuando se expusieron entre 27 y 32 °C. Sin embargo, Sweetman (1929) documentó que la humedad es también crucial para la existencia de esta plaga en los EE.UU.; en regiones con fuertes lluvias, la incidencia y el daño de E. varivestis fue mayor que en aquellos con menor precipitación. Una situación similar puede explicar la relación entre las poblaciones de E. difficilis y los niveles de precipitación en la barranca La Gloria.
La relación entre la precipitación y la dinámica poblacional de E. difficilis también puede explicarse indirectamente por el efecto positivo de la precipitación en la planta hospedera. En el presente estudio, las lluvias pudieron haber favorecido la recuperación de plantas dañadas, y consecuentemente, el incremento de las poblaciones del insecto. Aunque a finales del año se registraron plantas de B. geminiflora en la barranca, los cambios en su morfología y fisiología; tales como: el endurecimiento de tallos, estrechamiento de hojas y el desarrollo de tricomas glandulares (Rzedowski y Calderón 1995), probablemente limitaron la alimentación del coccinélido. Ha sido bien documentado que los tricomas glandulares son mecanismos de defensa de las plantas contra insectos herbívoros (Wagner et al. 2004).
En diciembre no se observaron poblaciones de E. difficilis, posiblemente debido al período de hibernación, tal como se menciona para otras especies de epilacninos como E. varivestis, E. niponica Lewis, 1896 y Henosepilachna vigintioctopunctata (Fabricus, 1775) (Coleoptera: Coccinellidae) (Sweetman 1929; Hirano 1985; Sawada y Ohgushi 1994). Se sabe que la migración e hibernación de algunos coccinélidos es afectada por la temperatura, la precipitación (Sweetman 1929) y probablemente, la falta de alimento. De acuerdo con los resultados, en la barranca La Gloria, estos tres factores ocurrieron al final del año, induciendo así la estivación del coccinélido. Sin embargo, se requiere desarrollar estudios específicos sobre la posible migración E. difficilis.
Las especies de depredadores registrados para E. difficilis son importantes agentes de control biológico. Las diferentes especies de la subfamilia Asopinae (Pentatomidae) han sido importantes enemigos naturales de coleópteros y lepidópteros plaga (Brailovsky y Mayorga 1994); por ejemplo, la especie P. maculiventris Say, 1832 (Hemiptera: Pentatomidae) ha sido objeto de múltiples estudios, incluyendo la multiplicación masiva para el control de plagas como E. varivestis (Hoffmann y Frodsham 1993; Sant'Ana et al. 1997). La vegetación silvestre es también un importante reservorio de enemigos naturales de plagas. Así, Logan et al. (1987) registraron en "hierba mora" silvestre (Solanum nigrum L.) de México hasta 18 especies de enemigos naturales, los que actúan como reguladores biológicos del escarabajo de la papa Leptinotarsa decemlineata Say, 1824 (Coleoptera: Chrysomelidae).
La alimentación de las especies de depredadores registrados en el presente estudio, incluyeron todas las etapas biológicas de E. difficilis, lo que sugiere un posible potencial para el manejo de coccinélidos plaga. P. nigropictus por ejemplo, es una especie interesante y sus registros frecuentes en campo sobre B. geminiflora, depredando adultos de E. difficilis, sugieren que es uno de los principales enemigos naturales de ese coccinélido. Además de los depredadores, el canibalismo también ocurrió en larvas de E. difficilis en campo, tal como ha sido notado en otros coccinélidos (Giorgi et al. 2009).
Aunque se sabe que los coccinélidos son atacados por varias especies de parasitoides y patógenos (Landis y Howard 1940; Beyene et al. 2007; Riddick et al. 2009), estos agentes de control no se observaron en este estudio. Beyene et al. (2007) registraron a los parasitoides como factor de mortalidad de huevos y pupas para el epilacnino Chnootriba similis Thunberg, 1781 (Coleoptera: Coccinellidae) en Etiopía; sin embargo, también sugieren que la mortalidad de las larvas era principalmente debido a los muchos depredadores presentes.
De acuerdo con las pruebas de especificidad, E. difficilis se alimenta solo en B. geminiflora. La familia Polemoniaceae tiene pocas especies cultivadas de importancia económica (Rzedowski y Calderón 1995); por lo tanto, se reduce el riesgo de que E. difficilis ataque cultivos. Sin embargo, se requieren más estudios sobre otras plantas de importancia económica como posibles hospederos del insecto.
Los epilacninos se han registrado en plantas de las familias Aristolochiaceae, Cucurbitaceae, Solanaceae, Berberidaceae, Asteraceae, Poaceae, Fabaceae, Urticaceae (sólo adultos), Convolvulaceae y Caryophyllaceae (Li y Cook 1961; Sawada y Ohgushi 1994; Giorgi et al. 2009; Szawaryn et al. 2015). El presente estudio adiciona la familia Polemoniaceae a la lista. El fuerte daño causado por E. difficilis a B. geminiflora sugiere que el insecto es un importante biorregulador de la planta.
Los resultados indican una amplia distribución regional de E. difficilis que van desde los climas cálidos hasta regiones relativamente más frías, lo que sugiere que el insecto sobrevive en todas las regiones donde crece su planta hospedera. Rzedowski y Calderón (1995) reportaron que B. geminiflora se encuentra desde México hasta Guatemala; Gordon (1975) examinó especímenes de E. difficilis de Guatemala y México (Chiapas, Durango, Jalisco y Sinaloa) sin especificar localidad y hospedero.
La adaptación de E. difficilis y su hospedera a regiones con diferentes condiciones climáticas sugieren que el epilacnino pudiera ser útil como hospedero alterno de enemigos naturales para el control de plagas. Diversos ejemplos documentan insectos fitófagos que prefieren plantas silvestres y los cultivos raramente son colonizados (Jacas y Urbaneja 2010; Rodríguez-Saona et al. 2012; Cortez-Madrigal et al. 2014), por lo que constituyen importantes hospedantes alternos para los enemigos naturales de plagas. De cinco especies de cultivos evaluados, sólo el pepino sufrió daños (30%) por adultos de E. difficilis, aunque todos los insectos murieron después.
La presencia de E. difficilis y su hospedera durante gran parte del año en la región de estudio, su especificidad e inocuidad a los cultivos evaluados, amplia distribución regional y, los enemigos naturales asociados, hacen de esta especie un buen candidato para ser utilizado como hospedero alternó de enemigos naturales de plagas y así poder ser utilizado en el control biológico de importantes plagas, como lo es E. varivestis.
Conclusiones
Los resultados del presente estudio son un importante aporte al conocimiento científico. Se registra por primera vez Epilachna difficilis en la planta Bonplandia geminiflora (Polemoniaceae); así, se aporta una familia más de plantas como hospederas de especies de epilacninos. Además, los resultados del presente estudio pudieran ser aprovechados en el manejo de plagas de especies relacionadas. La especialización del insecto y enemigos naturales asociados, así lo sugieren. Al no presentar riesgo como plaga, E. difficilis pudiera ser considerado un importante hospedero alterno de enemigos naturales de epilacninos de importancia económica.
Footnotes
Agradecimientos
Se agradece a Harry Urad Brailovsky Alperowitz, Departamento de Zoología del Instituto de Biología de la UNAM, México, D.F. por la identificación de los depredadores; a Ignacio García Ruiz, CIIDIR-IPN, Michoacán por la identificación de B. geminiflora; A Fabian Villalpando Barragán, por su apoyo en la edición de las fotografías. A los evaluadores anónimos por las observaciones y sugerencias para mejorar el presente manuscrito.