Abstract
Between December 2006 and May 2007 the transmission of an isolate of the Tomato yellow leaf curl virus (TYLCV) by Bemisia tabaci to several cultivated and wild solanaceous species was studied to determine their role as possible hosts of this virus. Plants of Solanum lycopersicum L., S. melongena L., S. hirtum Vahl, S. sisymbriifolium Lam., Datura stramonium L., D. inoxia Mill. Physalis angulata L., and P. ixocarpa Brot. were individually exposed during 48 h to B. tabaci adults reared on infected tomato plants. Control plants belonged to the same species but these were exposed to adults reared on virus free cotton plants. Thereafter, the plants were maintained inside B. tabaci test cages and observations were made to detect symptoms up to 30 days post exposure to the vector. Then foliar apex samples were taken for virus determinations through PCR. Symptoms of TYLCV infection were only observed on S. lycopersicum and D. stramonium at days 12 and 13, respectively, reaching 100% of the plants evaluated. TYLCV infection was corroborated through PCR. In the other plants exposed to infected adults, besides not showing symptoms, the virus was not detected by PCR. Additional observations it was detected that the insect did not form colonies on D. inoxia and S. sisymbriifolium. These results contribute information about the host range of this isolate of TYLCV in Venezuela, where this virus was recently reported for the first time in South America.
Introducción
El tomate, Solanum lycopersicum L. es una de las hortalizas más cultivadas en Venezuela cuya producción se destina tanto al consumo fresco como para uso industrial (Baptista y Felipe 1990; Fernández-Bravo et al. 2006). Entre los artrópodos que pueden limitar su rendimiento se encuentran gusanos perforadores de frutos, tales como Heliothis spp. (Lepidoptera: Noctuidae) en zonas bajas (< 400 msnm) donde se siembra una sola vez al año (Geraud-Pouey et al. 1995) y Neoleucinodes elegantalis Guenee, 1854 (Lepidoptera: Pyralidae) en zonas más altas (> 400 msnm) donde se cultiva todo el año (Fernández y Salas 1985; Geraud-Pouey et al. 1995). No obstante, Bemisia tabaci (Gennadius, 1889) (Hemiptera: Aleyrodidae) es probablemente el artrópodo de mayor relevancia en este y otros cultivos, pues además de los daños directos que causa a las plantas como insecto chupador, principalmente por su capacidad para trasmitir enfermedades virales, entre las cuales han adquirido especial relevancia las causadas por los Begomovirus (Polston y Anderson 1997; Rojas et al. 2000; Urbino et al. 2004).
Los Begomovirus pertenecen a la familia Geminiviridae que comprende virus de cápside icosahédrica geminada (partícula viral formada por dos porciones gemelas de 18 nm de diámetro) las cuales contienen cadenas simples circulares ADN de 2,5 a 3 Kb de tamaño (Hull 2002). La mayoría de los Begomovirus tienen genoma bipartito (ADN A y B), aunque algunos virus dentro de este grupo tienen genoma monopartito similar al ADN A de los Begomovirus anteriores, siendo uno de los más estudiado el TYLCV (Stanley et al. 2001). Los Bego-movirus son transmitidos exclusivamente por B. tabaci de manera circulativa (Jones 2003) y representan alrededor del 90% de los virus descritos dentro de la familia Geminiviridae (Fauquet y Stanley 2003).
El primer Begomovirus reportado en Venezuela fue el inicialmente referido como “un mosaico amarillo del tomate” (Debrot et al. 1963), el cual posteriormente fue denominado como virus del mosaico amarillo del tomate (Lastra y Uzcátegui 1975). La controversia taxonómica surgida a raíz de haber sido reportado y descrito el Potato yellow mosaic virus (PYMV) (Roberts et al. 1986; Coutts et al. 1991), el cual ha sido considerado como sinónimo del Tomato yellow mosaic virus (ToYMV) (Morales et al. 2001), fue discutida por Geraud-Pouey et al. (2009). Resulta interesante que las epifitias del PYMV (descrito como virus de papa, Solanum tuberosum L.,) sean mucho más comunes en tomate tanto en Venezuela como en otras regiones de América (Lastra y Uzcátegui 1975; Polston et al. 1998; Rojas et al. 2000; Urbino et al. 2004; Nava et al. 2006).
Dada la importancia adquirida por las enfermedades virales trasmitidas por B. tabaci, desde fines de los ochenta en Venezuela, comenzaron a realizarse inventarios de enfermedades virales sobre plantas sintomáticas (Nava et al. 1997, 1998a, 1998b), de los cuales se describieron dos Begomovirus bipartitos en tomate (Nava et al. 2006). Más recientemente, ha sido reportado para Venezuela y Suramérica el begomovirus monopartito, Tomato yellow leaf curl virus (TYLCV) (Zambrano et al. 2007) el cual parece estar ampliamente distribuido en el territorio nacional. Esta enfermedad viral ha causado cuantiosas pérdidas tanto en el nuevo como en el viejo mundo y en consecuencia, su importancia como problema fitosanitario ha sido ampliamente discutida (Polston et al. 1999; Moriones y Navas-Castillo 2000; Accotto et al. 2000).
B. tabaci coloniza más de 500 especies de plantas en 74 familias botánicas (Greathead 1986). Esta condición polífaga del insecto permite la transmisión de TYLCV en el campo tanto a especies cultivadas pertenecientes a otras familias botánicas (Navas-Castillo et al. 1999), como a otras solanáceas (Kashina et al. 2002) que en Venezuela se rotan o siembran en conjunto con el cultivo del tomate. Este virus puede también ser trasmitido a plantas silvestres (Sánchez-Campos et al. 2000; Kashina et al. 2002; García-Andrés et al. 2006), las cuales también crecen en los campos de cultivo y por tanto podrían constituir reservorios sintomáticos o asintomáticos de dichos virus (Umaharan et al. 1998; Salati et al. 2002).
Por tales razones, es importante, evaluar plantas cultivadas y silvestres como posibles hospederas de este Begomovirus en Venezuela. En consecuencia, este trabajo tuvo como fin evaluar la transmisión experimental de TYLCV por B. tabaci a algunas especies de solanáceas cultivadas y silvestres con el fin de aproximar su amplitud de hospederas que podrían constituir eslabones de la cadena epifitótica de esta enfermedad viral en el cultivo del tomate en Venezuela.
Materiales y Métodos
Ambiente experimental. Este trabajo fue conducido en condiciones de laboratorio (temperatura: 26,74 ± 1,5°C, Humedad Relativa (HR) 82 ± 3,7%) combinado con umbráculo (jaulasumbráculos, en el exterior del laboratorio, aproximadamente 34°C y HR de 87%) en el laboratorio MIPFH-UTF, Facultad de Agronomía, LUZ, Maracaibo, estado Zulia, Venezuela, durante diciembre 2006 - mayo 2007.
Del vector, del virus y de plantas fuentes. Las metodologías para la obtención de colonias de B. tabaci libre de virus, determinación del biotipo del vector, identificación del agente viral y mantenimiento de plantas fuentes, fueron detallados por Geraud-Pouey et al. (2009) y son aquí resumidas. Dado que el algodón Gossypium hirsutum L., ha sido reportado como planta no hospedera de TYLCV (Czosnek et al. 1993; Ghanim y Czosnek 2000), la colonia de B. tabaci libre de virus fue mantenida sobre esta especie de planta dentro de jaulas entomológicas en el laboratorio. De dicha colonia se obtuvieron adultos de B. tabaci no virulíferos para infestar las plantas utilizadas como testigos.
La determinación del biotipo B de B. tabaci en la colonia libre de virus fue confirmada mediante amplificación parcial del gen mitocondrial mtCOI que codifica para la enzima Citocromo Oxidasa I (Frohlich et al. 1999). Por otro lado, las plantas de tomate híbrido Río Orinoco (Petoseed, Saticoy, California, EE. UU.) utilizadas como fuentes del TYLCV también se mantuvieron en jaulas entomológicas dentro del laboratorio. En las mismas, a partir de un fragmento amplificado de 851 pares de bases que incluye la secuencia completa del gen que codifica la proteína de la cápside (Ling et al. 2006), se obtuvo un 96% de identidad nucleotídica con el aislado TYLCV Mild [Portugal] recién reportado para Venezuela por Zambrano et al. (2007).
Una vez culminado este período de inoculación, se retiraron las jaulas plásticas y para eliminar los adultos de B. tabaci, las plantas se asperjaron con una solución de imidacloprid (Relevo 500®, INICA, Cagua, Venezuela) preparada a 0,04% v/v de ingrediente activo. En ese momento las plantas se transplantaron a macetas plásticas (capacidad 2 l) y fueron pasadas a las jaulas umbráculos ya descritas.
Posterior al periodo de inoculación, las plantas se observaron a diario para detectar síntomas hasta los treinta días post exposición al vector, estimándose así el día de aparición de síntomas. Además se calculó el porcentaje de plantas sintomáticas para cada una de las repeticiones, obteniéndose así tres valores por tratamiento totalizando 48. Con el objeto de confirmar la transmisión del agente viral observada inicialmente por la aparición de síntomas así como para descartar la existencia de especies asintomáticas en aquellas plantas sometidas a moscas virulíferas, se tomaron muestras de ápices foliares en seis plantas, dos por repetición, para cada especie evaluada. Igual número de muestras fueron tomadas en los testigos.
Para evitar deterioro de las proteínas por putrefacción, cada muestra se depositó dentro de una copa de papel secante moldeada dentro de un envase de plástico transparente (2,8 cm x 4,5 cm, diámetro x altura, dimensiones internas), con tapa enroscada, conteniendo silica gel como desecante, en la mitad inferior. Para completar la rápida deshidratación, se cambió la silica gel al siguiente día.
Resultados y Discusión
La Tabla 1 muestra el tiempo de aparición de síntomas y el porcentaje de plantas sintomáticas para las especies expuestas a moscas blancas virulíferas y no virulíferas. Entre las primeras, solo S. lycopersicum y D. stramonium manifestaron síntomas de TYLCV. Dichos resultados fueron corroborados por PCR (Fig. 1). En el resto de las plantas infestadas con moscas blancas virulíferas, además de no manifestar síntomas, el virus no fue detectado por PCR. Ninguna de las plantas expuestas a moscas blancas no virulíferas mostró síntomas (Tabla 1), ni se detectó el virus mediante las PCR realizadas (Fig. 1).
Tiempo de aparición y porcentaje de plantas con síntomas para las diferentes especies inoculadas con adultos B. tabaci virulíferos y no virulíferos.
= Columnas con la misma letra indican que no hay diferencia significativa al P = 0,05.
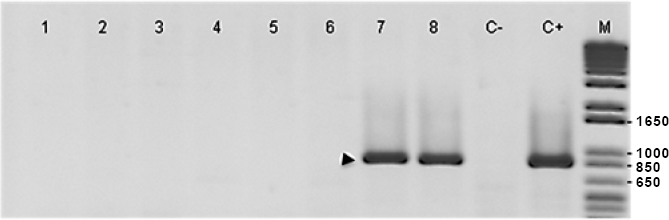
Diagnóstico mediante la PCR de la presencia de TYLCV en las diferentes especies de solanáceas infestadas con adultos virulíferos de B. tabaci. 1. Physalis ixocarpa, 2. P. angulata, 3. Solanum melongena, 4. S. hirtum, 5. S. sisymbriifolium, 6. Datura inoxia, 7. D. stramonium, 8. S. lycopersicum. C-: Control negativo, C+: Control Positivo; M: marcador 1Kb plus (InvitrogenTM) indicado tamaño de los fragmentos en pares de bases. Flecha indica 850 pares de bases.
El tiempo promedio de aparición de síntomas resultó 11,58 ±0,85 (amplitud: 11-15 días) y 12,95 ± 1,61 (amplitud: 11-14 días) para S. lycopersicum y D. stramonium respectivamente sin diferencias significativas entre éstas (Tabla 1). En tomate los síntomas se caracterizaron por acortamiento de los entrenudos apicales así como encrespado de las hojas terminales y amarillamiento acentuado hacia los bordes (Fig. 2A) comparado con las plantas sanas (Fig. 2B) mientras que en D. stramonium, las hojas tendían a ondularse mostrando también amarillamiento intervenal algo difuso (Fig. 2C), contrastante con la superficie plana y el color verde uniforme observado en las plantas sanas de esta especie (Fig. 2D).

Plantas de Solanum lycopersicum y de Datura stramonium con síntomas de infección por TYLCV (2A y 2C) y plantas asintomáticas (2B y 2D, expuestas a adultos de Bemisia tabaci no virulíferos.
En ambos casos, la presencia del virus fue detectada en el 100% de las plantas (Tabla 1). Esto indica que D. stramonium se comportó como un hospedero sintomático, el cual podría ser reservorio del referido virus en el campo. Esto corrobora experimentalmente para Venezuela, estudios que la han referido como hospedera sintomática de TYLCV tanto en el campo como en ensayos experimentales (Ramos et al. 1996; Kashina et al. 2002; Salati et al. 2002; De Blas et al. 2004).
A pesar que D. inoxia pertenece al mismo género que D. stramonium, no resultó infectada por este aislado de TYLCV (Tabla 1, Fig. 1). En ello aparentemente podría haber influido la inadaptabilidad de la mosca blanca a la planta pues en las infestaciones con adultos de B. tabaci se observó menor oviposición y no hubo formación de colonias (Tabla 2), ya que las escasas ninfas que se fijaron no sobrevivieron más allá del segundo estadío. Estos resultados contrastan con lo referido por Gilbertson (2007), quien señala a D. meteloides (sinónimo de D. inoxia) como hospedero de TYLCV. No obstante, este autor no da detalles de la metodología seguida. Variantes poblacionales que pueden ocurrir en especies de plantas así como en los aislados del virus, entre otros, podrían explicar tales diferencias.
Desarrollo de colonias de B. tabaci en las especies evaluadas. Número de adultos utilizados = 50. Plantas evaluadas por tratamientos = 3.
Tampoco se detectó TYLCV (Fig. 1) ni se desarrollaron colonias del insecto vector (Tabla 2) en S. sisymbriifolium. Esta planta posee una alta densidad de pequeños tricomas glandulares distribuidos sobre toda su superficie y que exudan sustancias pegajosas. Adultos de B. tabaci quedaron atrapados en esos tricomas. La importancia de esta incompatibilidad insecto-planta podría evaluarse como posible práctica para el manejo de este problema fitosanitario. Estudios realizados por Haider et al. (2001) utilizaron esta especie como patrón injertado sobre tomate más la aplicación de un insecticida, como parte de un programa de manejo integrado de plagas en ese cultivo y encontraron baja incidencia tanto de B. tabaci como de TYLCV en ese tratamiento comparado con las otras alternativas.
Por el contrario, tanto en S. hirtum, S. melongena, así como en las dos especies de Physalis, donde tampoco ocurrió infección viral (Fig. 1), B. tabaci formó colonias apreciables, de manera similar a D. stramonium. Ello descarta cualquier limitación debido a que el insecto vector no se alimente de la planta. Los resultados con S. melongena, coinciden con los obtenidos por Rubinstein y Czosnek (1997). Por el contrario los de P. angulata, contrastan con los de Yutaka et al. (2002). Asimismo, también se ha descrito que TYLCV pudo ser trasmitido mediante injerto desde tomate a P. ixocarpa (Valverde et al. 2001).
Conclusiones
Las plantas silvestres evaluadas ocurren comúnmente en campos de Venezuela donde se siembra tomate. Por esta razón estos trabajos contribuyen al conocimiento de la amplitud de hospederas de TYLCV como reservorios del virus en el campo. Estos resultados muestran que D. inoxia, S. sisymbriifolium, S. hirtum, S. melongena, Physalis angulata, y P. ixocarpa, no se infectaron con este aislado de TYLCV. En las dos primeras especies mencionadas podría influir la incompatibilidad entre el insecto vector y la planta. Las diferencias frente a lo observado en otras investigaciones en cuanto a la no detección del virus en D. inoxia, y las dos especies de Physalis sugieren variantes en el comportamiento de los organismos involucrados. Como se ha comentado anteriormente, variantes poblacionales de las especies de plantas o del aislado viral, podrían explicar las discrepancias de resultados.
Finalmente es importante resaltar que aunque la biología del vector sobre las diferentes hospederas no fue objeto de este trabajo, a la vista de lo obtenido, podría ser interesante realizar estos estudios especialmente en aquellas hospederas donde se observó posible antibiosis sobre el vector para eventualmente evaluarla como fuentes de resistencia o prácticas tendientes a disminuir las poblaciones de B. tabaci y así interferir con las relaciones de transmisión.
Footnotes
Agradecimientos
Al FONACIT por haber financiado parcialmente la presente investigación a través de las subvenciones “G-2000001610" y “Diseño de un Esterilizador de suelos”. A Enrique Moriones, de La Estación La Mayora, Málaga, España por las correcciones hechas a este manuscrito y a los evaluadores anónimos.
