Abstract
The whitefly Lecanoideus floccissimus is reported for the first time from material collected in Tabasco, Mexico. Furthermore, to identify the biotic and abiotic factors that regulate its populations and the causes that induce their increase in cocoa crops, periodic sampling was conducted during 2004 in two plantations under different conditions. One was located in Mantilla, Cunduacan, > 35 years old, with scarce canopy and surrounded by cocoa plantations. The other plantation was located in Habanero, Cárdenas, approximately 15 years old, abundant canopy and isolated from cocoa plantations. Through direct sampling and yellow traps, the incidence of the pest (percentage of infested trees), population abundance and natural enemies were determined. The effect of temperature and precipitation on pest incidence was evaluated. L. floccissimus was present all year round. In the old plantation, incidence was higher (72.31 ± 21.81%) than the young plantation (26.39 ± 13.17%). The opposite occurred in insect populations: the highest levels were recorded in the young plantation and the lowest in the old plantation. The main natural enemies were the predator Ceraeochrysa sp. and parasitoids of the family Aphelinidae; the greatest activity of the entomophages was on eggs and early instars. Of the abiotic factors, only temperature was correlated with the pest (r = 0.76-0.77). The rapid proliferation of L. floccissimus in cocoa crops in Tabasco could be explained by the age of cocoa plantations (> 35 years), as well as the low diversity and activity of natural enemies.
Introducción
Con una superficie de 60.000 ha, Tabasco es el principal productor de cacao Theobroma cacao L. en México (INEGI 2004) y una de las regiones productoras del mundo con menor incidencia de plagas. Tradicionalmente sólo cuatro especies eran consideradas problema: Toxoptera aurantii B. de F., 1841 (Hemiptera: Aphididae), Clastoptera sp. (Hemiptera: Cercopidae), Selenotrips rubrocinctus Girad, 1901 (Thysanoptera: Thripidae) y la “lagarta” Peosina mexicana Guenée, 1862 (Lepidoptera: Noctuidae) (Flores 1976; Sánchez 1995). Lo anterior puede considerarse una ventaja respecto a otras regiones del mundo, en donde el complejo de plagas y enfermedades es mayor (Entwistle 1972); sin embargo, no se descarta la introducción o resurgencia de nuevas plagas y enfermedades del cultivo, tal como ocurrió en 1991 cuando se observaron poblaciones de una especie de mosca blanca no registrada con anterioridad en la región. Aunque la presencia de este insecto causó interés científico, sus bajas poblaciones, pobre distribución en el Estado y, consecuentemente poco interés de los productores, no se le dio la importancia debida. Sin embargo, las altas poblaciones del insecto ocurridas durante 1998 motivaron a que los productores solicitaran apoyo gubernamental para el control de la plaga en cacaotales de los municipios de Cunduacán y Cárdenas, Tabasco. La especie fue identificada preliminarmente por la Dra. Laura D. Ortega Arenas y el Dr. Emilio Carapia Ruiz, como Lecanoideus floccissimus Martin, 1997.
La mosca blanca espiral L. floccissimus es originaria de Suramérica y descrita por Martin en 1997 (Martin et al. 1997; Carnero et al. 1999). Actualmente se distribuye en las regiones Neotropical (Colombia, Ecuador, Perú) y Paleártica (Islas Canarias y España) (Martin et al. 1997, 2000; EPPO 2003). El insecto ataca alrededor de 94 especies de plantas, principalmente plátano Musa sp., guayaba Psidium guajaba L., 1753, papayo Carica papaya L., 1753, mango Mangifera indica L. 1753, coco Cocos nucifera L., 1753; y las ornamentales como la “kentia” Howea forsteriana (C. Moore y F. Muell.) Becc., 1877, laurel de la India Ficus benjamina L., 1767, el falso pimentero Schinus terebinthifolius Raddi, 1820 y las “strelitzias” Strelitzia nicolai Regel y Koern, 1858 (Hernández-Suárez et al. 2000). Los daños ocasionados por L. floccissimus son similares a los de otros aleiródidos, pero potenciados por su mayor talla (3 mm). Por sus daños directos, al succionar la savia de la planta, y los indirectos, al ocasionar fuertes excreciones de mielecilla sobre la que hay una excesiva proliferación de hongos “fumagina”, puede causar caída prematura de hojas, y en infestaciones fuertes matar la planta. A diferencia de sus parientes cercanos L. floccissimus no transmite enfermedades de origen viral, aspecto que magnificaría la implementación de programas de control biológico en el manejo de la plaga (Hernández et al. 2002).
Por ser un insecto de reciente detección en Tabasco, con una fuerte incidencia que lo cataloga como plaga potencial del cacao y otros cultivos en la región; pero fundamentalmente, debido a la ausencia de información que permita diseñar estrategias de manejo, los objetivos planteados fueron: corroborar la identidad de L. floccissimus recolectados de cacao en Tabasco, México e identificar los factores bióticos y abióticos que se relacionan fuertemente con sus poblaciones.
Materiales y Métodos
Sitios de estudio
El estudio se realizó durante el 2004 en dos plantaciones de cacao en la región de “La Chontalpa”, Tabasco, México. El clima es cálido húmedo (Am) con abundantes lluvias en verano, precipitación media anual de 1.947 a 2.003,2 mm y humedad relativa promedio anual de 82% (INEGI 2004). Una plantación se ubicó en el Ejido Mantilla, municipio de Cunduacán (A); y la otra, en el Ejido Habanero, municipio de Cárdenas (B); ambas bajo diferentes sistemas de manejo como: edad de la plantación, densidad de sombra, cultivos aledaños, actividad humana, entre otros (Tabla 1). En ambas plantaciones no se aplicaron insecticidas.
Características de las plantaciones de cacao estudiadas en Tabasco, México. 2004.
S = Superficie (ha); P = Número de plantas/ha; D = Densidad de plantación; So = Sombra (árboles/ha); E = Edad de plantación (años); H = Actividad humana; CA = Cultivos aledaños.
Descripción morfológica
Las “pupas” y exuvias fueron procesadas siguiendo la técnica de montaje en portaobjetos descrita por Martin (1987). Las preparaciones se analizaron en un microscopio compuesto a 100, 400 y 1.000 aumentos, se realizaron mediciones con un micrómetro con aproximación máxima de 1 µm y se tomaron fotografías con un fotomicroscopio III Carl Zeiss con cámara Paxcam 3. La descripción se realizó usando la terminología detallada por Russell (1965), Martin (1987), Martin et al. (1997), Hodges y Evans (2005). Los ejemplares se depositaron en la colección entomológica del Colegio de Postgraduados, Campus Tabasco, Cárdenas, Tabasco, México.
Incidencia y niveles poblacionales de L. floccissimus
Se realizaron muestreos quincenales, con desfazamiento semanal entre plantación, de modo que el primer muestreo (23 de enero) fue en el Ejido Mantilla y ocho días después en Habanero; la decisión se tomó por lo laborioso de la actividad, y considerar el ciclo (36-53 días) relativamente largo de la plaga (Hernández y Carnero 2000) así lo permitía. Se practicaron dos tipos de muestreo: uno para conocer la incidencia o porcentaje de árboles infestados y el otro, para conocer los niveles poblacionales de los diferentes estados de la plaga.
La evaluación de incidencia se realizó quincenalmente y se midió con base en el número de árboles infestados en relación con el total de árboles de la plantación, con la ecuación:
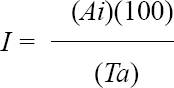
Para conocer el tamaño de muestra y determinar los niveles poblacionales de la plaga, se practicó un muestreo preliminar y mediante la fórmula descrita por Southwood (1976) se estimó el número de árboles y ramillas (cinco a ocho hojas) por árbol a registrar. El tamaño de la muestra para árboles fue tan grande, que sólo se tomó el 10%, de modo que en Mantilla se consideró una muestra de 40 árboles y en Habanero 21. Para ramillas, el tamaño de muestra estimado fue de seis por árbol; los árboles y ramillas seleccionadas fueron los mismos durante el estudio.
Además, se determinó la presencia y abundancia de depredadores y parasitoides asociados a la plaga. Para recolectar los parasitoides, se elaboraron trampas de emergencia con tela de “organza”, se colocaron sobre huevos y ninfas de la plaga presentes sobre las hojas y se revisaron quincenalmente. Adicionalmente, se usaron trampas amarillas pegajosas (30 x 30 cm) para detectar migraciones de adultos de la plaga. Se colocaron ocho trampas por plantación: seis en los linderos y dos en la parte media. Las trampas se colocaron a 2,5 m del suelo, amarradas a las ramas de dos árboles vecinos. Las trampas se revisaban quincenalmente, se registraban y retiraban los insectos capturados y, eventualmente se les adicionaba nuevo pegamento. Las trampas permanecieron en el mismo lugar durante el estudio. Los datos de temperatura y precipitación durante el estudio se obtuvieron de las estaciones meteorológicas de Samaria y González, municipio de Cárdenas localizadas ~20 km de los sitios de estudio.
Análisis estadístico
Un análisis de correlación lineal simple fue practicado entre las variables bióticas y abióticas; para la comparación de los niveles poblacionales entre sitios se uso la prueba “t” de Student (a = 0,05) con las fechas de muestreo como repetición, de modo que hubo 12 repeticiones. Complementariamente se usaron estadísticas descriptivas para el análisis de la distribución temporal de las poblaciones medias mensuales.
Resultados
Descripción morfológica
Especímenes in vivo
Cuerpo pupal color amarillento, pero la colonia completa con apariencia obscura por las copiosas cantidades de cera blanca, adornada con gruesas bandas en espiral de cera. Los adultos (3 mm) completamente blancos en apariencia, frecuentemente ocultos debajo de las secreciones cerosas de la colonia. Huevos colocados en masas en el envés de las hojas, dispuestos en hileras concéntricas irregulares. Las ninfas y adultos ocurren en densas colonias, que en ocasiones cubren completamente el envés de las hojas, por lo que se desprenden pequeñas partículas blancas al ser perturbadas (Figs. 1 A-C).
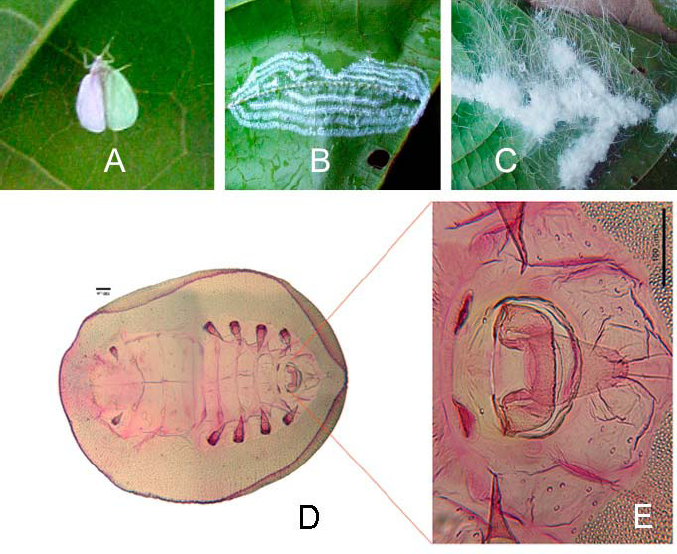
Lecanoideus floccissimus Martin en cacao Theobroma cacao L, en Tabasco, México:
Especímenes montados en portaobjetos
Cubierta pupal en forma oval; margen plegado ventralmente, al menos parcialmente, aunque aparenta mayor dimensión cuando son montados en laminillas; margen liso, pero donde éste se pliega aparenta ser irregular. Especimenes montados de 1,00 a 1,41 mm de largo, aparentando ser más aplanados anteriormente. Orificio vasiforme, opérculo y língula claramente definidos; línea del orificio vasiforme completa, enfatizando la língula lisa y sin ningún surco medio. Seta marginal posterior mayor a 100 µm de largo, las marginales anteriores ausentes; submargen interno con 12 pares (incluyendo el par caudal) de finas y largas setas mayores de 100 µm; un sólo par en la región cefálico posterior, meso y meta torácica y octavo segmento abdominal. Presencia de un par de grandes poros compuestos en la región cefálica y cuatro en la región abdominal; cefálico usualmente de 30-35 µm y abdominales de 40-50 µm en diámetro, cuyo proceso central puntiagudo, en material montado, dirigido invariablemente a la región medio posterior. Además, el VIII segmento abdominal con poros compuestos muy pequeños (10-20 µm) inconsistentemente presentes cerca de la línea media posterior al orificio vasiforme. Submargen comprende una amplia zona cubierta de poros simples dispuestos en forma dispersa, los cuales disminuyen en diámetro hacia la parte media. Cutícula de la parte submedia lisa y punteada sólo por poros ovoides septados. Antenas largas, casi alcanzando la parte posterior del espiráculo abdominal anterior; seta abdominal ventral de hasta 75 µm de longitud, situada posterior al orificio vasiforme (Figs. 1 D-E).
Condiciones climáticas
Se observaron diferencias en temperatura y precipitación entre las plantaciones de Mantilla y Habanero. Para la primera plantación los datos de ambas variables fueron de 22,7°C y 1.592,20 mm respectivamente. En Habanero la temperatura media anual fue de 22, 16°C y 1.660,50 mm en ese orden. Aunque en términos anuales fue poca la diferencia, analizadas en forma mensual las diferencias fueron mayores. Las diferencias en temperatura fluctuaron desde 0,30°C hasta 1,47°C favorables a Mantilla. Asimismo, aunque la precipitación anual fue mayor en Habanero, en siete de los 12 meses se observó mayor precipitación en Mantilla, lo que sugiere mayor uniformidad en la precipitación de esa plantación (Tabla 2).
Temperatura media y precipitación acumulada mensual durante el año 2004 en dos plantaciones de cacao de Tabasco, México.
(+) = Favorable a Mantilla; (-) Favorable a Habanero
/Temperatura media anual
/Precipitación acumulada anual.
Incidencia de L. floccissimus
La plaga estuvo presente durante el periodo de estudio y aunque la tendencia de las curvas fue similar en ambas plantaciones de cacao, se detectaron diferencias significativas (P = 0,0001) respecto a la incidencia del insecto. La incidencia media fue mayor en Mantilla (72,31 ± 21,81%) que en Habanero (26,39 ± 13,17%); En Mantilla el 50% de incidencia fue rebasado en el mes de marzo, en Habanero la incidencia siempre se mantuvo abajo del 50%. En ambas plantaciones se observaron dos fases de incremento: una de enero a mayo y la otra de junio a noviembre, mes en donde se alcanzó el máximo porcentaje de incidencia. La menor incidencia acumulada de L. floccissimus se registró en el mes de enero con un valor de 28,3% en Mantilla y 0% en Habanero (Fig. 2).
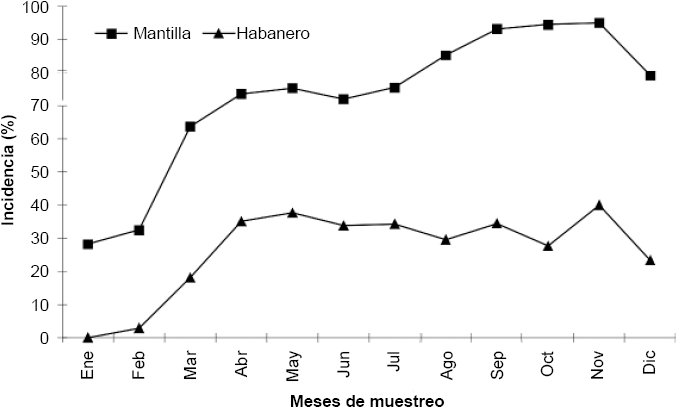
Incidencia de Lecanoideus floccissimus en el cultivo de cacao en dos localidades de La Chontalpa, Tabasco, 2004.
Niveles poblacionales de L. floccissimus
Contrario a lo ocurrido con la incidencia, el nivel poblacional medio de la plaga en sus diferentes estados de desarrollo fue mayor en la plantación de Habanero que en la de Mantilla (Tabla 3).
Valores medios de árboles infestados (incidencia), oviposturas, ninfas y adultos de L. floccissimus y sus enemigos naturales en dos plantaciones de cacao en Tabasco, México, 2004.
Medias ± desviación estándar dentro de hileras, seguidas de la misma letra no difieren estadísticamente (prueba t de Student, 22 g.l, α = 0,05).
Oviposturas
Aunque el número de oviposturas tendió a ser mayor en Habanero que en Mantilla, las diferencias no fueron significativas (Tabla 3). Temporalmente se registraron oviposturas en tres picos principales: en abril, agosto y octubre en Mantilla, con el mayor registro en octubre (Fig. 3A). En Habanero, los picos fueron en marzo, julio y noviembre, con la mayor abundancia en julio (Fig. 4A).
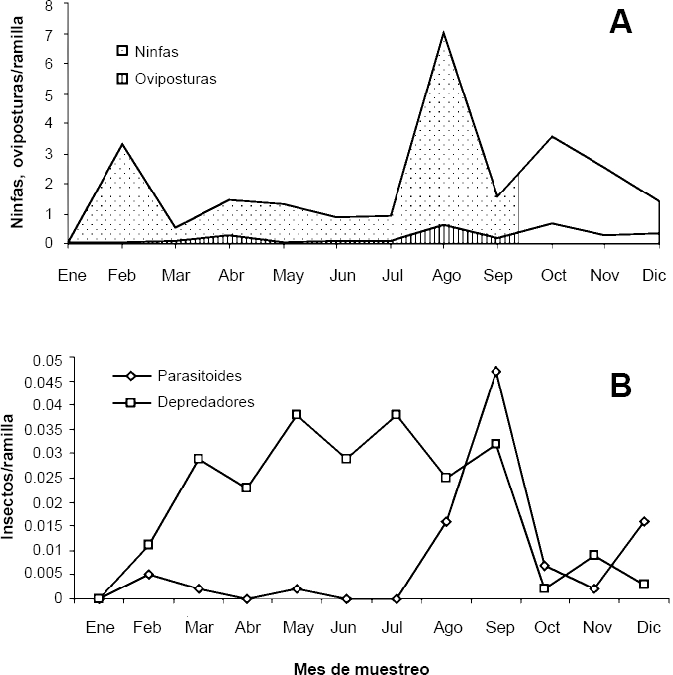
Distribución temporal de oviposturas, ninfas (
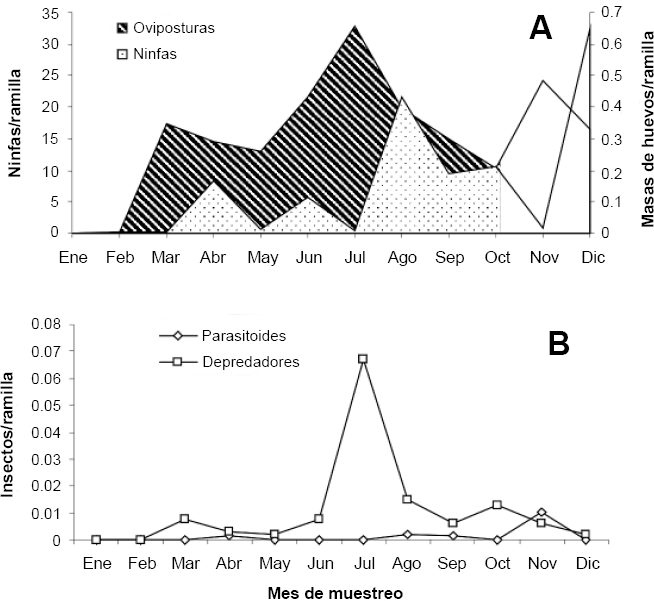
Distribución temporal de oviposturas, ninfas (
Ninfas
El número promedio de ninfas en Habanero fue de 7,5 ± 10,12, significativamente mayor (P = 0,05) que en Mantilla, con solo 1,8 ± 1,73 media de ninfas por ramilla (Tabla 3). En ambos sitios se registraron cinco picos poblacionales: febrero, abril, mayo, agosto y octubre, en Mantilla; en Habanero fue en abril, junio, agosto, octubre y diciembre, con el máximo nivel en diciembre. En ambas plantaciones las ninfas estuvieron ausentes en el mes de enero (Figs. 3A, 4A).
Enemigos naturales de L. floccissimus
Como parasitoides, se registraron individuos de la familia Aphelinidae con muy baja actividad parasítica en ambas plantaciones. El mal estado de los ejemplares impidió su identificación a especie. Al parecer hubo una tendencia a una mayor actividad en Mantilla que en Habanero; sin embargo, las diferencias no fueron significativas (Tabla 3).
Respecto a la distribución temporal de los parasitoides en Mantilla, se observaron picos en febrero, mayo, septiembre y diciembre, con el más alto nivel en septiembre; éste último pico coincidió con una fuerte reducción en las poblaciones de ninfas (Figs. 3A-B). En Habanero se registraron picos en abril, agosto y el más alto en noviembre que coincidió también con la reducción de ninfas en ese mes (Figs. 4A-B). Los parasitoides se registraron sobre oviposturas y ninfas de primer y segundo instar.
Al igual que los parasitoides, la actividad de los depredadores fue baja. En ambos sitios se registraron larvas de Ceraeochrysa sp. (Neuroptera: Chrysopidae), principalmente en huevos y ninfas de primero y segundo instar, y aunque la tendencia fue a tener mayores poblaciones en Mantilla, las diferencias estadísticas no fueron significativas (Tabla 3). En Mantilla se detectaron cinco picos poblacionales: marzo, mayo, julio, septiembre y noviembre, que en general correspondieron con las más bajas densidades de ninfas (Figs. 3A-B). En Habanero, la fluctuación de Ceraeochrysa se observó en marzo, julio y octubre (Fig. 4B).
Adultos
Se detectaron diferencias significativas (P = 0,05) respecto al valor medio de la densidad poblacional entre ambas plantaciones. En Habanero se registró la mayor población de adultos de L. floccissimus (Tabla 3) y al igual que las ninfas, se registraron cinco picos de máxima incidencia en marzo, mayo, julio, septiembre y noviembre, con la densidad más alta en marzo. En Mantilla los principales picos se registraron en marzo, julio, septiembre, noviembre y diciembre. En ambas plantaciones no hubo poblaciones de adultos durante los meses de enero y febrero y en diciembre no estuvieron en Habanero, situación que coincidió con las más bajas temperaturas (Tabla 2; Fig. 5).
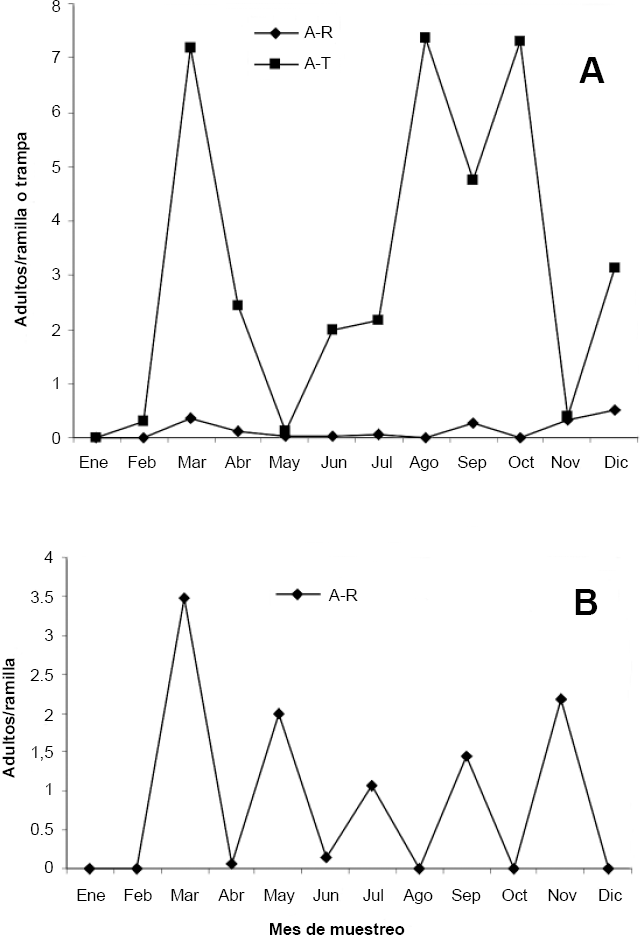
Fluctuación poblacional de Lecanoideus floccissimus en cacaotales de Tabasco mediante muestreos directos (A-R) de adultos en Mantilla (
Migración de adultos
La detección de adultos mediante trampas de color sólo se obtuvo en la plantación de Mantilla. De enero a mayo se registró una tendencia similar en la fluctuación obtenida con el muestreo visual y las trampas de color; sin embargo, a partir de junio las tendencias fueron marcadamente diferentes. Se registraron cuatro picos poblacionales: marzo, junio, agosto, octubre y diciembre (Figs. 5A-B).
Relación de L. floccissimus con los factores bióticos y abióticos
En Mantilla, se detectó una correlación positiva entre incidencia de L. floccissimus vs oviposturas (r = 0,62, P = 0,03); entre incidencia vs temperatura media mensual (r = 0,76, P = 0,003); y entre adultos capturados en trampas de color vs oviposturas (r = 0,66, P = 0,02) (Figs. 6A-C). En Habanero hubo correlaciones positivas entre oviposturas vs temperatura (r = 0,69, P = 0,01), incidencia vs temperatura (r = 0.77, P = 0,003), incidencia vs oviposturas (r = 0,76, P = 0,004) y, larvas de Ceraeochrysa sp. vs oviposturas (r = 0,69, P = 0,01) (Figs. 7A-C).
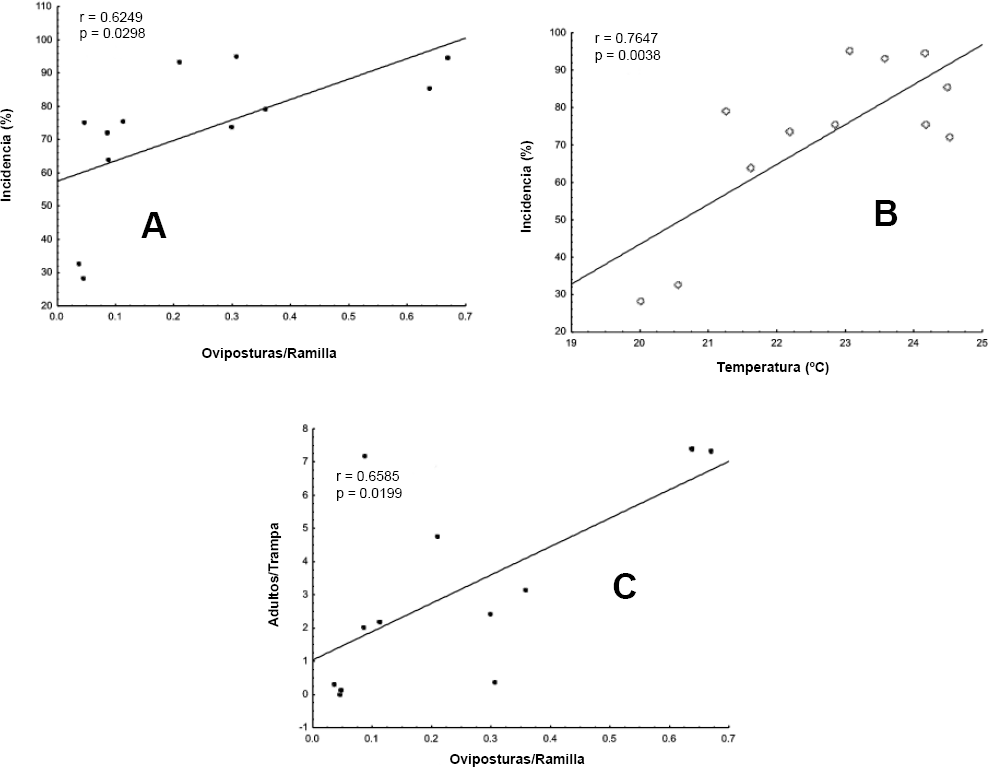
Dispersión de las diferentes variables correlacionadas en Mantilla, Cunduacán, Tabasco.
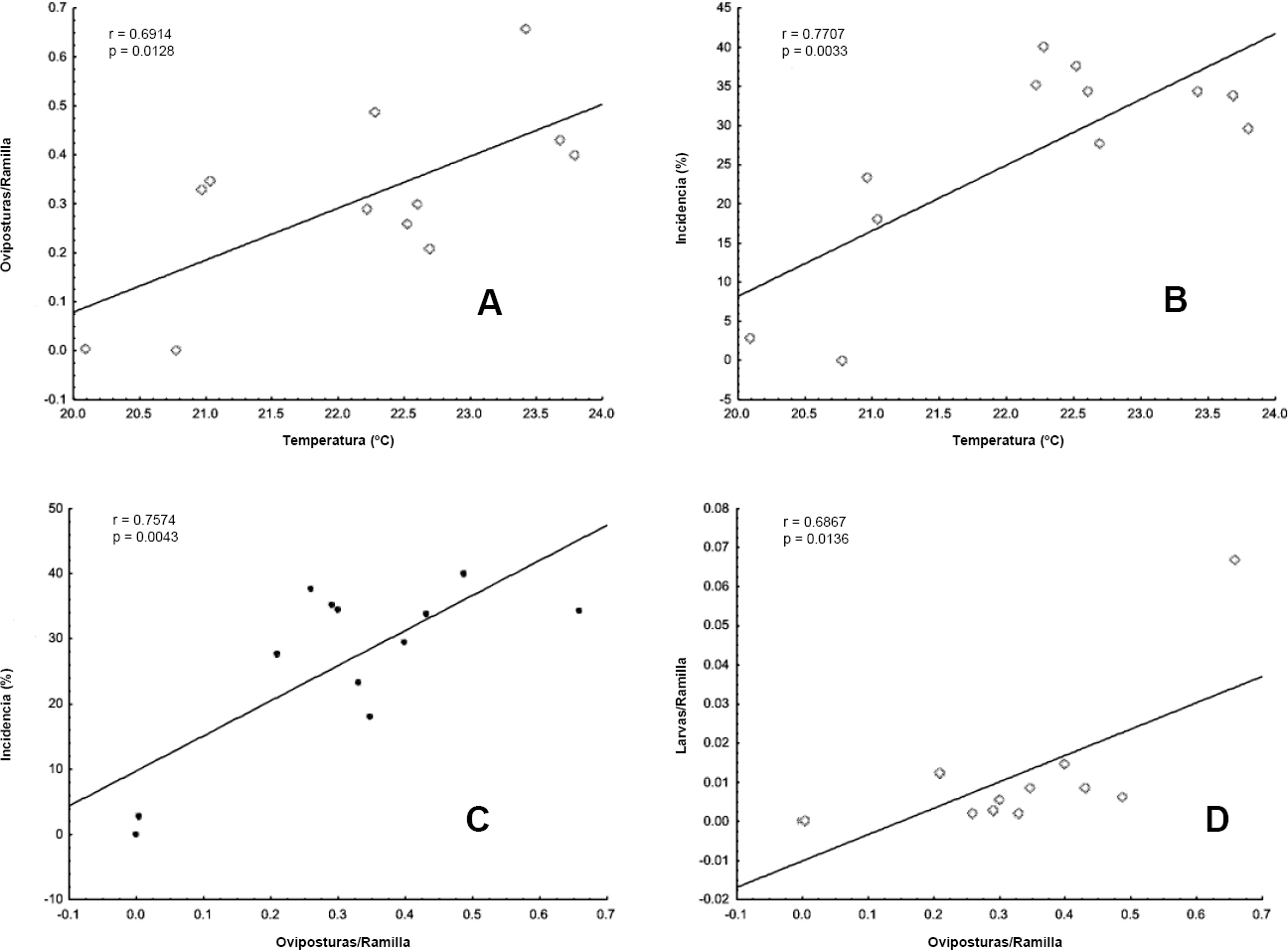
Dispersión de las diferentes variables correlacionadas en Habanero, Cárdenas, Tabasco.
Discusión
Al existir una mayor incidencia de L. floccissimus en Mantilla, se esperarían también mayores niveles poblacionales de la plaga en esa plantación, lo cual no ocurrió. Lo anterior conlleva necesariamente a dos cuestionamientos, primero ¿Qué determinó la mayor y menor incidencia de la plaga en Mantilla y Habanero, respectivamente? y, segundo ¿Qué favoreció las mayores poblaciones de la plaga en Habanero y las limitó en Mantilla? La aparente contradicción entre estos dos planteamientos pudiera explicarse mediante la siguiente discusión.
Es posible que la aparente falta de relación entre incidencia y densidad poblacional se deba a múltiples factores, entre ellos: edad de la plantación, nivel de sombreado, estado nutricional de las plantas, diversidad vegetal y actividades humanas dentro de la plantación. En Mantilla, sitio donde se encontró la mayor incidencia de la plaga, la plantación tenía alrededor de 35 años de edad, con menor densidad de árboles de sombra. Consecuentemente el menor nivel de sombra y la mayor radiación pudieron haber favorecido una mayor dispersión, reflejada ésta en mayor incidencia de la plaga. Contrariamente, la plantación de Habanero, con menor edad (15 años) y mayor densidad de árboles de sombra, fueron factores que posiblemente limitaron la dispersión del insecto. La falta de capturas de adultos en trampas de color en Habanero pudo estar relacionada con la dispersión de los adultos limitada por la mayor sombra en esa plantación. Como trampas de atracción visual, una de las recomendaciones para la utilización de trampas de color es mantener el suelo desnudo de vegetación (Taylor y Palmer 1972; Peña-Martínez et al. 2001).
Otro factor poco considerado en la dispersión de insectos pudo ser la actividad humana dentro de las plantaciones; en este caso, la ubicación de la plantación de Mantilla, con casas aledañas y libre transito de personas dentro de la plantación, así como la presencia de plantaciones contiguas de cacao, probablemente hayan contribuido a una mayor diseminación del insecto. En Habanero, la actividad humana fue mínima en comparación con Mantilla. Al respecto, D'Almeida et al. (1998) y Blanco-Metzler y Laprade (2000) señalan que la dispersión de Aleurodicus dispersus (Russell) (Hem: Aleyrodidae) está fuertemente ligada a los caminos y a la actividad de las personas.
Las diferencias en la dispersión del insecto entre ambas plantaciones pudiera explicar en parte la mayor densidad del insecto registrada en Habanero. Pudo ser que la reducida dispersión favoreció la concentración de altas poblaciones de la plaga en pocos árboles; de igual manera, las condiciones de mayor sombra en Habanero pudieron haber limitado el impacto de factores de mortalidad como: temperatura, precipitación y enemigos naturales. Contrariamente, en Mantilla esos factores pudieron contribuir de manera importante en la reducción de la plaga.
Aunque no se encontró una correlación entre densidad de la plaga y temperatura, la influencia de ésta en las poblaciones de L. floccissimus ha sido señalada para otras regiones. Hernández et al. (2002) observaron que temperaturas por debajo de 15°C y por encima de 30°C reducen las poblaciones del insecto; incluso, a 30°C el ciclo de desarrollo se vio interrumpido. Pudiera ser que las mayores temperaturas registradas en Mantilla respecto de Habanero (22,7°C vs 22,16°C) y magnificadas por el bajo nivel de sombra, hayan contribuido en la reducción de la densidad del insecto en esa plantación. En diez de los 12 meses se registraron diferencias hasta de 1,47°C favorables a Mantilla (Tabla 2).
Respecto a la precipitación, es factible suponer que la menor cobertura vegetal en Mantilla pudo favorecer un mayor impacto negativo de ese factor abiótico en la densidad de la plaga. Aunque la precipitación anual en ambas plantaciones fue similar, en algunos registros mensuales fue notoria la mayor precipitación en Mantilla (Tabla 2). Reportes previos señalan que precipitaciones intensas son causa de reducciones temporales de L. floccissimus (Carnero et al. 1999), principalmente en los estados de huevo y ninfa de primer instar (Hernández et al. 2002).
Además de los factores anteriores, el microclima de las plantaciones de cacao debe ser considerado en futuros estudios con L. floccissimus, tal como lo señalan Blanco-Metzler y Laprade (2000) para A. dispersus en bananos de Costa Rica. Aunque en nuestro estudio no se determinó el microclima, éste pudo influir en las diferencias de las variables bióticas; en este caso, en los enemigos naturales. Ya han sido señalados los bajos niveles de parasitismo que ocurren en el cultivo del cacao, lo que al parecer se debe a la ausencia de floración adecuada para los parasitoides y al exceso de sombra en el cultivo (Stary 1967; Cortéz 1994). Observaciones realizadas con poblaciones de L. floccissimus en árboles de guanábana (Annona muricata), un cultivo con mayor radiación solar que el cacao, registraron mayores niveles de parasitismo que los registrados en cacao.
Lo anterior pudiera explicar la tendencia a una mayor actividad de enemigos naturales en la plantación con menor sombra (Mantilla). Adicionalmente, se sabe que las abundantes secreciones céreas de L. floccissimus limitan la actividad de sus enemigos naturales solo a nivel de huevo y primero y segundo instares (Nijhof et al. 2000). Es probable que en plantaciones viejas como la de Mantilla, con mayor radiación y mayor impacto de la lluvia en las secreciones céreas, se favorezca una mayor actividad de los enemigos naturales de la plaga. La sincronización entre los principales picos de Ceraeochrysa sp. con las menores densidades de oviposturas y ninfas en Mantilla así lo sugieren (Figs. 3A-B).
El presente estudio aporta los primeros conocimientos sobre L. floccissimus en Tabasco México, y proporciona importantes elementos para iniciar programas de manejo de la plaga. Uno de ellos pudiera ser el manejo de las plantaciones, en donde la clave de la regulación de la plaga parece estar en el nivel de sombra del cultivo. Futuros estudios deben evaluar diferentes porcentajes de sombra en cacao y seleccionar el que desfavorezca la incidencia y niveles poblacionales de las principales plagas del cultivo, incluida L. floccissimus. Otro elemento de manejo debe ser la conservación e incremento de los enemigos naturales de la plaga.
Footnotes
Agradecimientos
A Vicente Emilio Carapia, Profesor-Investigador de la Universidad Autónoma de Morelos, México por su apoyo en la identificación de los especimenes. A la Fundación PRODUCE-Tabasco por el financiamiento del presente estudio.
