Abstract
To detect and quantify the amount of Propoxur in insects of forensic importance and search for entomotoxicologic indicators, the HPLC (High Performance Liquid Chromatography) technique was used on individuals collected during the ecological succession associated with the corpses of rabbits. Three rabbits were sacrificed with an overdose of Propoxur and a fourth control rabbit was sacrificed by cervical dislocation. The rabbits were checked over 28 days, three times a day (07:00, 13:00 and 18:00 hours). During this period, immature and adult insects were collected, and the ambient temperature, corporal temperature and weight loss were measured. From the collected material, 73 individuals from among the immatures (larvae I, II, III, pupae) and adults of the order Diptera and Coleoptera were selected and the component of interest was evaluated by HPLC. There was a positive result in 56% of the samples from larva I to adult in all the successional stages of decomposition. This technique allowed a high sensitivity from 0.1 g or less for each sample in the quantification of Propoxur residues in larvae and adults. Samples with a weight of 0.0029 g for Diptera and 0.029 g for Coleoptera were quantified. The minimum detected concentration (0,671 ppm) was found in stadium II larvae of Calliphoridae and Muscidae dipterans and the maximum quantified concentration (229,721 ppm) was found in stadium III larvae of Lucilia eximia (Diptera: Calliphoridae), with percentages of 0.04 and 0.34, respectively.
Introducción
La entomotoxicología es una herramienta que aplica análisis toxicológicos a insectos que se alimentan de carroña, con el fin de identificar drogas y toxinas tales como insecticidas, antidepresivos tricíclicos y estimulantes (barbitúricos, cocaína y anfetaminas) presentes en tejidos. También investiga los efectos causados por dichas sustancias en el desarrollo de los artrópodos para determinar el intervalo postmortem (IPM) (Introna et al. 2001) ya que la confiabilidad de la evidencia entomológica para la estimación de IPM puede depender de la presencia de productos en los tejidos de las larvas pues algunas toxinas pueden afectar la rata de crecimiento de las especies presentes en los cadáveres (Gagliano-Candela y Aventaggiato 2001; Goff and Lord 2001; Introna et al. 2001; Introna et al. 1990; Goff et al. 1993, 1991, 1989).
Por los métodos tradicionales de la toxicología, los productos de envenenamiento se recuperan mediante muestras de órganos internos, orina y sangre; sin embargo, en estados avanzados de descomposición esta técnica no es posible (Introna et al. 2001). De ahí que los insectos puedan ser una alternativa en la determinación de la presencia de sustancias en un cuerpo, dado que el análisis cualitativo en las larvas es una evidencia de la presencia de un compuesto determinado (Wolff et al. 2004; Bourel et al. 2001; Hédouin, et al. 2001; Introna et al., 2001; Bourel et al. 1999; Goff et al. 1997, 1993). La entomotoxicología utiliza técnicas tales como Análisis Radio Inmunológico (RIA), Cromatografía de Gases (GC), Cromatografía de Capa Fina (TLC), Cromatografía Gaseosa Acoplada a Masas (GC-MS) y Cromatografía Líquida de Alta Resolución (HPLC) (Introna et al. 2001).
El Propoxur es un producto ampliamente comercializado que no tiene prescripción ni restricciones para su compra y es de bajo costo. Es un carbamato muy persistente, cuyo ingrediente activo presenta un DL 50 de 100 mg/kg de peso. Es un insecticida de ingestión y contacto (FAO 1985).
Por lo anterior, el objetivo de este trabajo fue detectar cuantitativa y cualitativamente Propoxur en insectos asociados al proceso de descomposición cadavérica, como una metodología de apoyo a la investigación médica y judicial.
Materiales y Métodos
El trabajo se realizó en la ciudad de Medellín, Colombia, situada a una altitud de 1.450 msnm, en un área designada según Holdridge como bosque húmedo premontano (bh-P), con temperatura ambiental entre 18-24°C y pluviosidad media anual de 1.409 mm (IGAC 1997; Espinal 1985).
Para el estudio se utilizaron cuatro conejos (Sylvilagus brasiliensis L.) de 3,1-3,2 Kg. Uno de ellos, que se utilizó como control, fue sacrificado por dislocamiento cervical. A los otros tres se les inyectó con una dosis letal de 10 ml de Propoxur vía intra-cardíaca y se les suministró 1 ml vía oral. Previo al sacrificio todos los conejos fueron anestesiados con 0,7 ml de Ketalar, siguiendo el protocolo aprobado por el Comité de Bioética de la Universidad de Antioquia. Después del sacrificio se extrajeron 10 g de hígado de cada uno de los conejos para un posterior análisis toxicológico. Los conejos fueron colocados individualmente en jaulas metálicas de 60 x 50 x 40 cm separadas entre si a una distancia de 5 m.
Los insectos que se encontraban sobre los cadáveres fueron colectados diariamente durante 28 días entre los meses de junio y julio, tres veces al día: a las 7, 13 y 18 horas, y una vez al día se midió la temperatura ambiente, la temperatura corporal (rectal) y la pérdida de peso. Se recogieron tanto insectos inmaduros en todos los estadios (LI, LII, LIII, pupa), como adultos en orificios naturales (ojos, orejas, boca y ano); sobrevolando el cuerpo, bajo éste y en el suelo hasta una profundidad de 10 cm en un área de 40 x 60 cm. Una parte de los insectos colectados se fijó y almacenó en alcohol al 70% para la identificación taxonómica y otra parte, consistente en una muestra de individuos de todos los estadios provenientes de todos los sitios, se almacenó de forma individual en viales secos y se llevó a -20° C, al igual que una porción de 20 g de hígado proveniente de cada uno de los cuatro conejos a evaluar para la detección y cuantificación del Propoxur por HPLC.
Procesamiento de insectos en laboratorio.
Previo al procesamiento para detección en el HPLC, las muestras entomológicas guardadas en frío se separaron por estadio de desarrollo, previa determinación taxonómica e identificación del estado sucesional correspondiente a la fase de descomposición de cada conejo (Castillo 2001; Shalaby et al, 2000; Schoenly et al., 1996; Timms 1994). De igual forma se procedió con los insectos fijados en alcohol.
Separación y cuantificación del Propoxur por Cromatografía Líquida de Alta Resolución (HPLC).
El análisis se llevó a cabo en un cromatógrafo líquido (Gilson) con detector de arreglo de diodos (DAD) a una longitud de onda de 263 nm. Columna: Water BondapackC18: 3,9 x 300 mm, Guarda columna: WAT044480, W10861. Fase móvil: Acetonitrilo: Agua (50:50). Gradiente isocrático: temperatura ambiente y flujo de 1,2 ml/min (Fig. 1). El tiempo de elución del Propoxur fue de 4,4 minutos.
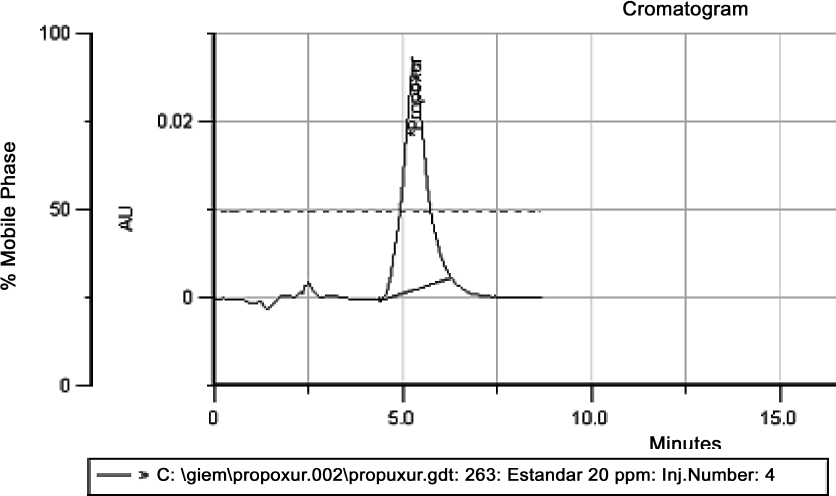
Cromatograma correspondiente al estándar de Propoxur (estándar primario).
Un máximo de 0,2 g de muestra de insecto o hígado fue sometido a la técnica cromatográfica luego de maceración y tres extracciones; mezcla Agua: ACN (50:50) con 0,5 ml de solución por extracción para un volumen total de 1,5 ml. Cada extracción se acompañó con el sonicador durante 10 minutos. Se centrifugó para separar el sobrenadante en tubos Eppendorf, y se le agregó 0,1 ml de etanol con el fin de precipitar las proteínas para volver a centrifugar. La solución sobrenadante se inyectó directamente en el cromatógrafo líquido.
La cuantificación se realizó por curva de calibración, para ello se prepararon diferentes diluciones del estándar de Propoxur y se inyectaron en el cromatógrafo (Tabla 1). Como estándar interno se empleó el Carbofurano lote 234-101B a un 99% de pureza de CHEM SERVICE, con esos datos se buscó la linealidad del método, graficando la relación área (uA)/ concentración (ppm) en función del logaritmo de la concentración (Fig. 2a), empleando el programa estadístico Statgraphics Plus 5.0. El factor de respuesta se encontró en el rango de 400 357,42 y 442 500,30, a un 95% de nivel de confianza. A partir de esos resultados, se determinaron los límites de cuantificación, siendo la concentración de 1,8 ppm el límite de donde se estimó que el Propoxur es cuantificable en un rango de linealidad de 1,8 a 58 ppm. Así mismo, se graficó el área en función de la concentración (Fig. 2b) y se obtuvo una relación lineal entre las variables, con un coeficiente de correlación = 0,99951 y R2 = 99,902%.
Lectura de las áreas para los estándares de Propoxur en la separación y cuantificación por Cromatografía Líquida de Alta Resolución (HPLC).
ppm= partes por millón, Área = unidades de área, Conc = concentración.
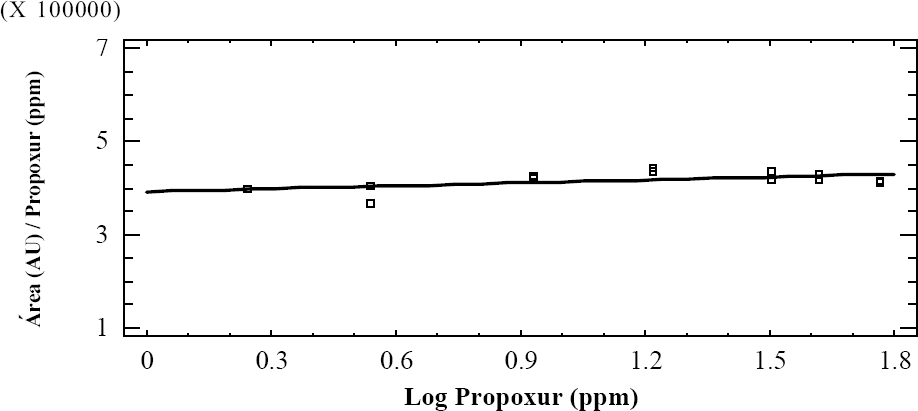
Evaluación de la linealidad del Propoxur: Relación Área (uA) versus el Logaritmo de la concentración.
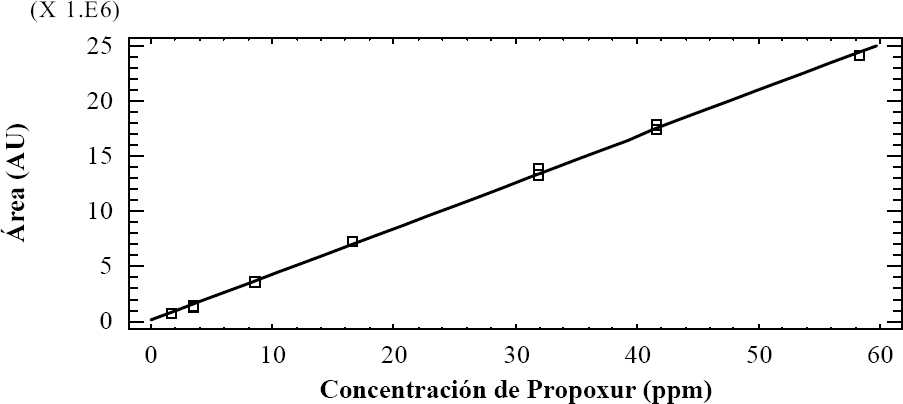
Curva de calibración del área en función de la concentración.
Para validar el método de extracción y separación del Propoxur, se tomaron larvas limpias del conejo control y se doparon con una concentración conocida de Propoxur (estándar primario); luego se procedió al proceso de extracción descrito anteriormente, con un porcentaje de recuperación del 82% (Fig. 3).
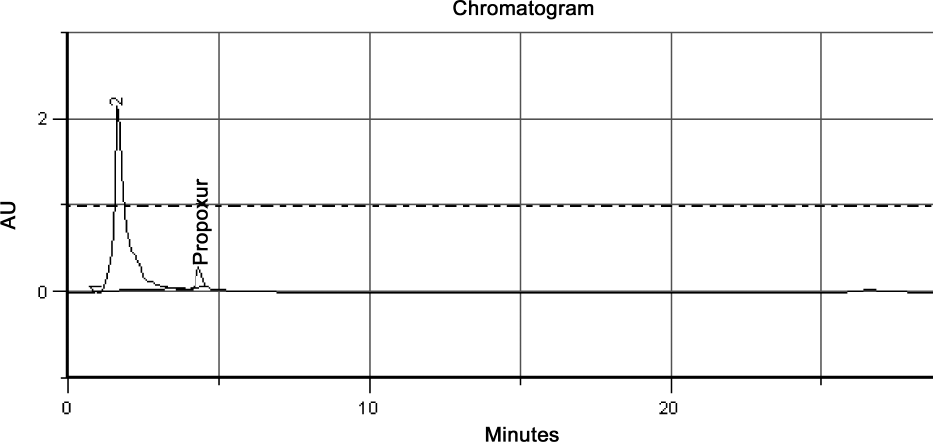
Cromatograma correspondiente a larvas control de Lucilia eximia, dopadas con Propoxur (estándar primario).
Resultados y Discusión
En la sucesión de artrópodos observada durante el proceso de la descomposición, se registraron cinco fases de descomposición: fresco, hinchado, descomposición activa, descomposición avanzada y momificado, no observándose la fase de restos. Se colectaron organismos pertenecientes a 16 órdenes (Diptera, Coleoptera, Hymenoptera, Lepidoptera, Blattaria, Orthoptera, Dermaptera, Hemiptera, Thysanura, Thysanoptera, Collembola, Acari, Araneae, Geophilomorpha, Isopoda, Oligochaeta) y a 36 familias distribuidos en todas las categorías ecológicas (Smith 1986): necrófagos (Calliphoridae, Muscidae -en parte-, Sarcophagidae, Phoridae, Sepsidae -en parte-, Cleridae, Trogidae, Acari); depredadores (Calliphoridae -en parte-; Muscidae -en parte-, Carabidae, Histeridae, Staphylinidae, Reduviidae -en parte-, Aranae, Geophilomorpha); omnívoros (Blattidae, Vespidae, Formicidae, Labiidae, Labiduridae, Isopoda) e incidentales (Apidae, Braconidae, Cydnidae, Gelastocoridae, Miridae, Reduviidae -en parte-, Chloropidae, Sphaeroceridae, Syrphidae, Tabanidae, Cicadellidae, Membracidae, Elateridae, Gryllidae, Lepismatidae, Thysanoptera, Hypogastruridae, Onychiuridae).
Del total de individuos colectados, se utilizó una muestra (N=73) para el análisis, obteniéndose un resultado positivo (detección y/o cuantificación del Propoxur) en 41 ejemplares entre larvas, pupas y adultos de Diptera y Coleoptera (Tabla 2), pertenecientes a los conejos uno y dos (Figs. 4a-c). En el conejo tres no hubo detección del producto, ni en el control. Las concentraciones de Propoxur que se pudieron cuantificar estuvieron entre 0,6771ppm en larva II de Muscidae y Calliphoridae y 229,712 ppm en larva III de Lucilia eximia Wiedemann, y con una área promedio de 284 104,25 y 96 391 120 respectivamente (Tabla 2).
Insectos en los cuales se detectó y cuantificó el Propoxur por el método de HPLC.
NC = no se cuantificó, aunque se detectó.
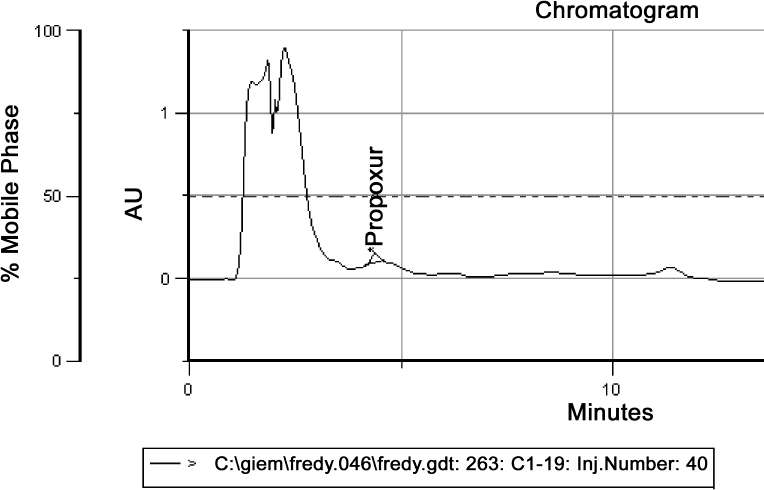
Cromatograma de detección del Propoxur en una muestra de Trox sp. (Coleoptera, Trogidae).
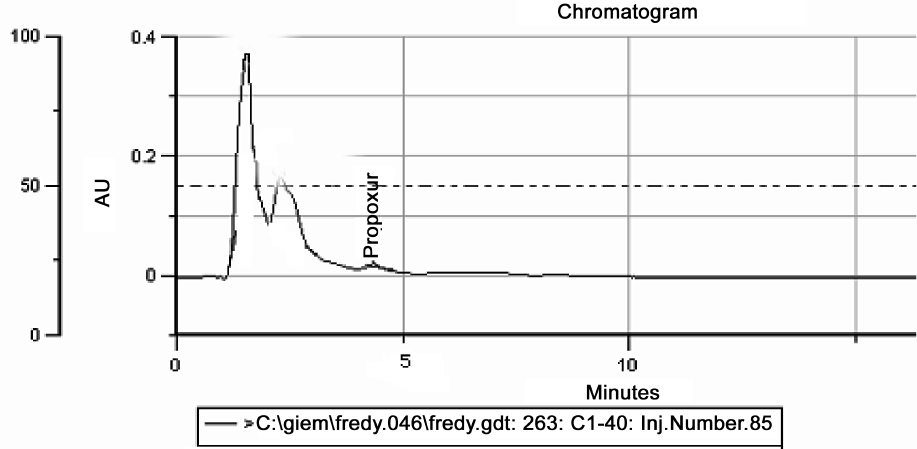
Cromatograma de detección del Propoxur en una muestra de Chrysomya albiceps (Diptera, Calliphoridae).
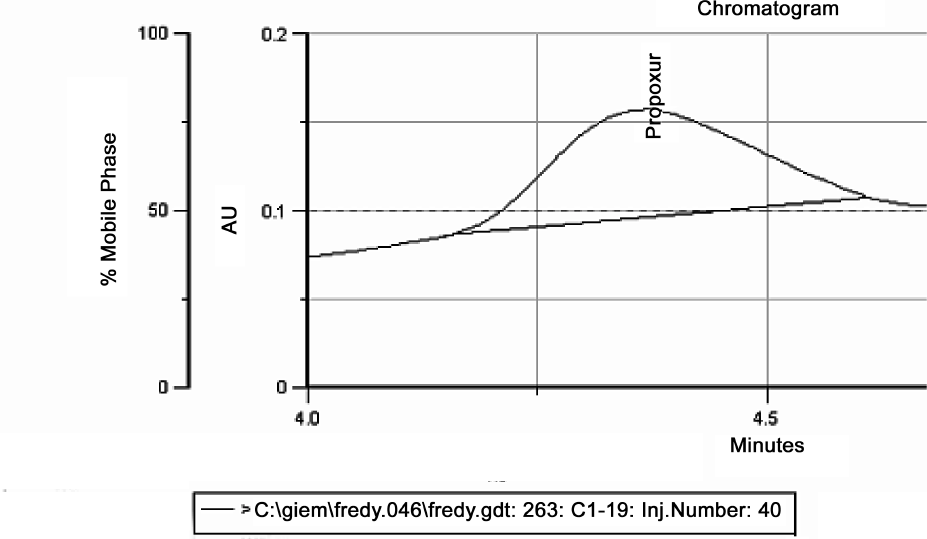
Ampliación del pico correspondiente al Propoxur, detectado en larva III de Cochliomyia macellaria (Diptera, Calliphoridae) luego de ser sometida al proceso de extracción, a una longitud de 263 nm.
En lo que respecta a las muestras de los hígados, no se encontró Propoxur en ninguno de los conejos sometidos al producto, ni en el control, lo que podría explicarse por el mecanismo de dispersión del Propoxur. Los carbamatos no se acumulan en el organismo; su biotransformación se realiza por hidrólisis, oxidación y conjugación y se eliminan rápidamente por vía urinaria. (Anónimo 2006).
En la sucesión se observó como grupos mayoritarios en estadio de larva individuos de Diptera y Coleoptera; del primer grupo se encontraron las familias Calliphoridae, Sarcophagidae, Muscidae y Phoridae y del segundo, Trogidae, Staphylinidae, Dermestidae y Cleridae. La familia Calliphoridae fue la primera en llegar y depositar sus huevecillos en todos los conejos, L. eximia, se recolectó en todas las fases de descomposición, disminuyendo en el periodo momificado. Cochliomya macellaria (Fabricius) estuvo presente en mayor cantidad en el periodo de hinchado al igual que la Chrysomya albiceps (Widemann), la cual fue encontrada hasta momificado. Chrysomya megacephala (Fabricius) estuvo presente sólo en el conejo dos desde activo a momificado. Larvas de Sarcophagidae fueron colectadas en todos los modelos desde el periodo hinchado hasta el momificado.
La familia Muscidae (Polietes sp.) predominó en todas las fases de descomposición. La familia Phoridae (Trophodeinus sp.) se colectó en el suelo a partir del periodo hinchado hasta el final del muestreo. En el segundo grupo, los coleópteros adultos de Trogidae (Trox sp.) predominaron desde hinchado hasta momificado. En este grupo se cuantificaron los mayores residuos del veneno; igualmente se obtuvo Staphylinidae (Aleocharinae), Dermestidae (Dermestes sp.) y Cleridae (Necrobia rufipes (DeGeer)); estos últimos de gran importancia en la entomología forense ya que predominan desde la fase de activo hasta la de momificado.
Los himenópteros, presentes en todas las fases de descomposición y que forman parte de la fauna local con carácter de oportunistas, fueron observados devorando larvas, en especial de Diptera. Los demás grupos, que fueron minoritarios (Hemiptera -Gelastocoridae-, Lepidoptera, Anthicidae, Collembola, algunos Formicidae y otros artrópodos -Isópodos y otros-) fueron considerados como incidentales ya que hacen parte de la fauna local.
En cuanto a la detección del Propoxur (Tabla 2), los resultados fueron positivos a partir del periodo en fresco para larvas I de Calliphoridae colectadas directamente del cuerpo, pero no fue posible la cuantificación. Para la fase de hinchado, se detectaron nueve larvas III de L. eximia, provenientes del suelo y del cuerpo. La detección en pupas se efectuó en ejemplares hallados enterrados a partir de la fase de descomposición avanzada, pertenecientes a Calliphoridae (una de C. albiceps y cuatro indeterminadas).
Para el caso de los Dermestes sp. y Trox sp., se detectó el Propoxur tanto en larvas como adultos y en N. rufipes, en adultos; estas especies fueron colectadas al interior del cuerpo de los conejos y aunque aparecen en periodos de descomposición desde hinchado hasta momificado (Trox sp.) o desde activo a momificado (Dermestes sp. y N. rufipes), son consideradas propias de las últimas fases de descomposición o, como ocurrió en este trabajo, de partes del cuerpo que sufren un proceso de esqueletización mucho antes que el resto del cuerpo como las patas o miembros inferiores al tener menor cantidad de tejido blando.
Con respecto al consumo de los cadáve-res, la presencia del veneno no alteró las etapas sucesionales en los insectos, pero sí las fases de descomposición. Esto fue debido quizás al mecanismo de dispersión del veneno.
La técnica del HPLC mostró ser una herramienta muy eficaz para la Entomotoxicología a partir de muestras con un peso desde 0,0029 g. Se detectó y cuantificó el Propoxur en larvas LI, II, III, pupa y adultos de Diptera; larvas y adultos de Coleoptera; en las etapas de sucesión de fresco, hinchado, avanzado y momificado. La concentración más alta detectada (0,5584 %) se presentó para los coleópteros (Trox sp.) en momificación.
Los estudios en entomotoxicología con fines forenses aunque han sido numerosos son muy escasos en lo que respecta a pesticidas; tan solo se tienen reportes de detección en el organofosforado malation, en el cual se realizaron extracciones por cromatografía gaseosa (GC) en larvas de Diptera (Gunatilake y Goff, 1989) y por cromatografía líquida de alta resolución (HPLC), en donde se obtuvieron resultados positivos larvas de Diptera y adultos de Coleoptera (Wolff et al. 2004).
Este es el primer estudio que se efectúa con Propoxur, con el cual, se pudo estandarizar un protocolo para cuantificar y detectar el carbamato en insectos de importancia médico-legal. Este trabajo demuestra la importancia de considerar la Entomotoxicología en Colombia como una herramienta eficaz de apoyo a las ciencias forenses.
