Abstract
The aim of this paper was to study the morphological changes in the development of Leishmania mexicana (MHOM/VE/72/AZV) and L. amazonensis (IFLA/BR/67/PH8) in Lutzomyia evansi. Females of Lu. evansi fed on a hamster tarsal lesion and were examined for infection at 24 h intervals from 24 h to 168 h post- feeding. The pattern of development of Le. mexicana and Le. amazonensis in Lu. evansi was suprapylarian consistent with what has been described for species of the Le. mexicana complex. Transformation from amastigote to procyclical forms occurred in both species at 24 - 48 h post-infection. The parasites showed their adaptation to the gut environment of Lu. evansi and development to mature forms: nectomonads, haptomonads and paramastigotes. The paramastigote form was observed in low percentage at 120 h post-infected ingestion in both species. The early depletion of nutrients in Lu. evansi, due to a faster rate of digestion (3 to 4 days), could explain the low percentage of development reaching the paramastigote forms and the absence of the metacyclical forms in this model.
Introducción
La competencia vectorial de especies flebotominas en la transmisión de Leishmania sp. depende de diversos factores que condicionan la susceptibilidad o refractariedad del insecto al protozoario (Nieves y Pimenta 2001).
Los estudios sobre competencia vectorial han sido realizados mediante la búsqueda de insectos naturalmente infectados y/o, al-ternativamente, mediante la infección y transmisión experimental, observándose que la fauna flebotomina neotropical muestra poca resistencia intrínseca al desarrollo de un gran número de especies de Leishmania, inclusive aquellas no transmitidas por estos insectos en la naturaleza (Killick-Kendrick 1979), a diferencia de la relación Phlebotomus-Leishmania del Viejo Mundo donde pareciera existir una especificidad.
Rojas (1991) señala que en América diferentes especies de Lutzomyia o Psychodopygus mastozoófilos pueden actuar como vectores, siempre y cuando se hallen en el área de la biocenosis leishmánica. En este contexto, Lutzomyia evansi (Núñez-Tovar), considerado vector alterno de leishmaniasis visceral en Colombia y Venezuela (Travi et al. 1990; Aguilar et al. 1998; Feliciangeli et al. 1999; Montoya et al. 2003), se ha encontrado en focos endémicos de Leishmaniasis donde las dos formas clínicas de la enfermedad coexisten. Montoya (1996), en San Andrés de Sotavento, Colombia, encuentra a Lu. evansi como la especie más abundante con una tasa de infección de 0,037% con parásitos tipificados como Le. chagasi y tasa de 0,018% con Leishmania sp, que por su patrón de desarrollo sugiere sea Le. panamensis.
En Venezuela, la presencia de Lu. evansi en focos endémicos donde son simpátricas las dos formas clínicas de la enfermedad ha sido señalada en la región oriental y en los andes (González et al. 1995, 1999; González 1998). En la región de los andes, Vívenes (2000) encuentra una tasa de infección natural de 0,23% con parásitos de desarrollo suprapilórico que, al ser inoculados a un hámster sano, desarrolla un granuloma blando no ulcerado y sin evidencia de invasión a vísceras. Desafortunadamente este aislado no pudo ser tipificado ya que un segundo repique a hámster no reprodujo la infección.
Estas observaciones motivaron la realización de estudios de infección experimental de Lu. evansi con parásitos del complejo Leishmania mexicana hallándose una tasa de infección experimental del 21,7% para Le. amazonensis y 29,4% para Le. mexicana y un incremento de la invasión parasitaria hacia la válvula esofágica cuando se ofreció, a los insectos, una segunda ingesta sanguínea sobre hámster sano (Vívenes et al. 2001).
El presente estudio tuvo como objetivo, observar los cambios morfológicos y pleomórficos desplegados por Le. mexicana y Le. amazonensis en Lu. evansi.
Materiales y Métodos
Parásitos
Le. mexicana: Cepa (MHOM/VE/72/AZV), mantenida por repiques sucesivos en hámster. Cepa cedida por el personal del Laboratorio de Inmunología, Facultad de Ciencias Universidad de Los Andes, Mérida. Le. amazonensis: Cepa (IFLA/BR/67/PH8) mantenida por repique en Mus musculus. Cepa donada por el Dr. José A. O'Daly del Centro de Microbiología y Biología Molecular, Instituto Venezolano de Investigaciones Científicas (IVIC), Caracas.
Inoculación
Hámsteres machos de 30 días de nacidos se inocularon a partir del tejido de la lesión tarsal de un hámster donador de las cepas (PH8 o AZV). Este tejido se maceró en 1 ml de solución salina fisiológica y se ajustó a una concentración de 2 X 104 parásitos/ 0,1 ml para ser inoculada por vía subcutánea en cada uno de los tarsos posteriores de los hámsteres experimentales.
Infección experimental
Hembras silvestres de Lu. evansi, procedentes de un área donde no han sido señalados casos de leishmaniasis cutánea o visceral, y con 24 h de ayuno, se separaron en tres lotes de 70 ejemplares en jaulas con cubierta de organdí. Seguidamente se les ofreció una ingesta sanguínea sobre una lesión tarsal de hámster de 30-40 días de evolución. Las hembras alimentadas se mantuvieron con solución saturada de sacarosa a temperatura de 26°C, 78% de humedad relativa y en completa oscuridad.
Cada 24 h hasta las 168 h post-ingesta infectiva, lotes de 10 ejemplares hembra de Lu. evansi se disecaron en busca de formas flageladas dentro del tracto digestivo. Los ejemplares se sumergieron previamente en solución jabonosa (solución salina 0,65%/ Triton), para eliminar pelos y escamas. Luego se lavaron en solución salina 0,85% para eliminar el detergente y, una a una, se disecó bajo lupa estereoscópica y se observó bajo el microscopio óptico a 400X. La presencia de formas flageladas, en el tracto digestivo de cada ejemplar, y su ubicación en diferentes porciones del tubo digestivo se anotaron para cada periodo de observación. El tracto digestivo de los insectos positivos, fue dilacerado en una lámina portaobjeto previamente cubierta con albúmina de huevo, sobre una gota de solución salina 0,85%. Una vez seca la preparación, se coloreó con Giemsa al 10% durante 30 min.
Las láminas se revisaron en microscopio óptico. Cada una de las formas parasitarias encontradas se dibujó con ayuda de una cámara clara sobre papel bond 22 X 22 cm. Se dibujaron 100 formas por período de observación y se clasificaron siguiendo la nomenclatura utilizada por Lawyers et al. (1990): amastigotas, procíclicos, nectomonas, haptomonas, paramastigotas y metacíclicos.
Resultados
La susceptibilidad de Lu. evansi a la infección por parásitos del complejo Le. mexicana varió entre 29,4% para Le. mexicana y 21,7% para Le. amazonensis, mostrando un patrón de desarrollo de tipo suprapilórico. Los resultados mostrados en este articulo están enfocados en la descripción de los cambios morfológicos y el curso de la infección de Le. mexicana y Le. amazonensis en el tracto digestivo de Lu. evansi cada 24 h durante siete días de observación.
Desarrollo de Leishmania mexicana en Lutzomyia evansi
A partir de las 24 h post-ingesta infectiva, el desarrollo de Le. mexicana en Lu. evansi estuvo caracterizado por la presencia de amastigotas en división y las primeras formas flageladas, procíclicos. Morfológicamente, las formas amastigotas presentaron cuerpos ovales de 5,9 ± 1 x 2,5 ± 0.5 µ, sin flagelo libre. A diferencia de éstas, los procíclicos mostraron cuerpos ligeramente alargados (6,8 ± 1,2 x 2,3 ± 0,5 μ) y flagelo (5,12 ± 4,0). Éstas correspondieron al 71% de las formas presentes a las 48 h post-infección (Fig. 1).
Avanzado el proceso de digestión sanguínea a las 72 h, momento en el cual los parásitos migran hacia el intestino medio toráxico y la válvula esofágica, se observaron formas de nectomonas. Éstas representaron el 93% de las formas presentes y se caracterizaron por poseer cuerpos alargados y flagelos libres, de igual o mayor longitud que los cuerpos. En promedio midieron 9,35 ± 2,2 x 2,1± 0,75 µ y flagelo de 13,5 ± 2,2. Al mismo tiempo se evidenció la presencia de haptomonas (7% de las formas observadas) (Fig. 1), con cuerpos similares a los procíclicos de 7,1± 1,5 x 2,4 ± 0,7 µ y flagelos de tamaño similar a los cuerpo 6,35 ± 2,4 μ.
Entre las 96 y 120 h post ingesta infectiva se inició la migración de los parásitos al esófago. En este periodo se observó un incremento de haptomonas (32,4% del total de formas observadas a las 120 h post-infección). El desarrollo hacia paramastigotas se observó entre las 120 y 144 h (3,4 y 1,9%, respectivamente) (Fig. 1), éstas se caracterizaron por poseer cinetoplasto yuxtapuesto al núcleo y sus cuerpos en promedio midieron 5,6 ± 1,1 x 2,9 ± 0,3 µ y los flagelos 11,3 ± 2,9 μ.
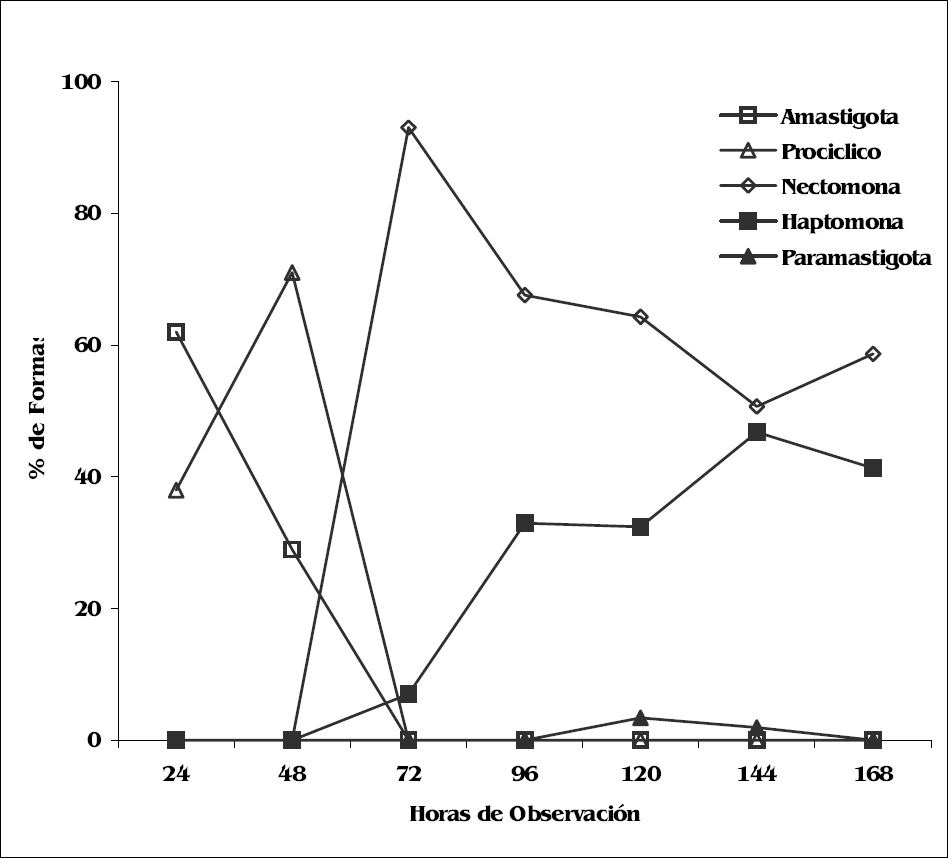
Desarrollo morfológico de Leishmania mexicana en Lutzomyia evansi durante 168 horas de observación, expresado en porcentaje de formas.
Al final del período (168 h post-ingesta) la población de promastigota de Le. mexicana, en el tracto digestivo del insecto, estuvo representada en su mayoría, por nectomonas (58,7%) y haptomonas (41,3%), sin la evidencia de paramastigotas.
Desarrollo de Leishmania amazonensis en Lutzomyia evansi
El desarrollo de Le. amazonensis en Lu. evansi mostró, en intestino medio abdominal, la presencia de amastigotas (con cuerpos de 6,6 ± 0,9 x 3,1 ± 0,6 μ) a las 24 h, y formas procíclicas (con cuerpos de 7,8 ± 1,5 x 3,8 ± 2,3 y flagelo de 5,33 ± 4,0 μ) a las 48 h, representando el 54,2 y 45,8%, respectivamente (Fig. 2).
La aparición de nectomonas (20%) se evidenció a las 48 h (Fig. 2). Éstas se visualizaron 24 h antes que para Le. mexicana (Fig. 1), mostraron cuerpos de 12,4 ± 2,1 x 1,9 ± 0,4 µ y flagelo de 15,6 ± 2,8. La nectomonas estuvieron presentes en el tracto digestivo de Lu. evansi durante los siete días de observación, en porcentajes mayores que los observados en infecciones con Le. mexicana.
El desarrollo de haptomonas de Le. amazonensis (con cuerpos de 9,2 ± 1,48 x 2,1 ± 0.5 μ y flagelo de 7,5 ± 2,3 μ), fue menor que el alcanzado por Le. mexicana para el mismo periodo de observación (144 h post-infección), siendo de 37,0 y 46,8%, respectivamente (Figs. 1 y 2).
La forma paramastigota con cuerpo de 8,8 x 3,5 µ y flagelo de 17,0 μ, se observó después de 120 h (1% de las formas presentes) (Fig. 2). En ninguno de los aislados se evidenció la forma metacíclica.
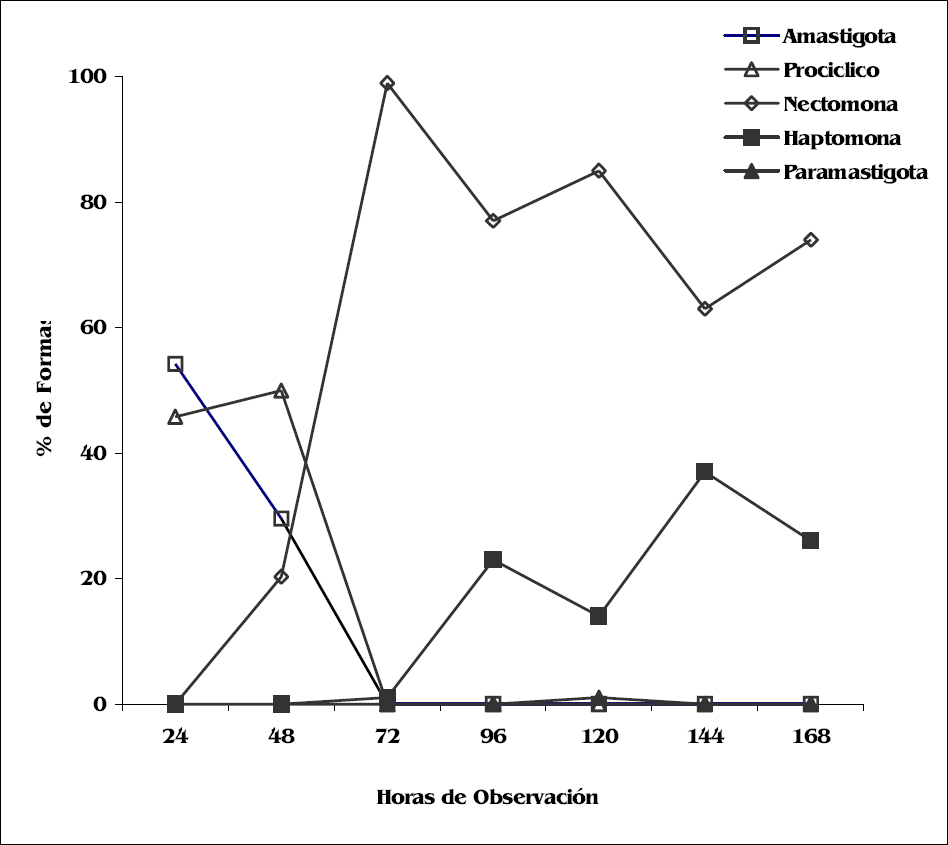
Desarrollo morfológico de Leishmania amazonensis en Lutzomyia evansi durante 168 horas de observación, expresado en porcentaje de formas.
Discusión
El patrón desarrollo de Le. mexicana y Le. amazonensis en Lu. evansi fue de tipo suprapilórico, tal como ha sido señalado para las especies del complejo Le. mexicana en sus vectores naturales (Lainson y Shaw 1987).
El predominio de amastigotas en división y las primeras formas flageladas o procíclicos, entre las 24 y 48 h post-ingesta infectiva, son indicativos de adaptación de los parásitos al microambiente intestinal. Según Pimenta et al. (1992), los procíclicos son una fase de promastigota, de baja infectividad al hospedador vertebrado, pero con capacidad de adhesión a las células epiteliales del intestino medio del flebotomo. La sobrevivencia y establecimiento de los flagelados en el tracto digestivo del insecto se garantiza por la acción de dos moléculas de superficie (glicoproteína Gp63 y los lipofosfoglicanos). La glicoproteína Gp63 interviene en la degradación de la membrana peritrófica, la regulación de enzimas proteolíticas en el intestino medio y la degradación de nutrientes, mientras que las moléculas de lipofosfoglicanos (LPG) sirven de anclaje al epitelio intestinal e impiden la eliminación de los parásitos durante el proceso de excreción (Pimenta et al. 1992, Ilgoutz y McConville 2001).
Las experiencias realizadas demuestran que ambas especies del complejo Le. mexicana fueron capaces de adaptarse a las diferentes regiones del tracto digestivo del insecto. Aunque en este trabajo no se determinó la unión de los flagelados al epitelio intestinal, su permanencia en el tracto digestivo, luego del proceso de excreción, puede considerarse como indicativo de este proceso.
Las formas nectomonas observadas entre 48 y 72 h y descritas como promastigotas de cuerpos alargados adheridos a la pared del intestino medio, sin modificación de su flagelo, constituyen las formas de sobrevida del parásito ya que éstas resisten a los movimientos peristálticos del intestino para evitar su eliminación durante el proceso de excreción (Molyneux y Killick-Kendrick 1987; Walters et al. 1993).
La colonización del cardias y válvula esofágica con formas nectomonas, inicia el proceso de transformación a haptomonas. Nieves (2000), al estudiar el desarrollo de Le. amazonensis en Lu. migonei señaló la aparición de un 25% de haptomonas a partir de las 48 h, incrementando la cifra progresivamente a partir de las 72 h post-ingesta infectiva. En Lu. evansi se observaron formas haptomonas a partir de las 72 h post-ingesta infectiva, alcanzando su máximo porcentaje a las 144 h. La invasión de estas formas, al cardias y válvula esofágica, ha sido descrita por varios autores y su adhesión a estos sitios se ha relacionado con los daños ocasionados por los parásitos a la íntima cuticular generando dificultad en el flujo de la sangre, durante la alimentación, lo cual favorecería la transmisión por reflujo de los parásitos ubicados en el intestino medio (Schlein et al. 1992).
Durante el desarrollo, fue notable, a partir de las 120 h post- ingesta infectiva, la presencia de flagelados con escasos movimientos. En algunos casos presentaron formas vacuoladas o lisadas. Walters et al. (1992), al respecto, señalan que tales efectos son observados en combinaciones parásito-vector con hospederos naturales y no naturales. Estas alteraciones son consideradas como indicadores de muerte natural de los flagelados, que persisten largo tiempo, luego de culminado el proceso digestivo. En el caso de Lu. evansi pudiera ser explicado por una disminución de nutrientes, entre las 72 y 96 h, al culminar el proceso digestivo (Oviedo et al. 1995).
La forma metacíclica, señalada como el estadio infectivo para vertebrados susceptibles, no fue observada en los ensayos realizados con las dos especies parasitarias. Hasta ahora los precursores de los metacíclicos infectivos se desconocen. Algunas observaciones han propuesto su origen a partir de paramastigota (Killick-Kendrick 1979), haptomonas (Lawyers et al. 1987) o nectomonas cortas presentes en el cardias (Walters et al. 1987). Observaciones realizadas por Nieves (2000), señalan que la aparición de metacíclicos coincide con la presencia de un número alto de nectomonas, y al mismo tiempo, con la aparición de paramastigotas.
Hart et al. (1981), en estudios in vitro, encontraron que la transformación de los diferentes morfotipos de Leishmania sp. se asocian con la presencia de ciertos nutrientes en el medio. En algunos casos, el proceso de transformación es considerado densodependiente del morfotipo precursor (Horward et al. 1987). En tal sentido, la disminución temprana de nutrientes y el escaso desarrollo de paramastigotas, por ambas especies de Leishmania, pudiesen ser la explicación para la ausencia de metacíclicos en el modelo estudiado.
Los resultados revelaron que Lu. evansi puede soportar el desarrollo de especies pertenecientes al complejo Le. mexicana, hasta la formación de paramastigotas, considerado precursor de la forma infectiva metacíclica.
Footnotes
Agradecimientos
A Gilberto Bastida por su colaboración durante las actividades de campo y a Alicia Jorquera, Leonardo De Sousa y Stefano Bonoli por la revisión y sugerencias hechas al manuscrito. Este trabajo fue soportado por FUNDACITE-Anzoátegui, Proyecto PI-008-02.
