Abstract
In alder, Alnus acuminata HBK, plantations of the río Blanco basin, near Manizales, Caldas, the attack of an insect that bores into the trunk and branches of these trees was recently detected. The insect makes holes and galleries especially in the trunk. This damage is associated with ambrosia fungi that cause wood rot and death of the tree. This work describes the biological stages, the damage, and the fungi associated with the borer especially after examination of trees with dry branches and poor foliage. Isolation of the fungus was made with samples obtained from the interior of the galleries and from lesions on the tree, including pathogenicity tests in the greenhouse. The insect was identified by Dr. Stephen L. Wood identified as a new species of Corthylus (Coleoptera: Scolytidae). The fungi associated with the interior of the galleries were identified as Fusarium solani, Fusarium sp., Verticillium sp. and a yeast similar to Pichia sp. Fusarium solani and Ceratocystis sp. were found in the lesion caused by the insect. Results showed that Corthylus n. sp., has a symbiotic association with several ambrosia fungi and one yeast. These fungi and yeast make the wood available to the insect, and this allows invasion of these organisms, finally causing the death of the tree. Additionally, the insect contributes to the dispersal of the fungi in the alder plantations. The pathogenicity tests with Ceratocystis sp., F. solani, and Fusarium sp., using trees of five months and four years old, were positive, showing establishment and progression of the lesion in the inoculated stem, reproducing the same symptoms observed in the field.
Introducción
El aliso, Alnus acuminata HBK, es un árbol nativo de las zonas altas de América tropi- cal, se encuentra distribuido desde México hasta el norte de Argentina. En Colombia crece entre los 1.700 y 3.300 msnm, en- contrándose naturalmente en las zonas de vida bosque húmedo montano bajo (bh- MB), bosque muy húmedo montano bajo (bmh - MB) y bosque pluvial o páramo pluvial montano (bp-M) en los departa- mentos de Caldas, Quindío y Risaralda, se adapta a temperaturas entre 8,5 y 18°C y precipitaciones anuales de 1.000 a 2.000 mm (Del Valle y González 1988). Este ár- bol es importante ya que suministra nitró- geno al suelo a través de bacterias nitrificantes, la hojarasca es de fácil des- composición con la consecuente produc- ción de materia orgánica, haciéndolo re-comendable para plantaciones protecto- ras y productoras -protectoras en cuencas hidrográficas (Muñoz 1971).
Recientemente las plantaciones de aliso localizadas en la cuenca de río Blanco, ubicada en el municipio de Manizales, Caldas, se han visto afectadas por un insecto barrenador de los troncos. Los ejemplares de este insecto, colectados en el interior de las galerías, se enviaron al Dr. Stephen L. Wood 5 , quien lo determinó como Corthylus n. sp. (Coleoptera: Scolytidae, Subfamilia: Scolytinae, Tribu: Corthylini), indicando que se trata de una nueva espe- cie. Réplicas de estos especímenes se en- cuentran en el Museo Entomológico “Marcial Benavides” de Cenicafé y también reposan ejemplares en el Life Sciences Museum, Brigham Young, University, Provo, EE.UU.
Comunicación personal. Dr. Stephen L. Wood, Brigham Young University, 290 MLBM, PROVO, UTAH 84602, USA., e-mail:
El daño producido por este insecto es considerable al causar una serie de orificios y galerías en el tronco. Asociado a este daño se observan hongos ambrosiales que causan pudrición de la madera y finalmente la muerte del árbol. Igualmente, estas galerías y orificios de penetración afectan la calidad de la madera.
En Colombia se han encontrado especies de Corthylus barrenando troncos y ramas de varias especies de guamo: Inga spectabilis Vahl, Inga edulis Mart, e Inga sp. Los estados causantes del daño son las larvas y los adultos (Posada 1989).
En México se registran varias especies de Corthylus: C. nudus Schedl atacando ár-boles de Alnus acuminata HBK, Casuarina equisetifolia L. ex J.R. & G. Forst., Populus balsamifera L., P. deltoides Bartr ex. Marsh y Salix babylonica L.; C. detrimentosus Schedi atacando Arbutos xalapensis H. B. K; C. fuscus Blandford en Amelanchier denticulata (H. B. K) Koch, Pyrus communis L. y Crataegus sp.; C. mexicanus Schedl en Malus sp. y Salix sp.; C. spinifer Schwarz en Persea americana Mill., Spondias mombin L., S. purpurea L. y Theobroma cacao L. (Cibrían et al. 1995). En Brasil se ha encontrado la especie C. convexicauda en plantaciones de Hevea brasiliensis (HBK.) Muell. y C. praealtus en Araucaria sp. (Cibrian et al. 1995).
En Norte América existen sólo tres especies: C. punctatissimus (Zimmerman), C. spinifer Schwarz y C. columbianus Hopkins. C. punctassimus ataca Acer saccharum en el sur de Ontario y Quebec; sin embargo, es plaga de muchos otros árboles forestales en el este de Estados Unidos. Su biolo- gía ha sido documentada por Finnegan (1967). Otra de estas especies, C. spinifer, se ha registrado en la Florida atacando plantaciones de Quercus sp. La especie C. columbianus, causa daños importantes en numerosas especies de madera dura en el este de Estados Unidos, su biología y asociación simbiótica con hongos ambrosiales ha sido estudiada en detalle por Kabir y Giese (1966a, 1966b) y Giese (1967).
La literatura indica que entre los insectos que revisten importancia económica en A. acuminata se encuentran defoliadores como: Nodonota irazuensis y Nodonota caparvula (Coleoptera: Chrysomelidae). Durante la estación seca se ha observado en Costa Rica un perforador del tronco Scolytodes alni Wood (Coleoptera: Scolytidae), este insecto causa los daños más severos en los fustes y ramas a nivel del líber (Arguedas et al. 1997). En Colombia se registran ataques de defoliadores del aliso en el departamento de Caldas. Bustillo y Villegas (1986a) hallaron el “picudito del aliso”, Bothynodontes sp. (Coleoptera: Curculionidae), defoliando árboles de tres años de edad en la cuenca de río Blanco. En otras zonas de Caldas también se registraron defoliaciones severas causadas por el medidor, Oxydia olivata (Dognin) (Lepidoptera: Geometridae); esta especie fue mantenida bajo control con la introducción del parásito de huevos, Telenomus alsophilae (Viereck) (Hymenoptera: Scelionidae) (Bustillo y Villegas 1986b).
Aunque no hay registros de ataques de coleópteros ambrosiales y de la corteza en plantaciones de aliso en Colombia, en los últimos años se ha observado un aumento de las poblaciones de esta especie de Scolytidae identificada como Corthylus n. sp., atacando árboles de distintas edades y de regeneración natural en la cuenca del río Blanco cerca a Manizales.
Los insectos de la familia Scolytidae constituyen un serio problema en forestales y frutales y son muy poco conocidos, especialmente por su tamaño pequeño (rara vez sobrepasan los 5 mm); además, pasan su vida dentro de ramas, troncos, peciolos de hojas, e incluso semillas. Construyen galerías de formas curiosas, tan características que por ellas se puede deducir la identidad de una tribu o género en particular. Su hábito barrenador es favorecido por la forma cilíndrica y alargada del cuerpo, así como por mandíbulas sumamente fuertes (Wood et al. 1991).
Otras de las características de esta familia es su ataque a una parte específica del hospedante. Algunas especies lo confinan a los conos o frutos de árboles, ramas delgadas, troncos pequeños, corteza, raíces o troncos recién caídos. Sin embargo, otras son muy agresivas y logran afectar tejido sano y vivo. Por lo general, los árboles que crecen en condiciones desfavorables, son más susceptibles al ataque de este grupo de barrenadores (Wood et al. 1992).
De acuerdo con el tipo de colonización, los Scolytidae se pueden agrupar en: espermófagos, se alimentan de semillas o de la cubierta más externa que las cubre; mielófagos, se alimentan de la médula de enredaderas; floeófagos, infestan el floema y xilomicetófagos, barrenadores de madera que tienen relaciones simbióticas con hongos del tipo “ambrosia”. Estos últimos representan el grupo más especializado en cuanto a selección del hospedante, debido a que inicialmente se alimentan de la madera y luego de las esporas de los hongos ambrosiales que crecen en las galerías hechas por el insecto adulto. Por lo tanto, la relación simbiótica hongo/insecto permite el desarrollo del hongo dentro de los orificios hechos en el árbol (Beaver 1989).
Estos hongos mutualistas los llevan los adultos de los insectos en invaginaciones de su integumento que se denominan micangias o micetangias, las cuales pueden tener gran variedad de formas y sirven para el almacenamiento, transporte y cultivo de estos hongos. Estas invaginaciones se pueden presentar en la cabeza, tórax ó en los élitros de estas especies de Scolytidae (Batra 1963; Francke-Grossmann 1963; Six y Paine 1996; Furniss et al. 1987). El hongo crece saprofíticamente en las galerías de cría que hacen en la madera y puede llegar a matar el árbol; sus esporas contaminan los adultos que emergen del árbol hospedero, para luego transmitirlas a árboles sanos.
La especie Corthylus columbianus Hopkins, plaga muy importante de muchos árboles forestales en el este de Estados Unidos, es un coleóptero ambrosial que se encuentra en simbiosis con varios hongos que lleva en su micangia y crecen en los túneles ó galerías que fabrica en los árboles, las larvas de este insecto se alimentan de estos hongos. El macho adulto inicia el ataque en los árboles y posee un par de micangias localizadas debajo del integumento del pronotum, una en cada lado de la región ventrolateral (Giese 1967). De estas micangias se lograron aislar y cultivar una levadura, Pichia sp. y los hongos Ceratocystis sp., Fusarium solani, F. tricinctum, F. oxysporum y Graphium sp. (Kabir y Giese 1966b).
Los hongos Ceratocystis y Fusarium se han encontrado asociados al ataque de muchos insectos ambrosiales especialmente de la familia Scolytidae, ocasionando marchitamientos, manchados vasculares y chancros, como es el caso de la muerte descendente en nogal negro Juglans nigra, enfermedad atribuida a Fusarium lateritium y F. oxysporum asociados al escarabajo ambrosial Xylosandrus germanus (Bonello et al. 2001). Fusarium circinatum en Pinus radiata, causa la enfermedad del chancro resinoso, donde se han identificado insectos vectores como escarabajos del género Pityophthorus (Coleoptera: Scolytidae), además las heridas hechas por el gorgojo Pissodes nemorensis y la polilla Rhyacionia subtropica ayudan al establecimiento del hongo porque las esporas presentes en el aire infectan las heridas frescas (Gordon et al. 2001). Morse y Blanchette (2002) mencionan a F. solani como el principal colonizador de heridas frescas en Acer negundo, más no como el agente causal del manchado rojo, por la inhabilidad del hongo para reproducir la lesión y atribuyen las áreas localizadas del manchado rojo frecuentemente encontra-das alrededor de la herida como producto de la oxidación de las células del árbol en donde se producen fenoles.
Krokene y Solheim (1998) confirman la asociación entre Ips typographus y Ceratocystis polonica en Picea abies, los cuales producen muerte de árboles por ataque en los haces vasculares y cambium, caracterizado por un manchado azul. Ceratocystis fimbriata en cacao, mango y eucalipto, presenta ataques asociados a insectos perforadores de la madera como Xyleborus sp., ocasionando muerte descendente en los árboles (Wingfield et al. 1993).
En este grupo de insectos, la habilidad para localizar un hospedante depende en gran medida de la capacidad de vuelo, en donde intervienen factores primarios en la atracción que ejercen sobre los organismos las oleoresinas, terpenos, alcoholes y otras sustancias emitidas por el tejido recién cortado o muerto (Wood et al. 1992). Por esta razón, el uso de trampas con alcoholes puede ser una herramienta promisoria para detectar su presencia y monitorear su abundancia a través del tiempo.
El objetivo de este trabajo fue describir los estados biológicos, el daño y los hongos ambrosiales asociados a la especie Corthylus n. sp., encontrada atacando plantaciones de aliso.
Materiales y Métodos
Este trabajo se realizó en la cuenca hidrográfica de río Blanco. Esta cuenca hace parte de la vertiente occidental de la cordillera central de los Andes colombianos, pertenece al municipio de Manizales y se encuentra a 3 km del casco urbano. Es una reserva natural protectora con gradientes altitudinales entre los 2.240 y los 3.790 m y una extensión de 4.343 ha. La pluviosidad promedio al año es de 2.500 mm y la temperatura promedio es de 11°C. La vegetación predominante son las plantaciones de aliso, que alternan con vegetación natural secundaria. En la reserva se tienen sembradas 795 ha de esta especie que ha sido establecida desde 1952, encontrando árboles de diferentes edades y de regeneración natural. Además, presenta abundante biodiversidad y es zona de protección de las fuentes hidrográficas que proporcionan el 30% del agua que utiliza el municipio de Manizales para suplir sus necesidades básicas.
Se realizaron cortes longitudinales utilizando una sierra sinfín para extraer los diferentes estados de los insectos y registrar el patrón de las galerías. Los estados inmaduros encontrados (larvas y pupas) se preservaron en una solución de alcohol al 70% más glicerina. Los adultos se dispusieron en alfileres entomológicos, parte de éstos se enviaron al Dr. Stephen L. Wood de la Universidad de Brigham Young, para la identificación de la especie y los ejemplares restantes se guardaron en el museo entomológico Marcial Benavides de Cenicafé. Los diversos estados del insecto y el daño causado se registraron fotográficamente. De igual manera, se colectaron otros insectos asociados a este árbol en las muestras analizadas.
Una parte de las muestras se dejó en cámara húmeda en condiciones de laboratorio y se observaron partes del tejido afectado en el estereoscopio y microscopio. Para el aislamiento de los hongos en medio de cultivo, se tomaron muestras de tallo (0,5 cm de longitud) del interior de las galerías y del avance de la lesión y se desinfestaron con hipoclorito de sodio al 0,05% y alcohol al 70% (sumergidos durante un minuto en cada solución), y luego se secaron las muestras con toallas de papel esterilizadas y se sembraron en cajas de Petri con PDA (Papa Dextrosa Agar + Tiamina 5 mg/l de medio), realizando repiques cada 5 - 6 días en PDA y Agar Extracto de Malta + Tiamina 5 mg/l de medio.
Una vez se obtuvieron los hongos purificados, se describió su morfología observando las estructuras en el microscopio y midiendo cada una de ellas con un micrómetro (25 mediciones en micras por cada estructura). La identificación del género de los hongos se hizo por comparación utilizando las claves de Barnett y Hunter (1998) y Hanlin (1990). Adicionalmente, se enviaron muestras al FABI (Forestry and Agricultural Biotechnology Institute) al estudiante de doctorado Mauricio Marín quien, mediante la secuenciación de microsatélites, identificó una de las especies de Fusarium encontrada tanto en las galerías como en el avance de la lesión y al Dr. Harry Evans del CABI Biosciences quién identificó el género Verticillium sp.
Se llevaron a cabo pruebas de patogenicidad en el invernadero y en el campo. En invernadero se utilizaron árboles de aliso de cinco meses de edad. Se realizaron dos tipos de inoculación, considerando que los hongos aislados están asociados a heridas hechas en el tallo por el insecto. Una herida en forma de U invertida a 20 cm del tallo con un bisturí desinfectado en alcohol al 90% y flameado, luego se inoculó una porción de 5 mmβ del crecimiento del hongo en medio de cultivo. La otra fue una punción en el tallo de 1 cm de profundidad hecha con una pinza estéril que se inoculó con una sus-pensión de esporas de cada hongo aislado. La concentración usada de F. solani fue de 2,3 x 106 microconidias/ml, de Fusarium sp. 2,5 x 106 microconidias/ml y de Ceratocystis sp. (anamorfo Chalara sp.) 1 x 106 conidias/ml. Luego, sobre las punciones y heridas, se proporcionó un ambiente húmedo con algodón y agua destilada estéril, sellado con “parafilm” durante 10 días. Como testigo se tuvieron cinco árboles, reemplazando el inóculo por agua destilada estéril. La evaluación de la infección se hizo 25 días después de la inoculación.
Para las pruebas de patogenicidad en el campo se utilizaron 10 árboles de cuatro años de edad, en los cuales se realizaron tres heridas en el tallo separadas por un metro de distancia de abajo hacia arriba. Las heridas se hicieron con un taladro desinfestado y flameado, luego se inocularon con una porción de 1 cmβ de crecimiento del hongo en medio de cultivo (AEM). También se dispuso una cámara húmeda que permaneció por 10 días. Se realizaron revisiones periódicas de las lesiones desarrolladas por cada uno de los hongos inoculados; sin embargo, la evaluación final se hizo a los 90 días después de la inoculación. Se tuvieron dos árboles testigo con tres heridas cada uno, reemplazando el inóculo por agua destilada estéril.
Resultados y Discusión
Identificación del insecto
En cuanto a la identificación de la especie causante del daño existía confusión ya que Cárdenas (2000) 6 , la identificó como Gnathotrichus sp. (Coleoptera: Scolytidae). Moreno y Blandón (2002) identificaron estos ejemplares como Amphicranus sp. (Coleoptera: Scolytidae: Subf: Ipinae). Sin embargo, cuando estos especímenes, colectados en río Blanco en trampas de alcohol, se enviaron al Dr. Wood, fueron identificados como una nueva especie de Corthylus. Los especímenes objeto del presente estudio no corresponden a los anteriores, de acuerdo con el Dr. Wood son diferentes y también los considera una nueva especie de Corthylus. El género Corthylus es muy numeroso y de distribución Neotropical, registrándose más de 60 especies, muchas producen ataques severos en árboles vivos durante varias generaciones sin matar el huésped.
Cárdenas M, R. 2000. Informe de la consultoría sobre un insecto que está atacando los alisos en la reserva de río Blanco. División de recursos naturales Aguas de Manizales, Manizales, Caldas 4 p.
Descripción del insecto
La larva es vermiforme, de color blanco, apoda y en forma de “C”, con las mandíbulas esclerotizadas, la sutura epicraneal es gruesa en la parte terminal (Fig. 1). Se encuentra en las cámaras de cría que se forman al converger las galerías transversales. La pupa es blanca cremosa, típicamente exarata, mostrando las partes típicas de un escolítido, el lado dorsal superior de la mandíbula está bien marcado pero se va perdiendo gradualmente con su desarrollo. El adulto mide 3,0 ± 0,1 mm de largo y 1,16 mm de ancho. El cuerpo es robusto, la cabeza y el tórax son de color marrón a negro y en la parte anterior de los élitros presentan una mancha de color marrón - amarillo, el resto es marrón - negro, en las áreas superior y lateral del pronoto presenta líneas de dientecillos (Fig. 2a y 2b). El declive de los élitros es levemente cóncavo y de color rojo obscuro y no presenta gránulos o protuberancias (Figs. 3b y 4b).
La especie presenta dimorfismo sexual; las hembras tienen la fachada cóncava con setas cortas y abundantes (Fig. 3a), la clava de la antena es muy larga, con el margen anterior ornamentado por un mechón de setas largas (Fig. 3c). El macho presenta la fachada convexa, sin setas (Fig. 4a), la porra de la antena no porta mechón de setas como lo descrito para la hembra (Fig. 4c).
El color de las patas es marrón-amarillo. El lado posterior de las tibias anteriores es engrosado y en el lado externo tiene más de dos dientes pequeños; lleva una espina en la base posterior de la tibia (Fig. 5).
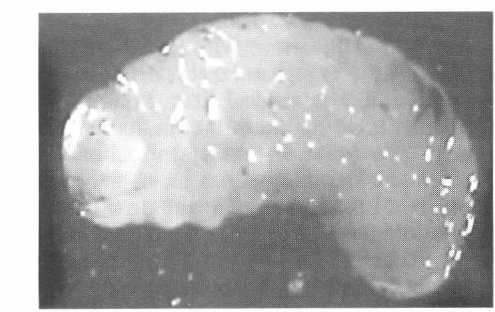
Larva de Corthylus n. sp.
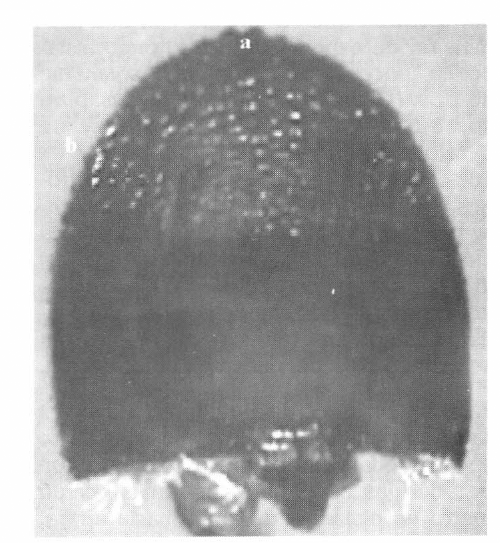
Pronoto de Corthylus n.sp. a. Dientecillos en el área superior. b. Líneas laterales de dientecillos.

Hembra de Corthylus n. sp. a. Fachada cóncava y con setas. b. Declive de los élitros levemente cóncavo c. Antena con la clava larga y el margen anterior ornamentado por un mechón de setas.

Macho de Corthylus n. sp. a. Fachada convexa y sin setas. b. Declive de los élitros levemente cóncavo. c. Margen anterior de la antena sin setas.
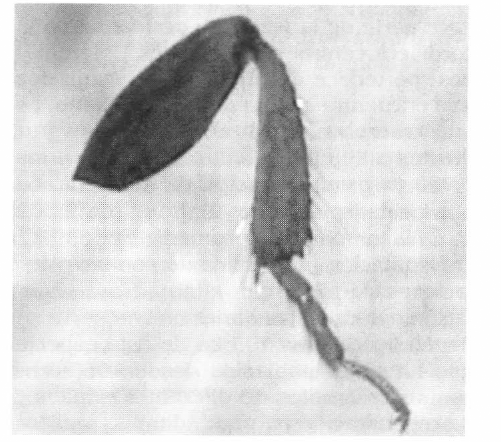
Pata anterior de Corthylus n. sp.
Signos de ataque
Los árboles infectados no se diferencian claramente de los sanos; sin embargo, existen evidencias en el tallo para detectar el ataque. En el árbol se observan orificios de entrada, y un exudado que se produce como reacción del árbol cuando el insecto realiza el orificio de penetración, además, ocurre una acumulación de aserrín blanquecino en la parte inferior del orificio de entrada.
Descripción del daño
El adulto realiza orificios de entrada redondeados de 2 mm de diámetro aproximadamente (Fig. 6a). La galería principal que hace el adulto se extiende en un plano horizontal, la cual se ramifica para crear las galerías de la progenie, las cuales pueden ser dos o tres perpendiculares al eje del tronco (Fig. 6b). Las galerías ramificadas convergen y forman cámaras, en éstas se observa mayor humedad y concentración de una masa negra, los huevos, larvas y pupas de Corthylus se encuentran en ellas. Los adultos emergen de las galerías realizadas por los padres.
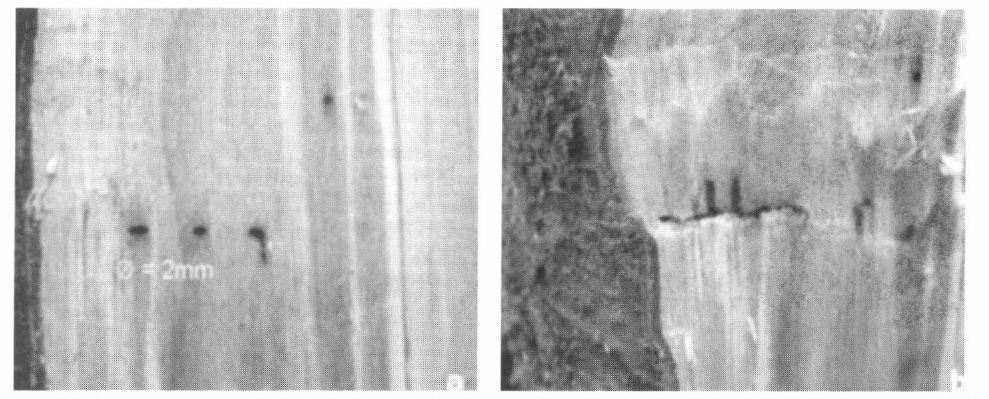
a. Orificios de entrada de Corthylus n. sp. b. Ramificación de la galería principal en dos o tres galerías perpendiculares al eje del tronco.
Importancia del daño
El insecto ataca el fuste de árboles vivos, de distintas edades y de regeneración natural. El daño mayor que causan es el manchado de la madera al introducir y transportar el hongo ambrosial que ocasiona la pudrición de la madera y finalmente la muerte del árbol (Fig. 7); en infestaciones severas los orificios y las galerías degradan la calidad de la madera.
Otros insectos asociados
Adicional a Corthylus n. sp., se registraron otros insectos asociados a estas plantaciones. Se encontró otra especie de Corthylus que de acuerdo con el Dr. Wood es diferente a la anterior y también es una nueva especie para la ciencia. También se observaron con frecuencia especímenes de Platypus sp. (Coleoptera: Platypodidae) en árboles en decadencia. Asociados a hongos de la familia Polyporaceae ubicados en la base del tallo de los árboles se registró una especie de Coleoptera de la familia Cisidae.
Identificación de los hongos fitopatógenos asociados al daño
Del interior de la galería del insecto se aislaron tres especies de hongos: Fusarium solani 7 , Fusarium sp. y Verticillium sp. 8 , además, una levadura que de acuerdo con la morfología se asemeja a Pichia sp. (Kabir y Giese 1966b). En el avance de la lesión se aislaron F. solani y Ceratocystis sp. (Fig. 8).
Identificada por Mauricio Marín, estudiante de doctorado Universidad de Pretoria, Pretoria, Sudáfrica FABI (Forestry and Agricultural Biotechnology Institute), mediante la secuenciación de microsatélites
Identificada por el Dr. Harry Evans. Research Group Co-ordinator. Biological Control of Weeds and Plant Diseases. CABI Biosciences (Ascot). Silwood Park Ascot, UK.
La especie F. solani, (teleomorfo Nectria haematococca) presenta crecimiento rápido en medio PDA 3,53 mm/día, la colonia es de color crema a blanco de aspecto algodonoso, el reverso es color crema cla-ro. Produce abundantes microconidias unicelulares, hialinas, de forma ovalada y cilíndrica de 11 x 5 µm en microconidió-foros ramificados con fiálidas simples que nacen en la parte lateral de la hifa; posee macroconidias multicelulares (3 - 5 tabiques), hialinas, en forma de canoa o curvadas, de 19 x 5 µm, con célula apical corta y redondeada y célula basal redondeada que termina en forma de pie, producidas en conidióforos cortos y ramificados. Las clamidosporas son globosas de pared celular lisa, de 5,2 x 5 µm, se observan en forma individual o en cadenas terminales cortas.
Fusarium sp. presenta un crecimiento de 3,53 mm/día, la coloración de la colonia en medio PDA es de color rojizo claro la que al cabo de 20 días se torna más intensa, además de percibirse un olor a levadura en el cultivo. Sus microconidias son hialinas, bicelulares, elipsoidales de un tamaño aproximado de 8,3 x 4,8 µm, son producidas en fialidas simples, conidióforos ramificados y pocas veces simples. Las macroconidias son menos frecuentes en forma de media luna con 3-5 septos, de 19 x 5 µm, producidas en esporodoquios laterales a la hifa. Las clamidosporas son globosas de 6 x 4,5 µm y de pared lisa.
Del hongo Ceratocystis sp. sólo se logró purificar su estado anamorfo Chalara sp. La colonia en el medio agar extracto de malta, es de color gris oscuro de crecimiento lento 1,38 mm/día, se percibe en la colonia un olor a fruta (banano). El micelio es septado, de color oscuro, produce conidias hialinas (endoconidias) de 22 x 5,3 µm en conidióforos con fialidas simples. Posee clamidosporas en cadenas o individuales, de 15 x 12 µm. El estado teleomorfo presenta peritecios globosos de color negro o marrón oscuro de cuello largo, la base del peritecio mide alrededor de 172 (largo) x 115 µm (ancho), con un cuello de 600 µm. Las ascosporas son hialinas, en forma de sombrero, de 7 x 5 µm, que son expulsadas en una masa mucilaginosa a través del cuello del peritecio (Fig. 9).
Verticillium sp. presenta un crecimiento lento tanto en el medio de cultivo SDA como PDA. La colonia inicialmente es de color blanco y se va tornando crema a medida que crece en tamaño; cuando empieza a producir esporas el aspecto es algodonoso y toma tonalidades amarillas. El reverso de la colonia va desde colores pálidos a amarillo profundo. Produce abundantes conidias unicelulares, hialinas, con formas cilíndricas que miden entre 3 y 6 µm y formas ovaladas que miden entre 3 x 7,5 µm hasta 6 x 10,5 µm y se observan agrupaciones de conidias muy características de este género. Las hifas son hialinas, delicadas, de tamaño variable de las que se desprenden de dos a tres fialidas que representan su forma verticilada. No se observaron clamidosporas.

Aspectos generales de la plantación de aliso a. Plantación de Alnus acuminata. b. Árbol con inicio de síntomas. c. Árboles marchitos y defoliados d. Árboles descopados por el viento.
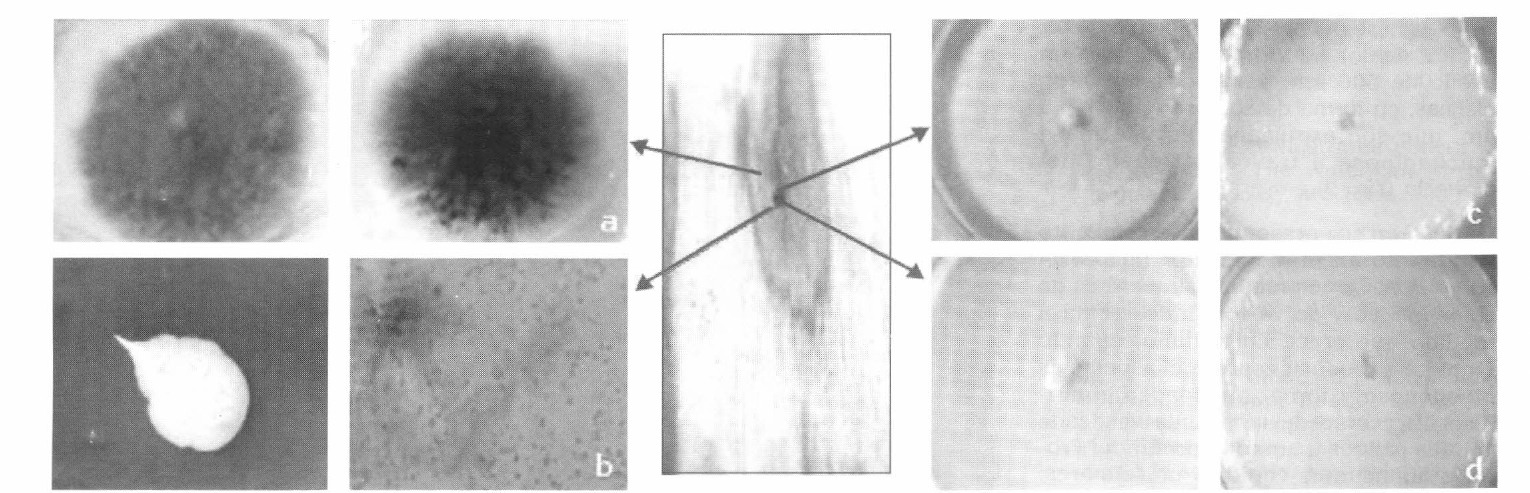
Hongos aislados de las galerías ocasionadas por Corthylus n. sp. en el tallo de aliso a. Ceratocystis sp. (anamorfo Chalara sp.) aislado del avance de la lesión. b. Levadura Pichia sp. aislada del interior de la galería c. Fusarium solani aislado del interior de la galería y avance de la lesión. d. Fusarium sp. aislado del interior de la galería.
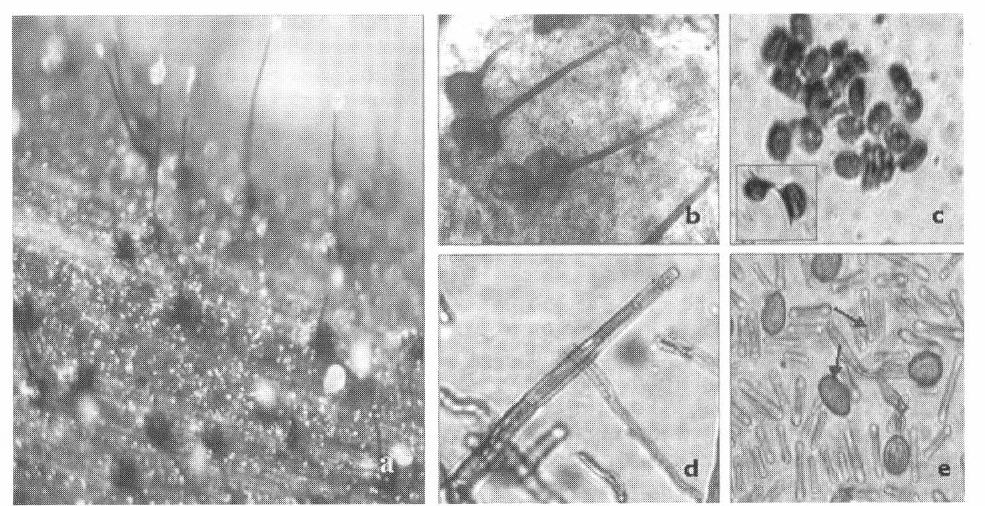
a. Peritecios de Ceratocystis sp. sobre el tejido afecado. b. Peritecios. c. Ascosporas. d. Conidióforo del estado anamorfo Chalara sp. e. Conidias y clamidosporas.
Lesiones causadas por los hongos
La levadura registrada que se asemeja a Pichia sp. presenta un crecimiento lento en los medios de cultivo SDA y PDA, el aspecto de la colonia es cremoso y de forma irregular. Las esporas varían en tamaño desde 3 hasta 9 µm.
Se encontraron tres tipos de lesiones en el tallo relacionados con la herida hecha por el insecto, un manchado de color marrón rojizo que avanza longitudinalmente de acuerdo con la galería, afectando los haces vasculares y las células del parénquima. Esta lesión fue la más frecuente en el campo, de la cual se aislaron las dos especies de Fusarium y Ceratocystis sp. Una lesión de color marrón que afecta directamente tejidos del parénquima en la albura del tronco y otra lesión en forma de rayado en el xilema. De estas dos últimas lesiones se aisló solamente Ceratocystis sp. (Fig. 10a, 10b y 10c). Es importante anotar que no se observaron otras especies de árboles con esta última sintomatología.
Las pruebas de patogenicidad de los hongos asociados a Corthylus n. sp. en el invernadero mostraron un establecimiento y avance superficial, observándose el manchado encontrado en el campo; solo en el 40% de los árboles inoculados con Fusarium solani se logró obtener avance de la lesión hacia el interior de la herida, esto señala que existe una estrecha relación entre el insecto y el hongo o que existen otros factores que intervienen en el establecimiento del hongo en la galería. La herida del testigo no presentó manchado, y comenzó a cicatrizar. Los hongos inoculados fueron reaislados y repicados en medio de cultivo PDA Y AEM.
Al realizar las pruebas de patogenicidad en el campo se obtuvo el establecimiento de los patógenos y el desarrollo de las lesiones características de cada hongo. Las especies de Fusarium desarrollaron lesiones superficiales de color rojizo con avance longitudinal (Fig. 11).
Las lesiones características de Ceratocystis sp. fueron de color marrón oscuro o gris, con avance longitudinal de 38 - 55 cm a los 45 ddi; sin embargo, a los 90 días despues de la inoculación, la infección de este hongo fue la única que avanzó en forma transversal en el tallo afectando el xilema y el cambium, replicando las lesiones más frecuentes encontradadas en el campo; señalando así que el ataque de Corthylus n. sp. en asociación con el hongo Ceratocystis sp. ocasiona la marchitez y muerte del árbol. Esto concuerda con la biología y comportamiento de este hongo registrados en otras especies forestales. Se considera que el insecto es un medio importante de dispersión de este patógeno; sin embargo, es necesario determinar la relación del hongo y el insecto y las condiciones para que el patógeno finalmente provoque la muerte del árbol. Los hongos del género Fusarium son invasores secundarios.
Los signos del ataque y el comportamiento de Corthylus n. sp., son muy similares a los registrados por Kabir y Giese (1966a) para Corthylus columbianus en Norte América. Ellos también registraron los hongos Ceratocystis sp., F. solani y Fusarium sp. y una levadura del género Pichia, asociadas a las galerías realizadas por este insecto.
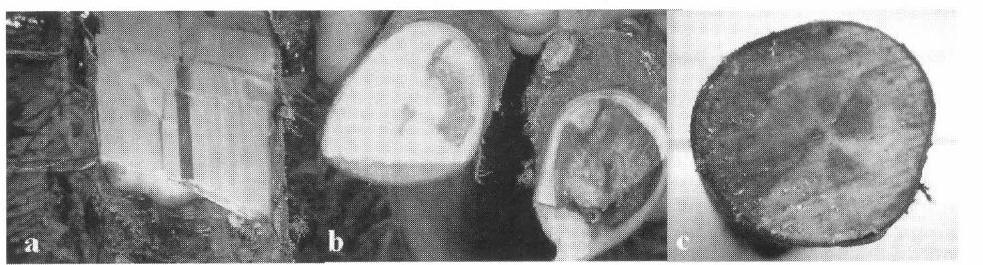
Manchado de la madera producida por el hongo ambrosial. a. Manchado de color café rojizo que avanza longitudinalmente de acuerdo con la galería. b. Lesión de color café que afecta directamente tejidos del parénquima en la albura del tronco. c. Lesión en forma de rayado en el xilema. Cortesía Dr. Ben Chang.
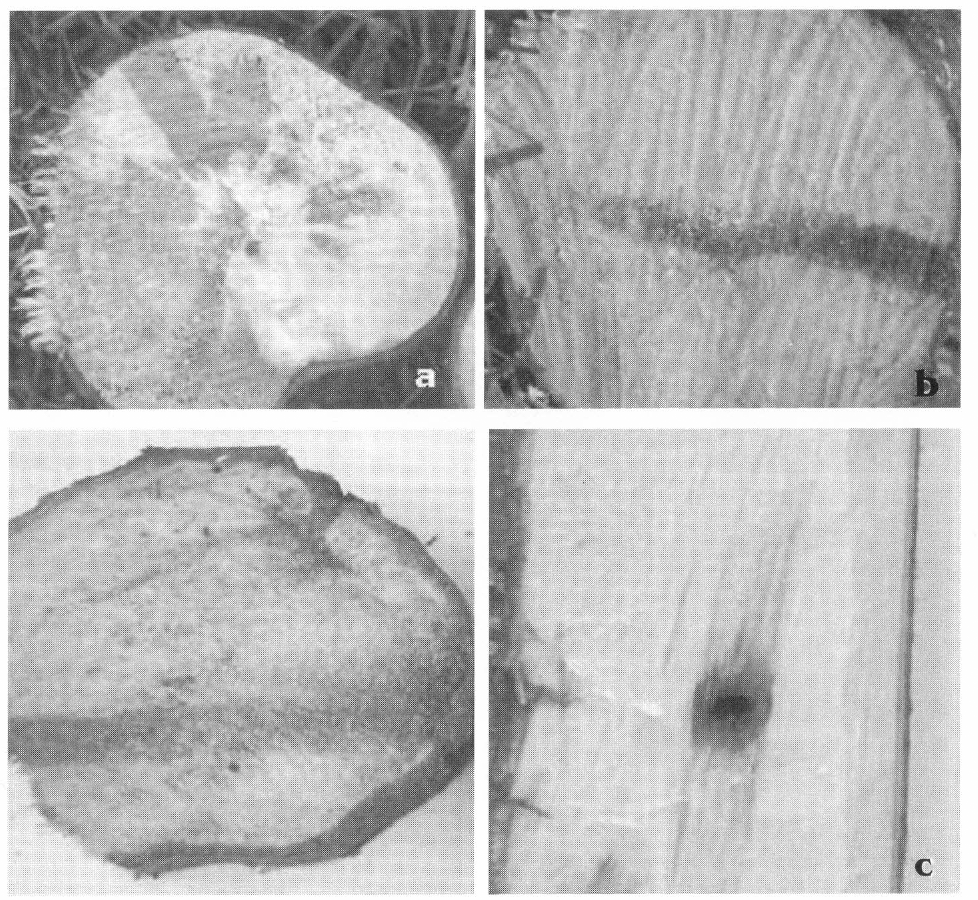
Prueba de patogenicidad. a. Infección con Ceratocystis sp. a los 90 días después de la inoculación. b. Infección desarrollada por Fusarium solani y Fusarium sp. c. Testigo (herida).
Conclusiones
Las observaciones de campo y de laboratorio constataron la presencia de una nueva especie de Corthylus atacando las plantaciones de aliso en la reserva forestal de río Blanco. Estos insectos están asociados en simbiosis con varios hongos como F. solani, Fusarium sp. y Ceratocystis sp. y una levadura. Los hongos y la levadura permiten la supervivencia del insecto y éstos, a su vez, colaboran con la invasión de los hongos, causando finalmente la muerte del árbol.
Es importante continuar estudios para determinar la posible presencia de estructuras especializadas como la micangia en estos insectos, para el transporte y diseminación de los hongos. También se hace necesario adelantar estudios sobre el impacto del insecto en esta reserva y desarrollar estrategias de manejo silvicultural que reduzcan la incidencia de la plaga y eviten el deterioro de la cuenca de río Blanco.
Footnotes
Agradecimientos
Los autores expresan sus agradecimientos al Dr. Stephen L. Wood especialista en la familia Scolytidae y profesor emérito de la Universidad de Brigham Young (Provo, EE.UU), por la identificación de las especies. Al Dr. Harry Evans por la asistencia en la identificación de los hongos. A Aguas de Manizales por la colaboración en la ejecución del trabajo. A Cenicafé por proporcionar el tiempo de sus investigadores y de su infraestructura de laboratorios para llevar a cabo esta investigación.
