Abstract
Soldiers of Nasutitermes sp., pests of Cordia alliodora (Ruiz & Pav.) Oken, family Boraginaceae, a tree of great economic and medicinal importance were inoculated in vitro with the fungus Metarhizium anisopliae (Metsch.) Sor. impregnated on canvases or filter paper at a concentration of 1x107 conidias/ml. Observations on the development of the fungal infection were made with a light microscope. The development of the fungus was observed on mounted slides with lactofenol blue, using a clarifying technique with KOH solutions at 5, 10, 15 and 20%. Infected termites died 1 to 3 days post-inoculation, the fungus penetrating the cuticle at 24 hours, colonizing the fat tissue at 72 hours and invading the internal organs (gut) after 72 hours of infection. At 120 hours a white compact mass of conidiophores began to emerge from the cuticle at the intersegmental regions of the ventral surface (legs, thorax) and mouthparts of the insects. After 144 hours of inoculation the mycelia changed to green, and at 192 hours the mycelia turned dark and powdery when the termite body was totally invaded.
Introducción
Las termitas se consideran como los insectos más nocivos y destructores en las zonas templadas y tropicales. Atacan la madera, construcciones, plásticos, textiles, cauchos, cultivos agrícolas y forestales (Garcés 1997; Harris 1971).
En el bosque tropical, la mayoría de las termitas que se han encontrado, pertenecen a las familias Kalotermitidae, Rhinotermitidae o Termitidae, de las cuales la subfamilia Nasutitermitinae representa más del 50% de las especies, siendo el género Nasutitermes el más abundante (Martius 1994). En Colombia se han registrado las tres familias mencionadas.
Nasutitermes spp., exopterigotas Neoptera son insectos sociales, representados en numerosos obreros y soldados no alados (Watson y Gay 1991; Borror et al. 1989). Atacan los árboles del nogal cafetero Cordia alliodora (Ruiz & Pav.) Oken de la familia Boraginaceae, que son de gran importancia económica y médica (Varón y Morales 1997).
Muchos autores han utilizado diferentes organismos en el control biológico de las termitas, como el virus de la polyhedrosis nuclear de Spodoptera littoralis (Hassan 1990), bacterias como Bacillus thuringiensis (Gavino 1984; Logan et al. 1990), nemátodos de la familia Steinernematidae y del género Steinernema carpocapsae (Coppel y Liang 1987; Mix y Beal 1985). Así mismo, han sido probados con notable éxito los hongos Beauveria bassiana y Metarhizium anisopliae (Yendol y Paschke 1965; Zoberi y Grace 1990; Sajap y Kaur 1990; Zoberi 1995; Alves et al. 1995; Milner et al. 1998; Delate et al. 1995).
Los hongos son uno de los agentes más promisorios para el uso como insecticidas biológicos (Milner y Staples 1996). Entre los hongos probados como agentes de control biológico en termitas están Aspergillus flavus, Entomophthora, Aspergillus sp. y Penicillium sp. (Espero 1984; L[j]utikova 1990). Además se utilizaron para controlar poblaciones de Stromatium fulvum (Villers) (Coleoptera: Cerambycidae) en plantaciones de Casuarina en Egipto (Hassan 1990). Igualmente M. anisopliae, Aspergillus fumigatus, Paecilomyces fumosoroseus y P. cicadae presentaron alta infectividad en termitas Coptotermes formosanus (Shiraki) bajo condiciones de laboratorio al aplicar suspensiones acuosas de 6,0 x 107 conidios/ ml a una termita cebo (Chai 1995). Conidiobolus coronatus produjo una mortalidad del 100% sobre esta misma especie de termita después de dos días de aplicación (Wells et al. 1995). Por otro lado, se comprobó que el ascomycete Cordycepiodeus es patógeno para las termitas Macrotermes subhyalinus (Rambur) que construyen montículos en Kenya (Ochiel et al. 1997).
Estudios en Australia demostraron que ciertos aislamientos de M. anisopliae pueden ser aplicados para matar colonias de termitas en termiteros, árboles y montículos. El método consiste en capturar termitas, infestarlas con el patógeno y reintroducirlas al termitero para iniciar el contagio entre ellas (Milner y Staples 1996; Berón 1983). Ensayos in vitro para probar la patogenicidad de este hongo en termitas Microcerotermes en diferentes concentraciones demostraron que produce una mortalidad del 51% a una concentración de 1 x 107 conidios/ml y del 80-100% por encima de dicha concentración (Zuluaga 2002).
M. anisopliae (Metsch.) Sor. es un hongo anamórfico (Kirk et al. 2001) aislado del escarabajo Anisoplia austriaca por Metchnikoff en 1879 y produce la muscardina verde en los insectos, por lo cual dicho hongo ha sido utilizado como agente microbiano contra insectos plaga (Tanada y Kaya 1993; Zimmermann, 1993; Steinhaus 1949). Es un hongo cosmopolita, saprófito, parásito de insectos, con un amplio rango de hospederos, que puede identificarse fácilmente por sus conidióforos ramificados y por sus conidios cilíndricos verdes, los cuales forman una capa densa y compacta. En el inicio del crecimiento las colonias presentan una coloración blanca y las colonias maduras se tornan amarillentas, verde oliváceas, verde oscuras y crema rosáceas o vináceas (Humber 1997; Tanada y Kaya 1993; Barnett 1967).
M. anisopliae posee dos variedades que se diferencian principalmente por el tamaño de sus conidios: la variedad más común anisopliae de conidios pequeños (3,5-9,0 µm) y la variedad major de conidios grandes (9,0-18 µm) (Kirk et al. 2001; Domsch et al. 1980). Este hongo crece fácilmente en medios sintéticos sólidos y líquidos, su temperatura óptima de crecimiento oscila entre 25-30°C y sus conidios pueden sobrevivir liofilizados hasta por 16 años (Tanada y Kaya 1993; Samson 1981; Steinhaus 1949). Produce metabolitos secundarios como destruxinas A, B, C, D, E y una desmetildestruxina B, los cuales son tóxicos y actúan como micotoxinas. Su toxicidad se da por la ingestión y a través del integumento y su efecto varía según la especie de insecto atacado, pudiendo causar parálisis tetánica y flácida in vivo, despolarizando membranas musculares al activar los canales de calcio; afecta varias organelas celulares (mitocondrias, retículos endoplasmáticos y membranas nucleares), paraliza células y causa disfunción del intestino medio, los túbulos de malpigio y los hemocitos. También ejercen una acción inmunodepresora en el insecto e inhiben la encapsulación multicelular del hongo (Aldana 1998; Tanada y Kaya 1993; Burges y Hussey 1971).
Entre los mecanismos de invasión de los hongos entomopatógenos están el de ingestión y el de contacto a través de la cutícula, siendo el más frecuente el de contacto. En éste, el hongo penetra la cutícula del insecto y llega al hemocele, donde libera una serie de metabolitos tóxicos que inhiben el sistema inmune del insecto, el cual finalmente muere debido a los daños mecánicos y fisiológicos sufridos (Boucias y Pendland 1988, 1991; Tanada y Kaya 1993; Aldana 1998). Por ingestión, el hongo ingresa por las partes bucales y el intestino, siendo estos canales alimentarios inhospitalarios a la penetración del hongo debido a los efectos de anaerobiosis, enzimas digestivas, pH adverso, velocidad del alimento y e! papel protector de la membrana peritrófica (Dillon y Charnley 1986).
La ontogenia del hongo M. anisopliae se observó mediante estudios histológicos en obreros de Coptotermes curvignatthus Holmgr. en Malasia (Sajap y Kaur 1990). Igualmente se realizaron estudios de infección bucal y a través del tracto digestivo por el hongo M. anisopliae de la langosta Schistocerca gregaria Forsk (Dillon y Charnley 1986).
El objetivo de este estudio fue evaluar el mecanismo de acción de M. anisopliae sobre los soldados y obreros de Nasutitermes sp. mediante la técnica de aclaramiento con hidróxido de potasio.
Materiales y Métodos
Área de estudio
Se realizaron cuatro colecciones de termitas en la quebrada la Volcana (Loma de los Balsos) sector del Poblado al sureste de Medellín, Antioquia (Colombia) caracterizada por presentar una zona de vida clasificada como bosque húmedo premontano (bh-P) con temperatura promedio de 20°C, precipitación media anual de 1.000-2.000 mm y una faja altitudinal de 1.450 msnm (Espinal 1990).
Colección y mantenimiento de las termitas
Las termitas Nasutitermes sp. se colectaron en un tronco de un árbol que pertenece al género Cordia (Familia: Boraginaceae). Se capturaron termitas de diferentes castas (soldados y obreros) realizando incisiones en el termitero y/o colectando trozos de madera del árbol. Las temitas se introdujeron, utilizando pincel, en recipientes plásticos o de vidrio a los cuales previamente se les adicionaron los sustratos provenientes del termitero y se cubrieron con vinilpel durante el transporte hacia el laboratorio.
Para la reproducción en el laboratorio se utilizaron recipientes de fibra de vidrio moldeado de 20 x 25 cm de diámetro; a los recipientes se les agregó una capa de grava gruesa 2 cm de espesor, seguida de una capa de grava fina del mismo espesor, finalmente una capa de 10 cm de tierra del mismo termitero con arena fina (25% en volumen) (Norme Française 1990). Estos recipientes se cubrieron con muselina; los bordes del recipiente se impregnaron con vaselina para evitar el escape de las termitas.
Las colonias se mantuvieron en oscuridad, con circulación de aire y a una temperatura de 26°C ± 2°C y 75% de humedad relativa. La humedad de la tierra, la temperatura y la humedad relativa dentro del termitero se controlaron diariamente (Norme Française 1990).
Cultivo del hongo
La cepa del hongo M. anisopliae (Ma 45), aislada de un coleóptero (de una subfamilia de la familia Melolonthidae) fue donada por CORPOICA (Corporación Colombiana de Investigación Agropecuaria). El hongo se cultivó en tubos y cajas de Petri con medio Agar Sabouraud Dextrosa (SDA) (Oxoid LTD., Basingstoke, Hampshire, England) a temperatura ambiente (21-26°C), durante 10-12 días y se almacenó a 4°C. La cepa se replicó cada quince días en SDA y se observaron los conidios y el micelio al microscopio (Aldana 1998; Zoberi y Grace 1990).
Pruebas de patogenicidad
Para las pruebas de patogenicidad se utilizaron más termitas soldados que obreros por ser la casta más numerosa dentro de la colonia estudiada. A partir de una solución madre de conidios obtenida de los cultivos del hongo se impregnaron durante 5 min, 10 lonas y 10 papeles de filtro circulares de 100 x 15 mm con una concentración de 1 x 107 conidios/ml. Las lonas y los papeles de filtro impregnados se introdujeron en frascos medianos que contenían sustrato proveniente del termitero y se adicionaron 5 termitas soldados (de 4 mm) y un obrero (de 3 mm de longitud) y se cubrieron con muselina. La supervivencia de las termitas se verificó diariamente durante ocho días. Como testigos se utilizaron lona y papel de filtro impregnados con agua destilada estéril. Estos ensayos se realizaron por triplicado.
Durante los ensayos se controlaron diariamente las condiciones de oscuridad, temperatura y humedad relativa y se verificó la actividad de las termitas.
En total, en los ensayos, se utilizaron 150 termitas soldados con el inóculo impregnado en el papel de filtro, 150 con el inóculo impregnado en lonas y 100 en cada testigo. Se trataron 30 obreros en cada inóculo y 10 en cada testigo.
Para observar la penetración del hongo en el insecto, se realizó la técnica de aclaramiento de la termita descrita por Stehr (1987), utilizando soluciones de KOH al 5, 10, 15 y 20% a diferentes tiempos (24, 48 y 72 h) de exposición. Luego, los insectos se sumergieron en una solución agua: alcohol (1:3v/v) y después en fenol puro. Posteriormente, se realizaron preparaciones del insecto en portaobjetos que se tiñeron con azul de lactofenol para observar hifas y esporas en las partes internas del cuerpo de la termita.
Micosis
Para evaluar el desarrollo del hongo y la presencia de daños en las termitas se colocaron los soldados muertos y obreros, en cajas de Petri estériles, con papel de filtro Whatman N° 1 húmedo, estéril y se observó la aparición de micelio durante ocho días.
Análisis estadístico
La mortalidad para los cuatro tratamientos (hongo en papel de filtro y en lona y agua destilada en papel de filtro y en lona) se comparó en cada día utilizando la prueba de homogeneidad de proporciones, la cual se realizó en el paquete estadístico Statxact 4.0.1 (Cytel Software Corporation, Cambridge, Ma).
Resultados y Discusión
El porcentaje de mortalidad de los soldados fue diferente tanto entre los tratamientos como entre los días. En efecto, la mortalidad en el primer día fue mayor cuando se usó agua destilada en papel de filtro (46%). En el segundo día la mortalidad mayor (82%) se presentó empleando el papel de filtro impregnado con el Metarhizium anisopliae mientras que la lona con el hongo resultó eficaz sólo al tercer día (Tabla 1). En la tabla 2 se presentan los porcentajes de mortalidad para los obreros. No se encontraron diferencias entre tratamientos en ninguno de los tres días. Se observó también que el porcentaje mayor de mortalidad ocurrió en el segundo día para todos los tratamientos. La comparación entre tratamientos se realizó para cada día, tanto para los soldados como para los obreros, según la metodología de Snedecor y Cochran 1978.
Mortalidad de los soldados Nasutitermes sp. con el hongo Metarhizium anisopliae según el tratamiento aplicado (porcentaje)
Mortalidad de los obreros Nasutitermes sp. con el hongo Metarhizium anisopliae según el tratamiento aplicado (porcentaje)
Las termitas obreros y soldados presentaron mortalidad al segundo día debido a la acción del hongo M. anisopliae, que se observó mediante la técnica de aclaración en KOH (10 y 15%) dentro el cuerpo de éstos, resultados que concuerdan con los estudios realizados por Sajap y kajur (1990); Milner et al. (1998) y Delate et al. (1995). Igualmente, los testigos presentaron mortalidad debido a factores como: la fragilidad natural (no permite ser sometidos a técnicas de asepsia en el laboratorio antes de los bioensayos) y a contaminantes naturales como Aspergillus flavus y Serratia marcescens (entomopatógenos) que habitan en su mismo nicho ecológico (Steinhaus 1949; Tanada y Kaya 1993; Martius 1998). Así mismo, los testigos se sometieron a la técnica de aclaración en КОН (10 у 15%) y no mostraron invasión en sus tejidos por el hongo M. anisopliae.
En cuanto a la forma de invasión del hongo M. anisopliae en las termitas, a las 24 h post-inóculo los conidios se observaron sobre la cutícula, superpuestos y estrechamente unidos a las setas y poros de las setas (Fig. 1), en las patas, en el fémur y tibia; tibia y tarsómeros, uñas tarsales y tergitos abdominales. Luego, éstos formaron tubos germinales continuando su crecimiento. Esto concuerda con los estudios realizados por Boucias y Pendland (1988) con M. anisopliae y B. bassiana donde se demostró que la topografía y propiedades químicas de la epicutícula facilitan la adhesión conidial y la orientación del tubo germinal, encontrando que los conidios de estos hongos tienen preferencia por toda la región del cuerpo del insecto y la superficie de la cutícula que contiene espinas cuticulares cortas.
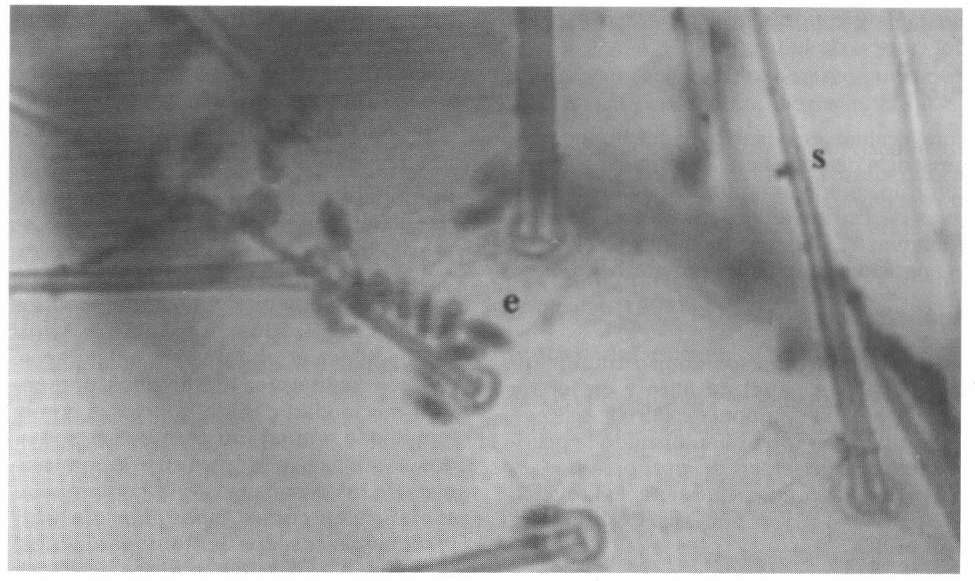
Esporas de M. anisopliae sobre la cutícula de soldados Nasutitermes sp. e: esporas. s: setas. 100X.
Además, la forma de invasión, iniciando en la cutícula, concuerda con los resultados descritos por Sajap y Kaur (1990) y Quarles y Bucks (1995) quienes realizaron ensayos en termitas Coptotermes curvignathus donde los conidios de M. anisopliae germinaron sobre la cutícula y el tubo germinal penetró dentro de la cutícula a las 24 h post-inoculación y luego en el exoesqueleto.
La interacción conidio-cutícula (unión de los carbohidratos del hongo M. anisopliae y las proteínas de la cutícula del insecto) no ha sido totalmente esclarecida (Latge et al. 1988).
Los tubos germinales formados por micopatógenos en artrópodos producen células apresoriales que secretan sustancias mucilaginosas y exoenzimas que ayudan a la penetración del hongo a través de la cutícula del insecto (Zacharuk (1970b); Schabel (1978); Travland (1979); Fargues (1984); Charnley (1984); Persson et al. 1984; St. Leger et al. 1986; Murrin y Nolan (1987); St. Leger et al. (1989a y b); sin embargo, dicha estructura no se observó en este estudio.
McCauley et al. (1968) y Zacharuck (1970a) observaron que los conidios de M. anisopliae se pueden unir a toda la superficie cuticular, remover fácilmente y permanecer unidos a la epicutícula asociada con pliegues protegidos. Sólo algunos micopatógenos terrestres reconocen específicamente la cutícula hospedante. Además, se encontró que los conidios de un linaje de M. anisopliae aislados del Scarabaeido (Scarab) Cetonia aurata se unen fácilmente a la cutícula de C. aurata, pero no a las larvas del Scarab Oryctes rhinoceros (Fargues 1984). En este estudio se observó claramente que los conidios de M. anisopliae se unen a la cutícula de Nasutitermes sp. (Fig. 1).
Una vez que los conidios llegan al interior de la cavidad del cuerpo, el hongo crece y mata el insecto. Aunque se ha observado que a las 48 h post-inoculación los cuerpos hifales son abundantes en el hemocele de las termitas, en las placas aclaradas con KOH y teñidas con azul de lactofenol, no se encontraron hifas en el hemocele debido a que la técnica de aclaramiento con KOH no permitió observar la invasión del hongo en el hemocele y a las 72 h de la infección se detectaron hifas invadiendo principalmente el tejido graso (Fig. 2) e intestino (Fig. 3), continuando hacia los tejidos musculares, nervioso y aparato digestivo, mostrando una invasión fúngica en todos los órganos de la termita Nasutitermes sp. Observaciones que concuerdan con los resultados obtenidos por Sajap y Kaur (1990) y Tanada y Kaya (1993) en las termitas C. curvignathus, donde el hongo M. anisopliae invadió extensivamente el tejido graso, los tejidos musculares e intestino en el período comprendido entre 60-72 h después de la infección.
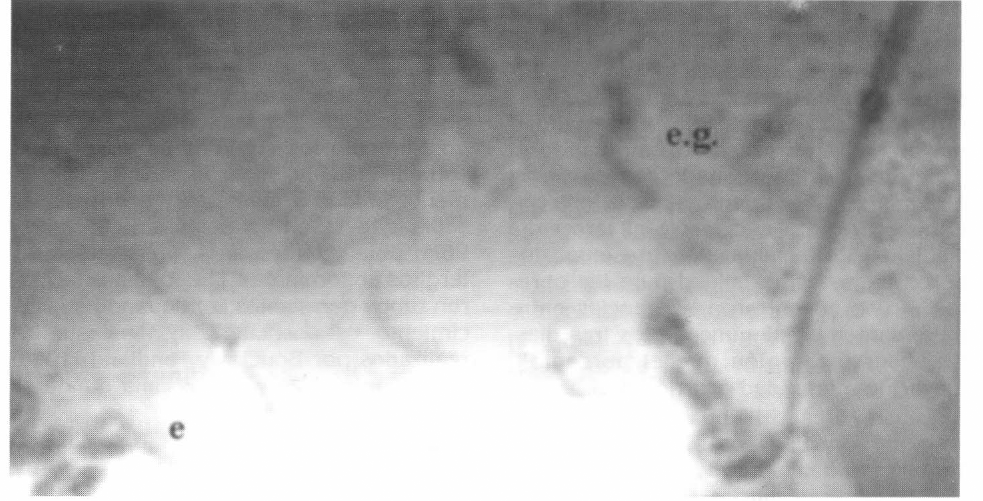
Esporas germinadas de M. anisopliae invadiendo el tejido graso de soldados Nasutitermes sp. e: esporas. eg: espora germinada. 100X.
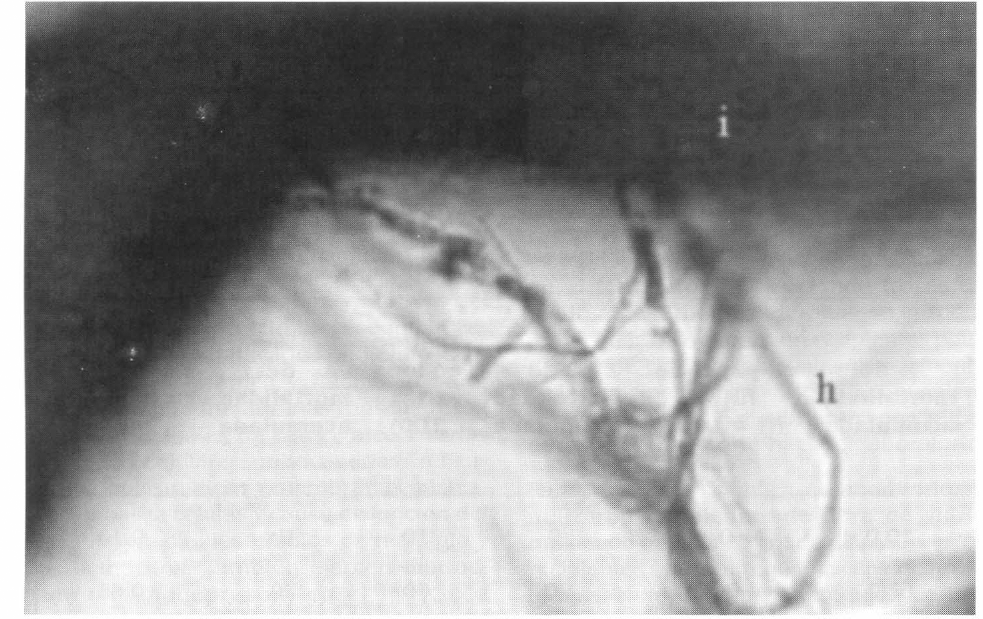
Hifa de M. anisopliae invadiendo el intestino de soldados Nasutitermes sp. i: intestino. h: hifa. 100X.
Aunque las termitas Nasutitermes sp. murieron entre 1-3 días después de la inoculación del hongo entomopatógeno, no se observó el micelio emergiendo de la cutícula del insecto hasta 96 h post-inoculación (Fig. 4a), lo que concuerda con los resultados obtenidos por Sajap y Kaur (1990) en C. curvignathus en los que la emergencia del micelio se presentó a las 100 h post infección.
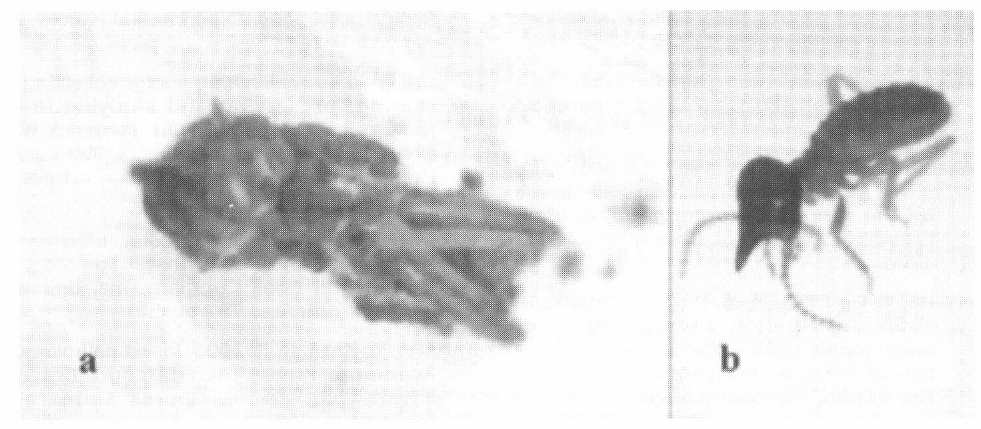
a. Un cadáver de soldado de Nasutitermes sp. completamente cubierto con conidióforos llevando conidios. b. Termita sana. 10X.
En este estudio se logró la infección de soldados termitas adultos que tienen cuerpos esclerotizados (Fig. 4b), los cuales ofrecen cierta resistencia hacia la acción fúngica ya que la cutícula melanizada es relativamente resistente al ataque enzimático por hongos (Charnley y St. Leger 1991). Los hongos usualmente causan mortalidades por uno de los siguientes aspectos: deficiencia nutricional, invasión y destrucción de tejidos (que puede ser antes o después de la muerte del insecto) y liberación de toxinas (Tanada y Kaya 1993).
La micosis se evaluó durante ocho días después de la inoculación del hongo M. anisopliae. El micelio en el cuerpo de la termita tomó coloraciones desde blanca hasta verde oliva claro, verde oliva oscuro con tintes grisáceos hasta verde oscuro, con un aspecto algodonoso al inicio del crecimiento hasta polvoso en la fase final. A las 96 h se observó micelio en forma de filamentos hialinos sobre la parte ventral del tórax y sobre las patas. A las 120 h las termitas presentaron un micelio blanco en forma de hilos transparentes ocupando todo el cuerpo de la termita. El hongo se encontró invadiendo la superficie ventral de la cabeza (gulamentón, prementón, ligula, palpos labiales; maxilas: galea, lacinia, palpos maxilares y mandíbulas). El micelio se observó de una coloración blanca con un aspecto algodonoso en la cabeza (gena y postgena), en forma de un escudo en la cervix, en la parte posterior del protórax, dorso-pleura, prosternum, mesosternum y metasternum, y en las articulaciones de las patas anteriores, medias y posteriores (articulaciones entre fémur y tibia, tibia y tarsómeros y uñas tarsales). El hongo no se encontró invadiendo la termita dorsalmente; solamente se observó micelio blanco en uno de los tergitos abdominales posteriores en la membrana intersegmental.
A las 144 h de la inoculación, el micelio blanco se tornó de color verde ocupando las mismas partes que se mencionaron anteriormente y el nasuto empezó a cubrirse de micelio en su parte apical. A las 168 h, la superficie dorsal del cuerpo de la termita se cubrió totalmente de un micelio hialino y en los tergitos abdominales posteriores se encontró micelio blanco. El micelio verde empezó a tomar una coloración verde oliva que proliferó en partes bucales, superficies dorso y ventro-laterales del tórax y en las articulaciones de las patas. A las 192 h el micelio verde se tornó más oscuro pero de consistencia polvosa e inició la invasión de la cabeza (piezas bucales, genas, postgenas), prosternum, mesosternum, metasternum y patas. El hongo llenó los tergitos torácicos y comenzó a cubrir los tergitos abdominales posteriores. Finalmente, la termita quedó invadida totalmente por el hongo.
Conclusión
El mecanismo de invasión del hongo M. anisopliae en la termita Nasutitermes sp. es vía integumentaria, iniciándose con la adherencia de la espora a la cutícula, la penetración al intestino y al tejido graso conllevando a la muerte del insecto y su posterior esporulación.
Footnotes
Agradecimientos
Los autores expresan los más sinceros agradecimientos al profesor Jaime Calle por la revisión y corrección del manuscrito, a los profesores Constantino Mantilla, Sandra Uribe S., Fabio Pineda G., José Rincón, Luis Carlos Mejía, Abel Díaz C. y a los compañeros del laboratorio de Micología y Microbiología del Instituto de Biología y del Pos-grado de Entomología de la Universidad Nacional Sede Medellín que contribuyeron a la ejecución de este trabajo. También al Comité para el Desarrollo de la Investigación (CODI), al Instituto de Biología Universidad de Antioquia y a la Universidad Nacional de Colombia Sede Medellín por la financiación y apoyo a este trabajo.
