Abstract
The entomopathogenic fungus Beauveria bassiana (Bals.) Vuillemin is a good tool for biological control of insects that attack economically important crops. This fungus produces a ciclohexadepsipeptide toxin that exhibits biological activity as an insecticide. The objective of this research was to produce polyclonal antibodies (Pabs) that could be used for the immunological quantification method in order to quantify of the production of beauvericin in seven (7) strains of B. bassiana (Bb) from the collection of Cenicafe-Colombia. Liquid cultures of Sabouraud's medium were inoculated with 3,0 x 105 conidia/ml of each isolate and these extracts were filtered and evaluated at 7, 9 and 11 days of growth. Pabs were obtained through two intramuscular injections in New Zealand white rabbits. The injections contained 2,5 mg of the emulsified immunogen with Freund's complete adjuvant for the first injection and with Freund's incomplete adjuvant for the second. The serological tests used in this experiment were ELISA and Dot-blot. The results showed differences in toxin production among seven isolates of the fungus B. bassiana. All isolations showed a peak of production between 9 and 11 days of culture. The levels of the beauvericin detected fluctuated between 1,16 µg/µl for isolate B. bassiana 9610 and 1,57 µg/µl for isolate B. bassiana 9205. This methodology will permit selection of the strains most efficient in toxin production, which could be incorporated into integrated pest management programs.
Introducción
Actualmente se utilizan en el país diferentes aislamientos del hongo Beauveria bassiana (Bals.) Vuillemin en el control biológico de insectos plaga como la broca del café Hypothenemus hampei (Ferrari) (Coleoptera: Scolytidae) (Bustillo et al. 1998). El potencial de este microorganismo en el control biológico de insectos ha permitido su inclusión en diversos programas de manejo integrado de plagas que atacan cultivos de importancia económica en el país (Ferron 1981). La acción del hongo sobre el insecto es facilitada principalmente por la acción de una gran variedad de metabolitos secundarios producidos a lo largo del proceso de infección. El proceso patogénico del hongo se inicia en la cutícula del insecto con la germinación de los conidios y la producción de hifas invasoras, los cuales penetran los tejidos a través de los intersticios y partes blandas del insecto (Castellanos 1997) dando inicio de esta forma a la actividad enzimática degradativa de la cutícula (Paterson et al. 1994; Delgado et al. 2001). Las hifas se ramifican, colonizan y llegan hasta la cavidad hemocélica del insecto, donde se produce una masa micelial por el crecimiento del hongo. En muchos casos, el insecto puede ser colonizado totalmente por el hongo (Fig. 1). Además, se liberan toxinas, las cuales están implicadas en bloquear el desarrollo fisiológico y causar la muerte del insecto (Paterson et al. 1994; Castellanos 1997). Éstas determinan la gravedad de la enfermedad producida y la capacidad del hongo para bloquear los mecanismos de respuesta inmune del insecto (Vey et al. 1985; Ignoffo y Mandava 1988; Eyal et al. 1994; Abbas et al. 1995).
Las micotoxinas son metabolitos fúngicos secundarios que hacen parte de los mecanismos de infección y pueden dar lugar a una respuesta tóxica en diferentes organismos. Ellos son producidos por una serie de reacciones consecutivas, las cuales son catalizadas por enzimas intermediarias del metabolismo primario (Volcy y Pardo 1994). Los métodos más utilizados para la identificación y cuantificación de analitos de interés biológico como las micotoxinas son la Cromatografía de Gases (GC), la Cromatografía Líquida de Alta Eficiencia (HPLC), y la Espectrometría de masas (MS), entre otros (Uribe et al. 1997). Estas metodologías son por lo general muy costosas y requieren de personal altamente calificado en el manejo del instrumental (Wilson et al. 1998).
En Colombia, se han realizado pocos estudios sobre la acción y la producción de las micotoxinas como beauvericina por parte del hongo B. bassiana. Por esto, se hace necesario desarrollar metodologías sensibles, rápidas, confiables, económicas y de fácil aplicación que permitan cuantificar la producción de esta micotoxina por los diferentes aislamientos del hongo B. bassiana y relacionarlo con la patogenicidad del hongo sobre los insectos plaga (Smith et al. 1981; Castellanos 1997). En este estudio se aplicó una metodología para producir anticuerpos policlonales contra beauvericina (BEA), para detectar y cuantificar la presencia de la toxina en cultivos líquidos del hongo B. bassiana.
Materiales y Métodos
Material Biológico
Se utilizaron conejos de raza Nueva Zelanda de un año de edad y con un peso aproximado de 5 kg. Los conejos se sangraron antes de ser inoculados con el antígeno, y el suero se utilizó como blanco para las diferentes pruebas inmunológicas.
Preparación del inmunógeno
El inmunógeno empleado para la producción de anticuerpos policlonales se preparó disolviendo 2,5 mg de la micotoxina beauvericina (Sigma chemical Co. B 7510) (Sigma 2001), con 1,5 ml de una solución Etanol: Agua en proporción 2:1. Posteriormente, esta solución se mezcló con 3 ml de adjuvante completo de Freund's para la primera aplicación y adjuvante incompleto para la segunda. Finalmente, la solución se emulsificó durante 5 min.
Inoculación de los conejos
Una vez preparada la solución del inmunógeno se procedió a realizar la primera inoculación por vía intramuscular inyectando 0,7 ml del antígeno en tres partes diferentes del cuerpo del conejo. Posteriormente, los conejos se trasladaron al bioterio bajo condiciones normales de alimentación y cuidado. La segunda inoculación a los conejos se llevó a cabo a los 28 días de forma similar a la inoculación inicial con el objeto de buscar una producción masiva de los anticuerpos contra la toxina.
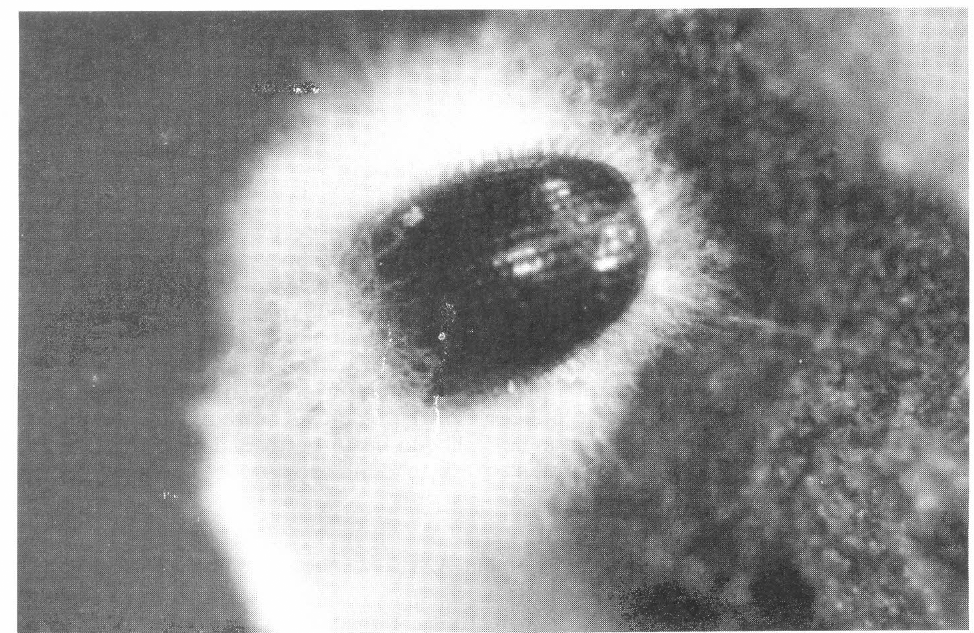
Adulto de la broca del café (Hypothenemus hampei) infectado por el hongo Beauveria bassiana. (Bb 9205).
Obtención del antisuero
Después de 10 días de la última inoculación, los conejos se introdujeron en un cajón de madera de modo que el animal quedara inmóvil. Se ubicaron canales sanguíneos de buena irrigación en ambos lados de los ojos y se introdujeron en ellos cánulas de vidrio con el fin de colectar la sangre; también se extrajo sangre realizando pequeñas incisiones en las orejas del conejo con la ayuda de un bisturí estéril. En ambos casos, el área fue cuidadosamente desinfectada con una solución de etanol al 70%. La sangre colectada se dejó a temperatura ambiente durante 24 h y posteriormente se centrifugó a 14. 000 rpm durante 20 min. El antisuero obtenido se almacenó en alícuotas de 50 µl a -80°C y se usó como fuente de los anticuerpos policlonales contra beauvericina (AntiBEA).
Reactivación de los aislamientos del hongo Beauveria bassiana
Los aislamientos de B. Dassiana Bb 9205, Bb 9620, Bb 9601, Bb 9616 y Bb 9618, Bb 9610 y Bb 9010 provenientes de la micoteca perteneciente al Centro Nacional de Investigaciones de Café, CENICAFE - Colombia, se reactivaron en medio sólido Sabouraud complementado con broca macerada al 0,4%. Todos estos aislamientos se seleccionaron por sus diferentes grados de patogenicidad sobre adultos de la broca del café Hypothenemus hampei (Tabla 1).
Aislamientos de B. bassiana seleccionados para la cuantificación de BEA de acuerdo con su origen, hospedante, patogenicidad y tipo de aislamiento
Escala de patogenicidad: Grupo 1: 0-25%; Grupo 2: 26-50%; Grupo 3: 51-80%; Grupo 4: 81-100%. Fuente: Vélez et al. (1998), y Estrada et al. (1999).
Obtención de los cultivos líquidos del hongo Beauveria bassiana
A erlenmeyers de 500 ml se adicionaron 200 ml del medio de cultivo líquido Sabouraud conteniendo 0,4% de cutícula de broca. Posteriormente, el medio se esterilizó por autoclave a 121°C y 15 libras de presión durante 15 min (Kucera 1971; Jegorov et al. 1998). La inoculación de los hongos en este medio se hizo a partir de una solución madre de 1 x 109 conidios/ml preparada en 10 ml de agua conteniendo tween 80 al 0,1% y glicerol al 0,25% (Vélez et al. 1997). A partir de esta solución se realizaron diluciones seriadas hasta obtener una dilución de 10−4. Tres recipientes se inocularon con los diferentes aislamientos de B. bassiana a una concentración de 3 x 105 conidios/ ml. Los medios de cultivo se dejaron durante 11 días en agitación rotacional a 110 rpm a 27±1° C y HR 80%.
Procesamiento de las muestras
Los cultivos líquidos se colectaron a los 7, 9 y 11 días de crecimiento, y se filtraron al vacío utilizando papel Whatman #1. El extracto líquido se centrifugó a 15.000 rpm durante 30 min, y la toxina presente en el sobrenadante se concentró haciendo uso de membranas con un punto de exclusión de 3 Kda (Buchawaldt y Jensen 1991; Jegorov et al. 1998; Kershaw et al. 1999).
Preparación de la solución patrón de beauvericina
Se preparó una solución madre disolviendo 500 µg de beauvericina comercial (Sigma Chemical, C45H57N3O; masa molecular 784 y 97% de pureza), en 1 ml de metanol puro. Posteriormente, se realizaron diluciones para ser usadas como patrones tanto en la prueba Dot-blot, como para la obtención de la curva de calibración a usar en la metodología de ELISA.
Detección de la micotoxina mediante la metodología de Dot-blot
La presencia de beauvericina en los extractos líquidos del hongo se llevó a cabo aplicando alícuotas de 5 µl de los cultivos líquidos filtrados y los patrones de beauvericina, sobre una membrana de nitrocelulosa, la cual había sido tratada previamente sumergiéndola en una solución de metanol al 20% durante 30 min, y secada a 50°C. Seguidamente, la membrana se dejó durante 30 min en solución de bloqueo (solución amortiguadora Tris-salino (TBS) conteniendo gelatina al 1%).
Después, la membrana se lavó con agua destilada estéril (ADE) y se incubó con la misma solución amortiguadora conteniendo el primer anticuerpo (AntiBEA) a una concentración de 10 µl/ml, durante 1 h a temperatura ambiente. Posteriormente, se realizaron dos lavados de 15 min cada uno con solución amortiguadora Tris-salino más Tween 20 al 0,1% (TTBS), y un lavado con TBS. Paso seguido, la membrana se incubó nuevamente durante 1 h a temperatura ambiente con 5 µl del segundo anticuerpo (Antirabbit conjugado a la enzima peroxidasa) disuelto en 30 ml de la solución de bloqueo. Cumplido este tiempo, se repitieron los mismos tres lavados como en el paso anterior. Finalmente, la presencia de la toxina sobre la membrana fue revelada, sumergiéndola en una solución preparada con 30 ml TBS, a la cual se le adicionaron 50 µl de peróxido de hidrógeno y 30 mg de 4-cloro-1naftol disuelto en 10 ml de metanol.
Cuantificación de la micotoxina mediante la metodología ELISA (Enzyme - Linked Inmunosorbent Assay)
Se aplicaron 200 µl de cada extracto a pozos de un microplato ELISA para su fijación durante 24 h a 8°C (Ball 1974). Posteriormente, el plato se lavó tres veces con solución de TTBS (2) y con TBS (1), у se procedió a bloquear los pozos durante 1 h adicionando 200 µl de Tween 20. Se repitieron los tres lavados de igual forma como en la etapa anterior, y se continuó con la incubación del plato por 2 h a 37°C con 700 µl del primer anticuerpo (AntiBEA) disueltos en 30 ml de solución de bloqueo. De nuevo se repitieron los tres lavados con TTBS (2) y con TBS (1) y se incubó el plato por 2 h a 37°C con 5 µl del segundo anticuerpo (Antirabbit conjugado a la enzima peroxidasa) disuelto en 30 ml de solución de bloqueo.
Finalmente, se lavaron nuevamente los pozos y se reveló, adicionando a cada pozo 200 µl de una solución de 1 mg de Tetrametilbenzidina (TMB) disuelta en 10 ml de TBS, conteniendo 5 µl de peróxido de H2O2. Finalmente, se llevó a cabo la lectura de absorbancia en un lector ELISA a una a de 490 nm. La estimación de la concentración de beauvericina (µg/µl) en cada una de las muestras se hizo por interpolación en una curva patrón con concentraciones conocidas de la toxina (Datos no mostrados).
Análisis estadístico
A los resultados obtenidos de los análisis Dot-blot y ELISA se les aplicó estadística descriptiva.
Resultados y Discusión
Metodología Dot-Blot
Con el objetivo de evaluar la especificidad de los anticuerpos policlonales producidos, se procedió a aplicar, sobre membranas de nitrocelulosa, diferentes cantidades de una solución patrón de beauvericina. A partir de los 5 min de aplicada la solución de revelado sobre las membranas de nitrocelulosa se observaron cambios en el sitio donde se aplicaron los patrones de la toxina. Los puntos de color azul aparecen por la acción enzimática de la enzima peroxidasa sobre el sustrato 4-cloro-1-naftol (Sigma 2001). No se detectaron manchas en aquellos puntos donde se aplicaron soluciones blanco sin la toxina. El resultado anterior indica que mediante la metodología utilizada, fue posible la obtención de anticuerpos policlonales contra la micotoxina, y además corrobora la presencia y utilidad de dichos anticuerpos AntiBEA en la detección y cuantificación de beauvericina proveniente de aislamientos de B. bassiana a través de la prueba serológica Dot-blot (Fig. 2). Manchas de características iguales aparecieron sobre las membranas de nitrocelulosa cuando se probaron cultivos líquidos de los hongos Bb 9620 y Bb 9205 correspondientes a diferentes días de crecimiento. Igualmente, se pudo observar mayor intensidad en los puntos correspondientes al día 9 de crecimiento del aislamiento Bb 9205 (Fig. 3), lo cual indica una mayor producción de la toxina a este tiempo, similar a los resultados encontrados por Uribe et al. (1997) en el aislamiento Bb 9401 haciendo uso de cromatografía líquida de alta eficiencia (HPLC).
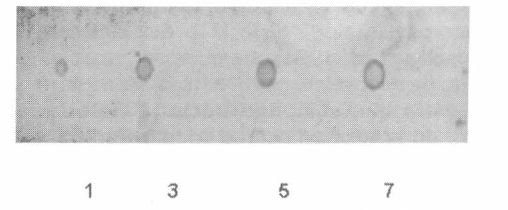
Prueba Dot-blot (Reacción antígeno-anticuerpo) con anticuerpos policlonales AntiBEA. 1, 3, 5 y 7 µl de solución patrón de beauvericina pura (0,5 µg / µl).

Detección de beauvericina en cultivos líquidos filtrados de B. bassiana. Línea 1. 1, 3, 5 у 7 µl del medio de cultivo de Bb 9620 al día 9 de crecimiento. Línea 2. 3 y 5 µl del medio de cultivo de Bb 9205 al día 9 y al día 11 de crecimiento, respectivamente.
Metodología ELISA
A través de esta metodología se observó que los valores mayores de producción de beauvericina se presentaron en los aislamientos Bb 9205; con pico de producción de la toxina de 1,567 µg/µl al día 9, y en el aislamiento Bb 9010 con un pico de producción al día 11 de 1,542 µg/µl. Los valores más bajos de producción de esta toxina se presentaron en los aislamientos Bb 9616 al día 9 y Bb 9610 al día 7 con 1,083 µg/µl y 1,164 µg/µl, respectivamente. En general para todos los aislamientos los valores de producción de toxina fueron muy similares al día 7, fluctuando entre 1,333 µg/µl para Bb 9620 y 1,164 µg/µl para Bb 9610, mientras que la producción estimada de toxina para los días 9 y 11 de crecimiento en todos los aislamientos mostraron valores más contrastantes (Tabla 2). Otros estudios como los de Genthner y Middaugh (1994) y Gupta et al. (1995) confirman la variabilidad que existe en la producción de beauvericina por diferentes aislamientos del hongo.
Cuantificación mediante ELISA de la producción de beauvericina por diferentes aislamientos del hongo entomopatógeno Beauveria bassiana (Bals) Vuill.
Aspectos como el medio de crecimiento, el tiempo de obtención, la cantidad de micelio producida y el metabolismo del hongo entre otros, influyen notoriamente en la producción de las toxinas (Rombach 1988).
La mayoría de los estudios de toxicidad con beauvericina han sido realizados probando su actividad biológica contra insectos. Sin embargo, estudios recientes llevados a cabo in vitro, muestran alta toxicidad de esta toxina hacia murine y líneas celulares humanas (Di Paola et al. 1994; Ojcious et al. 1999). Así mismo, a este ciclopéptido se le atribuyen propiedades insecticidas y antimicrobiales (Thakur y Smith 1997; Dev y Koul 1997; Nilanonta et al. 2000).
Los resultados encontrados en este estudio muestran una mayor producción de beauvericina por parte del aislamiento Bb 9205m, el cual es usado actualmente para el control biológico de la broca del café (Bustillo et al. 1991). La curva de producción de la toxina para este aislamiento muestra que el hongo inicia la exportación de la toxina hacia el medio líquido a partir del día 5 de crecimiento (Datos no mostrados). Esto sugiere que dicho péptido juega un papel importante en la patogenicidad de B. bassiana sobre el insecto, determinando al parecer la real capacidad del hongo para afectar de manera negativa al insecto y bloquear sus mecanismos de respuesta hasta provocarle la muerte (Vey et al. 1985; Ignofo y Mandava 1988; Eyal et al. 1994). En este estudio se encontró que existe una estrecha relación entre el contenido de la toxina en el medio de cultivo y la patogenicidad de cada uno de los aislamientos de B. bassiana que fueron analizados (Vélez et al. 1998) (Fig. 4). Zacharuk en 1973, con resultados similares, concluyó que la toxina causa en el hospedero degeneración progresiva de los tejidos, cambios estructurales de las membranas y deshidratación. Así mismo, durante la patogénesis se evidencian cambios en la actividad eléctrica de los nervios causada por el incremento del consumo de oxígeno en un intento del insecto por restablecerse (Evlakhova y Rakitin 1968). Zizca y Weiser (1993) probaron “in vitro” el efecto de la beauvericina sobre larvas de Culex pipiens, encontrando que aún con bajas concentraciones de la toxina (0,1 mg / ml) aplicadas tópicamente sobre el insecto se obtiene una mortalidad del 44% en 48 h. De igual manera, encontraron que el principal síntoma de intoxicación presentado fue la vacuolización generalizada y el efecto tóxico en las mitocondrias, las cuales se hincharon y tomaron aspecto de vacuolas esféricas. Además, la cromatina de los núcleos se concentró en forma de gránulos alargados a lo largo de la membrana nuclear, siendo más afectado el epitelio de las moscas rompiéndose la membrana basal.
Aunque B. bassiana produce también las toxinas oosporeina, bassianolide y beauveriolide, las cuales son péptidos estructuralmente relacionados con beauvericina, su toxicidad para animales, plantas e insectos es desconocida (Namatam et al. 1999; Mochizuki et al. 1993). Otros estudios muestran que beauvericina no es tóxico para ciertos insectos (Champlin y Grula 1979). En este estudio fue posible detectar y cuantificar beauvericina en concentraciones bajas, a partir de cultivos líquidos de B. bassiana en medio Sabouraud, haciendo uso de inmunoensayos basados en los anticuerpos policlonales (AntiBEA) producidos. Hasta la fecha se han desarrollado numerosos métodos para detectar micotoxinas especialmente en alimentos (Wilson et al. 1998); en contraste con los pocos estudios sobre metabolitos producidos por hongos entomopatógenos usados como micoinsecticidas, micoherbicidas y/o micoparásitos (Strasser et al. 2000; Vey et al. 2001).
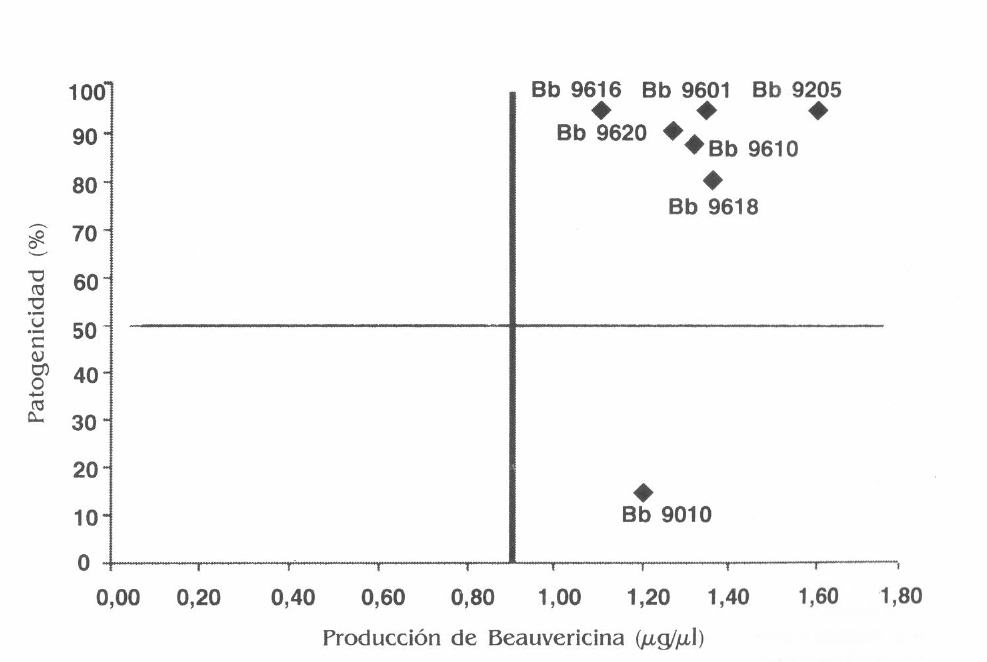
Relación entre la patogenicidad y la producción de beauvericina al día 9 de cultivo para cada uno de los aislamientos de B. bassiana.
La metodología utilizada en el presente estudio permitirá rastrear el metabolito tóxico en una amplia gama de muestras biológicas, identificar las condiciones que regulan la producción de la toxina, apoyará el estudio de las propiedades de la toxina a nivel celular en el insecto y determinará si este tipo de metabolito tiene acción insecticida, nematicida, antimicrobiana o citotóxica. De igual manera, esta metodología se puede utilizar como diagnóstico para profundizar en el modo de acción del metabolito tóxico (destrucción de membranas, inhibición de ATPasas, mitosis o citoquinesis) sobre insectos plaga (Strasser et al. 2000) con el fin de establecer criterios de selección de cepas del hongo B. bassiana que sean más eficientes para el control biológico de plagas, apoyando de esta forma la producción de formulaciones y la incorporación del hongo en programas de manejo integrado de plagas.
Estos resultados constituyen una ayuda valiosa en la búsqueda de moléculas bioactivas de interés entomológico y muy especialmente de genes que puedan ser utilizados en el desarrollo futuro de material de café resistente, mediante la transformación genética del cultivo.
Conclusiones
Se logró la detección y cuantificación de la toxina beauvericina (micotoxina de interés entomológico), en cultivos líquidos provenientes de diferentes aislamientos de B. bassiana, mediante la aplicación de pruebas serológicas (Dot blot y ELISA) basadas en la producción de anticuerpos policlonales.
Los aislamientos del hongo B. bassiana que fueron evaluados produjeron, bajo condiciones de cultivo en medio líquido, niveles diferentes de la toxina, lo cual podría reflejar diferencias genéticas importantes o diferencias en su especificidad hacia el insecto hospedero. En virtud de lo anterior, la concentración de la toxina podría ser incorporada como un nuevo criterio de selección de aislamientos del hongo B. bassiana, en la búsqueda de formulaciones más eficientes para el control biológico de la broca del café.
Footnotes
Agradecimientos
El presente estudio se realizó gracias al apoyo financiero del Instituto Colombiano para el Desarrollo de la Ciencia y la Tecnología “Francisco José de Caldas” COLCIENCIAS y la Federación Nacional de Cafeteros a través de su Centro Nacional de investigaciones de Café CENICAFE. Los autores también agradecen a la Universidad Católica de Manizales por su colaboración y a la Universidad de Caldas por la asistencia técnica y asesoría en la producción de los anticuerpos policlonales.
