Abstract
The nematode Neoaplectana carpocapsae Weiser strain 00-136, was pathogenic to larvae and prepupae of the forest defoliator Oxydia trychíata Guenée) under simulated field conditions. The technique presented to mass produce the nematode is considered useful and economical its commercial production.
It is necessary to carry out field experiments to corroborate the results obtained under simulated conditions. However, it is believed that the soil of pine plantations have the humidity required for the survival of the nematode a critical condition that has limited the use of N. carpocapsae in many crops.
Introduccion
Dentro de los agentes de control biológico de plagas, los nemátodos parásitos de insectos constituyen un grupo relativamente nuevo, sobre el cual no existe mucha información con relación a su uso en niveles comerciales. Es idispensable conocer las posibilidades que ofrece en nuestro medio forestal colombiano el nemátodo Neoaplectana carpocapsae Weiser en el control del Oxydia trychiata (Guenée) (Lepidoptera: Geometridae). En este trabajo se presentan los resultados sobre la patogenicidad del nemátodo en los diversos estados inmaduros del medidor gigante y la técnica desarrollada para multiplicarlo masivamente en el laboratorio.
Revision De Literatura
Los insectos y los nemátodos han desarrollado muchas relaciones entre si. La más importante desde el punto de vista de control de insectos está constituída en aquella en que el nemátodo después de matar al insecto, libera una bacteria esencial para su nutrición. Esta condición tan especializada ha sido desarrollada por la familia Neoaplectanidae, la cual ha llegado a relacionarse simbióticamente con bacterias específicas.
El nemátodo denominado DD-136 es conocido desde 1954 cuando el Dr. Walter Hough lo encontró en Virginia en larvas de Cydia (Carpocapsa) pomonella (L.) y fue considerado por Steiner como una nueva especie de Neoaplectana (Dutky y Hough, 1955). Más tarde Dutky (1959) registró la asociación de este nemátodo con una bacteria, pero fueron Poinar y Thomas (1965) los que aislaron la bacteria de la cavidad intestinal del nemátodo y la nombraron Achromobacter nematophilus Poinar y Thomas.
La asociación entre la bacteria y el nemátodo es del tipo mutualístico. La bacteria es protegida por las formas juveniles infectivas del Neoaplectana y una vez que éstas penetran en una larva hospedante liberan la bacteria. A su turno, la bacteria al causar septicemia en el insecto provee el ambiente necesario para la reproducción del nemátodo dentro del huésped (Poinar y Thomas, 1966).
El nemátodo N. carpocapsae fue descrito por Weiser de larvas de C. pomonella colectadas en Checoslovaquia en 1955. Pero fue solo 12 años más tarde cuando Poinar (1967) demostró que el DD-136 era en efecto una raza de N. carpocapsae.
La familia Neoaplectanidae incluye el género Neoaplectana, el cual contiene alrededor de 10 especies. Estos nemátodos se diferencian de otros principalmente, por la típica estructura de la cabeza y por la forma de la cola y la genitalia de los machos (Welch 1963). De la especie N. carpocapsae se conocen actualmente tres razas, la DD-136, la Checoslovaca y la raza rusa referida como "raza agriotos" que fue encontrada recientemente por Poinar et al (1971). Se ha demostrado que la bacteria asociada con estas razas es la misma.
El N. carpocapsae ataca gran número de insectos masticadores, variando su grado de efectividad de acuerdo al insecto (Poinar, 1971). Se han desarrollado técnicas para la producción masiva de este nemátodo usando larvas de la polilla de la cera, Galleria mellonella (L.) (Dutky et al, 1964) y alimento para perros (House et al, 1955) con excelentes resultados.
El nemátodo DD-136 ha sido utilizado en ensayos de campo (Drooz, 1960) y en pequeña escala comercial para el control de insectos plagas de cultivos agrícolas (Dutky, 1959; Welch y Briand, 1961 a, b). El principal problema en los ensayos de campo ha sido la humedad, ya que el nemátodo requiere altos contenidos de humedad para trabajar exitósamente. Webster y Bronskill (1968) obtuvieron buenos resultados en ensayos de laboratorio mediante la adición de una sustancia retenedora de agua, un retardante de la evaporación y un surfactante. Ellos lograron asi aumentar el promedio de mortalidad de las larvas de Pristiphora erichsonii (Htg.) de 24 a 90 o/o.
Recientemente, Simons y Poinar (1973) demostraron que los estados juveniles infectivos de N. carpocapsae son capaces de sobrevivir humedades relativas muy por debajo del punto de marchitamiento de las plantas. Ellos sugieren que la aplicación de los nemátodos neoaplectanidos al suelo es más práctica que la aplicación a las partes aéreas de las plantas donde pueden estar sometidos a una rápida y letal desecación.
Materiales Y Metodos
A. Multiplicación del nemátodo
En apiarios comerciales en Santa Fé de Antioquia se colectaron larvas de la polilla de la cera, G. mellonella y se llevaron al laboratorio de Entomología de la Estación Experimental "Tulio Ospina" del ICA donde se alimentaron con una dieta artificial, elaborada en base a la desarrollada por Beck (1960), y la que se presenta a continuación con los siguientes ingredientes:
Para prepararla se procedió así: El cereal, la levadura en polvo y la cera de abeja se mezclaron con suficiente éter etílico para disolver la cera.
Después de mezclados totalmente y una vez evaporado el éter, el cereal y la levadura quedaron uniformemente cubiertos con la cera de abeja. Posteriormente, se unieron la miel, el glicerol y el agua, mezcla que se adicionó a los ingredientes secos, mezclándolos completamente. Una vez lista la dieta se refrigeró por 24 horas, para disminuir su pegajosidad y tornarla más friable.
Se logró asi establecer un cultivo permanente del insecto, el cual se utilizó para la multiplicación del nemátodo. El nemátodo usado fue Neoaplectana carpocapsae raza DD-136 proveniente de la Universidad de Wisconsin. Las formas encapsuladas del segundo estado juvenil del nemátodo se conservaron en una solución de formalina al 0.1 o/o mantenida en la nevera a 7° С.
Para infectar las larvas de G. mellonella se colocaron 4 ml de la suspensión de nemátodos en un plato de petri con dos hojas de papel filtro, en el fondo (Fig. 1a); luego en cada plato se colocaron unas 10 larvas próximas a empupar y se cubrió (Figs. 1b, 1c); después de unos dos o tres días, las larvas se transfirieron a una trampa, consistente en un plato de petri colocado en posición invertida dentro de un recipiente grande; el plato de petri se cubrió con una hoja de papel filtro de 12,5 cm de diámetro y el recipiente se llenó con suficiente solución de formalina al 0.1 o/o hasta casi cubrir el plato de petri (Fig. 1d). Al cabo de unos 10 días, los segundos estados juveniles migraron de las larvas desintegradas al líquido del recipiente a través de la superficie húmeda del papel filtro. Luego de esta trampa los juveniles se transfirieron y almacenaron en una nevera en erlenmeyers taponados con algodón.
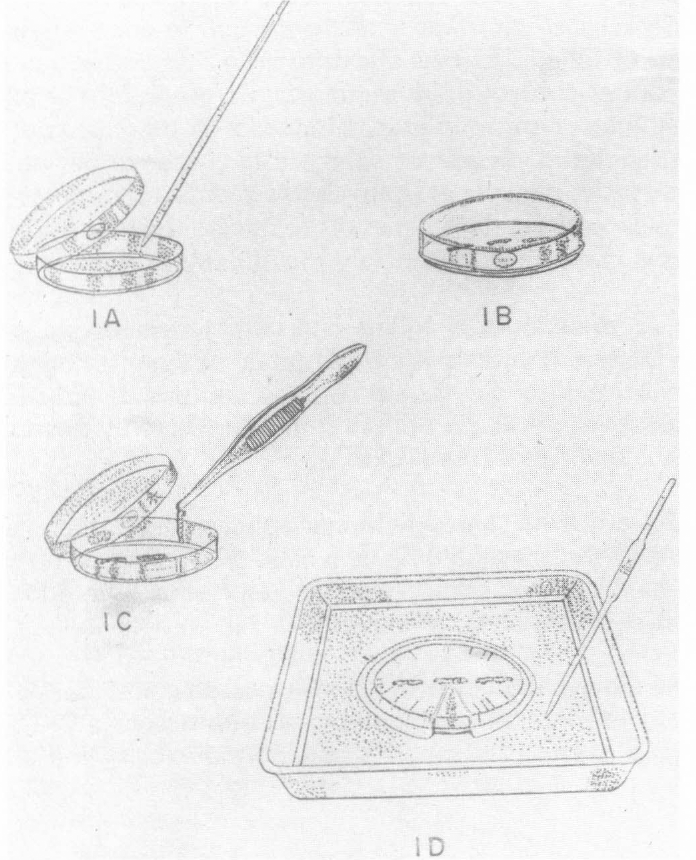
Método para la propagación del Neoaplectana carpocapsae:
Infección de las larvas con la suspensión del nemátodo
Se llevó un registro sobre el número de nemátodos producidos por cada larva de G.mellonella.
B. Estudios de patogenicidad con larvas, prepupas y pupas de O. trychiata
Se colectaron en el campo larvas de tercero, cuarto y quinto ínstar así como prepupas y pupas del medidor gigante del ciprés. De cada uno de los ínstares se colocaron cinco larvas en recipientes de vidrio de un galón de capacidad, al cual se había introducido follaje de ciprés; para cada ínstar se hicieron cinco replicaciones para un total de 25 larvas por ínstar. Luego se asperjó el follaje del ciprés con nemátodos, simulando una aspersión en el campo. Para el caso de las prepupas y pupas, que normalmente se encuentran en el suelo, se simuló el ambiente colocando cinco de cada una en recipientes de vidrio cubriéndolas con aserrín. La aspersión de nemátodos se hizo sobre el aserrín humedecido. Por cada estado se prepararon cinco replicaciones.
Todas las aspersiones con nemátodos se hicieron utilizando una concentración de 470 nemátodos por mililitro y empleando 8 ml por recipiente.
Una vez que las larvas murieron, fueron trasladadas a recipientes trampas, tal como se hizo con G. mellonella. También se llevaron registros períodicos sobre mortalidad y producción de nemátodos.
Para evaluar el número de nemátodos presentes en cada cosecha se tomaron dos muestras de 1,0 ml de la suspensión del nemátodo y se contó en un vidrio de reloj. Este resultado se promedio y relacionó con el volumen total de la suspensión y el número total de larvas de G. mellonella y O. trychiata.
C. Aislamiento de la bacteria A. nematophilus
Se emplearon dos técnicas diferentes. En el primer procedimiento, las larvas de O. trychiata se infectaron con DD-136 como se indicó anteriormente. Después de 24 horas, cuando las larvas habían muerto por la acción del nemátodo, éstas se esterilizaron sumergiéndolas en hipoclorito de sodio por cinco minutos. Luego se maceraron las larvas en 1,0 ml de agua destilada. Una alicuota de esta suspensión se cultivó en agar nutritivo incubando los platos a 30° C, y haciendo observaciones diarias para detectar cualquier crecimiento bacterial.
En el otro procedimiento se siguió la técnica descrita por Poinar (1966). Las formas juveniles infectivas de DD-136 se colectaron de larvas de O. trychiata infectadas las cuales se esterilizaron superficialmente con hipoclorito de sodio.
Luego se centrifugó una alicuota del nemátodo a 1.000 r.p.m. durante 10 minutos, se desechó la parte superior, quedando los nemátodos concentrados en el fondo. Estos se transfirieron a una laminilla cóncava esterilizada a la cual se la adicionó hemolinfa de O. trychiata. En caso de estar la bacteria en el nemátodo, es liberada en 24 horas en la hemolinfa. Al cabo de 48 horas se tomaron muestras de este cultivo y se inocularon en agar nutritivo para observar crecimientos bacteriales.
Resultados Y Discusion
La cría masiva de G. mellonella fué bastante éxitosa. La manipulación de los insectos es fácil y la dieta empleada es barata y eficiente, lo cual facilita la producción masiva del nemátodo para usarlo en una forma comercial en el campo.
El nemátodo N. carpocapsae raza DD-136, ataca las larvas y el estado de prepupa del O. trychiata, no así las pupas. Se observó que algunas prepupas atacadas alcanzan a empupar pero mueren antes de emerger el adulto por la acción del nemátodo y la bacteria mutualística A. nematophilus. La eficiencia del nemátodo es mayor en larvas de último ínstar y en las prepupas. Como se puede apreciar en la Tabla 1 la mayor producción de nemátodos se obtuvo en el quinto ínstar con un promedio de 28.380 nemátodos por larva siendo superada por el estado de prepupa con el que se obtuvo un promedio de 44.761 nemátodos por cada prepupa. A pesar de ser ésta una alta producción no es comparable con la obtenida usando prepupas de G. mellonella, que produjeron 60.378 nemátodos por prepupa (Tabla 2).
Número promedio de Neoaplectana carpocapsae producidos por cada larva de tercero, cuarto, quinto ínstar y por cada prepupa de O. trychiata obtenido al tratar 25 especímenes por prueba.
Número promedio de Neoap!ectana carpocapsae producidos por cada prepupa de Galleria mellonella, obtenido al tratar 51 prepupas.
No se considera práctico hacer las aspersiones del nemátodo para atacar las larvas que se encuentren en el follaje. Es más eficiente dirigir las aspersiones para el control del insecto cuando empiece a bajar al suelo para empupar. El estado de prepupa, por su quietud, es el más susceptible al ataque del nemátodo; además el suelo de las plantaciones forestales conserva una mayor humedad que permite una mayor supervivencia y movilidad del nemátodo
Las aspersiones al follaje con nemátodos son poco efectivas debido a la dificultad de obtener un buen cubrimiento del follaje con los equipos de aplicación disponibles y por la rápida desecación y posterior muerte del nemátodo.
Sin embargo, antes de iniciar aplicaciones comerciales es indispensable llevar a cabo ensayos de campo con el fin de comprobar los resultados obtenidos bajo condiciones simuladas.
El almacenamiento de las formas juveniles del N. carpocapsae se puede hacer en una nevera a 7° C, suspendiéndolas en una solución de formalina al 0.1 o/o, dentro de un recipiente de vidrio taponado con algodón. En esta forma ha sido posible mantener nemátodos vivos por más de un año.
La bacteria mutualística A. nematophilus pudo aislarse con ambos procedimientos. Esta bacteria crece formando a las 24 horas colonias grises circulares, de 1,0 mm de diámetro, convexas y con márgenes irregulares. Los análisis de caracterización hechos a las 24 horas de crecimiento están de acuerdo con las características descritas por Poinar y Thomas (1965) y Poinar et al (1971) para A. nematophilus.
