Abstract
Summary
During the last decade, Garcia Rovira province (Santander department, Colombia) has had some problems with greenhouse whitefly control, "Trialeurodes vaporariorum (Westwood)", which affects several crops of this province. Some Fusarium species can be considered promissory entomopathogenic for biological control of sucking insects (aphids, scales and white flies). The goal of this study was to know the Fusarium species predominant in the zone, from leaves and/or folioles of tobacco and kidney beans with T. vaporariorum. 168 colonies of Fusarium were isolated and identified, according to their macroscopic characteristics (morphology, coloration and diameter) developed on Potato Dextrose Agar (PDA) and their microscopic characteristics (macroconidia, microconidia, conidiophores and chlamydoconidia) on Carnation Leaf Agar (CLA). Species identification of all isolated colonies was carried out by contrasting obtained characteristics on PDA and CLA with different identification keys available up to date. Thirteen Fusarium species were isolated and identified from T. vaporariorum. They were: F. sambucinum, F. graminearum, F. compactum, F.equiseti, F. avenaceum, F. longipes, F. reticulatum, F. oxysporum, F. heterosporum, F.culmorum, F. lateritium, F. coccophilum, and F. crookwellense. Further research must prove whether these species can be involved with T. vaporariorum population control.
Introducción
En el mundo, durante la última década, las moscas blancas se han convertido en uno de los grupos de plagas de mayor impacto económico por ser de difícil control. Dentro de las especies que afectan cultivos, tanto en campo abierto como invernadero, sobresalen Trialeurodes vaporariorum (Westwood) y Bemisia tabaci (Gennadius), las cuales atacan un amplio rango de cultivos (hortalizas, frutales y ornamentales) y ocasionan grandes pérdidas (López-Ávila 1993). Estas dos especies causan daño directo por la extracción de savia que provoca la caída del follaje y evita la maduración de los frutos, así como el crecimiento de fumagina sobre la melaza excretada, que dificulta la fotosíntesis y deteriora los frutos (Hilje 1993). También tienen la capacidad de actuar como vector de virus. Actualmente, la situación se ha hecho más compleja con B. tabaci debido a la presencia de biotipos (Hilje 1993).
En algunas regiones de Colombia, como la provincia de García Rovira (Santander), la infestación por mosca blanca ha constituido, en los últimos años, uno de los problemas económicos más importantes, puesto que el uso excesivo de productos químicos para su control, ha favorecido el desarrollo de altos niveles de resistencia a insecticidas químicos, los cuales además tienen un impacto negativo en los enemigos naturales (parasitoides, depredadores y entomopatógenos) de las moscas blancas. Todos estos aspectos han incentivado el estudio de microorganismos nativos posiblemente entomopatógenos en áreas determinadas, proporcionando herramientas básicas en el control de este insecto plaga.
El control biológico se presenta como una de las alternativas más promisorias en cualquier programa de manejo integrado de plagas, por lo cual su estudio es fundamental. Los agentes patogénicos de moscas blancas conocidos hasta el momento han sido los hongos, pues son los únicos capaces de infectar, penetrar y colonizar a través de la cutícula del insecto (Manzano et al. 1999). Aunque son muchos los entomopatógenos registrados actuando sobre la mosca blanca de los invernaderos, se destacan los hongos Acremonium spp., Aschersonia aleyrodis, Aphanocladium album, Beauveria bassiana, Fusarium verticilloides, Paecilomyces fumosoroseus, Trichothecium roseum, Verticillium fusisporum y V. lecanii. De ellos, sólo A. aleyrodis y V. lecanii han sido explorados como potenciales para el control de este insecto en diferentes cultivos (Madrigal 1994); por lo tanto, nace la necesidad de ampliar y enfatizar el control biológico de este insecto empleando otros hongos entomopatógenos como Fusarium.
Fusarium ha sido reconocido como uno de los hongos de mayor impacto económico y social a nivel mundial, puesto que se ha asociado con enfermedades en un amplio rango de plantas, animales e incluso en humanos. Además, está incluido dentro de los tres géneros productores de micotoxinas. Por otra parte, existen especies que son comunes en el suelo, actúan como saprofitas (Burgess et al. 1994) y entomopatógenas en varios grupos de insectos pertenecientes al orden: Homoptera (Delphacidae, Psyllidae, Aphididae, Cercopidae y Aleyrodidae), Hemiptera (Miridae), Coleoptera (Curculionidae y Tenebrioidae), Diptera (Muscidae, Bibionidae y Psychodidae) y Lepidoptera (Noctuidae, Phycitinae y Plutellidae), (Humber 1992).
Según los registros de Humber (1992), López-Ávila et al. (2001) y Fransen (1990), en la familia Aleyrodidae se encuentran varias especies de Fusarium saprofitas desarrollándose en inmaduros muertos o atacando ninfas de B. tabaci en Brasil (Bahía), México, Estados Unidos (California) y en Colombia en el departamento del Magdalena; sin embargo, la causa aparente de la muerte de las moscas blancas es por la producción de micotoxinas antes de que se evidencie el crecimiento micelial del hongo en las ninfas (Fransen 1990). Madrigal (1994), Vélez (1997) y Fransen (1990) registran aislamientos de F. verticilloides en T. vaporariorum. Este es un hongo saprofito o patógeno de plantas, pero aún no se conoce si es infeccioso para T. vaporariorum o sólo crece en los cadáveres de este insecto (Fransen 1990). Por lo tanto, es importante conocer cuáles especies de Fusarium pertenecen a la micobiota de T. vaporariorum en cada región y dilucidar su efecto entomopatogénico.
Fusarium tiene amplia distribución y representación en las principales regiones geográficas del mundo, algunas especies son cosmopolitas, otras tienden a predominar en las regiones tropicales - subtropicales o en climas templados, cálidos o fríos. Son pocas las especies y subespecies que están restringidas a algunas regiones o íntimamente asociadas a una(s) especie(s) particular de planta(s) (Burgess et al. 1994). Este género se clasifica en la clase Hyphomycetes dentro de la subdivisión Deuteromycotina, también denominados hongos imperfectos, puesto que han perdido su capacidad para formar esporas sexuales o se desconoce su estado teleoformo (Seifert 2000; Burgess et al. 1994).
En este estudio se identificaron 13 especies diferentes de Fusarium aisladas de T. vaporariorum en cultivos de tabaco (Nicotiana tabacum) y fríjol (Phaseolus vulgaris) de la provincia de García Rovira, Santander. Se estableció y caracterizó cuáles de estas especies aisladas predominaban en la micobiota del insecto, confrontándolas con las ya conocidas como entomopatógenas, con el fin de considerar su posible utilización como controladores biológicos de estos insectos chupadores, teniendo en cuenta el riesgo que representan las especies de Fusarium como patógenos de plantas y potentes productores de micotoxinas.
Materiales y Métodos
La investigación se llevó a cabo en las áreas productoras de tabaco y fríjol infestadas con mosca blanca de la provincia de García Rovira, del departamento de Santander, en los municipios de Capitanejo, Cerrito, Concepción, Enciso y San José de Miranda. El material biológico obtenido se escogió al azar en los cultivos hospedantes, seis hojas y/o foliolos con presencia de mosca blanca y en buen estado, ubicadas en los sitios con mayor densidad foliar (zona de autosombra); según la recomendación de Mier et al. (1991), quién sugiere obtener las muestras de estas zonas, las cuales propician el desarrollo de los insectos y los hongos. Siguiendo el método empleado por Anderson et al. (1997), cada hoja se introdujo en una bolsa plástica que en su interior contenía una toalla absorbente estéril y externamente una cinta adhesiva para su cierre; este material de recolección fue previamente esterilizado en el laboratorio.
Para el aislamiento primario de mohos asociados a ninfas y/o adultos de T. vaporariorum obtenidos de hojas y/o foliolos de tabaco y fríjol, se colectaron seis muestras en campo por cada sitio de muestreo, de lo cual se obtuvieron al azar 120 individuos aparentemente sanos. En la determinación de la micobiota presente en el insecto se utilizaron tres medios diferentes de cultivo: Medio Completo (MC) (Riba y Ravelojoana 1984; Calle 2000); Sabouraud al 4% (SDAY/4) (Rodríguez 1984a, b; Humber 1992) y PDA (Mier et al. 1991; García 1996) y dos procesos de desinfección: uno de ellos fue depositando directamente 60 cadáveres de T. vaporariorum sobre los medios de cultivo (MC, SDAY/4 y PDA) con una pinza entomológica estéril colocando diez individuos por cada caja de petri; en el otro, los cadáveres se sometieron a desinfección previa con hipoclorito de sodio al 0,4%. Para este proceso de desinfección fue necesario esterilizar frascos pequeños de vidrio, gasas y agua destilada en autoclave a 121°C por 15 minutos. Además, se diluyó el hipoclorito de sodio comercial de 5,4 a 0,4% utilizando agua destilada estéril. Teniendo todos los elementos estériles para la desinfección y los individuos de mosca blanca seleccionados (60 individuos), las moscas se desinfectaron en 1 ml de hipoclorito de sodio al 0,4% contenidos en un recipiente de vidrio estéril, agitando constantemente por dos minutos y se enjuagaron con 3 ml de agua destilada estéril por un minuto. Siguiendo la recomendación de Mier et al. (1991), se colectaron los individuos sobre una gasa estéril y se colocaron sobre los medios de cultivo. Los tres medios de cultivo propuestos se distribuyeron en seis cajas de petri desechables estériles, por duplicado, para cada uno de los 14 sitios de muestreo.
A partir de los cultivos iniciales, las colonias con características macroscópicas y/ o microscópicas similares a Fusarium se codificaron y aislaron en MC y/o Czapek Yeast Extract Agar (CYA) para su posterior identificación. Tres inóculos equidistantes de las colonias sospechosas se sembraron en PDA y CLA contenidos en cajas de petri de 100 x 15 mm. Las cajas con PDA se incubaron a 25 y 30°C para determinar la velocidad de crecimiento de las colonias de Fusarium, y las de CLA a 25°C con fotoperíodos de 12 horas; para ello se utilizó una lámpara de luz fluorescente ubicada a 45 cm de distancia de las cajas durante ocho días hasta un mes, en condiciones alternantes de luz-oscuridad. Además, para obtener el patrón de coloración característico de cada una de las especies sospechosas se utilizaron tubos tapa rosca 16 x 120 mm que contenían PDA en pico de flauta. Estos tubos se sometieron a las mismas condiciones de incubación del CLA (Burgess et al. 1994; Nelson et al. 1983; Samson et al. 1995). De cada uno de estos cultivos se efectuaron montajes entre lámina y laminilla utilizando azul de lactofenol, con el fin de registrar las características microscópicas desarrolladas por estas colonias, además se registraron las características macroscópicas mediante observaciones directas de tubos y cajas de petri (Burgess et al. 1994; Nelson et al. 1983; Samson et al. 1995).
En PDA se analizaron las características macroscópicas (exudado, diámetro de la colonia, pigmento, color del micelio y reverso), mientras que en CLA se estudiaron las características microscópicas (macroconidias, microconidias, conidióforos y clamydoconidias) (Seifert 2000; Pitt y Hocking 1997). Mediante la utilización de un microscopio de luz invertida, se observaron las colonias obtenidas en CLA con el fin de verificar la disposición de las conidias en el conidióforo (Burgess et al. 1994).
La determinación de cada una de las especies de las colonias aisladas se efectuó mediante la confrontación de la información obtenida a partir de las colonias en PDA y CLA con las diferentes claves de identificación disponibles hasta la fecha: Burgess et al. (1994), Nelson et al. (1983) y Seifert (2000).
Resultados y Discusión
En el aislamiento primario de mohos a partir de 1.680 adultos y/o ninfas de T. vaporariorum se obtuvieron las colonias de Fusarium. El 40% de las colonias de Fusarium aisladas provenían de MC, el 33% de SDAY/4 y el 27% de PDA (Fig. 1). MC permitió el desarrollo mayor y mejor de las colonias de Fusarium presentes en T. vaporariorum, puesto que se evidenció un porcentaje alto de colonias y mayor velocidad de germinación; de los tres medios utilizados, MC es el más complejo por su composición nutricional (10 g glucosa, 0,36 g KH₂PO₄, 1,42 g Na₂HPO₄, 1 g KCI, 0,6 g MgSO₄.7H₂O, 0,7 g NH₄NO₃, 5 g de extracto de levadura y 20 g de agar en 1.000 ml de agua destilada estéril) y es un medio óptimo, rutinariamente empleado en producción de hongos entomopatógenos (Gómez de Oliveira et al. 1997; Riba y Ravelojoana 1984).
Para la identificación de las especies de Fusarium se utilizó PDA y CLA, medios de cultivo que proporcionan las características morfológicas, macroscópicas y microscópicas desarrolladas para la taxonomía y clasificación de este género. El PDA es un medio que ayuda a la preservación de los aislados; sin embargo, por su alto contenido de carbohidratos promueve las mutaciones de algunas especies, disminuye la esporulación y puede alterar la forma de la conidia, mientras que CLA es un medio bastante pobre en nutrientes, el cual estimula la esporulación más que el crecimiento micelial, además permite la observación y el desarrollo de forma natural en el hospedero o sustrato en que se encuentre el hongo. No necesariamente se deben utilizar las hojas de clavel para la esporulación y las características naturales del hongo, puesto que cualquier sustrato vegetal estéril y libre de agroquímicos es propicio para su desarrollo; sin embargo, en este estudio fueron utilizadas hojas de clavel puesto que las claves de identificación empleadas, se basan en las características microscópicas desarrolladas por Fusarium en CLA. También, la luz es un factor adicional que se utiliza tanto en PDA como en CLA para la pigmentación y esporulación de las colonias (Nelson et al. 1983; Seifert 2000; Burgess et al. 1994).
Se aislaron 13 especies de Fusarium: F. sambucinum, F. graminearum, F. compactum, F. equiseti, F. avenaceum, F. longipes, F. reticulatum, F. oxysporum, F. heterosporum, F. culmorum, F. lateritium, F. coccophilum y F. crookwellense. De las 168 colonias de Fusarium aisladas sólo siete no se lograron identificar a nivel de especie (4%) (Fig. 2). Para el aislamiento inicial de las colonias no identificadas se utilizó MC y CYA, observándose la formación de macroconidias en media luna características del género Fusarium. Estas colonias se repicaron a CLA y PDA para su respectiva clasificación a nivel de especie; sin embargo, en estos medios no se logró la esporulación de las colonias inicialmente. En posteriores repiques se obtuvo formación de macroconidias atípicas (ensanchamiento de las células apicales, algunas no presentaban formación de septaciones marcadas, desarrollo de clamydoconidias al interior de las células intermedias de las macroconidias y macroconidias de tamaños superiores a los señalados), las cuales no correspondían a ninguna de las especies registradas a la fecha.
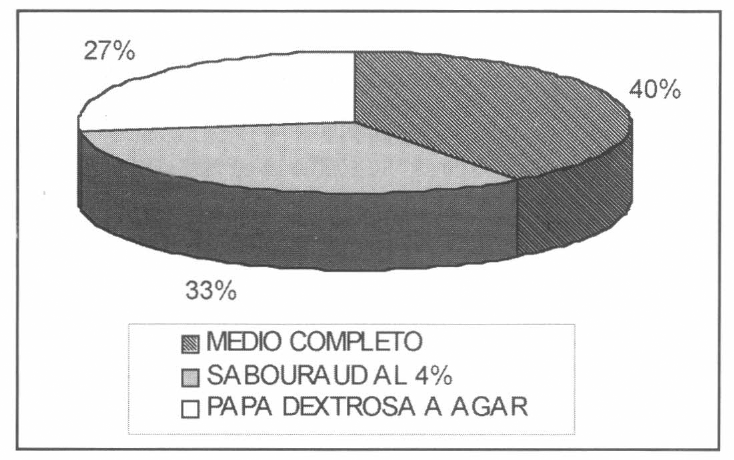
Porcentaje de colonias de Fusarium aisladas de T. vaporariorum en MC, SDAY/4 y PDA.
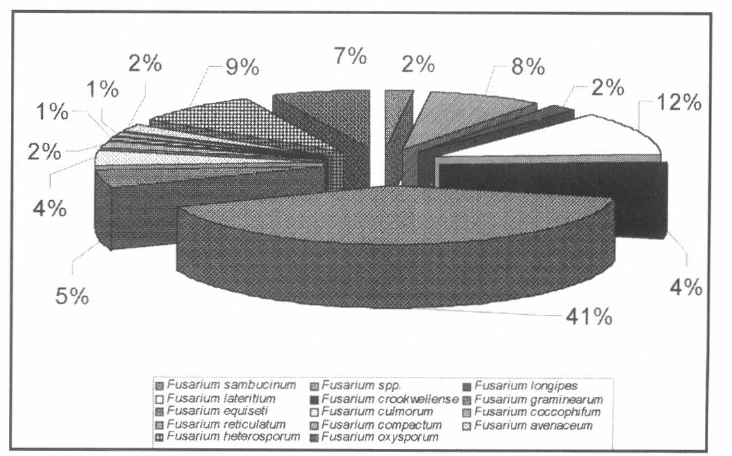
Porcentaje por especies de Fusarium aisladas de T. vaporariorum de la Provincia de García Rovira, Santander.
La mayoría de las especies del género Fusarium son notoriamente inestables y se degeneran rápidamente después de múltiples repiques, siendo ésta la limitación más común en la identificación de este género (Nelson et al. 1983; Pitt y Hocking 1997); además de otras causas como la utilización de medios de cultivos demasiados ricos en su composición, la acumulación de dióxido de carbono al cerrar la caja de petri, mutaciones espontáneas, contaminación bacteriana o cambios genéticos (Seifert 2000).
Las especies de Fusarium con mayor número de colonias aisladas fueron: F. equiseti (41 colonias: 67%), F. compactum (20 colonias: 12%), F. oxysporum (15 colonias: 9%), F. sambucinum (14 colonias: 8%) y F. crookwellense (12 colonias: 7%) debido a que son especies de amplia distribución por el mundo, en zonas templadas y subtrópicos, encontrándose en suelos, materiales vegetales y algunos insectos (Burgess et al. 1994; Seifert 2000; Nelson et al. 1983, Pitt y Hocking 1997; Samson et al. 1995; Humber 1992). F. equiseti fue la especie predominante en el aislamiento posiblemente por su alta tasa y velocidad de crecimiento, lo cual favoreció su adaptación en los tres medios de cultivo propuestos e inhibió el desarrollo de otras especies de Fusarium. La mayoría de especies de Fusarium aisladas no presentaron microconidias, excepto algunas colonias de F. oxysporum y F. sambucinum (15,38%).
Dentro de las especies de Fusarium que la literatura registra como entomopatógenas y que se aislaron en este estudio, se encuentran: F. avenaceum en masas de huevos de Lepidoptera: Lymantriidae en Estados Unidos; F. coccophilium en Homoptera: Diaspididae en Washington (Estados Unidos); F. lateritium en adultos de Hymenoptera: Ichnumonidae en Polonia y en Homoptera: Psyllidae Nueva Guinea; F. oxysporum en pupa de Diptera: Anthomyiidae Canadá y F. sambucinum en el quinto ínstar larval de Lepidoptera: Lymantriidae en Virginia (Estados Unidos) (Humber 1992), lo cual motiva a estudiar y comprobar la patogenicidad de estas especies y su mecanismo de infección en mosca blanca para que proporcionen nuevas alternativas en el control biológico de estos insectos plaga.
Conclusiones
El mayor número de colonias de Fusarium aisladas se obtuvieron en MC (40%) posiblemente debido a que este medio posee compuestos que proporcionan potasio, fósforo, sodio, magnesio, nitrógeno entre otros, elementos nutricionales muy importantes para el desarrollo de hongos (principalmente para mohos), los cuales no están presentes en PDA ni en SDAY/4.
A partir de este estudio se concluye que el género Fusarium representa un porcentaje significativo (27,45%) de la micobiota de Trialeurodes vaporariorum de la zona de estudio, encontrándose una amplia variedad de especies (13 diferentes), de las cuales predominan F. equiseti y F. compасtum. F. equiseti presenta abundantes clamidoconidias, característica que le permite resistir y desarrollarse en zonas de climas variados, como es el caso de la zona de estudio.
Es importante resaltar que dentro de las especies aisladas se encuentran, F. avenaceum, F. coccophilium, F. lateritium, F. oxysporum y F. sambucinum, conocidas como entomopatógenas; sin embargo, se requiere establecer su posible utilización como biocontroladores, puesto que algunas de ellas son productoras de micotoxinas e incluso fitopatógenas para algunos cultivos de la zona, como es el caso de F. oxysporum.
Recomendaciones
En el planteamiento de investigaciones relacionadas con organismos entomopatógenos se recomienda tener en cuenta las variables controladas y no controladas tanto en campo como en laboratorio, las condiciones ambientales del sitio de muestreo y la realización de réplicas, debido a que estos factores pueden influir directa o indirectamente en el aislamiento e identificación del patógeno, así como en los resultados obtenidos de los datos recolectados.
Además, se sugiere realizar estudios encaminados a evaluar el efecto de los componentes nutricionales de cada uno de los tres medios de cultivo utilizados en el aislamiento primario de las especies de Fusarium asociadas con T. vaporariorum; evaluar el efecto del desinfectante (hipoclorito de sodio al 0,4%) usado en estas especies registradas como entomopatógenas de T. vaporariorum; determinar mediante bioensayos la patogenicidad de las especies de Fusarium y sus posibles mecanismos de infección en el insecto (invasión cutánea o producción de metabolitos tóxicos) y establecer el impacto ecológico de las especies de Fusarium en los cultivos de la región en estudio.
Agradecimientos
Los autores expresan sus agradecimientos al Doctor Richard A. Humber (Collection of Entomopathogenic Fungal Cultures, Cornell University) por su aporte bibliográfico y contribución científica a esta investigación; a la Universidad Industrial de Santander "UIS" especialmente a las Escuelas de Bacteriología y Laboratorio Clínico por su asesoría, aceptación y colaboración y a la Compañía Colombiana de Tabaco por su apoyo logístico y económico, en particular al Doctor José Daniel Tinoco Gutiérrez.
