Abstract
Summary
Insects of the genus Rhodnius belonging to the domestic and silvatic habitat were analyzed by molecular techniques to determine the reinfestation possibility of the human dwellings to guide the control programs and epidemiological survellaince. Dendrographs, Fst (0.2421) and Nm (1.05) were generated using informatic packages. These results suggest that genetic flow between the two populations is null, that is to say, they are isolated. However, 4 individuals captured in the houses, were characterized as belonging to the wild population when rDNA was amplified, and also this individuals grouped inside of the wild population cluster, this also suggest a possible migration of wild individuals to domiciliated areas, therefore it is recommended a periodic monitoring of human dwellings to prevent possible reinfestations.
Introducción
Rhodnius prolixus (Stal, 1859) es un insecto de gran importancia epidemiológica. En Colombia es el vector principal de Trypanosoma cruzi, agente causal de la enfermedad de Chagas que afecta cerca de 16 millones de personas en Latinoamérica (WHO 2001). En el país, el 3,3% de la población se encuentra infectada y un 10% bajo riesgo de contraer la infección (Guhl y Schofield 1996).
La enfermedad de Chagas, a pesar de existir solamente en las Américas, es considerada por el Banco Mundial como una de las enfermedades parasitarias más importantes en el mundo, ocupando el tercer lugar después de la malaria y la esquistosomosis (Schofield 1997).
Actualmente, la forma de control más efectiva es mediante la interrupción de la transmisión vectorial y transfusional del parásito, por lo cual se diseñaron y desarrollaron en varios países del cono sur, programas de control vectorial basados en la erradicación del insecto de las viviendas por medio de rociamiento químico de acción residual (WHO 1997).
Se han encontrado en Colombia ejemplares de Rhodnius colombiensis, los cuales se encuentran en el hábitat silvestre (Moreno et al. 1999). Esta especie está muy relacionada con Rhodnius prolixus hasta el punto de ser considerada, hasta hace pocos años, como una población de Rhodnius prolixus, el cual es el vector más importante de la enfermedad de Chagas en Colombia. Es posible encontrar que las viviendas intervenidas presenten reinfestación por estos triatomíneos. Estas dos especies son morfológicamente similares, de ahí la importancia de llevar a cabo estudios moleculares que provean herramientas para identificar el origen de los insectos reinfestantes y así orientar apropiadamente los programas de control o vigilancia epidemiológica.
Debido a que posee espaciadores internos que evolucionan rápidamente y a que se compone de repeticiones en bloque que de inicio dan una considerable cantidad de ADN blanco, el ADN ribosomal utilizando la técnica de PCR, ha sido ampliamente usado en el estudio filogenético de artrópodos vectores de enfermedades (Porter y Collins 1991). Puesto que las regiones variables del ADN ribosomal están flanqueadas por regiones altamente conservadas, es posible utilizar iniciadores universales ITS (White et al. 1990), para amplificar las regiones variables, las cuales pueden llegar a diferir entre especies de un mismo género e incluso entre poblaciones de una misma especie permitiendo diferenciarlas (Paskewitz y Collins 1990).
La técnica de RAPDs ha sido usada en estudios para diagnóstico de especies, diferenciación de poblaciones y mapeo genético (Williams et al. 1991). Las ventajas de esta técnica son básicamente las mismas que para un PCR clásico: la poса cantidad de ADN necesaria, la detección no radioactiva de los productos y el tiempo de procesamiento corto. Adicionalmente, no es necesario conocer la secuencia o partes de ésta para llevar a cabo la reacción (Apostol et al. 1993).
En estudios previos desarrollados por nuestro grupo de investigación, se comprobó la utilidad de estas dos técnicas moleculares para diferenciar poblaciones silvestres y domésticas del género Rhodnius (Jaramillo et al. 2001).
El objetivo principal de este trabajo fue determinar la posibilidad de reinfestación por parte de la población silvestre y probar una herramienta para diferenciar entre individuos silvestres y domiciliados y de esta manera orientar apropiadamente los programas de control y vigilancia epidemiológica. Este trabajo tuvo lugar en el Centro de Investigaciones en Microbiología y Parasitología Tropical de la Universidad de los Andes, Bogotá, Colombia.
Materiales y Métodos
Recolección de insectos
La colección de insectos de origen silvestre y domiciliado se llevó a cabo en el municipio de Coyaima en el departamento del Tolima, ubicado a 1.392 msnm con una temperatura media anual de 28°C.
Los insectos estudiados fueron provistos por el Centro de Investigaciones en Microbiología y Parasitología Tropical, CIMPAT de la Universidad de los Andes y el Laboratorio de Parasitología de la Universidad del Tolima.
Población domiciliada
Se procesaron 39 individuos del género Rhodnius, capturados dentro de viviendas de Coyaima-Tolima. Se consideraron poblaciones domiciliarias a los insectos capturados dentro de viviendas, en donde además se encontraron individuos de diferentes estadios, huevos y heces, lo cual evidencia la permanencia del insecto en la vivienda humana.
Población silvestre
Se procesaron 41 individuos capturados en hábitat silvestres cercanos a viviendas humanas (500 m aprox.), específicamente sobre palmas Athalea butyracea.
Identificación morfológica de los insectos
La diferenciación morfológica de las dos especies suele dificultarse. Después de capturar varios cientos de Rhodnius colombiensis en palmas de Attalea butyraceae y varios miles de R. prolixus dentro de las viviendas humanas, se ha notado que la coloración del cuerpo de R. prolixus es un poco más oscura que la coloración de R. colombiensis; sin embargo, la determinación morfológica definitiva se logra mediante disección y análisis comparativo de las siguientes estructuras fálicas: el falosoma, el proceso del falosoma, los procesos de la conjuntiva 2 y 3, el proceso del endosoma y el proceso mediano del pigóforo, todas estas estructuras examinadas en individuos adultos, de conformidad con la descripción de Moreno et al. (1999).
En el municipio de Coyaima (Tolima), Jaramillo et al. (2001) efectuaron la diferenciación morfológica de 62 R. prolixus capturados en el interior de las viviendas y 62 R. colombiensis capturados en palmas de Attalea butyraceae siguiendo las características de la genitalia, descritas por Moreno et al. (1999). Las diferencias morfológicas entre las dos especies fueron consistentes con las diferencias moleculares observadas previamente por los autores utilizando análisis de RAPD y amplificación de rDNA. Por las razones anteriores, se podría esperar en la región de Coyaima (Tolima) que cualquier individuo capturado en Attalea butyraceae corresponda a R. colombiensis o cualquier individuo capturado en el interior de las viviendas humanas corresponda a R. prolixus. Para el desarrollo del presente trabajo, se capturaron 39 individuos en el interior de las viviendas y 41 individuos en palmas de A. butyraceae. Los insectos se rotularon como R. prolixus y R. colombiensis sin estudio previo de la genitalia, con la finalidad de utilizar herramientas moleculares y verificar si todo individuo capturado en palmas o en el domicilio, corresponde respectivamente a R. prolixus y a R. colombiensis o, por el contrario, existe movimiento de individuos silvestres hacia las áreas domiciliares o viceversa. Utilizando esta valiosa herramienta, se caracterizaron los individuos colectados en este estudio como se describe posteriormente.
Extracción de ADN
El ADN se obtuvo a partir de las patas de los especímenes después de haber sido trituradas con un dispositivo plástico (pellet pestle) especial para tubos de microcentrífuga de 1,5 ml.
La extracción de ADN se llevó a cabo con el kit comercial QIAmp tissue kit de QIAGEN siguiendo el protocolo recomendado por el fabricante con algunas modificaciones como dejar en proteinasa K toda la noche y resuspender en un volumen menor (200 ml) de TE, con el fin de concentrar la muestra.
Cuantificación de ADN
Las cuantificaciones se hicieron con base en lecturas espectrofotométricas empleando el espectrofotómetro Beckman "Du-Series 60" que opera en un rango entre 200 y 900 nm. Este modelo utiliza módulos llamados "soft-pacs", que contienen programas de aplicación especializados. En este caso se utilizó el "soft-pac" para ácidos nucleicos.
Amplificación azarosa de polimorfismos de ADN - RAPDS
Las reacciones se llevaron a cabo utilizando el kit Ready to Go RAPD de Pharmacia®, con los iniciadores 1, 2, 5 y 6, cuya secuencia aparece en la tabla 1.
Se rehidrató la perla del kit con 19 ul de agua destilada estéril y 5 ul de iniciador. Después de mezclar en un vortex, se dividió el volumen en 4 tubos eppendorf de 0,5 ml y a cada uno se le agregaron 2 ul de ADN para un volumen final de 8 ul.
Perfil térmico
Se empleó el siguiente perfil térmico, recomendado en el kit "Ready to go RAPD de Pharmacia": 95°C, 5 min; (95°C, 1 min; 36°C, 1 min; 72°C, 2 min) 45 ciclos. Los RAPDS se corrieron en una máquina de PCR PTC-100 MJ-Research. No hubo necesidad de ajustar ninguna parte del ciclo puesto que se obtuvieron buenos resultados desde el principio.
Detección de amplicones
Se realizó mediante electroforesis en geles de poliacrilamida al 6% teñidos con nitrato de plata. Para la tinción de los geles se realizaron dos procedimientos. El primer procedimiento comienza con la fijación de los productos mediante una solución etanol-acética, seguida de la tinción con plata, la cual se revela con formaldehído disuelto en solución básica (Vallejo, comunicación personal).
El segundo procedimiento se hizo utilizando el Kit de tinción de Amersham Pharmacia® o "DNA Silver Staining Kit" siguiendo el protocolo sugerido por el fabricante. Cabe anotar que con este kit se obtuvieron resultados mejores que con el primer procedimiento.
Secuencia de los iniciadores empleados en la reacción de RAPD
Análisis de los geles
Se compararon las bandas más intensas de cada gel y se construyó una matriz de datos de acuerdo con Welsh et al. (1992). La matriz de 0 y 1 se usó para construir otra matriz empleando el índice de Disimilaridad de Jaccard. Esta última se colapsó para construir dendrogramas empleando el algoritmo UPGMA (Unweighted Pair Group with Averaging) mediante el software SYNTAX (Podani 1993). Las matrices también fueron procesadas con el sofware RAPDPLOT (Kambhampati et al. 1992). Este programa calcula similitudes entre las muestras utilizando los índices de similitud de Nei y Li (1985) o un puntaje obtenido por el porcentaje de ceros y unos compartidos cuando se utilizan marcadores de RAPDs.
Una vez realizados los dendrogramas se calculó la tasa de migración efectiva (Nm) a partir de la estimación del F estadístico (Fst) empleando el programa POPGENE versión 1.31 diseñado por Francis C. Yeh y Rong-cai Yang de la Universidad de Alberta (1999).
Este programa calcula el Fst según el método de Wright, el cual está dado por la ecuación Fst = Sβ/(q(1-q)), donde Sβ, es la varianza en la frecuencia de un alelo RAPD entre las subpoblaciones y q es el promedio de la frecuencia entre todas las subpoblaciones.
Reacción en cadena de la polimerasa para amplificar ADN ribosomal (rDNA - PCR)
Debido a que la secuencia de los genes ribosomales de algunas especies de Rhodnius se conocieron hasta hace muy poco (Monteiro et al. 2000), pero se sabe que estos genes son conservados entre las especies, se utilizaron iniciadores "universales" que anillan en regiones específicas del gen. Las parejas de iniciadores utilizadas fueron ITS1-ITS4 e ITS5-ITS4, cuya secuencia es mostrada en la tabla 2.
Las reacciones se hicieron utilizando el kit ampli-Taq DNA polimerasa de GIBCO BRL. Estas reacciones se llevaron a cabo en una máquina de PCR PTC-100 MJ-Research.
Los volúmenes y concentraciones utilizados en la reacción de PCR se muestran en las tablas 3 y 4. Estos se estandarizaron en estudios previos por el grupo de investigación (Jaramillo et al. 2001).
Secuencias de los iniciadores empleados en las reacciones de PCR.
Concentración y cantidad de reactivos utilizados para las amplificaciones con los iniciadores ITS 5 - ITS 4.
Concentración y cantidad de reactivos utilizados para las amplificaciones con los iniciadores ITS 1 - ITS 4.
Perfil térmico
Se hizo un PCR "touchdown", el cual permite la realización de la reacción abarcando un rango de temperaturas de anillaje. Se utilizó esta modalidad de PCR puesto que se trabajó con iniciadores universales diseñados sobre secuencias consenso de especies diferentes a R. prolixus. El perfil térmico utilizado fue el siguiente: 1. 94°C, 1 min; 2. 92°C, 30 seg; 3. 55°C 30 seg (-0.5°C/ciclo); 4. 72°C, 40 seg; 5. 10 veces desde el paso 2; 6. 92°C, 30 seg; 7. 50°C, 30 seg; 8. 72°C, 1 min; 9. 23 veces desde el paso 6; 10. 4°C.
Detección de los productos
La visualización de los productos se realizó en geles de agarosa al 1,5% teñidos con bromuro de etidio (1 ug/ml). Después de que se completó el PCR, el volumen de reacción de 25 µl se mezcló con buffer de carga (6X) para completar un volumen de 30 µl. Se sembraron 15 µl de muestra y 5 µl de marcador de peso molecular de 100pb marca PROMEGA, luego se realizó la electroforesis y se visualizó mediante luz ultravioleta.
Análisis de los geles de agarosa
Las fotos de los geles se tomaron con una cámara fotográfica digital marca photoPC700, se capturaron con el programa photoPC700 y analizaron mediante el programa photo editor. Las imágenes digitalizadas se analizaron y el tamaño de las bandas se calculó mediante una regresión lineal.
Resultados
Cuantificación de ADN
Las concentraciones de los ADN extraídos, variaron en un rango entre 0,010 ng/µl y 10 ng/µl.
Rapds
La amplificación de marcadores RAPD-PCR, utilizando los iniciadores 1, 2, 5 y 6 en las poblaciones evaluadas, se caracterizó por presentar patrones de bandeo definidos para cada una de las poblaciones (Fig. 1).
Existen diferencias entre los patrones de cada población. El análisis de comparación de los patrones de amplificación y clusters sugiere ausencia de flujo genético entre las poblaciones. El concepto del análisis utilizado es estimar la distancia genética calculando el índice de disimilaridad de Jaccard entre todos los pares de individuos a partir de las matrices binarias y construir dendrogramas por comparación entre todos los individuos con el algoritmo UPGMA, utilizando el programa SYNTAX (Fig. 2).
Se calculó el F estadístico (Fst), introducido inicialmente por Wright (1951) como medio para describir la estructura de apareamiento de poblaciones naturales. Con el programa POPGENE se obtuvo un valor de Fst = 0.3387. A partir del Fst se puede calcular la tasa de migración, cuyo valor fue Nm = 0.9763.
Pcr-Rdna
Tamaño de las bandas
Utilizando la pareja de iniciadores ITS5-ITS4, los insectos de la población domiciliada presentan una banda de 1.115 pb y los de la población silvestre presentan una banda a 1.175 pb (Fig. 3).
Utilizando la pareja de iniciadores ITS1-ITS4, todos los insectos amplificados para la población domiciliada muestran una banda de 1.102 pb, mientras que la banda amplificada para la población silvestre tiene 1.171 pb (Fig. 4).
En algunos individuos domiciliados aparece una banda adicional de 533 pb al igual que en algunos individuos silvestres donde se observa una banda a 582 pb cuando se amplifica con los iniciadores ITS 5 - ITS 4 (Fig. 3, carril 2).
Igualmente, cuando se amplifica con los iniciadores ITS 1 - ITS 4 en algunos individuos de las dos poblaciones aparece una banda adicional de aproximadamente 556 pb.
Discusión
El análisis de los dendrogramas sugiere que se trata de dos poblaciones con ausencia de flujo genético, debido a que la primera ramificación que se genera agrupa a todos los individuos de una misma población en un cluster. Hay 4 individuos que, aunque fueron colectados dentro de las casas, agrupan en el cluster de la población silvestre y que al amplificar el rDNA presentan una banda de 1.171 pb con los iniciadores ITS 1 - ITS 4 y de 1.175 pb con los iniciadores ITS 5 - ITS 4, lo que indica que estos 4 insectos pertenecen a la especie R. colombiensis. La vivienda donde se encontraron estos 4 insectos había sido fumigada hace un año con insecticidas de acción residual contemplados en el control vectorial de la enfermedad de Chagas. Este hallazgo es muy importante puesto que indicaría un posible movimiento de individuos silvestres hacia áreas domiciliares, los cuales eventualmente podrían radicarse en la vivienda; sin embargo, no es un indicativo de que exista flujo genético entre las poblaciones. Una vez formada la matriz, se calculó la tasa de migración efectiva (Nm) y el Fst. El valor máximo posible de un Fst estadístico es 1, entre mayor sea el valor más diferenciadas son las poblaciones; aunque pueden existir valores negativos, estos son interpretados como Fst = 0 (Long 1986). Los valores obtenidos para Nm indican el número aproximado de individuos que migran de una población a otra en una generación. Para mantener homogeneidad genética entre poblaciones se requiere mínimo de un individuo migrante por generación, a lo cual corresponde un Fst de 0,2. Valores de Fst superiores a 0,2 indican aislamiento genético entre las poblaciones. El valor promedio del Fst, calculado para las poblaciones estudiadas, fue 0,3387 a partir del cual se estima una tasa de migración efectiva promedio de 0,9763 individuos por generación, lo cual es insuficiente para mantener las dos poblaciones genéticamente homogéneas (Apostol et al. 1996). Es importante aclarar que estos valores fueron calculados sin tener en cuenta los cuatro individuos silvestres encontrados en las casas. También se calculó el Fst teniendo en cuenta estos insectos y se obtuvo un valor de 0,2421 con un Nm= 1,05. Aunque este valor es mayor que uno es todavía muy bajo, además, el Fst está indicando que no se puede considerar que exista flujo genético entre las poblaciones. Parece ser que estos cuatro individuos no afectan lo suficiente el valor del Fst, aunque sí se obtiene un número más bajo en este caso.
Los valores de Nm y Fst se pueden interpretar por comparación con otros valores publicados (Bossart y Scriber 1995).
Para Aedes aegypti se registró un valor de Nm = 11,7 (Apostol et al. 1996) y para mariposas de la especie Papilo glaucus se halló un valor de Fst = -0,0032 (Bossart y Scriber 1995). Tanto A. aegypti como P. glaucus presentan flujo genético. Comparando estos valores con los obtenidos para las poblaciones estudiadas, sugiere que se trata de dos poblaciones con ausencia de flujo genético actual.
Por lo general, las poblaciones silvestres de la mayoría de especies, presentan mayor variabilidad que las poblaciones domiciliadas de la misma especie (Guhl y Schofield 1996). En estudios preliminares se ha encontrado que la población silvestre bifurca dentro del dendrograma en un valor mayor a la población doméstica (Jaramillo et al. 2001). Esto puede evidenciarse también en los resultados obtenidos, debido a que el cluster de la población silvestre bifurca 0,05 unidades superior al cluster de la población doméstica. Adicionalmente, se puede observar en el dendrograma que la población silvestre presenta más ramificaciones que la población doméstica (Fig 2). Este resultado implica que la población silvestre presenta mayor variabilidad genética. Este aspecto es de gran relevancia con respecto al control de la transmisión de la enfermedad, debido a que podría influir positivamente en los resultados de procesos de rociamiento químico porque la menor variabilidad por parte de la población doméstica podría implicar una menor posibilidad de respuesta o resistencia a insecticidas empleados en los programas de control vectorial (Schofield et al. 1999).
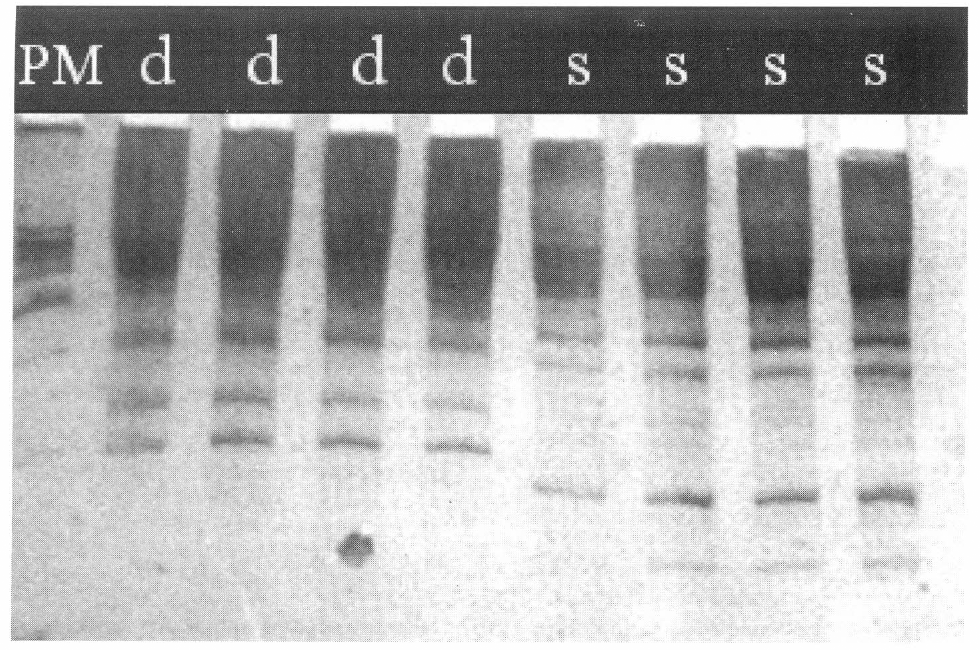
Patrón de amplificación generado por el primer RTG 2. Gel de poliacrilamida al 6%, teñido con Nitrato de Plata. d: Patrón de amplificación de insectos domiciliados. s: Patrón de amplificación de insectos silvestres. PM: Marcador molecular. Carril 1: Marcador Peso Molecular. Carril 2-5: R. prolixus. Carril 6-9: R. colombiensis.
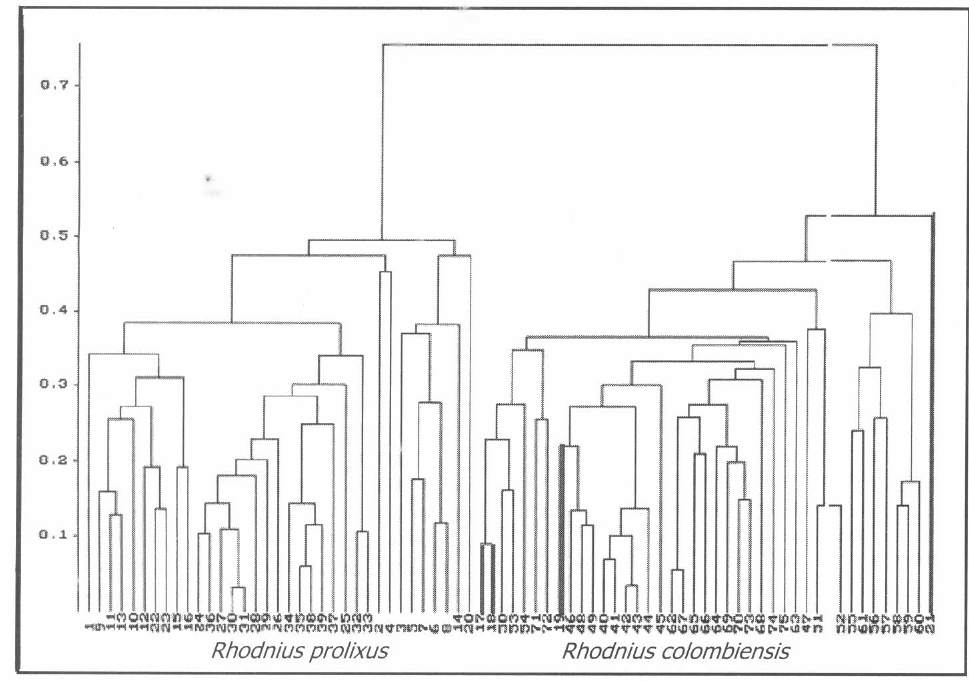
Dendrograma generado para poblaciones silvestre y domiciliada de Rhodnius en Colombia. Los valores en el eje y indican el coeficiente de disimilitud y los del eje x los individuos analizados. Las líneas gruesas corresponden a insectos encontrados dentro de las casas que agrupan en la población silvestre.
Estos resultados son importantes puesto que corroboran lo encontrado por Moreno et al. (1999), quienes indicaron que la considerada población silvestre correspondía a una especie diferente que se denominó Rhodnius colombiensis.
Al emplear la técnica de PCR en genes ribosomales, de los insectos silvestres y domésticos amplificados con las dos parejas de iniciadores, algunos presentan dos bandas, una más pequeña que la otra. Las dos bandas son de mayor tamaño para el silvestre que para el doméstico (aproximadamente 50pb). La presencia de la segunda banda no es constante y en algunos individuos es muy tenue.
Las dos parejas de iniciadores amplifican parte de la región ribosomal menor (18S), el espaciador interno transcrito 1 (ITS1), la región 5.8S, el espaciador interno transcrito 2 (ITS2) y parte del gen 28S. El fragmento amplificado con la pareja de iniciadores ITS 1 - ITS 4, como es de esperarse, tiene una longitud menor a la región amplificada por los iniciadores ITS 5 - ITS 4, puesto que el iniciador ITS 5 está ubicado más hacia el extremo 5' del gen 185 que el iniciador ITS 1. Utilizando las dos parejas de iniciadores se observa una clara diferencia entre las dos poblaciones de Rhodnius.
Conclusiones
Se empleó la técnica RAPDs la cual permite evidenciar polimorfismos de ADN con relativa facilidad aún en insectos pequeños o partes de los mismos como en este estudio, así mismo esta técnica revela diferencias en poblaciones con ausencia de variabilidad alozímica (Black 1993).
Se pudo establecer que los oligonucleótidos RTG 1-6 son aptos para la finalidad de este estudio, pero solamente se utilizaron los iniciadores RTG 1, 2, 5 y 6, pues se obtiene un buen bandeo y suficientes marcadores para el análisis. Cada uno de estos iniciadores generó un patrón de amplificación el cual podría servir en un futuro como base para el análisis y comparación de nuevos ejemplares de Rhodnius para establecer el origen silvestre o domiciliado de los mismos.
Las variaciones encontradas entre los individuos de las dos poblaciones, dado que se empleó la técnica de RAPDs y asumiendo que tienen un ancestro común, son debidas a cuatro tipos de mutaciones que esta técnica revela: Mutaciones puntuales en el sitio de anillaje, inversión en uno de los sitios de anillaje, inserción y deleción dentro de la región amplificada (Black 1993).
Teniendo en cuenta que uno de los propósitos de esta investigación fue validar marcadores moleculares que permitan diferenciar al insecto silvestre del doméstico, cuya morfología es muy similar, se aprecia que la realización del PCR utilizando iniciadores ribosomales es suficiente para este propósito. La técnica de PCR tiene la ventaja de que es relativamente rápida ya que el procedimiento involucra la extracción del ADN genómico, la preparación de las reacciones de PCR y la electroforesis de los productos en geles de agarosa teñidos con bromuro de etidio. Además, debido a que el PCR es un proceso de amplificación, requiere pocas cantidades de ADN.
El hecho de poder distinguir las dos poblaciones a través de PCR permite definir con seguridad, después de una reinfestación, el origen del insecto encontrado y de esta manera tomar las medidas de prevención adecuadas.
Aunque la ausencia de flujo genético entre las poblaciones de Rhodnius, parece indicar que la población silvestre no representa riesgo epidemiológico en el proceso de transmisión de la enfermedad de Chagas, es importante tener en cuenta que se encontraron cuatro individuos silvestres dentro del domicilio, por lo cual el monitoreo periódico de las viviendas es de suma importancia para evaluar la migración de insectos hacia las viviendas. El desarrollo de marcadores morfométricos, bioquímicos y moleculares que permitan la caracterización de las poblaciones silvestres, serán de gran utilidad para la vigilancia epidemiológica futura con el fin de detectar cualquier cambio adaptativo hacia los ambientes peridomésticos y domésticos en esta región del país. La reducción en la variabilidad de las poblaciones domésticas mencionadas anteriormente, tiene consecuencias muy importantes en las medidas de control. Una variabilidad reducida implica que cualquier medida de control que funcione en una localidad dada, podría ser efectiva cuando se aplique en otras. Además, la selección hacia atributos como resistencia a insecticidas es mucho menor, debido a que el pool genético del cual puedan surgir genotipos resistentes tiene una variabilidad limitada (Schofield et al. 1999). En cierta forma se podría afirmar que debido a estas razones estos insectos son vulnerables a las medidas de control.
El hecho de haber encontrado individuos R. colombiensis reinfestantes indicaría que es necesario poner más atención a los programas de fumigación. Las posibles reinfestaciones posiblemente se deban a que la vigilancia no ha sido efectiva. Desafortunadamente la vigilancia implica visitas y contacto frecuente con las comunidades involucradas, lo que en Colombia se ha hecho difícil debido a la crítica situación de orden público por la que el país ha atravesado los últimos años. Además, a pesar de que se logre controlar la transmisión vectorial dentro de las casas, es importante advertir a los habitantes de la zona del peligro que se puede correr en el campo por la presencia de vectores silvestres.
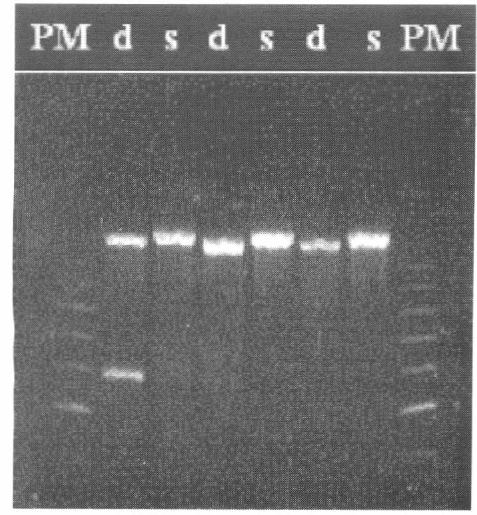
Electroforesis en gel de agarosa al 1%. Iniciadores ITS 5-ITS 4. d = Rhodnius doméstico, s = Rhodnius silvestre, PM = Marcador molecular (100pb).
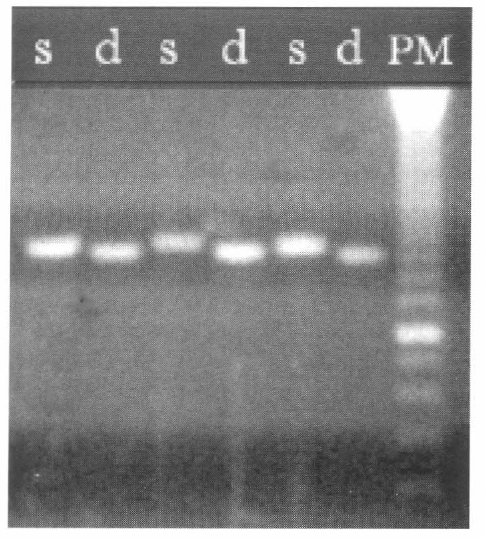
Electroforesis en gel de agarosa al 1%. Iniciadores ITS 1-ITS 4. d = Rhodnius doméstico, s = Rhodnius silvestre, PM = Marcador molecular (100bp).
Agradecimientos
En especial se agradece a la Fundación para la Promoción de la Investigación y la Tecnología por la financiación completa de este trabajo.
