Abstract
Summary
In the last decade Tecia solanivora Povolny has become one of the most significant pest in Colombian potato growing areas. In the past T. solanivora control strategies have been developed using chemical pesticides, although recently some alternative biological control and crop management practices have been used. The use of entomopathogenic microorganisms such as baculovirus and bacteria for T. solanivora control offers a new useful tool for developing an integrate pest management program. Earlier works explored the potential use of Bacillus thuringiensis strains in T. solanivora control. However, Bt Cry proteins specific to this insect have not been yet identified. In accordance with this, we analyzed the specificity of 7 Bt Cryl proteins (Cry1Aa, Cry1Ab, Cry1Ac, Cry1Ba, Cry1Ca, Cry1Da and CrylEa) toward the first instar T. solanivora larvae. At the same time we designed an easy and reproducible bioassay method based in natural diet. Proteins were evaluated at 4 µg/cmβ dose, which was the LC50 of HD1 strain, used as a positive control in bioassays. Results showed a higher toxicity of Cry1Ac compared with the other Cryl proteins evaluated. Cry1Ac caused a 20% average mortality while no more than 7% were obtained with the rest of the proteins. In order to confirm these findings we evaluated HD73 strain which posses only Cry1Ac and Cry2A genes and recombinant E. coli strain with only Cry2A gene. As we expected, the bioassays indicated a high toxicity of HD73 and low toxicity of Cry2A protein, showing average moralities over 70% and below 10%, respectively. Results indicated that Cry1Ac is specific to T. solanivora, however, it seems that interaction with other proteins enhances CrylAc activity as observed in bioassays with HD1 and HD73 strains where Cryl proteins besides Cry1Ac are present.
Introducción
La polilla guatemalteca de la papa Tecia solanivora Povolny, desde su introducción a Colombia en 1983, se ha constituido en uno de los principales factores de pérdidas en el rendimiento de dicho cultivo. Esta plaga se registró por primera vez en 1985 y desde esa época se han incrementado sus poblaciones hasta tal punto que a finales del siglo pasado fue una de las causas de las pérdidas cercanas al 100% del total de la producción de papa en el país (Ñústez et al. 1998). En Boyacá y Cundinamarca, que son las principales zonas productoras de papa de Colombia, se han estimado daños entre el 50 y 80% en los tubérculos tanto en campo como en almacenamiento (Hernández y Varela 1998). Actualmente esta plaga se encuentra distribuida en todas las zonas productoras de papa del país y su control se ha hecho empleando principlamente insecticidas químicos con eficiencias de control menores del 50% (Andrew y Acosta 1998).
Teniendo en cuenta las limitaciones de la estrategia química para el control de T. solanivora, se han venido proponiendo otras alternativas de control tendientes al desarrollo de un esquema de manejo integrado de la plaga, involucrando elementos de control cultural, etológico y biológico (Ñústez et al. 1998). Dentro de las estrategias de control biológico se ha explorado el uso de microorganismos entomopatógenos como virus (Arias et al. 1998; Trillos 1998), hongos (Sánchez et al. 1998), nemátodos (Alvarado et al. 1998; Parada y Luque 2001) y bacterias, estas últimas evaluando cepas nativas y/o productos comerciales con la bacteria Bacillus thuringiensis, lográndose identificar cepas nativas y productos con alguna actividad tóxica contra T. solanivora (Aristizábal y Londoño 1998; Pérez et al. 1997; Tejada et al. 1998; Bosa et al. 1998, Castelblanco 2000).
B. thuringiensis es una bacteria entomopatógena con características propias que la hacen promisoria para ser introducida en programas MIP de la polilla guatemalteca de la papa; a pesar de esto, aún no se conoce cuál de las proteínas tóxicas que produce dicha bacteria es específica hacia este insecto. Se hace por lo tanto necesario realizar estudios al respecto, que permitan identificar cuál proteína Cry de B. thuringiensis presenta una actividad tóxica específica y así definir y optimizar su empleo como agente de control biológico de T. solanivora, ya sea empleándola como ingrediente activo de productos comerciales para aplicación directa o como fuente de genes para el desarrollo de plantas transgénicas resistentes a este insecto (Estrada 1997).
De acuerdo con lo anterior, el presente trabajo se orientó hacia la identificación de la o las proteínas Cry de B. thuringiensis con actividad tóxica específica hacia T. solanivora, empleando para tal fin siete proteínas Cryl y dos cepas de referencia de esta bacteria.
Materiales y Métodos
Material entomológico
El material entomológico se obtuvo a partir de una cría de T. solanivora mantenida bajo condiciones de laboratorio (60% HR y 15°C, en promedio), en el laboratorio de entomología del Instituto de Biotecnología de la Universidad Nacional de Colombia, en dieta natural consistente en tubérculos de papa pastusa. Los adultos se mantuvieron en frascos de vidrio y se alimentaron con una solución de agua-miel impregnada en un algodón. Las oviposiciones se recolectaron semanalmente y se colocaron en recipientes plásticos para esperar la emergencia de las larvas. Las larvas neonatas se emplearon en los bioensayos y para el mantenimiento de la cría.
Cepas bacterianas
Los bioensayos se realizaron empleando tres tipos de cepas bacterianas: una cepa de Bt de referencia, una cepa nativa y siete cepas recombinantes de Escherichia coli que poseen genes Cryl individuales. Las cepas de referencia empleadas, HD1 y HD73 poseen los genes cry1Aa, cry1Ab y cry1Ac la primera y crylAc y cry2A la segunda. Las cepas de E. coli presentan los genes crylAa, cry1Ab, crylAc, cry1Ba, cry1Ca, cry1Da, crylEa y Cry2A. Cada gen codifica para su correspondiente proteína Cry. Se seleccionaron estas últimas cepas por poseer de forma individual tanto los genes cry, que presenta en combinación la cepa de referencia HD1 y que han sido identificadas como activos hacia larvas de primer ínstar de T. solanivora (Pérez et al. 1997; Castelblanco 2000), como otros que potencialmente pueden tener actividad tóxica contra este insecto.
Todas las cepas se crecieron en medio líquido Luria Bertani. Las cepas de referencia se hicieron crecer hasta alcanzar una esporulación del 95%, recuperándose la biomasa por centrifugación y obteniéndose la mezcla espora-cristal después de sucesivos lavados con agua destilada-estéril. Las proteínas producidas por las cepas recombinantes se purificaron siguiendo el método de Regev et al. (1996). La proteína obtenida en ambos casos se cuantificó con el método de Lowry (Perbal 1988).
Método de bioensayo
El método del bioensayo se estandarizó mediante la realización de ensayos preliminares con la cepa de referencia HD1, en los cuales se evaluó la mortalidad de las larvas, la reproducibilidad del ensayo, la facilidad de realización y la cantidad de proteína requerida para realizar el bioensayo.
Se evaluaron tres tipos de métodos: El primero consistió en la inmersión de prismas de papa de 0,25 cm³ en las muestras a evaluar por 5 min en agitación constante. Luego los prismas se dejaron secar al ambiente y se colocaron en placas para cultivo celular de 24 pozos. En cada pozo se puso un prisma de papa y se infestó con una larva de T. solanivora. El segundo método consistió en un cilindro de papa de 1 cm de diámetro por 1,5 cm de alto, dispuesto en un vaso desechable y rodeado con parafina o agar para disminuir la superficie de alimentación del insecto. Dicha superficie se contaminó con las muestras a evaluar. Una vez seca la muestra se infestó la papa con 1 larva de T. solanivora. En el último método se empleó una dieta artificial preparada con puré de papa casero o puré comercial, adicionándole sustancias preservantes y agar para darle consistencia a la dieta (Pérez et al. 1997). La dieta se dispensó en placas de 24 pozos similares a las del primer método y se contaminó superficialmente con la muestra. Una vez seca la muestra, se infestó cada pozo con una larva de T. solanivora.
Cada ensayo se realizó por duplicado empleando 30 larvas de primer ínstar de T. solanivora por cada réplica. La lectura de los bioensayos se realizó a los 10 días, contabilizando el número de larvas muertas en cada método evaluado.
Determinación de las concentraciones letales de la cepa HD1
Empleando el método de bioensayo seleccionado se realizaron bioensayos para determinar las concentraciones letales 10, 50 y 90 de la cepa de referencia HD1. Para tal fin, se realizó un bioensayo empleando 7 dosis de la cepa y un testigo relativo con agua destilada. Se emplearon 48 larvas por tratamiento con dos repeticiones cada uno y el ensayo se hizo por duplicado. Se realizó la lectura del bioensayo a los 7 días, determinando el número de larvas muertas por dosis. Los datos obtenidos se procesaron mediante el paquete estadístico PROBIT POLO-PC.
Evaluación de las proteínas Cryl
Las proteínas Cryl y la cepa HD73 se evaluaron con el método seleccionado, empleando la dosis obtenida como CL50 de la cepa de referencia HD1. En cada ensayo se emplearon 48 larvas por tratamiento y tres repeticiones de cada uno. Así mismo, se utilizó un tratamiento testigo consistente en la solución buffer empleada en la purificación de las proteínas evaluadas. La lectura del bioensayo se realizó a los 7 días contabilizando el número de larvas muertas y los respectivos porcentajes de mortalidad con cada proteína. Se empleó un diseño de bloques al azar. Los datos obtenidos como número de individuos muertos por tratamiento se transformaron como X+1. Los datos transformados se sometieron a análisis de varianza y prueba de comparación múltiple de Duncan con α de 0.05.
Resultados y Discusión
Método de bioensayo
El método de inmersión de los prismas en la suspensión de la muestra se evaluó empleando una suspensión de liofilizado de B. thuringiensis, cepa HD1, a las concentraciones de 25 y 100 ug/ml. Los valores promedios de mortalidad obtenidos correspondieron a 68,3 ug/ml y 91,4 ug/ml, respectivamente. El análisis de varianza indicó que no hubo diferencias significativas entre las réplicas pero sí entre las dosis (P<0.01, n=30). El coeficiente de variación para el bioensayo fue de 8,2%, siendo aceptable para los bioensayos con B. thuringiensis (Dulmage 1981; Lecuona 1996). De acuerdo con los resultados obtenidos, este método de bioensayo presentó buenas perspectivas para ser empleado en las evaluaciones posteriores.
En los ensayos con parafina se emplearon 60 unidades por tratamiento y el mismo número de larvas de primer ínstar de T. solanivora. En el ensayo con parafina la preservación de la dieta fue buena en todos los tratamientos y hubo un coeficiente de variación aceptable del 9,0%. Sin embargo, no se observaron diferencias entre las dosis evaluadas (2,5 y 25 ug de proteína/cmβ) y el testigo (P<0,01, n=60). Esto se debió a que en algunos casos se presentó separación de la parafina de la papa, dejando espacios por donde las larvas pudieron consumir dieta sin toxina. Así mismo, este método resultó bastante dispendioso lo cual causa errores de manipulación y por consiguiente un incremento en el error experimental.
En el ensayo con agar la dieta también se preservó muy bien y el coeficiente de variación fue del 10,9%. Igual que como sucedió con el método anterior, no se observaron diferencias significativas entre las dos dosis evaluadas y el testigo (P<0,01). Además, este método resultó dispendioso, lo cual disminuye la reproducibilidad y sensibilidad del mismo.
Los resultados obtenidos en los bioensayos que emplearon puré de papa casero o comercial, dieron resultados muy variables no habiendo reproducibilidad entre las repeticiones. Por otro lado, estos ensayos presentaron los porcentajes más altos de mortalidad en el testigo, superando el 30% y no permitieron un desarrollo normal de las larvas, como lo debería hacer una dieta artificial adecuada. Lo anterior hizo que los resultados obtenidos no fueran confiables por lo que no fueron tenidos en cuenta para los posteriores análisis. Los resultados obtenidos con este tipo de bioensayo no concuerdan con los obtenidos por Pérez et al. (1997), quienes utilizando una dieta similar, realizaron bioensayos con cepas nativas de B. thuringiensis y larvas de primer ínstar de T. solanivora. Aunque ellos señalaron que el 90% de las larvas sobrevivieron los 7 días de la evaluación, no se especifica si la dieta realmente soportó el desarrollo de T. solanivora durante todo su ciclo de vida. Este debería ser el criterio esencial para el empleo de una dieta en evaluaciones de entomopatógenos, ya que se garantiza que en realidad no haya ningún efecto colateral sobre el desarrollo nutricional y fisiológico de un insecto que pueda influir en los resultados obtenidos.
La variabilidad de los resultados obtenidos y específicamente la mortalidad alta en el testigo se atribuyen a características de las dietas a base de puré, que difieren mucho de la dieta natural, en características como textura, olor, nutrientes y presencia de sustancias preservantes en el caso del puré comercial. De acuerdo con los resultados, los métodos de bioensayo que emplean puré como sustrato alimenticio se descartaron. Por lo tanto, en el presente trabajo se decidió realizar los bioensayos empleando únicamente dieta natural.
Los resultados obtenidos con la evaluación de los diferentes métodos de bioensayo indicaron que el mejor método para la evaluación de las cepas y proteínas de B. thuringiensis es el que emplea prismas de papa, porque garantiza la reproducibilidad de los resultados y es lo suficientemente sensible como para detectar diferencias entre los tratamientos.
Una vez seleccionado el método general de bioensayo se realizó un ajuste respecto a la forma de contaminar los prismas de papa con las muestras a evaluar. Debido a que en el método inicial se embebían todos los trozos simultáneamente, se necesitaba gran cantidad de muestra, lo cual en el caso específico de las proteínas recombinantes resultaba difícil de obtener. Por lo tanto, se optimizó este aspecto realizando la contaminación directa de los prismas de papa con micropipeta y un volumen de muestra tal, que permitiera impregnar homogéneamente el prisma de papa.
Concentraciones letales de la cepa de referencia
En la determinación de las concentraciones letales de la cepa de referencia HD1 se empleó un rango de dosis entre 0,5 y 10 µg de proteína por cmβ de dieta. Los resultados promedio obtenidos en los bioensayos realizados se observan en la figura 1.
Los datos obtenidos en los bioensayos se procesaron mediante el paquete estadístico PROBIT POLO PC, encontrándose como CL50 de la cepa de referencia HD1 un valor de 4,37 µg de proteína/ cmβ de dieta (Tabla 1).
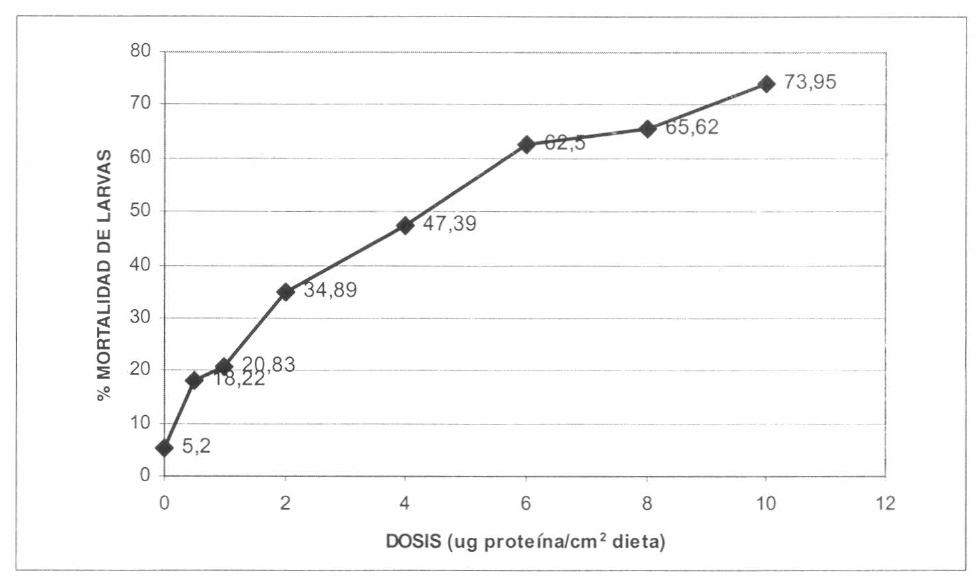
Porcentajes promedio de mortalidad de larvas de primer ínstar de Tecia solanivora Povolny obtenidos en la determinación de la CL50 de la cepa de referencia HD1 Var Kurstaki.
Análisis PROBIT de los resultados obtenidos en los bioensayos con la cepa de referencia HD1 Var. Kurstaki y larvas de primer ínstar de Tecia solanivora Povolny.
Concentraciones letales en µg de proteína por cmβ de dieta natural. Estimación de la toxicidad con límites de confianza al 95%.
Si se tienen en cuenta los datos de CL50 para la cepa HD1 registrados por Pérez et al. (1997) y se convierten a las mismas unidades que se emplearon en este trabajo (µg/ cmβ), se encuentra que el valor obtenido es mayor al señalado por dichos autores, quienes obtuvieron una CL50 de 2,84 µg/cmβ. Sin embargo, ya que dicha diferencia no es muy amplia, puede ser atribuible a los diferentes métodos de bioensayo empleados en ambos trabajos, ya que factores como el tipo de alimento utilizado y diferentes métodos de suministro de las proteínas en la dieta pueden originar respuestas diferentes en el insecto empleado.
Evaluación de las proteínas Cry1
El análisis de varianza de los datos obtenidos en los bioensayos con las proteínas Cryl evaluadas, indicó diferencias altamente significativas entre los tratamientos (P<0,01). Los valores promedio de mortalidad obtenidos oscilaron entre 19,26% para la proteína CrylAc, que resultó la proteína más tóxica y 1,56% para la proteína Cry1D, que fue la menos tóxica. Las proteínas Cry1Aa, Cry1Ab, Cry1B y Cry1C presentaron porcentajes de mortalidad promedio de 6,24, 6,76, 4,16 y 5,72, respectivamente. El análisis de Duncan indicó diferencias entre los promedios de individuos muertos obtenidos con la proteína Cry1Ac y las demás proteínas evaluadas (α=0.05). Las mortalidades promedio de las proteínas Cry1Aa, Cry1Ab, Cry1B, Cry1C y Cry2A fueron similares entre sí y las proteínas Cry1E y Cry1D fueron diferentes a las anteriores, pero similares entre sí (α = 0.05) (Fig. 2). Estas dos últimas proteínas fueron las menos tóxicas para las larvas de T. solanivora, no mostrando diferencias estadísticas (α=0.05) con el testigo empleado en los bioensayos, el cual tuvo una mortalidad promedio de 3,12%.
Los datos anteriores indican que la proteína Cry1Ac presentó la actividad tóxica más alta contra las larvas de T. solanivora. Pérez et al. (1997) propusieron que las proteínas CrylAa, Cry1Ab, CrylAc de la cepa HD1 y las proteínas Cry1Ab, Cry1B y Cry1D de una cepa nativa denominada Bt-40 que evaluaron eran las responsables de la actividad de dichas cepas; sin embargo, por tratarse de cepas con genes múltiples no pudieron determinar exactamente la proteína responsable de la toxicidad. Los datos obtenidos en el presente trabajo permiten proponer que la proteína Cry1Ac ejerce un papel fundamental en la mayor actividad tóxica de la cepa HD1 (CL50 de 56,9 µg/ml), respecto de la cepa nativa Bt-40 (CL50 de 95,52 µg/ml).
Por otro lado, la proteína Cry1Ab puede ser la responsable de la actividad tóxica de algunas cepas nativas, ya que esta fue la segunda proteína más activa de los bioensayos realizados causando mortalidades hasta del 10%. Esto estaría de acuerdo con lo propuesto por Castelblanco (2000), quien evaluó varias cepas nativas de B. thuringiensis que presentaban genes Cry1 y concluyó que la actividad tóxica de algunas de las cepas se debía a la presencia del gen Cry1Ab. Igualmente, se puede relacionar la toxicidad observada con la proteína Cry1Ab con los valores altos de mortalidad (>90%) de larvas de P. operculella, obtenidos por Cañedo y Lagnoui (2001), cuando evaluaron plantas transgénicas de papa parda pastusa a las cuales se les introdujo el gen cry1Ab de B. thuringiensis. Lo anterior, debido a las similitudes de P. operculella con T. solanivora, por las cuales dichos autores proponen la evaluación de la resistencia de estas plantas transgénicas hacia T. solanivora.
La corroboración de la actividad tóxica específica de la proteína Cry1Ac se obtuvo con los ensayos realizados con la cepa HD73 (con genes cry1Ac y cry2A, únicamente) y la cepa E. coli recombinante con el gen cry2A (Fig. 3). En dichos bioensayos, empleando la CL50 de la cepa HD1, la ceра HD73 presentó una mortalidad promedio de 77,6%, atribuible principalmente a la presencia de la proteína Cry1Ac, según los resultados preliminares. Se descarta un efecto tóxico causado por la proteína Cry2A ya que en las evaluaciones preliminares con esta proteína, en forma individual, se obtuvo un valor de mortalidad promedio de tan sólo el 5%.
Es importante tener en cuenta que en algunos casos las proteínas Cry presentes en una cepa determinada pueden estar expresadas de forma diferencial constituyendo cada una un porcentaje diferente del total de proteína presente en el cristal proteico. De esta forma, y debido a que en la mayoría de cepas nativas de B. thuringiensis existe más de una proteína Cry presente, es de esperarse que la actividad tóxica varíe, aunque las cepas contengan el mismo tipo y número de genes cry. Por lo tanto, esto explicaría la variabilidad de los resultados obtenidos en los trabajos realizados hasta el momento con cepas nativas de B. thuringiensis (Pérez et al. 1997; Castelblanco 2000), que aunque poseen los mismos genes identificados por técnicas moleculares, su toxicidad hacia larvas de T. solanivora no es la misma.
Por otro lado, la presencia o ausencia de una protoxina particular Cry1A puede afectar de forma marcada la solubilidad de todo el cristal proteico, debido posiblemente a las uniones disulfuro presentes entre estas protoxinas relacionadas, afectando así la disponibilidad de un protoxina dentro del intestino larval y por consiguiente la efectividad tóxica del cristal completo (Aronson 1995). Lo anterior también podría explicar la variación en la toxicidad de cepas nativas que poseen el gen Cry1Ac en diferentes combinaciones con otros genes tipo Cryl.
Los resultados aquí presentados representan un aporte para el desarrollo de nuevas estrategias biológicas para el control de la polilla guatemalteca de la papa. Surge así la recomendación que aquellas cepas nativas que contengan en su genoma el gen cry1Ac y expresen dicha proteína, son susceptibles de ser evaluadas como potenciales ingredientes activos de bioplaguicidas para el control de T. solanivora en papa en almacenamiento; así mismo, dicho gen debe ser tenido en cuenta para ser empleado en aquellos trabajos que busquen el desarrollo de plantas de papa resistentes a esta plaga. Adicionalmente, se puede continuar la exploración de otros genes potencialmente útiles para el control de esta plaga, como el caso del gen cry5 el cual causó mortalidades hasta del 100% en larvas de Phothorimaea opercullella Zeller que atacaron tubérculos de papa transformada genéticamente con dicho gen (Mohammed et al. 2000).
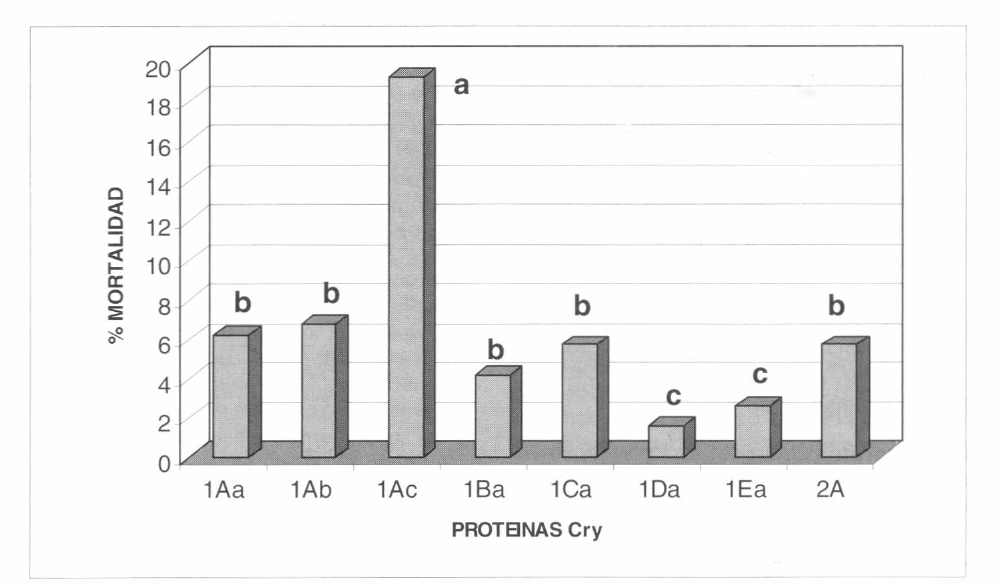
Resultados de mortalidad de larvas obtenidos en los bioensayos con las proteínas Cry de Bacillus thuringiensis y larvas de primer ínstar de Tecia solanivora Povolny. Dosis empleada 4,37 µg de proteína/cmβ de dieta. Los promedios con letras iguales no presentaron diferencias significativas con prueba de Duncan (α= 0.05).
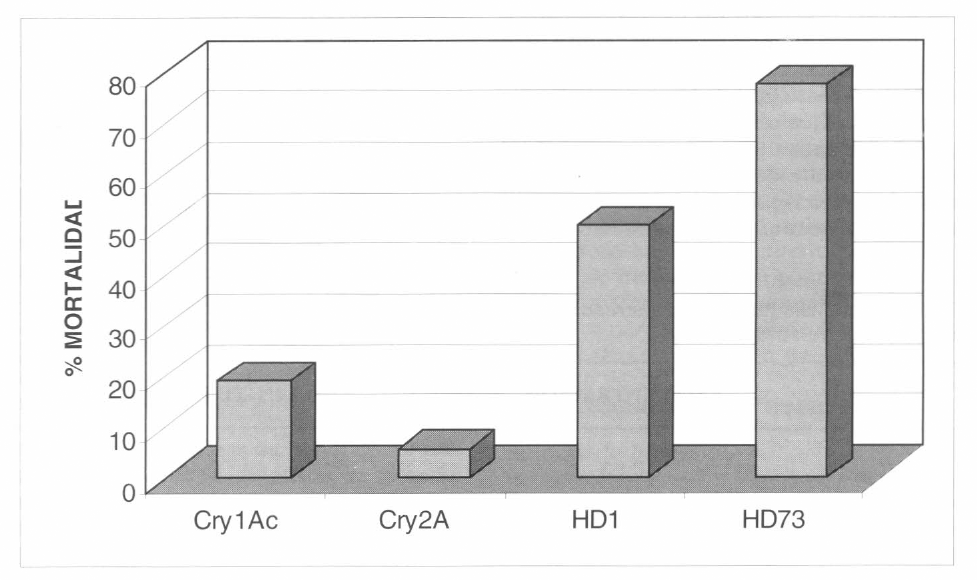
Comparación de los porcentajes de mortalidad obtenidos en los bioensayos con larvas de primer ínstar de Tecia solanivora Povolny y proteínas y cepas de B. thuringiensis. Dosis empleada 4,37 µg de proteína/ cmβ de dieta.
Conclusiones
Se determinó que la proteína CrylAc de B. thuringiensis presenta la mayor actividad tóxica específica hacia larvas de primer ínstar de T. solanivora.
Se evidenció que la actividad tóxica hacia T. solanivora de la proteína CrylAc, en algunos casos, puede ser incrementada por la presencia de otras proteínas Cryl.
Se desarrolló un método de bioensayo basado en dieta natural reproducible, sensible y fácil para realizar bioensayos de evaluación de la toxicidad de proteínas y/o cepas de B. thuringiensis hacia T. solanivora.
Agradecimientos
Los autores agradecen al estudiante de Ingeniería Agronómica Alejandro Aranguren por su apoyo en la realización de los bioensayos y mantenimiento de la cría del insecto. Igualmente, al Instituto de Biotecnología de la Universidad Nacional de Colombia y a Colciencias por la financiación de este trabajo.
