Abstract
The leaf cutting ants are important agricultural pests in Colombia and other countries. Although several have been used for the control of these insects, it remains unknowledge of some basic aspects regarding to their relationship with the mutualist fungus and the taxonomic and phylogenetic relationships between them. The mitochondrial DNA appears as an important tool in studies of molecular entomology for the taxonomy and also for the establishment of evolutive relations in both insects and mutualist fungus. In the present study we amplified and sequenced a fragment of 405 bp from the mitochondrial ribosomal large subunit in leaf cutting ants from Medellín. The identity of the sequences was verified comparing them with sequences for this region previously publicated for insects beloging to the order Diptera. There were determinated high contents of adenina and timina (80%) a common characteristic in mitochondrial DNA of insects and a similarity of 48.5% and 50.3% was found in sequences from ants when compared with Anopheles gambiae and Lutzomyia longipalpis respectively.
Introducción
Las hormigas arrieras constituyen una de las plagas agrícolas de mayor importancia en Colombia y otros países causando pérdidas en gran número de cultivos; su daño consiste en cortar las hojas de las plantas reduciendo sustancialmente el área foliar, disminuyendo la capacidad fotosintética y afectando la producción en especies de importancia económica (Cherrett 1989; Serna 1992). Estos insectos tienen un gran número de hospederos y llevan con frecuencia los cultivos a productividades muy bajas, calculándose que las pérdidas exceden la cifra de los mil millones de dólares (Evans 1993; Rehner et al. 1994; Serna y Correa 1995).
La mayoría de los estudios realizados en relación con estas hormigas se han orientado hacia el control químico y/o biológico y en menor proporción se han incluido aspectos como la simbiosis mutualista con el hongo, taxonomía y estimación de los daños económicos (Serna 1992; Serna y Correa 1995; Bolton 1997; Yepes y Madrigal 1998).
Además de su utilidad en los estudios evolutivos, la entomología molecular aparece como una herramienta importante en la identificación de especies, ya que las secuencias de ADN incorporan numerosos caracteres taxonómicos facilitando el estudio de diversos grupos de insectos (Simon et al. 1994; Flook y Rowell 1997). Igualmente, el ADN mitocondrial por su relativa rápida tasa de cambio y su herencia materna se ha utilizado con éxito para entender relaciones taxonómicas y filogenéticas entre insectos y los organismos con los cuales estos se asocian (De Salle et al. 1992; Nigro y Graputo 1993; Simon et al. 1994; Kambhampati 1995; Kambhampati et al. 1996). La unidad larga ribosomal se ha utilizado exitosamente para estudiar insectos de los órdenes Diptera y Orthoptera, además secuencias parciales de la pequeña subunidad ribosomal y otros genes mitocondriales se han incluido en el estudio de las hormigas cortadoras y el hongo mutualista del cual se alimentan (Hinkle et al. 1994). Con esta investigación preliminar se pretende implementar la utilización de secuencias de ADN mitocondrial en el estudio de hormigas cortadoras de diferentes regiones de Colombia en aspectos básicos que faciliten a mediano y largo plazo actividades de control. Para ello se amplificó y secuenció un fragmento de 405 pares de bases de la unidad larga ribosomal mitocondrial en soldados de Atta cephalotes provenientes del campo, usando oligonucleótidos diseñados con base en las secuencias de esta región publicadas para insectos como Apis mellifera, Drosophila melanogaster y Anopheles gambiae.
Materiales y Métodos
Especímenes
Las secuencias fueron obtenidas a partir de 6 especímenes de A. cephalotes capturados en Medellín; la identificación taxonómica de los especímenes fue realizada mediante criterios morfológicos.
Aislamiento y Amplificación de ADN por técnicas de PCR
Los especímenes se colectaron y preservaron en isopropanol al 100%. Para la extracción de ADN sólo se utilizó el tórax de cada especímen donde se encuentra la mayor proporción de mitocondrias (Futuyma 1998) y el ADN se aisló por el método de Collins y Porter (1990). Brevemente, los tórax se maceraron en buffer de lisis y se incubaron a 35°C durante 30 minutos. El ADN mitocondrial se purificó utilizando el kit Wizard TM Maxipreps (Promega), con esta metodología se obtuvieron entre 50-200 ug de ADN por individuo.
El fragmento de la unidad larga ribosomal mitocondrial se amplificó utilizando los oligonucleótidos LRJ12966 (AAA AAA ATT ACG CTG TTA TCC CTA A) y LRN13393 (C (G/A)C CTG TTT AAC AAA AAC AT) construidos de acuerdo con las secuencias presentadas en el trabajo publicado por Monteiro et al. (1999) para estudiar insectos del orden Hemiptera.
Después de una fase de desnaturalización del ADN a 94°C durante 3 minutos, los parámetros de amplificación para los siguientes 35 ciclos de la reacción en cadena de la polimerasa (PCR) se desnaturalizaron por 1 minuto a 93°C, se alinearon por 1 minuto a 50°C y se extendieron por 1 minuto a 72°C. Para verificar la amplificación, parte de la muestra fue sometida a electroforesis en un gel de agarosa al 1% con bromuro de etidio y se comparó con el marcador de peso molecular 1 kb (Promega). El ADN amplificado se purificó usando Wizard PCR preps (Promega).
Antes de secuenciar los fragmentos de ADN se purificaron usando columnas (Microspin s-300 HR Columns, Pharmacia Biotech, Inc.). Los productos resultantes se secuenciaron utilizando el kit Big dye con Amplitaq DNA polimereasa FS (Perkin Elmer) durante 24 ciclos bajo las siguientes condiciones: 30 segundos a 96°C, 15 segundos a 50°C y 4 minutos a 60°C. El ADN se precipitó utilizando etanol al 70% y se resuspendió en formamida-dextran antes de correrse en un gel de acrilamida al 4.8% (Page Plus and Amresco) durante 7 horas en un secuenciador ABI prism 377 utilizando el respectivo módulo de corrido.
Los productos de PCR se secuenciaron directamente en ambos sentidos de la doble cadena y se analizaron con el paquete estadístico GCG (Genetics Computer Group). Las secuencias se editaron usando el programa Sequencing Navigator (Perkin Elmer) comparándolas en ambos sentidos de la doble cadena para cada especímen de cada uno de los cuales se secuenciaron dos productos de PCR.
La identidad de las secuencias fue verificada mediante comparación con la secuencia de A. gambiae (Diptera: Culicidae) cuyo genoma mitocondrial completo fue publicado por Beard et al. (1993) y Lutzomyia longipalpis (Diptera: Psychodidae) por la disponibilidad de esta secuencia publicada por Uribe et al. (1998).
La variabilidad haplotípica, la composición en términos de nucleótidos y la similitud en relación con las secuencias referencia fueron igualmente determinadas.
Resultados
Amplificación de ADN ribosomal mitocondrial mediante PCR
La figura 1 muestra la amplificación del fragmento de 405 pb de los especímenes en un gel de agarosa al 1%; el tamaño de la banda fue verificado por comparación con el marcador de Promega 1 kb que aparece en las líneas extremas de la fotografía del gel.
Secuencias
La figura 2 muestra la secuencia consensus para A. cephalotes obtenida mediante reversa complemento y comparación de las secuencias en ambos sentidos de la doble cadena del fragmento de la unidad ribosomal mitocondrial; no se observó variabilidad entre las secuencias obtenidas de diferentes productos de PCR en un mismo individuo ni entre individuos, lo cual sugiere que probablemente pertenecían a un mismo grupo familiar.
La composición de las bases nitrogenadas fue: A: 36.3%, G: 4.7%, T: 43.7%, C: 15.3%. Una mayor proporción de A-T (80%) en total es consistente con la composición de estas bases encontrada en secuencias de ADN mitocondrial de otros insectos (Simon et al. 1994).
Las secuencias obtenidas para A. cephalotes corresponden a las posiciones 12905-13310 de la secuencia referencia de A. gambiae y la similitud fue de 48.5% entre ellas; al comparar las secuencias de A. cephalotes y A. gambiae (Fig.3) se encontraron 211 sitios polimórficos; la mayoría de los cambios observados fueron transversiones (cambio de purina por pirimidina y visceversa) del tipo AxT (46%), en menor proporción se observaron otras transversiones como AxC (11.8%), TxG (2.37%), GxC (0.95%) y transiciones (cambio de purina por purina y/o pirimidina por pirimidina) como TxC (19%) y GxA (8.1%).
La figura 4 muestra la comparación entre las secuencias de la región estudiada en A. gambiae, L. longipalpis (orden Diptera) y A. cephalotes (orden Hymenoptera). El alinea-miento múltiple que resultó en 410 posiciones señala una mayor similitud entre las secuencias de los dípteros (Anopheles-Lutzomyia) 69%, en comparación con la similitud entre Atta-Lutzomyia 50.3% y Atta-Anopheles 48.5% (Hymenoptera-Diptera).
Asi mismo, se observaron diferencias en cuanto a las inserciones y deleciones en las secuencias; entre Anopheles y Atta se encontraron 5 deleciones en las posiciones 111, 112, 113, 294 y 295 del alineamiento y 20 inserciones en las posiciones 154-167, 366-369 y 396-397 mientras que entre los dípteros Anopheles y Lutzomyia el número de deleciones e inserciones fue menor 3 y 7 respectivamente en las posiciones 111, 112, 113 y 165, 166, 167, 368, 369, 396, 397.
La comparación con secuencias homólogas y en especial con A. gambiae confirma la identidad de la secuencia y la utilidad de los oligonucleótidos usados en este estudio para amplificar esta región de mtRNA.
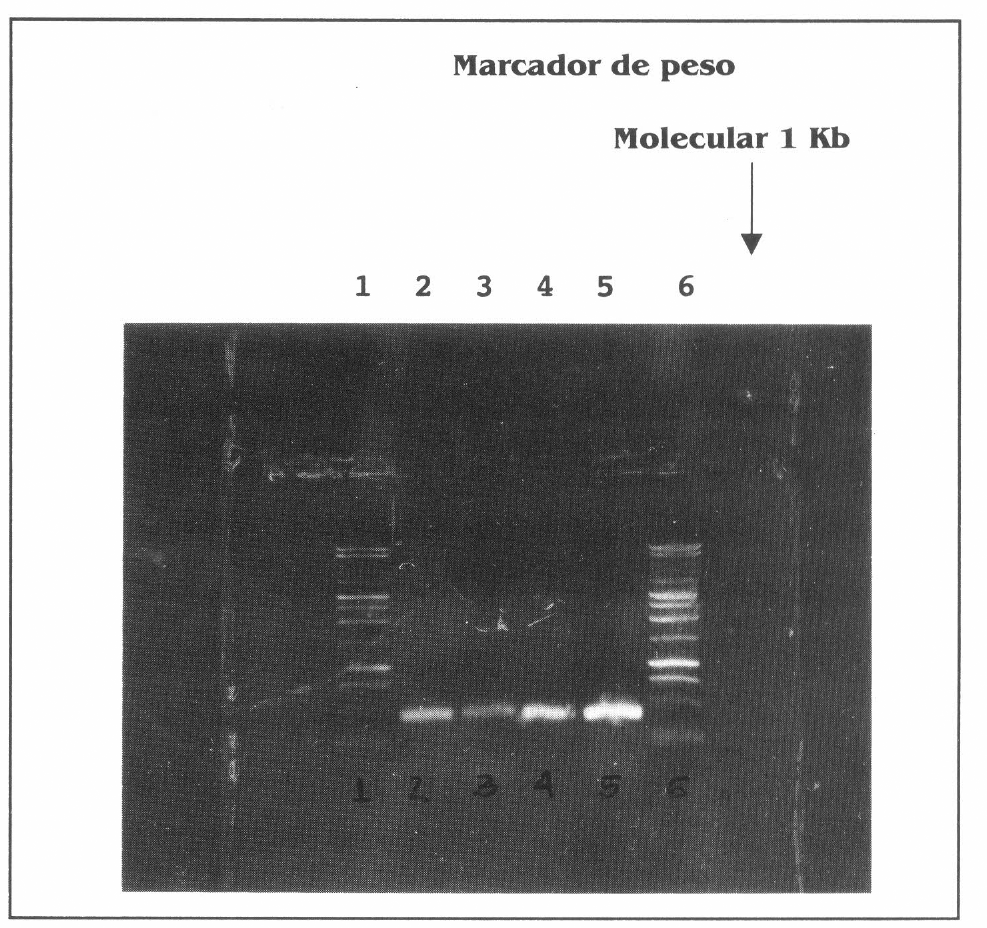
Gel de agarosa al 1% verificando la amplificación del fragmento de la pequeña unidad ribosomal en Atta cephalotes. Los carriles 2-5 corresponden a productos de PCR, las líneas de los extremos (1 y 6) corresponden al marcador de peso molecular 1kb (Promega).

Secuencia consensus del fragmento de la unidad larga ribosomal (405 pb) entre los diferentes especímenes y productos de PCR en Atta cephalotes después de comparar las secuencias en ambos sentidos de la doble cadena. H: hormiga (Atta cephalotes).
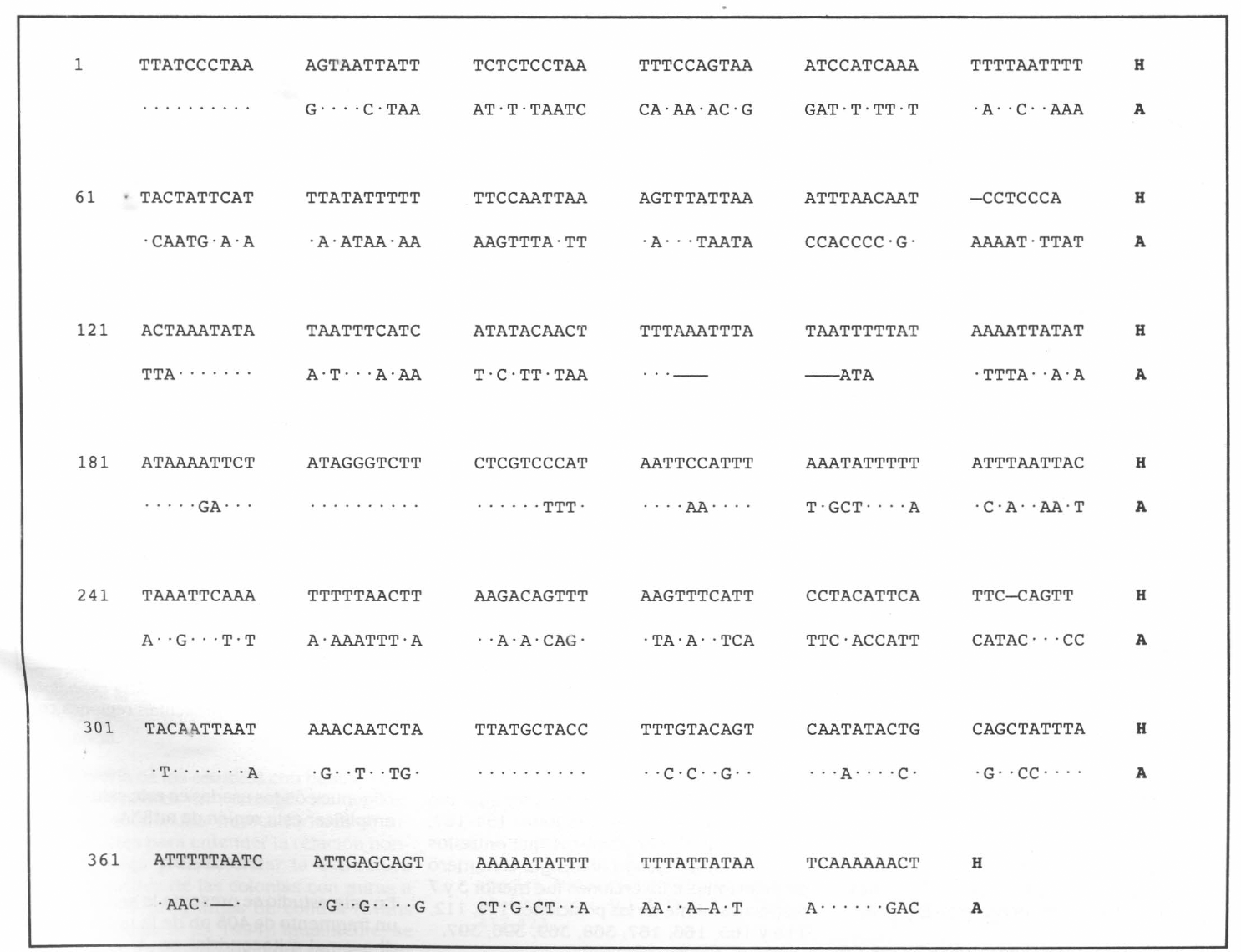
Comparación del fragmento secuenciado en Atta cephalotes de Medellín y la secuencia referencia de Anopheles gambiae (Beard et al. 1993). A: Anopheles gambiae, H: hormiga (Atta cephalotes). Las regiones conservadas entre las secuencias aparecen en puntos, las líneas señalan deleciones o inserciones de nucleótidos entre las secuencias.
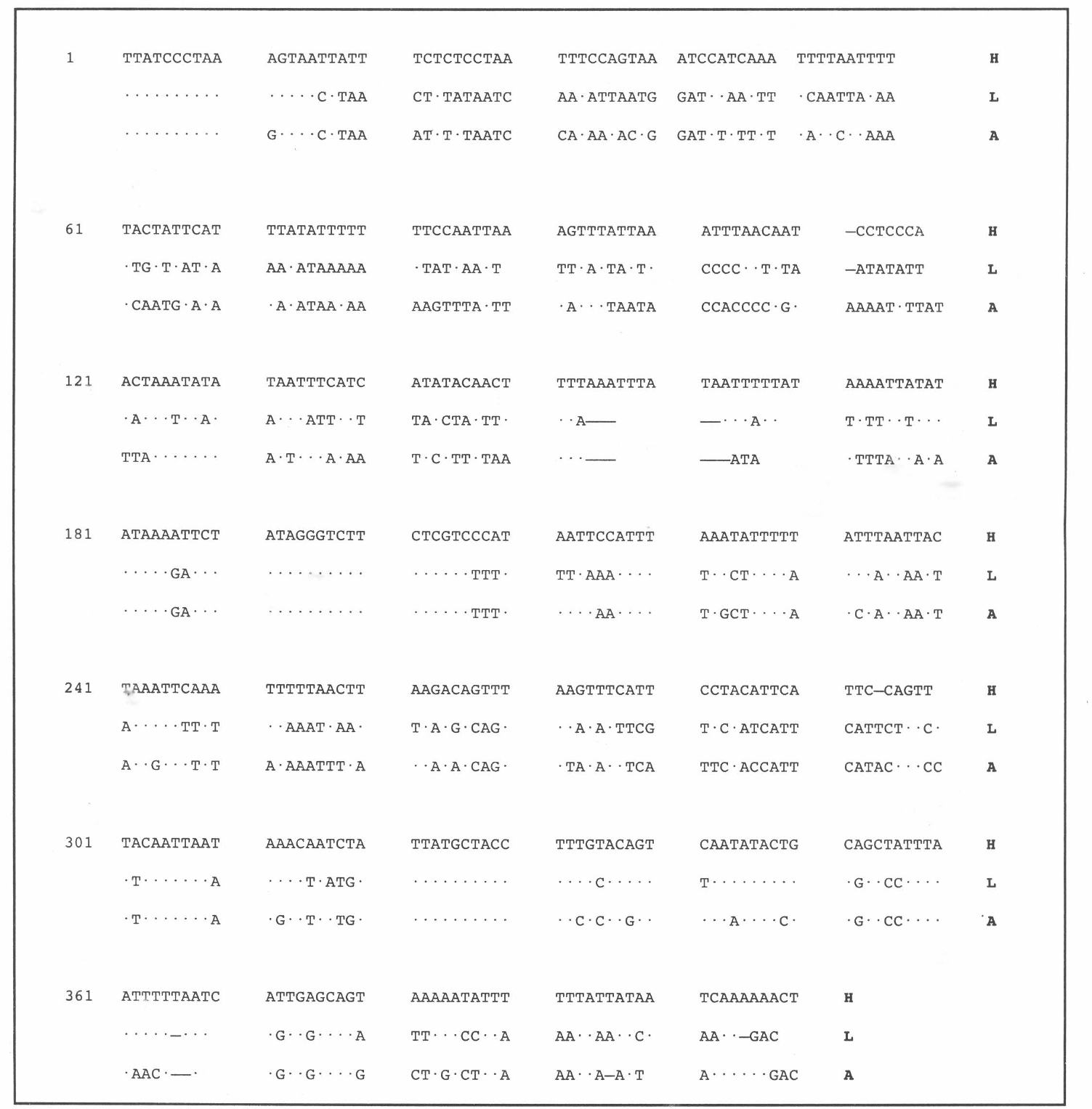
Comparación entre las secuencias de Anopheles gambiae y Lutzomyia longipalpis (ambos del orden Diptera) con Atta cephalotes (orden Hymenoptera) H: hormiga (Atta cephalotes); A: Anopheles gambiae; L: Lutzomyia longipalpis. Los puntos representan regiones conservadas y las líneas deleciones o inserciones entre las secuencias.
Discusión
En este estudio se presenta la secuencia de un fragmento de 405 pb de la unidad larga ribosomal mitocondrial en A. cephalotes con utilidad potencial para estudios taxonómicos y filogenéticos entre hormigas, así como la relación hormiga-hongo con interesantes implicaciones en las actividades de control.
Regiones homólogas se han amplificado y secuenciado en otros insectos principalmente dipteros de importancia mèdica, pero no en hormigas cortadoras de hojas. Otras regiones mitocondriales han empezado recientemente a utilizase en el estudio de hormigas de los géneros Atta y Camponotus como el Citocromo oxidasa I (COI), Citocromo oxidasa II (COII) y regiones de ARN de transferencia tARN (Evans 1993; Rehner et al. 1994; Reporte del Gen Bank U75350).
La mayoría de estudios en insectos han revelado altas proporciones en A-T y las secuencias provenientes de las hormigas incluidas en este estudio corresponden a estos valores, con un promedio de 80% en total, similar al observado en otros insectos como L. longipalpis (Uribe et al. 1998) y A. gambiae (Beard et al. 1993) 70% у 81%, respectivamente. Así mismo, la región homóloga en 32 especies de cucarachas mostró un promedio de 72% en A-T (Kambhampati 1995) y en miembros de la familia Cicadelidae, Fang et al. (1993) observaron un promedio de 73% en A-T.
La variabilidad en el contenido de A-T en secuencias de mtADN en insectos ha sido previamente demostrada y estudiada en Hymenoptera (Apis mellifera) donde al parecer la cantidad de A-T alcanza extremas proporciones (Crozier et al. 1989).
Las comparaciones de las secuencias en el alineamiento de A. cephalotes con A. gambiae y L. longipalpis representando los órdenes Diptera e Hymenoptera, mostraron una mayor similitud entre las secuencias de los dípteros en comparación con las hormigas, obsevándose variaciones importantes en sustituciones nucleótidicas y/o deleciones-inserciones; así, el promedio de las transversiones entre Anopheles y Atta -diferentes órdenes- fue mayor (31.5%) que el observado entre Lutzomyia y Anopheles (17.75%) -ambos del orden Diptera.
Adicionalmente, tanto el número de deleciones como inserciones fué menor entre los dípteros que entre éstos y la hormiga. Esta variabilidad en las sustituciones nucleotídicas confirma la existencia de diferencias en la dinámica evolutiva de la unidad larga ribosomal (Gen 16S rARN) entre insectos propuesta por Kambhampatti et al. (1996) y sugiere la necesidad de estudios detallados en grupos particulares y niveles de divergencia.
La mayoría de los estudios con base en datos moleculares en hormigas incluyen el uso de secuencias mitocondriales y microsatélites para entender la relación hongo-hormiga y caracterizar la estructura sociogenética de las colonias con miras a estructurar programas de control (Evans 1993; Rehner et al. 1994). Igualmente, se han secuenciado las unidades ribosomales pequeña y larga en gran número de simbiontes del género Atta que corresponden a hongos del orden Agaricales y se han obtenido secuencias de ADN que revelan particularidades de las asociaciones hongo-hormiga gracias a las cuales las hormigas logran sobrepasar las defensas de las plantas (Holldobler y Wilson 1990; Evans 1993; Rehner et al. 1994; Gertsch et al. 1997).
En el presente estudio se comprobó que los oligonucleótidos LRJ12966 y LRN 13393 diseñados con base en las secuencias de otros insectos y las condiciones de PCR y obtención de secuencias previamente descritas, permiten amplificar un fragmento de 405 pb de uso potencial en estudios taxonómicos y moleculares en hormigas, y en especial como una herramienta para entender la relaciones con el hongo del cual se alimentan, cuya unidad larga ribosomal es objeto de amplificación y obtención de secuencias en la actualidad (Uribe sin publicar).
Footnotes
Agradecimientos
Al Doctor Charles Porter del CDC de Atlanta por su asesoría en el trabajo molecular.
A Eduar Bejarano y Judy Natalia Jiménez por su ayuda en la edición de las secuencias.
El trabajo molecular en el Center for Diseases Control CDC Atlanta Georgia se realizó gracias al soporte (Beca-escolar) del Instituto Colombiano para el desarrollo de la Ciencia y la Tecnología Francisco José de Caldas COLCIENCIAS para Sandra Uribe durante su doctorado.
