Abstract
The presence of the Bemisia tabaci (Gennadius) B biotype was confirmed in Colombia by means of biochemical, molecular and etiological tests. The biochemical identification consisted in the determination of non-specific esterase banding patterns. Polymorphism among samples collected in Córdoba, Sucre, Atlántico, Valle del Cauca and Cundinamarca was found, and almost all of the samples were identified as the B biotype, by comparison with A biotype samples drawn from a colony mantained at CIAT for several years. High degree of polymorphism was found in the B biotype, which was widespread in the area, attacking 23 species of crop plants and 11 weeds. Similarity between a/ß esterase patterns of the two biotypes was only 20%. At the molecular level, RAPD amplification products obtained with the primers OPA-04, OPA-11 and OPA-17 were also found to be different between biotypes A and B. Furthermore, after feeding the two biotypes on four cucurbit species, the silverleaf symptom was induced only on Cucurbita moschata (Duchesne) by B biotype nymphs, 21 days after the infestation. The B biotype was found to be more aggressive since it successfully colonized C. mixta Pang., C. pepo L., C. ficifolia Bouché y C. moschata, 23 to 33% faster than biotype A.
Introducción
La mosca blanca Bemisia tabaci (Gennadius) es una especie distribuida de forma generalizada en regiones tropicales y subtropicales, y se ha encontrado atacando un amplio rango de hospedantes que incluyen plantas cultivadas y silvestres (Brown et al. 1995a). Este insecto fue considerado como plaga de relativa importancia durante mucho tiempo hasta los 70s, principalmente a causa de su eficiencia como vector de virus. Sin embargo, a partir de los 80s, B. tabaci produjo grandes pérdidas en el sur de Estados Unidos, no sólo como vector sino también a causa del daño mecánico y de la excesiva excreción de melazas (Perring 1996). Particularmente, en 1991 se perdieron cerca de 500 millones de dolares a causa de los severos ataques de la mosca blanca en gran variedad de cultivos que incluyeron alfalfa, brócoli, algodón, tomate y papa, entre otros (Perring et al. 1993). Debido a la similitud morfológica con B. tabaci, la cual existía en la zona desde 1894, se identificó esta nueva forma de Bemisia, mucho más agresiva, como biotipo B (raza Florida, raza Poinsettia, o B. argentifolii (Bellows y Perring)) para distinguirla de la B. tabaci nativa (raza California, raza algodón, raza A o biotipo A) (Perring 1996).
La severidad del daño es uno de los factores que ha permitido distinguir los dos biotipos ya que mediante caracteres morfológicos no es posible. Se conocen además algunos caracteres biológicos y relacionados con el hospedante que son útiles para la identificación. Así, el biotipo B presenta un rango de hospedantes más amplio el cual ataca mayores densidades de población que el A y tiene la capacidad de inducir desórdenes fisiológicos manifestados por síntomas característicos en tomate, crucíferas y algunas cucurbitáceas, entre otros (Brown et al. 1995a). A nivel de campo, estos síntomas han sido definitivos para la identificación y confirmación de la presencia del biotipo B.
Para Colombia, los primeros indicios de la presencia del biotipo B surgieron a finales de 1994 cuando se observaron en la Costa Atlántica grandes pérdidas en algodón debido a la excesiva excreción de melazas, y a principios de 1995 por la maduración no uniforme de los frutos de tomate y el desarrollo de plateado en hojas de algunas cucurbitáceas (C. Cardona y N. Jimenez, comunicación personal). Esto motivó que a partir de 1995 se iniciaran muestreos con el fin de identificar biotipos de B. tabaci, a nivel bioquímico revelando la actividad de esterasas no específicas, a nivel molecular mediante la amplificación al azar de fragmentos de ADN (RAPDs) y por la inducción de plateado de hojas en cuatro especies de Curcurbita sp., así como la identificación de varios hospedantes del biotipo B en Colombia.
Materiales y Métodos
Colección y cría
Se realizaron colectas de moscas blancas cubriendo el mayor número de hospedantes posible en abril y octubre de 1995, y en junio de 1996 en municipios de los departamentos de Córdoba, Sucre y Atlántico. De agosto a diciembre de 1996, los muestreos se realizaron en el Valle del Cauca con el fin de establecer la identidad de las moscas blancas por medio de la electroforesis de isoenzimas (esterasas) y el análisis de RAPDs (Tabla 1). Los biotipos A y B de B. tabaci se mantuvieron en colonias de cría sobre Phaseolus vulgaris L. (var. ICA Pijao), a una temperatura de 20-22 °C y 40-50% de HR. El biotipo B se colectó sobre Arachis sp. en Palmira (Valle del Cauca) y se utilizó como testigo en todos los ensayos. Además se utilizaron también como testigos Trialeurodes vaporariorum (Westwood) criado en la misma variedad de P. vulgaris a una temperatura de 18°C y 70% de HR y Bemisia tuberculata Bondar criada en yuca.
Análisis de esterasas no específicas
Se colectaron adultos vivos en los sitios de estudio, se congelaron inmediatamente en nitrógeno líquido y se mantuvieron a -80°C hasta su utilización. Se maceraron hembras individuales en 20 µl de 1.6% Triton X-100 el cual contenía 10% sacarosa y 0.01% de azul de bromofenol. Luego de homogenizar, se centrifugó a 14000 rpm por 5 minutos. Se tomaron 10 µl de esta solución y se sometieron a electroforesis nativa en poliacrilamida, en un gel de separación al 7.5% y uno de concentración al 4.0% en 0.155M ácido bórico pH 8.2 y 0.05% Triton X-100. El tiempo de corrida duró entre cinco y seis horas a 150 voltios constantes. Las esterasas se visualizaron luego de la adición de los substratos, 0.025% α-naftil acetato y 0.025% ß-naftil acetato disueltos en 0.1 M fosfato de potasio pH 6.0. Luego de 10 minutos se agregó Fast Blue RR a una concentración de 0.037%. Los patrones de bandas se registraron y compararon entre sí.
RAPDs (Polimorfismos en ADN amplificado al azar)
Para la extracción de ADN, cada adulto se maceró en 200 µl de 50mM EDTA, 500mM NaCl, 10mM ß-mercaptoetanol. Posteriormente, se agregaron 20 µl de SDS al 10% y se incubó a 65 °C por 10 minutos. Se añadieron 20 µl de 5M acetato de potasio y se centrifugó 10 minutos a 10000 rpm. El ADN se precipitó por la adición de 0.5 volumenes de isopropanol frío. El pellet resultante se lavó en etanol al 70% y luego de secarlo se resuspendió en 50 µl de 10mM Tris-HCL, 1mM EDTA pH 8.0. La amplificación de 10 µl del ADN molde se realizó en un volumen final de 25 µl. Cada reacción tenía 2.5 µl de buffer (100mM Tris-HCl, pH 8.3; 500mM KCl), 3.0mM MgCl₂, 0.15mM dNTPs, 0.8mM cebador, 0.2 µl BSA (10 mg/ml) y 1.5U Taq polimerasa. El ADN fue amplificado según el siguiente ciclo de temperaturas: (1) 94°C por 5 min, (2) 40°C por 2 min, (3) 72°C por 3 min, (4) 94°C por 1 min, (5) 40°C por 1.5 min, (6) 72°C por 2 min, (7) volver al paso 4, y repetir el ciclo 35 veces, (8) 4°C hasta su utilización. Los productos de la amplificación se separaron en geles de agarosa al 1.5% en TAE (Sambrook et al. 1989). Los geles se corrieron a 60 voltios constantes por 5-6 horas.
Areas de muestreo y colección de moscas blancas en Colombia¹)
1) Datos tomados de Diccionario Geográfico de Colombia. Instituto Geográfico "Agustín Codazzi". Subdirección de Investigación y Divulgación Geográfica. 2a Ed. Bogotá, 1980.
2) Planta de poinsettia procedente de un invernadero.
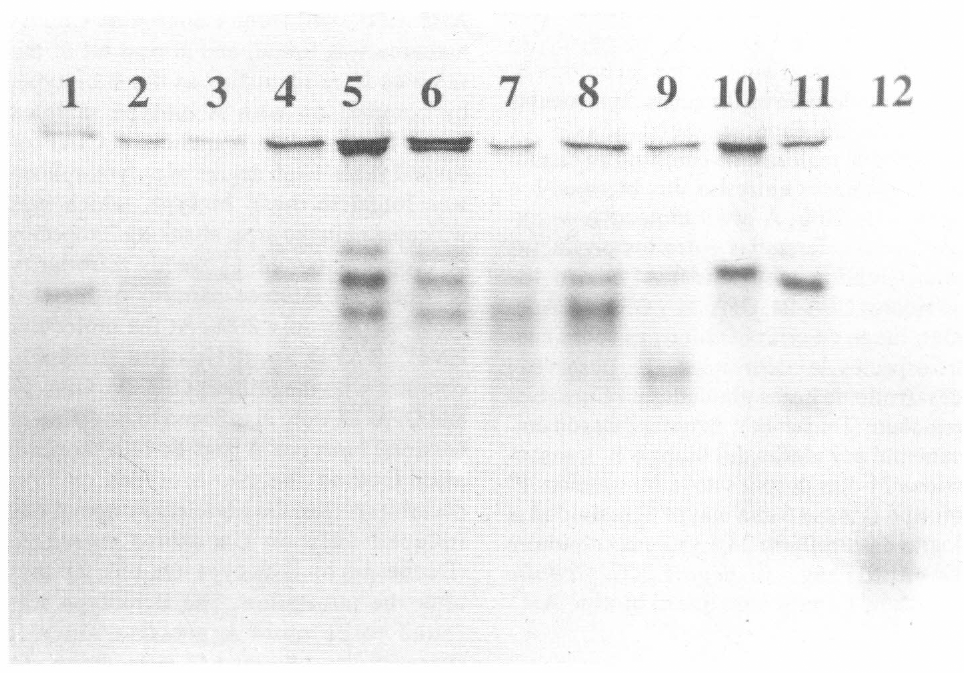
Patrones de esterasas no específicas de moscas blancas. 1 y 11, Bemisia tabaci biotipo A; 2-4, biotipo B colectado en Córdoba sobre ahuyama, tomate y col; 5 y 6, biotipo A colectado sobre col en Córdoba; 7-9, biotipo B colectado en Atlántico sobre tomate, ahuyama y tomate, respectivamente; 10, biotipo colectado sobre poinsettia procedente de Cundinamarca; 12, Trialeurodes vaporariorum.
Hospedantes registrados para el biotipo B de Bemisia tabaci en Colombia
Sobrevivencia y días a emergencia de adultos de los biotipos A y B de Bemisia tabaci en cuatro especies de cucurbitáceas
1 -, No determinado
2 ND, No hubo desarrollo de inmaduros
Inducción de plateado de hojas en cucurbitáceas
Plantas de ahuyama (Cucurbita mixta Pang.), calabaza (C. ficifolia Bouché), calabacín (C. pepo L.), y zapallo [C. moschata (Duchesne)] se distribuyeron en dos jaulas, cada una de las cuales se infestó con uno de los biotipos de B. tabaci con un nivel de infestación de 10 adultos/planta. Transcurridos 15 días después de la infestación, se estableció la población inicial mediante el conteo de huevos y ninfas por planta. El plateado de hojas se evaluó utilizando la siguiente escala: 1, ausencia de síntomas; 2, plateado en venas principales; 3, el plateado comienza a extenderse entre las venas y cubre por lo menos la mitad de la hoja; 4, el plateado cubre todo el haz pero no es muy intenso y 5, plateado muy intenso en todo el haz. Al final, se hicieron recuentos de adultos emergidos y se calcularon porcentajes de emergencia y días a emergencia.
Resultados y Discusión
Esterasas no específicas
Las isoenzimas han mostrado ser útiles como marcadores genéticos en la evaluación de la variabilidad de las moscas blancas a nivel de género y especie (Prabhaker et al. 1987; Wool et al. 1989). Más recientemente, el análisis de esterasas no específicas ha permitido confirmar la identidad de poblaciones del biotipo B en América tropical en 11 países, sin incluir Colombia (Brown 1993).
Luego de procesar las muestras colectadas, se observaron diferencias en la actividad de α/B esterasas entre las moscas blancas colectadas en campo y la B. tabaci tradicional. Así, el biotipo A, tomado de la colonia de cría presentó un patrón único correspondiente a cuatro bandas mientras que el biotipo B presentó hasta seis patrones de esterasas diferentes, conformados por bandas no comparables en su migración en el gel con las de B. tabaci (Fig. 1). Al igual que Brown et al. (l995b) también se encontraron diferencias respecto a la degradación del substrato, es decir, el biotipo B presentó bandas rojas las cuales corresponden a la hidrólisis del α-naftil acetato, a diferencia del biotipo A el cual sólo presentó bandas negras (degradación de α-naftil acetáto). Luego del análisis de las muestras disponibles, se identificó una banda B común a todos los individuos del biotipo B, la cual se utilizó como marcador bioquímico pues permitió establecer con certeza la identidad del biotipo en cuestión (Figs. 1 y 2). Sin embargo, debido al polimorfismo encontrado en las poblaciones naturales del biotipo B, los patrones de bandas fueron analizados bajo el índice de similitud de Jaccard con el paquete estadístico NTSYS-pc versión 1.8 (Rohlf 1994), lo cual permitió establecer que la similitud entre los dos biotipos fue apenas del 20% (Fig. 2). Luego de los análisis se encontró que el biotipo B fue mucho más frecuente que el A, el cual sólo se colectó en Col (Fig. 2). Como resultado, se estableció una lista preliminar de hospedantes del biotipo B en Colombia la cual comprende 23 especies cultivadas y 11 silvestres (Tabla 2). Se destaca la yuca por ser la primera vez que se registra B. tabaci en Colombia sobre este hospedante.
RAPDs
La técnica de RAPDs ha sido utilizada para generar marcadores moleculares que han mostrado ser útiles en la identificación de varios insectos (Black et al. 1992). Para este estudio, se realizó la amplificación del ADN de las muestras colectadas con los cebadores OPA-04, OPA-11 y OPA 17. Igual que Gawel y Bartlett (1993) todos los productos amplificados mostraron polimorfismo entre los biotipos A y B de B. tabaci. Sin embargo, los mejores resultados se obtuvieron con el cebador OPA-04 para el cual se observaron principalmente tres fragmentos de ADN amplificado en el biotipo B correspondientes a 1252 pares de bases (pb), 1130 pb y 577 pb, ausentes en el biotipo A, para el cual se logró la amplificación de dos fragmentos de 1030 pb y 840 pb (Fig. 3).
Inducción de plateado de hojas
La capacidad para inducir alteraciones fitotóxicas expresadas como hojas plateadas en especies de curcurbitáceas ha sido asociada directamente con la presencia de estados inmaduros del biotipo B de B. tabaci (Costa y Brown 1991). En el presente trabajo también se observó la inducción del síntoma unicamente por el biotipo B, en hojas superiores de C. moschata a partir de los 21 días después de infestación. El plateado de hojas progresó hasta el extremo superior de la escala (Fig. 4). También se observó el síntoma en C. pepo y en C. mixta pero muy leve, correspondiente a 2 en la escala, en las pocas hojas que resultaron afectadas. Aunque el síntoma principal fue el plateado de hojas, este se vió acompañado de otros como reticulación, amarillamiento, encorvamiento y deterioro de las hojas, además de clorosis en venas y tallos.
En cuanto a los aspectos biológicos de las moscas blancas, se observó que el biotipo B pudo colonizar exitosamente las cuatro especies de cucurbitáceas evaluadas en este estudio mientras que el biotipo A no pudo establecerse en C. ficifolia ni en C. moschata. El biotipo A logró sobrevivir a adulto en C. mixta en un 61.4% y en C. pepo sólo en un 1.4%, a diferencia del B que pudo hacerlo en las cuatro especies de plantas infestadas lo cual muestra su mayor adaptación y agresividad (Tabla 3). Se observó además que el biotipo B se desarrolló en un tiempo menor que el A.
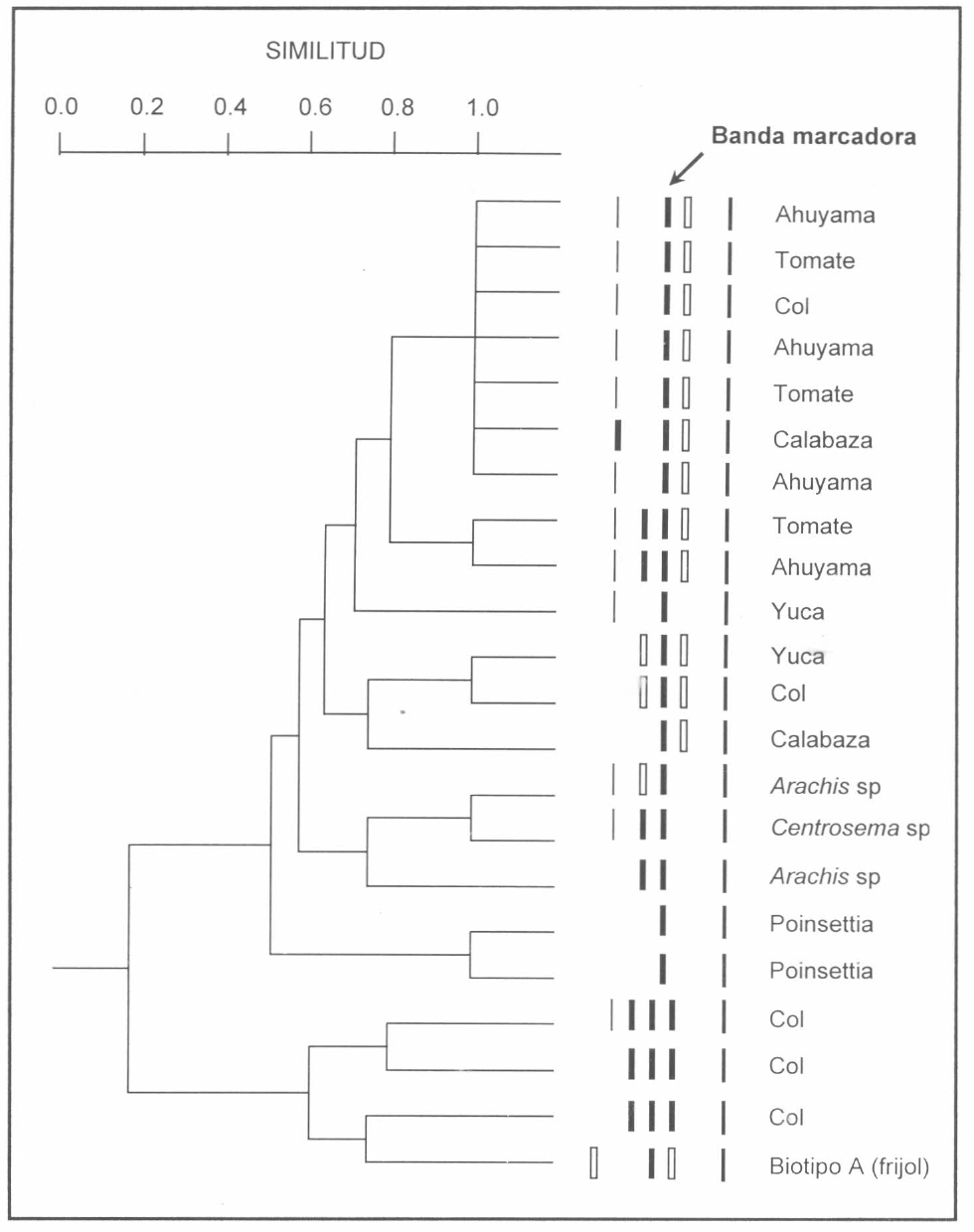
Dendrograma y zimograma de los biotipos A y B de Bemisia tabaci. Se señala la planta hospedante y la banda marcadora que caracteriza al biotipo B.
Otros síntomas que confirmaron la presencia del biotipo B en Colombia fueron la deformación de hojas y clorosis en tallos de lechuga y el rayado longitudinal de los tallos en col (Fig. 5). Además, se tienen registros de la ocurrencia de madurez desuniforme de los frutos de tomate en la Costa Atlántica.
Los indicios de la presencia del biotipo B en Colombia por las altas poblaciones registradas en la Costa Atlántica desde finales de 1994 se confirmaron mediante las diferencias encontradas en los patrones de α/B esterasas y de marcadores RAPDs, junto con la presencia de síntomas característicos en lechuga, col y en C. moschata. La confirmación del biotipo B de B. tabaci en Colombia constituye una alerta para la economía nacional por el gran potencial de daño que caracteriza esta plaga y su fácil diseminación a través de cultivos ornamentales que han servido como vehículo para su dispersión.
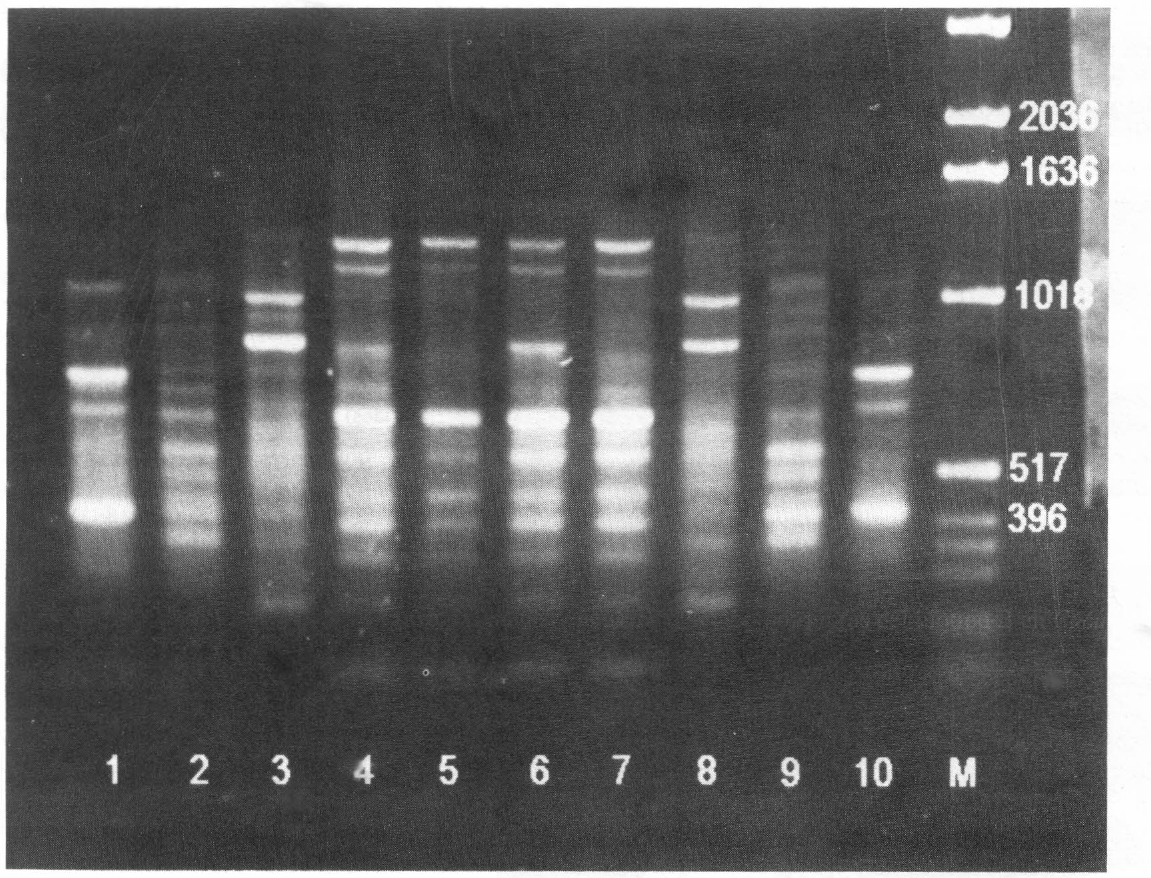
Identificación de los biotipos A y B de Bemisia tabaci mediante RAPD. Amplificación del primer OPA-04. 1 y 10, Trialeurodes vaporariorum; 2 y 9, B. tuberculata; 3 y 8, B. tabaci biotipo A; 4-7, biotipo B colectado sobre ahuyama, tomate, col y poinsettia, respectivamente; M, marcador 1Kb ladder; se señala el tamaño de los fragmentos de ADN en pares de bases (pb).

Plateado de hojas inducido por ninfas del biotipo B en Cucurbita moschata. Contraste con una planta sin síntomas, infestada con el biotipo A.
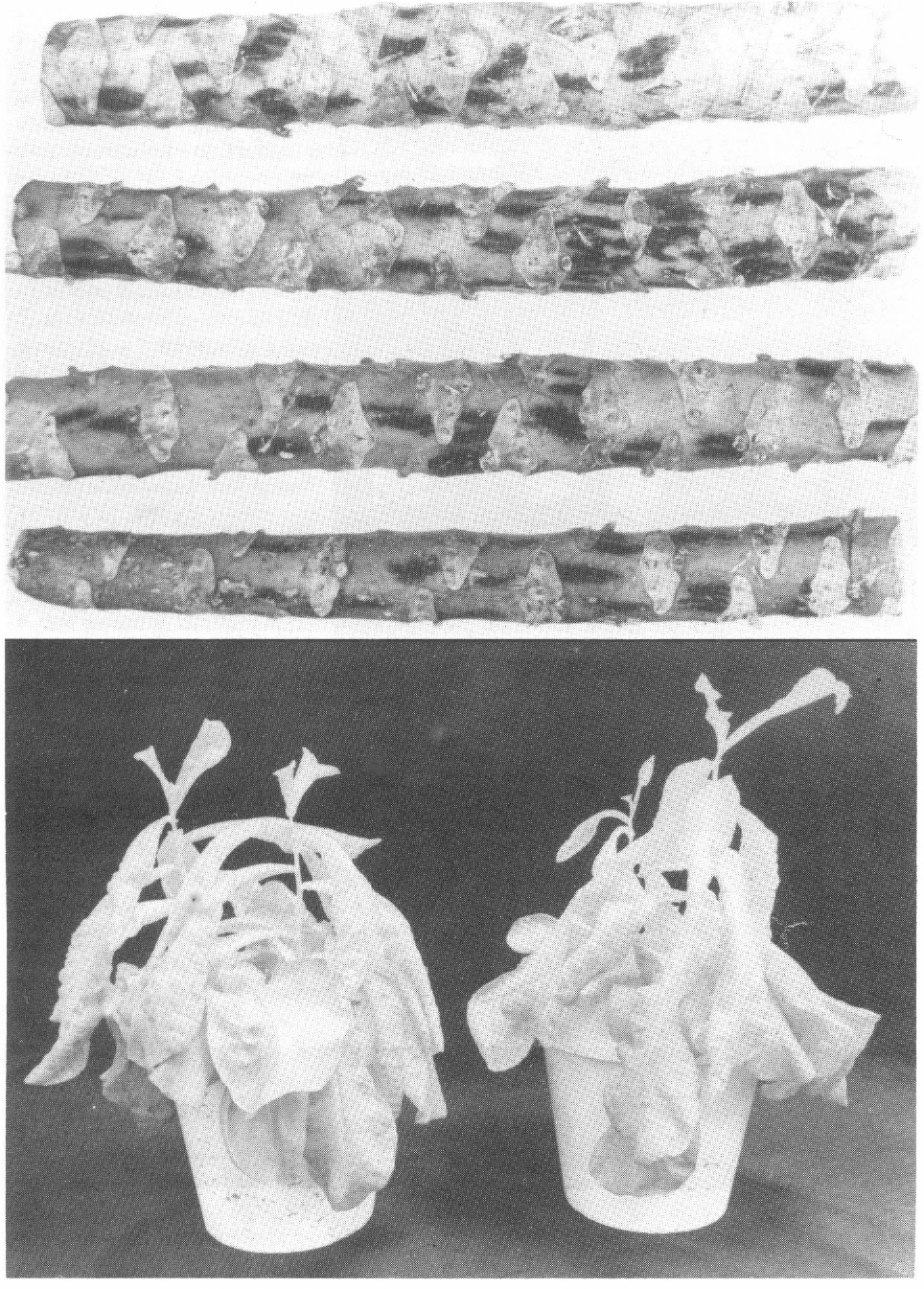
Algunas alteraciones fitotóxicas inducidas por el biotipo B en col y lechuga.
