Abstract
An invasion of the llanera locust Rhammatocerus schistocercoides (Rehn) occurred in 1994 in the Oriental Plains of Colombia. This insect implies a potential risk for cultures like rice, sorghum and sugar cane. According to the potential that biological control represents, the objective of the present work was to select under laboratory and field conditions, natives strains of Metarhizium anisopliae (Metschnikov) to control the llanera locust. In laboratory (28°C and relative humidity 70%) three natives strains of M. anisopliae (M3, M5 and M11) were evaluated over the eighth instar nymphs of R. schistocercoides. The M5 strain produced at the eleventh day a 100% of mortality in locust, while the M3 and the M11 strains produced the 100% of mortality at the thirteen day. The median lethal doses (LD50) was determined for the three strains, using the statistical program PROBIT. A LD50 of 5 conidia/insect was found for the M5 strain and 7 conidia/ insect for the strains M3 and M11. This results did not present significatives differences between them (f=0.78; gl=4; p<0.05). In order to evaluate biological control of strains under field conditions (36°C and R.H 56%), strains were reactivated, massively produced and formulated by mean of conidia encapsulation with ultraviolet protectors. The assay was carried out in cages containing adult locusts separated in two groups. The first group was treated with formulated fungus suspended in an oil-water emulsion, the other group was treated with non formulated fungus (naked conidia). Strains of M. anisopliae were applied in two concentrations (1x107 and 1x108 conidia/ml) using an ultralow volume sprayer. After seventeen days, M. anisopliae produced 67.8%, 64.1% and 56.5% mortality when applied the formulated strains M5, M11 and M3 respectively. These results were significantly different (f=4.66; gl=12; p<0.05) to the obtained when applied non formulated conidia (naked conidia). In the later case, were found mortality percentages of 9.5%, 26.4% and 28.2% for the strains M5, M11 and M3 respectively. We could demonstrate that the formulation permits a good entomopathogenic activity of the fungus under field conditions, because confere tolerance to the conidia towards adverse conditions.
Introducción
En Colombia, a principios de la presente década, la langosta Rhammatocerus schistocercoides no era reconocida como plaga; sólo a partir de 1994, con la invasión hacia la altillanura del departamento del Meta, se pudo establecer el peligro potencial que este insecto representa para cultivos de importancia económica y el daño que puede causar sobre pasturas nativas e introducidas, las cuales son utilizadas para la alimentación del ganado de la región.
La eficiencia baja del control químico de las langostas en el mundo ha direccionado el interés de los investigadores hacia el uso de alternativas de control más seguros como el control biológico mediante la utilización de hongos entomopatógenos (Prior 1995).
Metarhizium anisopliae (Deuteromycotina: Phialosporaceae) se aisla de un amplio rango de órdenes de insectos. Su actividad infectiva en la langosta se realiza por medio de la invasión mediante la degradación de su cutícula por medio de enzimas especializadas (St. Leger et al. 1991). Posteriormente, la muerte es ocasionada por la liberación de toxinas en la hemolinfa del insecto y por la colonización de ésta por parte del hongo (Lysenko y Kucera 1973).
Este hongo ha demostrado, bajo condiciones controladas de laboratorio, su capacidad biocontroladora contra la langosta llanera R. schistocercoides. Es así como en un trabajo realizado por Zamora (1996), se evaluó la actividad entomopatogénica de 3 cepas de M. anisopliae (dos nativas y una foránea) y una cepa foránea de M. flavoviridae sobre langostas adultas. Las cepas nativas produjeron el 100% de mortalidad al día octavo y noveno, mientras que las cepas foráneas de M. flavoviridae y de M. anisopliae produjeron el 100% de mortalidad al día décimo y décimo segundo día.
Sin embargo, al ser aplicado en campo éste se ve afectado por condiciones medioambientales tales como las temperaturas altas, la humedad relativa baja y la radiación ultravioleta (Roberts y Yendol 1973; Moore et al. 1993). Es por ésto que en el Laboratorio de Control Biológico de CORPOICA se desarrollaron dos preformulaciones basadas en el recubrimiento de las esporas mediante microencapsulación con los protectores solares CBUV01 y CBUV02. El polvo obtenido fue diseñado para reconstituirse en una emulsión formada por aceite vegetal y tensioactivos. Esta formulación mostró una protección a la luz ultravioleta del 100% (Gómez y Villamizar 1996).
Debido a que hasta el momento en Colombia no se habían encontrado cepas nativas de M. anisopliae eficientes en el control de la langosta llanera, y además, que éstas no habían sido probadas con formulaciones que las protegiera ante condiciones medioambientales adversas, el objetivo del presente trabajo fue el de seleccionar, mediante ensayos de laboratorio y campo, cepas nativas de M. anisopliae para el control de la langosta llanera R. schistocercoides.
Materiales y Métodos
En el Centro de Investigaciones Tibaitatá se evaluaron 3 cepas nativas de M. anisopliae provenientes del banco de cepas del Laboratorio de Control Biológico de Corpoica. Estas fueron escogidas de acuerdo con la efectividad mostrada en pruebas preliminares sobre langostas y otras plagas (Tabla 1).
Cepas de Metarhizium anisopliae evaluadas
Cada una de las cepas fue reactivada en 10 langostas de octavo ínstar, a las cuales se les aplicó 50 microlitros de la suspensión fúngica. Se mantuvieron en cuarentena a una temperatura de 25°C durante 10 días. De los individuos muertos, que mostraron esporulación, se realizó un aislamiento de la cepa en el medio Saboureaud - Rosa de Bengala (S.R.B) (3g neopeptona, 2g sacarosa, 6.4g agar-agar, 1.6g gelatina 0.15g Rosa de Bengala en 1000 ml e.s.p. de agua destilada).
El bioensayo preliminar, para evaluar la actividad insecticida de las cepas M3, M5 y M11 de M. anisopliae en laboratorio, se llevó a cabo a una temperatura de 27°C (±2°C), HR 70% (±10%) y fotoperíodo de 12 horas luz. Se realizó con ninfas de octavo ínstar de R. schistocercoides, las cuales se encontraban recluidas en jaulas de madera de 0.5 m de ancho x 0.5 m de largo x 0.6 m de alto. En cada jaula se colocaron 30 individuos, un vaso plástico con agua que contenía de 60 a 70 g de cortes de pasto kikuyo y una esponja constantemente humedecida. Se tuvieron 90 individuos por tratamiento.
El diseño experimental fue completamente al azar, con tres réplicas por tratamiento. Se tomaron dos controles: a) Control tratado (individuos asperjados sólo con tween 80 al 0.1%); b) Control absoluto (individuos no asperjados).
A partir de cultivos de M. anisopliae, reactivadas y crecidas en medio S.R.B. durante 10 días, se realizó una suspensión fúngica que contenía una concentración de 1x108 propágulos/ml. Dicha concentración fue obtenida mediante conteo de los conidios en la cámara de Neubauer. La aplicación del hongo se realizó mediante la aspersión de 20 ml de la suspensión al total de indiviudos por jaula por medio de atomizadores con un tamaño de gota que varió entre 150 a 250 micras. Para evitar una contaminación cruzada entre las jaulas, éstas se cubrieron durante 24 horas con bolsas plásticas.
Se realizó un registro diario de la mortalidad y para verificar la causa de la muerte por el hongo, los individuos muertos fueron desinfectados con hipoclorito al 5% por tres minutos y puestos en cámaras húmedas hasta observar la esporulación típica de M. anisopliae.
En el bioensayo realizado en el laboratorio para la determinación de la dosis letal media (DL50), las condiciones ambientales, mantenimiento de las langostas, número de individuos por tratamiento y diseño experimental fueron iguales a las descritas anteriormente. Se utilizaron langostas adultas y las cepas fueron reactivadas como se mencionó anteriormente. Se obtuvo una suspensión inicial de cada una de las cepas del hongo que contenía una concentración de 1x108 propágulos/ml. A partir de ésta, mediante diluciones seriadas, se obtuvieron 5 diluciones que contenían (1x107, 1x106, 1x105, 1x104 y 1x103 propágulos/ml). De cada dilución se tomó un volumen de 20 microlitros con una micropipeta y se aplicó tópicamente a nivel del pronoto y primer tergo del insecto. Los individuos tratados fueron depositados en la jaula correspondiente. La forma de evaluación, el registro de mortalidad diaria y el montaje de insectos en cámara húmeda, se llevó a cabo del mismo modo descrito para el ensayo anterior.
Para el bioensayo de campo (temperatura 36°C y HR 56% promedio), en el cual se evaluó la actividad biocontroladora sobre adultos de las 3 cepas de M. anisopliae formuladas y sin formular, se sometieron a un proceso de reactivación; posteriormente, en el Laboratorio de Control Biológico de Corpoica, se sometieron al procedimiento de producción masiva y formulación mediante encapsulación de los conidios con un protector de luz ultravioleta. Estas cepas se enviaron al Centro de Investigación Carimagua como un polvo para suspender en una emulsión aceite-agua que contenía conidios formulados o conidios sin formular (desnudos). Cada frasco contenía 2g de polvo que se reconstituyó en una base autoemulsificable y se llevó a un volumen final requerido de 100 ml.
El diseño experimental fue de bloques al azar con tres réplicas. Se evaluaron doce tratamientos en total y 60 individuos por tratamiento, divididos en dos concentraciones para cada una de las cepas (1x107 y 1x108 propágulos/ml), así como en sus dos presentaciones: conidios formulados (f) y conidios desnudos (cd), es decir, sin recubrimiento.
Las langostas que para el momento del experimento se encontraban en estado adulto, se recluyeron en jaulas de muselina de 1.2 mβ de área y 1.8 m³ de volumen; cada jaula se encontraba separada a 5 m de distancia entre ellas. Diariamente las langostas se alimentaron con arroz de 20 días de sembrado y se les suministró agua.
El hongo se aplicó en horas de la tarde (4:00 p.m.) por medio de la aspersión de 20 ml de la suspensión por cada jaula, mediante la utilización de una bomba de ultra bajo volumen MICRON-ULVA®, utilizando una boquilla que proveía un tamaño de gota de 50 micras.
El registro de mortalidad se hizo diariamente por medio de dos recolecciones (mañana y tarde). Los individuos muertos o con signo de infección se guardaron en bolsas de papel marcadas con el tratamiento. Posteriormente, sigiuendo los procedimientos descritos, éstas se colocaron en cámaras húmedas para verificar la causa de la muerte.
Los resultados se sometieron a un análisis de varianza y a la prueba del rango múltiple de Duncan.
Resultados y Discusión
En el bioensayo preliminar realizado bajo condiciones de laboratorio, las tres cepas nativas de M. anisopliae no presentaron diferencias significativas en el porcentaje de mortalidad acumulado producido en los insectos (f=0.96; gl=4; p<0.05), de acuerdo al análisis de varianza. Sin embargo, sí se observaron diferencias significativas respecto a los controles (no tratados con el hongo) (f=3.5; gl=4; p<0.05).
A pesar de que todas las cepas alcanzaron a producir el 100% de mortalidad en las langostas de octavo ínstar, existió diferencia en el tiempo letal 100. La cepa M5 produjo el 100% de mortalidad al día once de iniciado el ensayo y las cepas M3 y M11 alcanzaron este valor de mortalidad al día trece (Fig 1).
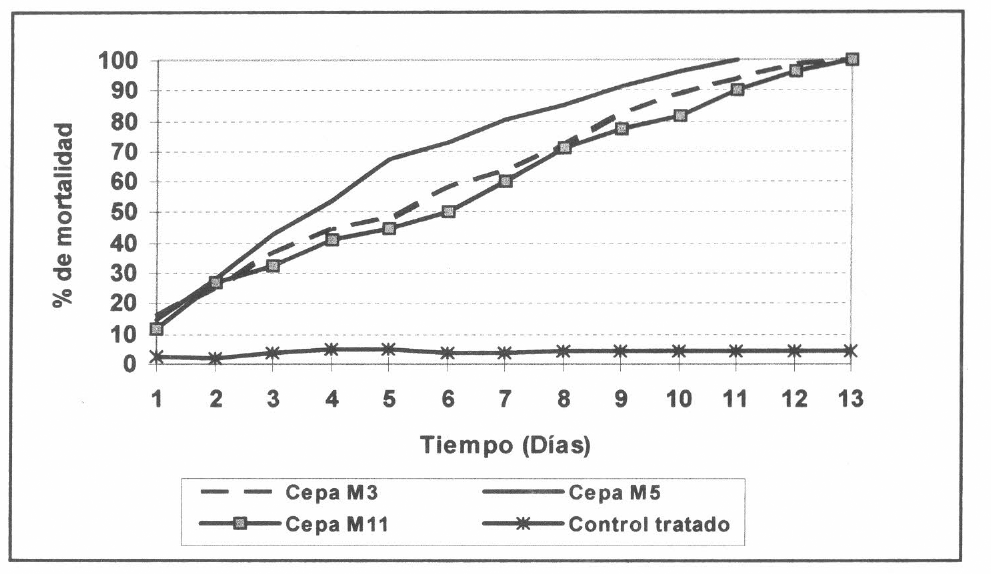
Actividad insecticida de tres cepas nativas de M. anisopliae sobre ninfas de octavo ínstar de R. schistocercoides.
Las diferencias encontradas entre las cepas con respecto al tiempo de mortalidad podrían ser dadas por diferencias en la virulencia debido posiblemente a distintos rangos de afinidad química entre el hongo y la epicutícula del insecto.
Cabe anotar que la cepa M5 comenzó a mostrar una actividad patogénica más marcada que las otras dos cepas (M3 y M11) hacia el tercer día, mostrando su máximo pico en el día quinto, momento en el cual presentó en promedio 21% más de mortalidad. Posteriormente, de forma gradual comenzó a disminuir esta diferencia hasta el día once, en que se presentó una diferencia promedio del 8%. Estas diferencias pudieron deberse a que las cepas M3 y M11 provocaron inicialmente respuestas de defensa en el insecto, y con el paso de los días se pudieron haber recuperado y vencido estas defensas.
Dado que en el ensayo anterior no se presentaron diferencias significativas en la mortalidad ocasionada por las tres cepas evaluadas, con éstas se determinó la dosis letal 50. Los resultados se analizaron por medio del programa estadístico Probit con un coeficiente de significancia de 0.05.
Se encontró de nuevo que la mortalidad producida por las tres cepas en las langostas adultas no presentó diferencias significativas (f=0.78; gl=4; p<0.05). Aunque en esta ocasión la cepa M5 produjo el 100% de mortalidad al día 9 con su mayor dosificación, comparado con las cepas M3 y M11 que para ese día produjeron 96.3% y 92.8% de mortalidad, respectivamente para la misma dosificación. De todas maneras, fueron porcentajes mayores comparados con los obtenidos en el ensayo anterior al noveno día, ya que las cepas M3 y M11 produjeron un 82.5% y un 77.5% de mortalidad, respectivamente (Figs. 2-4).
La disminución del tiempo letal 100 en la mortalidad de las langostas, con respecto al primer bioensayo, podría ser debido a que las cepas se reactivaron en el insecto antes de iniciar el ensayo de DL50. Esta reactivación pudo haber ocasionado una selección de células con mayor capacidad virulenta y por ende, una estimulación en la actividad entomopatogénica del hongo. De otra parte, en este ensayo se utilizaron langostas adultas, las cuales podrían ser más susceptibles al hongo que las langostas jóvenes.
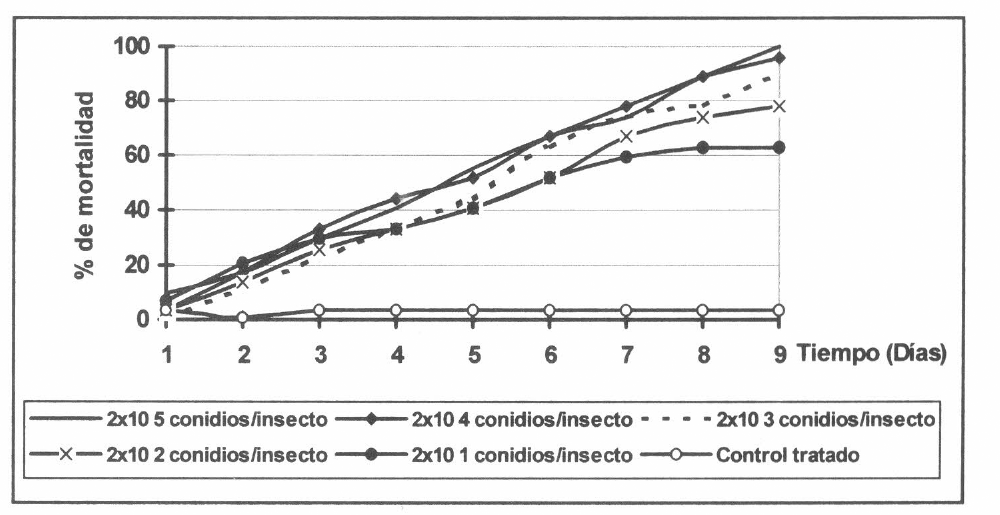
Efecto de diferentes dosificaciones de la cepa M5 sobre la mortalidad acumulada de adultos de R. schistocercoides.
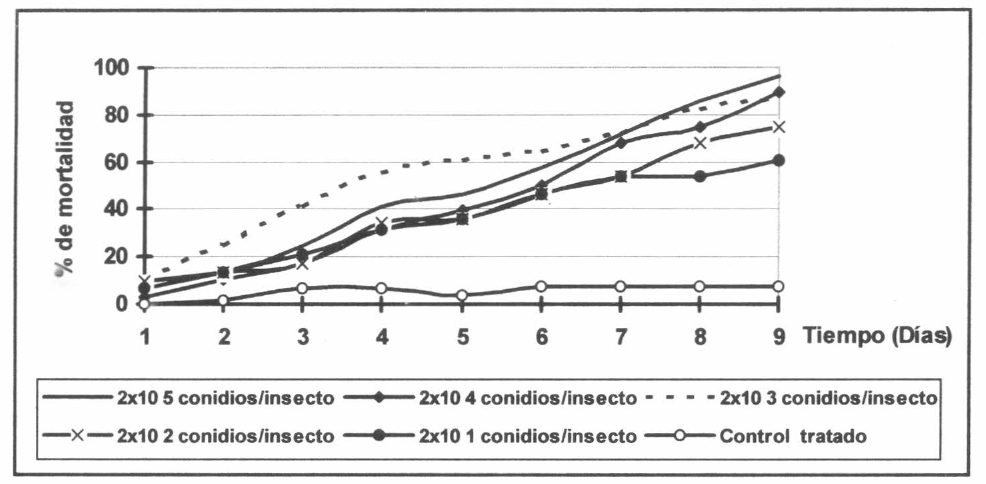
Efecto de diferentes dosificaciones de la cepa M3 sobre la mortalidad acumulada de adultos de R. schistocercoides.
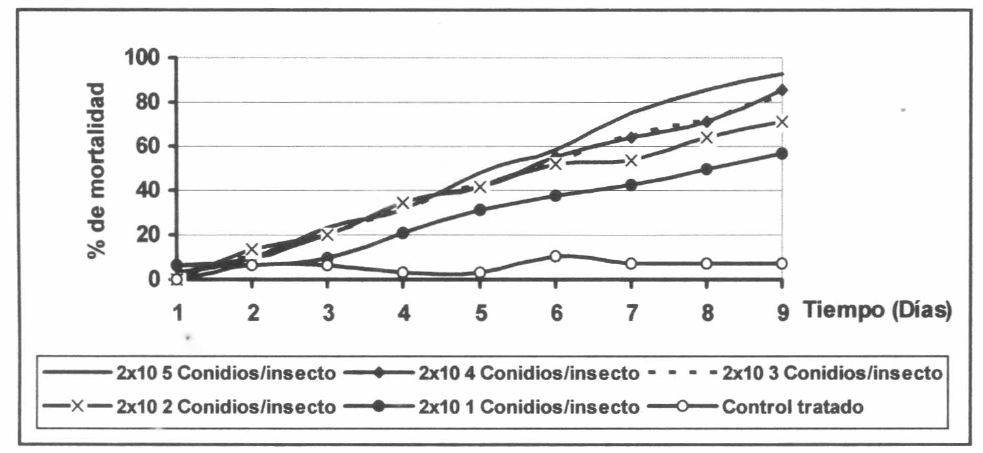
Efecto de diferentes dosificaciones de la cepa M 11 sobre la mortalidad acumulada de adultos de R. schistocercoides.
La dosis letal 50 obtenida para la cepa M5 fue de 5 conidias/insecto, mientras que para las cepas M3 y M ll fue de 7 conidias/insecto.
Estos resultados contrastaron grandemente con los obtenidos por Milnery Prior (1994) cuando utilizaron en condiciones controladas cepas de M. flavoviridae para el control de la langosta australiana Chortoicetes tenninifera (Orthoptera:Acrididae), resultando una DL50 de 417 conidios/insecto, También difirieron de los resultados obtenidos por Bateman et al. (1993) en condiciones controladas de laboratorio, cuando usó como biocontrolador a M. flavoviridae sobre S. gregaria (Orthoptera: Acrididae) y encontró una DL50 de 8.900 conidioslinsecto.
La pequeña cantidad de inóculo necesaria para producir mortalidad en R. schistocercoides podría indicar que las cepas nativas de M. anisopliae, evaluadas en laboratorio, poseen una actividad biocontroladora bastante promisoria, que podría ser debida a la adaptación del hongo a las condiciones particulares del insecto, tales como una afinidad química a su epicutícula, la capacidad que pueda tener cada conidio del hongo para penetrar e infectar rápidamente al insecto o la adaptación del hongo a las condiciones climáticas del trópico.
Aunque no se encontraron diferencias significativas entre las cepas ensayadas en laboratorio se decidió evaluarlas en campo, en Carimagua, Meta.
Las cepas formuladas (f) aplicadas a una concentración de l x 108 propágulos/ml produjeron los mayores porcentajes de mortalidad al décimo séptimo día de haberse iniciado el ensayo, siendo de 67.8% para la cepa M5, de 64.1 % para la cepa M 11 Y de 56.5% para la cepa M3. El análisis de varianza y la prueba de rango múltiple de Duncan mostraron que éstos resultados fueron significativamente menores (f=4.66; gl=12; p<0.05) cuando se asperjaron las langostas con las cepas sin formular (cd), ya que la cepa M5 produjo un 9.5% de mortalidad, la cepa M3 produjo un 28.2% y la cepa M 11 produjo un 26.4%. Cabe resaltar que al comparar los resultados de la mortalidad producidos por las cepas formuladas, no presentaron diferencias significativas entre sí. Al comparar los resultados de la mortalidad producida por las cepas sin formular, se encontraron diferencias significativas entre la cepa M5 y las cepas M3 y Mil (f=4.3; gl=5; p<0.05). Estas dos últimas no presentaron diferencias significativas entre sí (Figs. 5 Y 6).
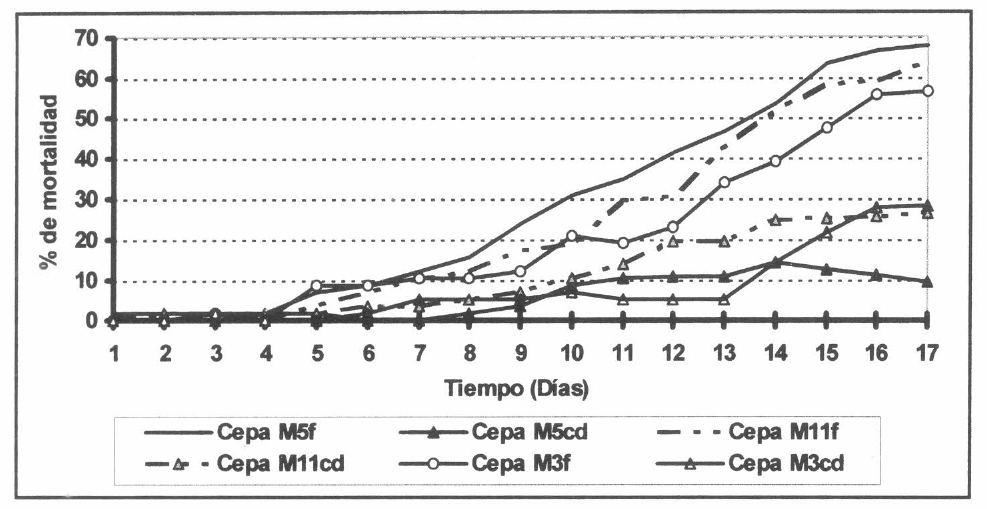
Efecto biocontrolador en campo sobre adultos de R. schistocercoides de las cepas formuladas y no formuladas a una concentración de 1x108 propágulos/ml.
A pesar de las diferencias mencionadas entre los tratamientos, cabe destacar que hasta el cuarto día todos los tratamientos conservaron un promedio de mortalidad bajo (1.7%) y que a partir de ahí las cepas formuladas comenzaron a causar más mortalidad que las cepas no formuladas. Este comportamiento coincidió con el hecho de que aproximadamente en el cuarto día concluye el primer aso infectivo del hongo, que es la penetración de la cutícula y la llegada de éste a la hemolinfa, lo que desencadena las reacciones enzimáticas del hongo y la invasión y muerte de las langostas. El aumento constante de la mortalidad desde el cuarto día hasta el día diecisiete, podría deberse a una segunda infección causada por los conidios del hongo que permanecieron viables y latentes en la tierra o en la cutícula del insecto, como lo sugieren Lomer et al. (1993) Y Milner et al. (1994). Esta viabilidad se pudo deber porque la formulación le confirió protección a los conidios el tiempo necesario hasta que éstas encontraran las condiciones ambientales propicias para salir de su latencia. Teniendo en cuenta que el ensayo se realizó a una temperatura promedio de 36°C y a una humedad relativa promedio del 56%, las cuales representan condiciones adversas para cualquier hongo en campo, cabe destacar el papel importante de la formulación para preservar las características entomopatogénicas de M. anisopliae.
Cuando las langostas fueron asperjadas con el hongo formulado a una concentración de 1x 107 propágulos/ml, se encontró para la cepa M5 una mortalidad de 54.7%, para la cepa M3 de 49.1 % Y para la cepa M 11 de 52,8%; no presentando diferencias significativas entre ellas (f=O.98; gl=5; p<0.05). Al ser asperjadas las langostas con los conidios desnudos (sin formular), los porcentajes de mortalidad fueron de 7,6% para la cepa M5, 16.9% para la cepa M3 y 13.2% para la cepa M 11; sin diferencias significativas entre ellas. Para este caso, también se encontraron diferencias significativas entre la mortalidad ocasionada por las cepas formuladas y la causada por las cepas sin formular (f=4.2; gl= 12; p<0.05).
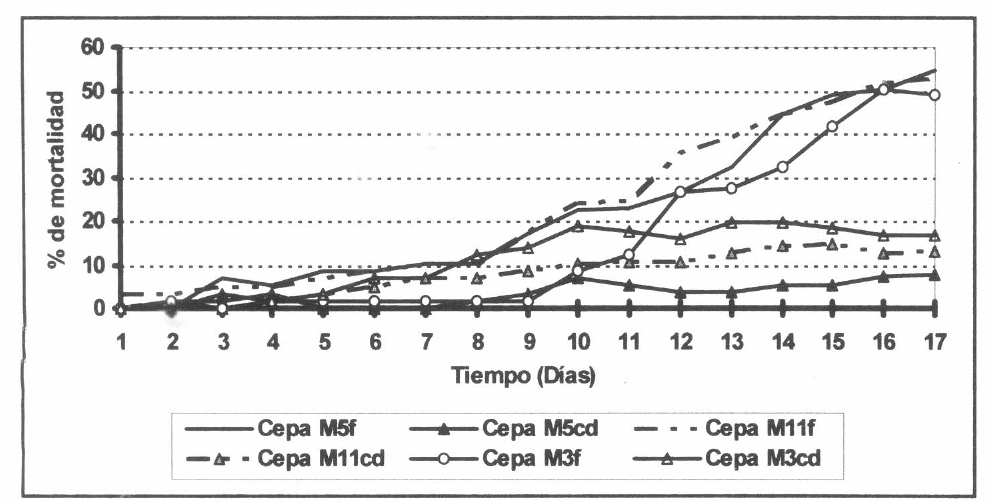
Efecto biocontrolador en campo sobre adultos de R. schistocercoides de las cepas formuladas y no formuladas a una concentración de 1x107 propágulos/ml.
Para los resultados de biocontrol obtenidos en campo, es de resaltar que la formulación mediante la encapsulación de los conidios con protectores de luz ultravioleta, al conferirle protección al hongo en condiciones medioambientales adversas, permite que éste exprese su actividad biocontroladora.
Conclusiones
Se seleccionaron las cepas nativas de M. anisopliae M3, M5 Y MIl, pues mostraron ser promisorias para el control de la langosta Ilanera R. schistocercoides, debido a su alta actividad entomopatogénica en laboratorio y campo,
Las tres cepas evaluadas demostraron ser virulentas para la plaga de acuerdo con las dosis letales bajas que presentaron.
Bajo condiciones de campo, las cepas formuladas con protectores de luz ultravioleta presentaron significativamente mayor actividad biocontroladora que las cepas sin formular, lo que demuestra que la formulación no afecta la actividad entomopatogénica del hongo.
Footnotes
Agradecimientos
Los autores expresan su agradecimiento a todo el personal del Laboratorio de Control Biológico del Centro de Investigaciones Tibaitatá y al personal del Centro de Investigaciones Carimagua de CORPOICA_ A su vez, agradecen al ICA y a PRONATA por el apoyo financiero para la elaboración del trabajo,
