Abstract
The incidence of rice hoja blanca virus (RHBV) is increasing in Colombia. The ability to transmit the RHBV is a genetically controlled trait in the vector T. orizicolus. Since in nature there are many factors that influence the percentage of T. orizicolus that are vectors, this study was undertaken to determine the percentage of the insect with the genetic capability to transmit RHBV. In several rice growing regions of Colombia, samples of T. orizicolus were collected from fields that had different levels of RHBV infestation. The percentage of insects with the genetic capability to transmit RHBV was always higher than the percentage of insects that were viruliferous vectors in the field. This method is useful as an indicator and has helped identify the rice growing regions in Colombia that are at greatest risk of epidemics of RHBV.
Introducción
El insecto Tagosodes orizicolus (Muir) es el vector del virus de la hoja blanca del arroz (RHBV), el cual ha ocasionado grandes pérdidas económicas en América Latina (Zeigler y Morales 1990). Se han señalado epidemias de RHBV aproximadamente cada 10-15 años y luego la enfermedad virtualmente desaparece (Zeigler et al. 1994). La última epidemia de RHBV en Colombia fue en 1982, alcanzando pérdidas hasta de 100% (Vargas 1985; Varon et al. 1987; Vergel et al. 1993).
El RHBV es transmitido por el insecto de una manera persistente propagativa y pasa transováricamente a la progenie (Morales y Niessen 1985; Galvez 1968; Zeigler et al. 1994). Además, el virus causa un efecto deletéreo en insectos virulíferos, los cuales sobreviven menos que insectos libres de virus (Jennings y Pineda 1971). Se piensa que el efecto que el virus causa en el insecto, junto con la lenta multiplicación de plantas infectadas en el campo, son los responsables por la naturaleza cíclica de la enfermedad.
Los mecanismos de transmisión del virus al insecto son por alimentación directa sobre plantas enfermas y transováricamente (insecto-insecto) (Zeigler y Morales 1990). Cuando el virus es adquirido de plantas enfermas, el período promedio de incubación en el insecto vector, antes de la transmisión, es de 20 a 25 días, sin embargo, cuando el virus es adquirido transováricamente puede ser transmitido en los primeros ínstares ninfales (Zeigler et al. 1994).
No todos los insectos tienen la capacidad de transmitir el RHBV pues ello depende de un único gen recesivo (Zeigler y Morales 1990). En condiciones de campo, normalmente, menos del 2% de la población son vectores virulíferos. De acuerdo con esta habilidad, en una población dada de T. orizicolus, existen: insectos con capacidad genética de transmitir el virus, e insectos no vectores que no transmiten el virus aún después de que éste sea adquirido por alimentación y tenga un suficiente período de incubación. Los insectos con capacidad genética de transmitir el virus se subdividen en: vectores virulíferos (activos), los cuales transmiten el virus activamente en el campo (CIAT 1986) y vectores no virulíferos (potenciales) los cuales después de adquirir el virus por alimentación y un suficiente período de incubación, pueden transmitirlo a las plantas o a sus descendientes (Zeigler y Morales 1990; CIAT 1982; CIAT 1985).
Experiencias de epidemias anteriores indican que un 12-15% de "vectores virulíferos" son suficientes para iniciar una epidemia (CIAT 1982). Actualmente se desconoce el porcentaje de estos vectores, por lo que es necesario obtener mayor información para predecir este riesgo. El objetivo de este trabajo es determinar el porcentaje de vectores con capacidad genética de transmitir el virus de las zonas arroceras del país y establecer la tendencia de éstos durante las diferentes épocas del año.
Materiales y Métodos
Inóculo de Hoja Blanca
Plantas sanas de la variedad Bluebonnet 50, susceptible a RHBV fueron multiplicadas en potes de 10 cm de diámetro en los invernaderos del Centro Internacional de Agricultura Tropical (CIAT), Palmira, Colombia. Cuando las plantas tenían entre 15-20 días, después de emergencia, fueron transferidas a jaulas e inoculadas con 8-10 ninfas virulíferas, por planta, provenientes de la colonia vectora del CIAT, con un porcentaje de vectores activos mayor del 70%. Aproximadamente 5 días después de la inoculación, las plantas fueron tratadas con el insecticida (Lambda cihalotrina) o lavadas con agua para matar los insectos. A los 15-20 días después de haber removido los insectos, se seleccionaron las plantas que presentaron síntomas de RHBV, para utilizarlas como fuente de inóculo de las ninfas que fueron recolectadas en el campo.
Determinación de Vectores Virulíferos Genéticos (VVG)
Poblaciones de ninfas de T. orizicolus, de primero a cuarto instar, fueron recolectadas en lotes de 30 a 35 días de edad, en cuatro zonas arroceras del país (aproximadamente 1000 ninfas por zona); se alimentaron sobre plantas con RHBV por tres días y después los insectos individuales fueron transferidos a plantas sanas, de 10 a 15 días de edad, dentro de tubos de acetato cubiertos con una tela fina de nylon. Los insectos permanecieron individualmente en plantas sanas de la variedad susceptible Bluebonnet 50 por 21 días. El número promedio de insectos analizados por localidad fue de 180. Cada ninfa y planta fueron identificadas con un número hasta el final de la prueba.
El porcentaje de VVG se determinó mediante la transmisión directa del RHBV a plantas sanas, contando el número de éstas que presentaban síntomas de la enfermedad después de 15 días de retirados los insectos. Además, la presencia de RHBV se corroboró en los insectos, por medio de la prueba serológica inmunoenzimática de doble emparedado de anticuerpos (DAS-ELISA) (Fig. 1) (Clark y Adams 1977).
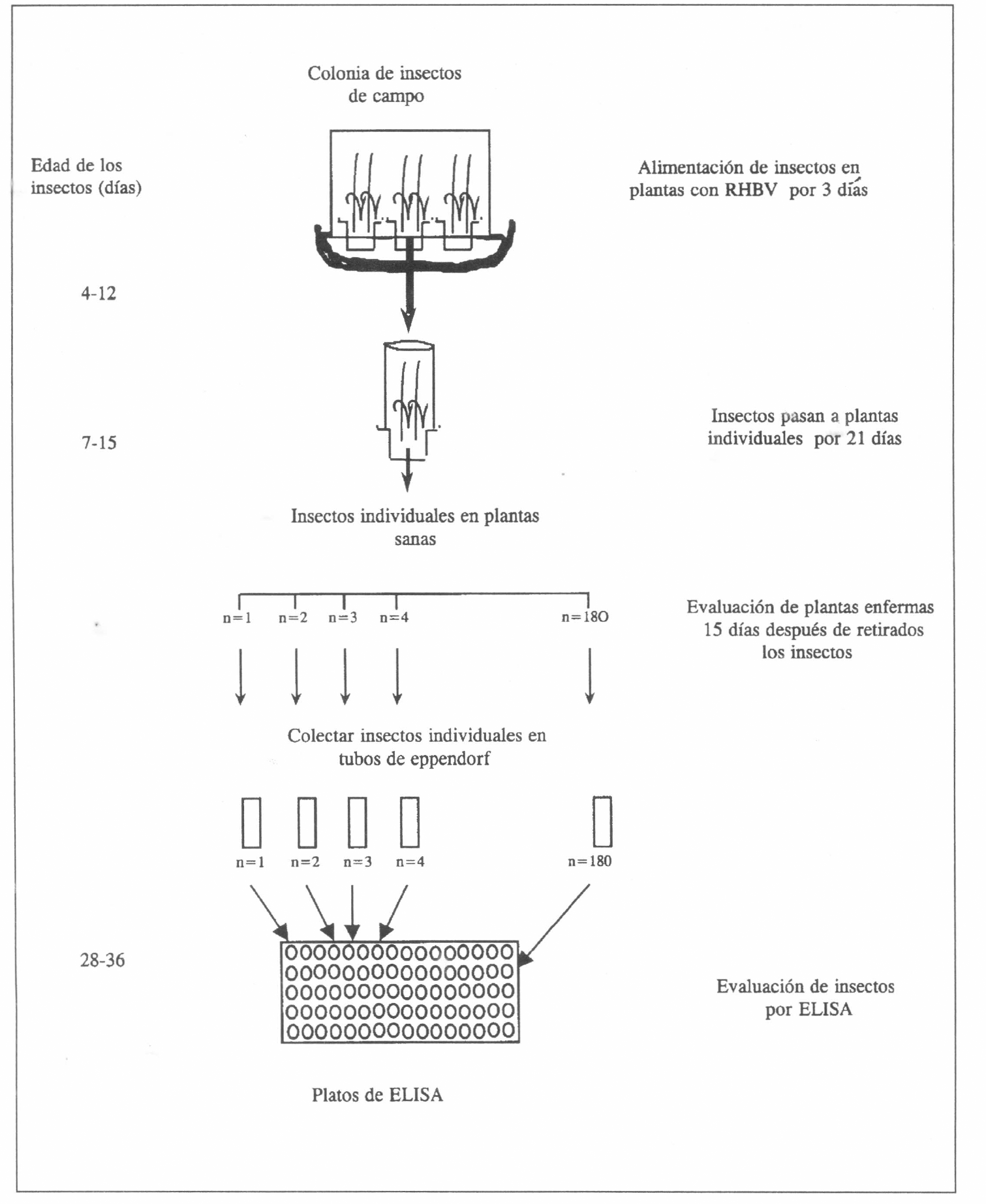
Detección de vectores virulíferos genéticos
Determinación de Vectores Virulíferos de Campo (VVC)
Simultáneamente a la recolección de las ninfas en el campo para la detección de VVG, también se recolectaron 180 insectos adultos de T. orizicolus para ser evaluados contra RHBV por DAS-ELISA y determinar el porcentaje de VVC en cada zona.
Determinación de RHBV
La presencia del virus, tanto en plantas como en insectos, se comprobó con DAS-ELISA. Para realizar esta prueba, microplatos de poliestireno (Dynatech Laboratores, Inc.) se cubrieron con la Inmuno-globulina (Ig) específica al RHBV (Morales y Niessen 1983), diluída 1/4000 en tampón carbonato de sodio, pH 9.6 y se incubaron por 4 horas a 37°C. Las muestras homogenizadas en dilución 1/10 con tampón fosfato salino (PBS) mas 0.2% de Tween-20 y 2% de polivinilpirrolidona PM 40.000 (PVP-40) se adicionaron a los platos y se dejaron a 4°C durante toda la noche. El conjugado específico (Ig marcado con la enzima fosfatasa alcalina) se agregó en una dilución 1/4000 con tampón PBS-Tween incubándose a 37°C por 4 horas. La detección del complejo antígeno-anticuerpo-conjugado se realizó utilizando como substrato de color una solución fresca de p-nitrofenil fosfato (Sigma, Cat. 104-105) a una concentración de 1 mg/ml en tampón de dietanolamina 9.7%, pH 9.8. La reacción colorimétrica resultante fue medida en valores de absorbencia a 405 nm en un espectofotómetro (Bio-Teck Instruments, Microplate Reader EL 308), a los 30 y 60 minutos, respectivamente, de haberse agregado el substrato, sin detener la reacción, considerándose como positivos los valores mayores de 0.2. En todos los platos se incluyeron como controles positivos: un insecto vector probado y una muestra de planta con síntomas de RHBV; como controles negativos: un insecto sano y una muestra de planta sana y como blanco una muestra del tampón usado para macerar los insectos. Entre los diferentes pasos del procedimiento, los platos se lavaron con el tampón PBS-Tween durante tres minutos por tres veces y se adicionaron volúmenes de 100 microlitros por pozo de cada solución. Para el análisis estadístico se utilizaron como mínimo 180 insectos por cada localidad. La comparación entre localidades fue determinada mediante el análisis de Chi-cuadrado en tablas de contingencia de 2x2, probabilidad de 0.05%.
Determinación de vectores de RHBV y plantas enfermas en zonas arroceras de Colombia (Año 1996-1997)
Insectos con capacidad genética de transmitir el RHBV en invernadero (activos + potenciales). Prueba de ELISA (180 insectos por localidad/prueba)
Determinación visual de plantas con síntomas de RHBV en invernadero (Var. Bluebonet 50).
Insectos con capacidad genética de transmitir el RHBV activamente en campo (activos). Prueba de ELISA (180 insectos por localidad/ prueba)
Determinación de incidencia de RHBV en campo por el método del marco 0.5 x 0.5 mβ (promedio de 10 lanzamientos).
Porcentajes en las columnas seguidos por la misma letra no son significativamente diferentes (Análisis de Chi-cuadrado P=0.05%).
N/D No Determinado.
Evaluación del Porcentaje de Incidencia de RHBV en Campo (ICHB)
Ingenieros Agrónomos de la Federación Nacional de Arroceros visitaron los mismos lotes donde anteriormente se habían recolectados los insectos para la detección de VVG y VVC (aproximadamente entre 60 a 80 días de edad del cultivo), para evaluar la ICHB de la siguiente manera: se tomaron 10 puntos al azar dentro de cada lote, lanzando un marco de PVC de 0.5 mβ y en cada uno de estos puntos se contó el número de macollas con RHBV y el número de macollas totales y se calculó el porcentaje de incidencia con la siguiente fórmula:
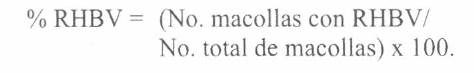
Resultados y Discusión
Detección de Vectores Virulíferos Genéticos
Después de alimentar forzadamente las ninfas de T. orizicolus por tres días en plantas con RHBV y ser transferidas por 21 días sobre plantas sanas, los insectos que transmitieron el RHBV a las plantas y fueron positivos por la prueba de DAS-ELISA se denominaron Vectores Virulíferos Genéticos (VVG). Los insectos adultos de T. orizicolus que se sometieron a la prueba de DAS-ELISA inmediatamente después de ser recolectados en el campo y fueron positivos se denominaron Vectores Virulíferos de Campo (VVC).
Se encontraron diferencias significativas en el porcentaje de VVG, porcentaje de VVC y ICHB entre las diferentes zonas (Tabla 1). Las zonas de Valle (Jamundí) y Tolima (Saldaña) presentaron porcentajes bajos de ICHB, posiblemente debido a baja virulencia de los VVC (1.1 y 1.6%, respectivamente). La zona de Cesar (Valledupar), por el contrario, presentó un porcentaje de VVC alto (5.3%) y una ICHB baja (0.9%), posiblemente debido a un conteo temprano de plantas enfermas, sin permitir un lapso de 30-40 días para observar los síntomas de RHBV o a un número menor de insectos por 10 pases dobles de jama (PDJ) (Tabla 1).
Las zonas de Meta (Castilla - var. Caribe 8), Meta (Castilla - var. Oryzica 1) y Tolima (Ambalema - var. Oryzica 1) presentaron los valores más altos de VVC (5.1%, 9.3% y 8.3%, respectivamente), estadísticamente similares y sin embargo existieron diferencias significativas en los valores de ICHB (17.3%, 6.3% y 10.0%, respectivamente) (Tabla 1). Estas inconsistencias en la ICHB pueden ser explicadas por varios factores: monocultivo de una sola variedad, migración de insectos entre variedades susceptibles y resistentes de áreas anexas, manejo del cultivo, condiciones ambientales, número de insectos por PDJ, etc. Por ejemplo, en la zona de Cesar el 90 % del área es sembrada durante todo el año con la variedad Oryzica 1 tolerante al RHBV, mientras que en el Meta y Tolima, variedades susceptibles y resistentes se siembran en el mismo semestre (Cica 8, Oryzica Caribe 8, Oryzica 1, Oryzica Yacu 9, Selecta 320). Los resultados anteriormente expuestos sugieren que es importante considerar el manejo de las variedades a sembrar en las diferentes zonas arroceras, según el comportamiento de las poblaciones de T. orizicolus en campo.
En Valle (Jamundí - var. Selecta 320) y Tolima (Saldaña - var. Oryzica 1) se presentaron los menores porcentajes de plantas enfermas y VVG de todas las áreas arroceras muestreadas (Tabla 1), debido posiblemente a las variedades sembradas y a los bajos porcentajes de VVC encontrados, sugiriendo que el riesgo de una epidemia de RHBV en estas zonas es más bajo que en las demás zonas arroceras del país. Por otra parte, en Cesar-Valledupar que presentó bajos porcentajes de plantas enfermas y porcentajes intermedios de VVC y VVG, se mantiene el riesgo de una epidemia si se incrementa el área de siembra con variedades susceptibles al RHBV.
En Tolima-Ambalema y Meta-Castilla (Fig. 2) se presentaron valores de VVC (9.3 % y 8.3%) cercanos a los obtenidos en epidemias anteriores (12 a 15%), como también los valores más altos de VVG de todas las zonas arroceras del país (16.7% y 21%, respectivamente). Lo anterior indica que estas áreas presentan un riesgo alto de desarrollar epidemias localizadas si se continúan sembrando materiales susceptibles al RHBV y deben ser consideradas como "focos de alto nivel de hoja blanca". El porcentaje de VVG fue siempre mayor que el porcentaje de VVC en todas las zonas arroceras muestreadas (Fig. 2).
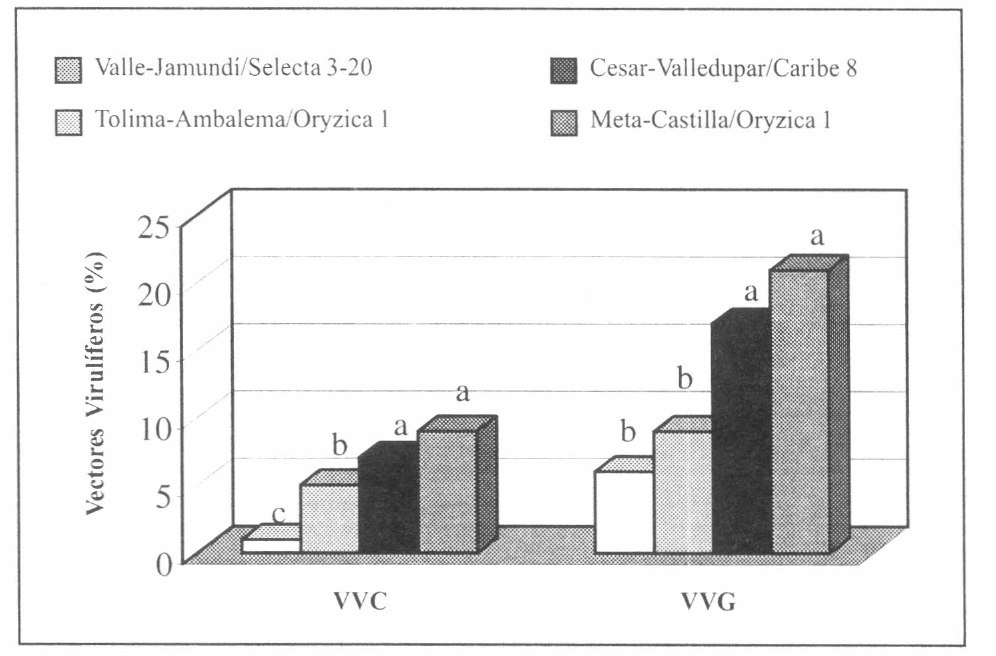
Determinación de vectores virulíferos de RHBV en zonas arroceras de Colombia
El análisis de correlación lineal entre %VVG y %VVC reveló una alta asociación (r = 0.97, p = 0.006) con la ecuación de regresión: VVG = 2.09 + 1.84 VVC, siendo adecuada para estimar VVG cuando VVC es menor del 10%. Lo anterior indica que existe una relación directa entre VVC y el número total de insectos que tienen la capacidad genética de transmitir el virus (vectores virulíferos + vectores no virulíferos).
El efecto de la región y variedad sobre el RHBV es presentado en la figura 3. En dos zonas diferentes del Tolima (Saldaña y Ambalema) se presentaron diferencias significativas en el porcentaje de VVC y ICHB. Estos resultados sugieren que la determinación del porcentaje de VVC depende de la zona donde se realice el muestreo y la variedad sembrada. La determinación del porcentaje de VVC indica la virulencia de los insectos en un momento determinado en una zona, mientras que la determinación del porcentaje de VVG indica la capacidad genética de la población de insectos, la cual no depende de la variedad ni cambia rápidamente en el tiempo. Al determinar la capacidad genética de una población de insectos, se mide la frecuencia de los genes de resistencia de los individuos que son homocigotos recesivos de esa población. Por esta razón, la manera más segura para determinar el riesgo de una epidemia de RHBV es determinando el número total de insectos que tienen la capacidad genética de transmitir el RHBV. Los resultados también indican que existen poblaciones de insectos con capacidad genética de transmitir el RHBV hasta un 21%, lo cual supera los niveles de vectores virulíferos señalados en epidemias anteriores.
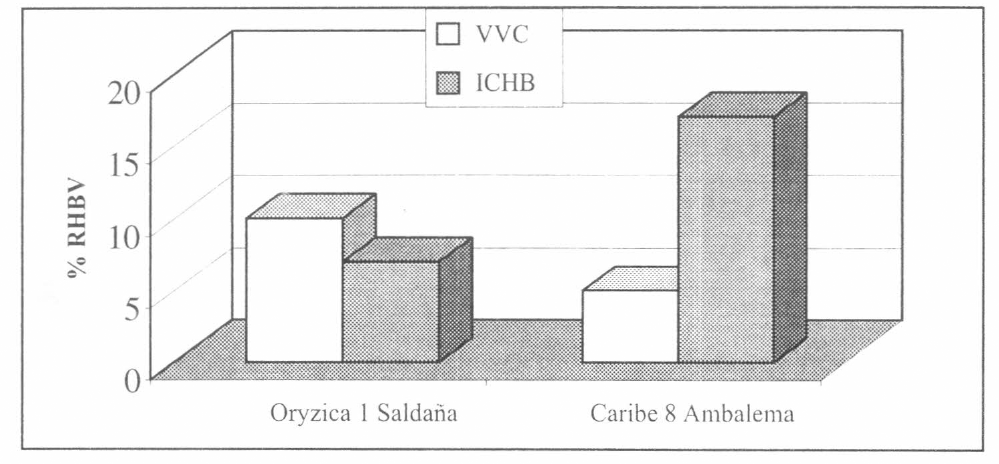
Comparación de variedades y regiones al RHBV en campo.
Conclusiones
En esta investigación se realizó un procedimiento que mostró que todos los insectos que tienen la capacidad genética de transmitir el virus son vectores. Lo anterior significa que tanto vectores virulíferos (activos) como vectores no virulíferos (potenciales), se calculan conjuntamente en vectores virulíferos genéticos (VVG), indicando de una manera más precisa el riesgo temprano de una epidemia de RHBV. Los resultados anteriores sugieren que entre los factores que ocasionan una epidemia de RHBV, además de la variedad y número de T. orizicolus, el porcentaje de vectores virulíferos genéticos juega un papel importante. Variedades susceptibles como Oryzica Caribe 8 son más severamente afectadas que variedades que presentan resistencia al virus en campo. La susceptibilidad de las variedades tiene importantes implicaciones epidemiológicas. Si se siembran variedades "resistentes" cerca a cultivos establecidos de variedades susceptibles con altos porcentajes de vectores virulíferos, se puede presentar un alto porcentaje de plantas infectadas en la variedad resistente. De acuerdo con la evaluación del porcentaje de vectores virulíferos genéticos se deben planificar acciones específicas dirigidas a cada una de las zonas arroceras del país para reducir el riesgo de epidemias. En zonas donde el porcentaje de vectores virulíferos genéticos sea alto no se debe continuar sembrando variedades susceptibles. El alto porcentaje de vectores virulíferos genéticos en las zonas de Tolima y Meta, sugieren que sólo falta una mayor fuente de inóculo para que se inicie una epidemia de RHBV. La determinación del porcentaje de insectos con capacidad genética de transmitir el virus es un aviso temprano del riesgo que tiene un área de presentar una epidemia de RHBV, comparándola con otras. Es probable que el incremento actual de virulencia del insecto sea el inicio de una nueva epidemia de RHBV en Colombia. Se requiere más información para tener un claro entendimiento de la población de insectos vectores y de los factores que promueven la formación de una epidemia de RHBV.
