Abstract
The in vitro production of the mycotoxin beauvericin by Beauveria bassiana 9401 originally isolated from Lutzomyia sp. (Diptera: Psychodidae) potential vector of Leishmaniosis was determined. The mycotoxin was detected in fractions obtained from crude extracts of dry mycelia, the identification and quantification of the mycotoxin was done by Liquid Chromatography High Performance HPLC; approximately 2.7% of crude extract was beauvericin. The cytotoxic effects of beauvericin in Aedes albopictus C6/36 cell line defined as morphological alterations and diminution in cellular viability was demonstrated, the CL50 value of an fraction with 10% of beauvericin for cells was estimated as 25 ng/ml.
Introducción
El hongo Beauveria bassiana es uno de los entomopatógenos más ampliamente estudiados por su potencial como agente de control biológico; debido a su frecuente utilización y a las grandes cantidades de esporas que se aplican en el campo, aspectos como su patogenicidad y su seguridad para organismos no blanco, están siendo constantemente reevaluados.
En cuanto a la patogenicidad la producción de micotoxinas como la beauvericina ha generado gran interés, ya que al parecer estas sustancias son responsables en buena parte del grado de patogenicidad de este hongo y se constituyen en la forma principal para bloquear los mecanismos de respuesta inmune del insecto (Vey et al. 1985; Khachatourians 1991; Eyal et al. 1994).
Adicionalmente, estudios recientes realizados por la agencia de protección ambiental de los Estados Unidos (EPA) con beauvericina producida por aislamientos de B. bassiana, utilizados en ecosistemas acuáticos para controlar larvas de mosquitos, mostraron alto grado de citotoxicidad en camarones, peces y cangrejos de estuario, lo cual ha generado importantes controversias en cuanto al papel de esta micotoxina en relación con la inocuidad del hongo para otros organismos (Hamil et al. 1969; Genthner y Middaugh 1992; Genthner et al. 1994; Middaugh et al. 1994).
A pesar de que B. bassiana es un entomopatógeno ampliamente utilizado en programas de biocontrol y a la importancia que revisten micotoxinas como la beauvericina producida por este hongo, en paises como Colombia se han realizado pocos estudios sobre el mecanismo de acción de la misma o sobre su producción por los aislamientos del hongo y se carece de una metodología estándar que permita caracterizar los diferentes aislamientos en cuanto a tal producción. Estos estudios son necesarios si se considera que, de acuerdo con algunos autores, tanto la producción como la toxicidad de la beauvericina varían dependiendo de la procedencia del aislamiento (West y Briggs 1968; Susuki et al. 1977; Quiot et al. 1993; Roberts 1986; Kchachatourians 1991).
En la presente investigación, modificando algunas metodologías previamente descritas que aparecen en la literatura, se estandarizó una metodología de laboratorio que permitió determinar la presencia de beauvericina en extractos procedentes del micelio del aislamiento 9401 de B. bassiana, un aislamiento que reviste especial interés por su patogenicidad, comprobada hacia insectos de importancia médica como Aedes sp. y Lutzomyia sp.
Se pretende que esta metodología pueda ser utilizada para detectar la producción de beauvericina por otros aislamientos de este hongo y que a su vez facilite el aislamiento y purificación para posteriores estudios sobre el mecanismo de acción.
Con el objeto de verificar el efecto citotóxico de la beauvericina, se realizaron algunas pruebas in vitro con la línea celular C6/36 de Aedes albopictus evaluando la citotoxidad en términos de alteraciones morfológicas y disminución en la viabilidad celular. La citoxicidad encontrada en esta línea celular vislumbra la posibilidad de estudiar y entender el mecanismo de acción de la micotoxina a nivel molecular usando esta línea como modelo in vitro para las pruebas.
Materiales y Métodos
Cultivo y preservación del hongo Beauveria bassiana
El hongo se mantuvo por cultivo en medio sólido Sabouraud Dextrosa Agar (SDA); para la obtención de conidias se utilizó la técnica de Rombach (1988) inoculándose el hongo durante dos semanas al cabo de las cuales se retiró el hongo con la ayuda de un bisturí estéril y se preparó una solución madre de esporas con agua destilada estéril (10 ml) más Tween 80 al 0,1%, se realizaron diluciones de 10−3 y conteo en la cámara de Neubauer para obtener la concentración de esporas deseada.
Las conidias fueron sembradas en caldo Sabouraud a una concentración de 140 x 106, en erlenmeyers que contenían 250 ml de medio que fueron dejados en agitación durante diez días al cabo de los cuales el hongo se cosechó al vacío mediante un embudo de filtración determinándose el peso en mg después de secarse a 35°C durante 2 horas; antes de secarse la masa micelial fue lavada tres veces con agua destilada estéril.
Obtención de extractos y determinación de la beauvericina
Para la obtención de los extractos el micelio seco fue suspendido en metanol durante una semana, posteriormente éste fué separado mediante filtración y el metanol fue eliminado por rotaevaporación, los extractos metanólicos fueron resuspendidos en acetato de etilo durante un día y finalmente, después de eliminar el acetato de etilo por rotaevaporación se determinó el peso de extracto en mg por gramo de micelio seco.
El fraccionamiento de los extractos se realizó mediante columnas de cromatografía utilizando como soporte inerte sílica gel, previa determinación de la fase o eluente por cromatografía de capa fina.
Las fracciones más puras, con migración similar a la beauvericina en capa fina y que en infrarojo presentaron las señales características de beauvericina C=O(éster) 1745 y C=O(amida) 1660, fueron llevadas a cromatografía líquida de alta performancia HPLC para verificar, mediante comparación con el estándar, la presencia de la micotoxina (Zocher y Kleinhauff 1982).
Para la separación en el HPLC se utilizó una columna C18 octadecilsilano fase reversa, con una longitud de 30 cm, diámetro interno 4 y tamaño de partícula 5 micras; como diluyente se usó metanol y como fase móvil acetonitrilo - agua en un gradiente lineal de 0 a 20 minutos iniciando 70:30 y terminando 90:10. A partir de 21 minutos acetonitrilo 100% hasta los 25 minutos.
El volumen de inyección fue 100 µlts y el flujo constante de 1 mililitro por minuto; este procedimiento fue realizado de acuerdo con las metodologías modificadas de Genthner et al. (1994) y Gupta et al. (1995).
La cantidad de micotoxina detectada en las muestras fue expresada como mg de toxina por mg de fracción.
La proporción en porcentaje de micotoxina en el extracto crudo fue calculada teniendo en cuenta la cantidad de muestra en miligramos obtenida del extracto.
Pruebas en la línea celular
La línea celular C6/36 de Aedes albopictus K.R.P Singh (1967) fue mantenida en medio esencial mínimo MEM con sales más suplementos: suero fetal bovino SFB, L-glutamina 0,1% y mezcla de vitaminas 1%.
Las células fueron cultivadas a una concentración inicial de 6x105 en botellas para cultivo celular e incubadas a 33° C en medio de crecimiento con SFB al 10%, posteriormente fueron desprendidas con un policía de caucho y resuspendidas durante dos días en medio MEM con SFB al 2%.
Al momento de las pruebas se verificó la viabilidad de las células mediante dilución 1:10 con colorante vital eosina al 0,1% contando las células viables con la ayuda de un hemocitómetro; se realizaron las pruebas con poblaciones celulares cuya viabilidad fue igual o superior al 90%, de acuerdo con lo establecido por Phillips (1973).
Para las pruebas, las células fueron dispensadas en placas para cultivo celular de 25 pozos a una concentración de 7,5 x 104 células por pozo e incubadas con SFB al 10% durante cuatro horas, posteriormente el medio de cultivo de las células fue reemplazado por medio fresco en el cual había sido diluída una fracción con 10% de beauvericina detectada por HPLC.
Las diluciones de la fracción con la micotoxina en el medio de cultivo celular fueron 1/2, 1/10, 1/100 y 1/1000, cada una de las cuales fue considerada como un tratamiento. Se realizaron tres réplicas por cada tratamiento y se utilizaron como controles células sin tratar y células tratadas con una fracción en la cual no se detectó beauvericina mediante HPLC.
Las células se incubaron y se realizó recuento y determinación de viabilidad a las 24 horas. La citoxicidad fue evaluada en términos de disminución en la viabilidad medida con colorante vital eosina, alteraciones morfológicas y dosis letal 50 DL50, este valor fue determinado mediante el modelo de regresión lineal, curva sigmoidea dosis-respuesta con pendiente fija (prisma).
Resultados y Discusión
Obtención de los extractos y detección de la beauvericina
El peso de extracto final en acetato de etilo fue 36.4 mg/g de micelio seco; al comparar los tiempos de retención y los cromatogramas del estándar con las fracciones obtenidas a partir de los extractos del hongo se verificó la presencia de la micotoxina en las fracciones obtenidas utilizando como eluentes hexano, diclorometano, acetato de etilo, en proporción: 8: 1,5: 0,5 y diclorometano: hexano 9,8: 2,0. Los picos con tiempos de retención de 12,8 y 12,6 corresponden a la beauvericina, el tiempo de retención del estándar fue 12.8 (Fig 1).
La cantidad de beauvericina fue determinada como 0,1 y 0.0038 mg/mg de fracción llevada al HPLC, el porcentaje de la micotoxina en el extracto crudo fue 2.7% y la producción estimada de la micotoxina por gramo de micelio seco 0.72 mg.
Estos resultados comparados con los obtenidos por Genthner et al. (1994) y Gupta et al. (1995), en estudios similares con otros aislamientos de B. bassiana, confirman la variabilidad en la producción de la beauvericina por los diferentes aislamientos del hongo; es decir, en cuanto al rendimiento o cantidad obtenida por gramo de micelio seco; sin embargo, debe considerarse que las diferencias en las técnicas utilizadas para la extracción y cuantificación de la toxina pueden constituir en si mismas una fuente de variación.
Igualmente, el crecimiento, la producción de micelio y de esporas y por lo tanto de micotoxinas, como resultado del metabolismo del hongo, están seguramente influenciados por aspectos como el medio de cultivo utilizado así como el tiempo y la forma de incubación del mismo: estacionaria o en agitación (Rombach 1988).
Pruebas de citotoxicidad
La disminución en la viabilidad de las células de Aedes albopictus tratadas con la fracción con 10% de beauvericina aparece en la figura 2; se observó que los efectos fueron marcados con las concentraciones más altas y que disminuyeron a medida que aumentó el factor de dilución en el medio de cultivo celular.
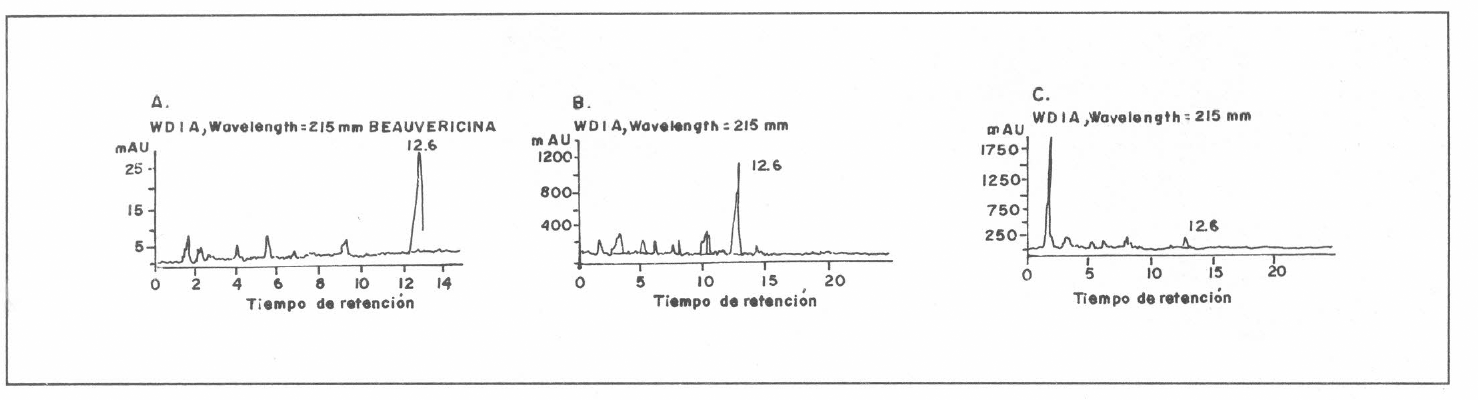
Perfil de separación HPLC para la beauvericina. A. Beauvericin (Sigma chemical Co.) B., C. Fracciones obtenidas a partir de extractos de Bb.9401.
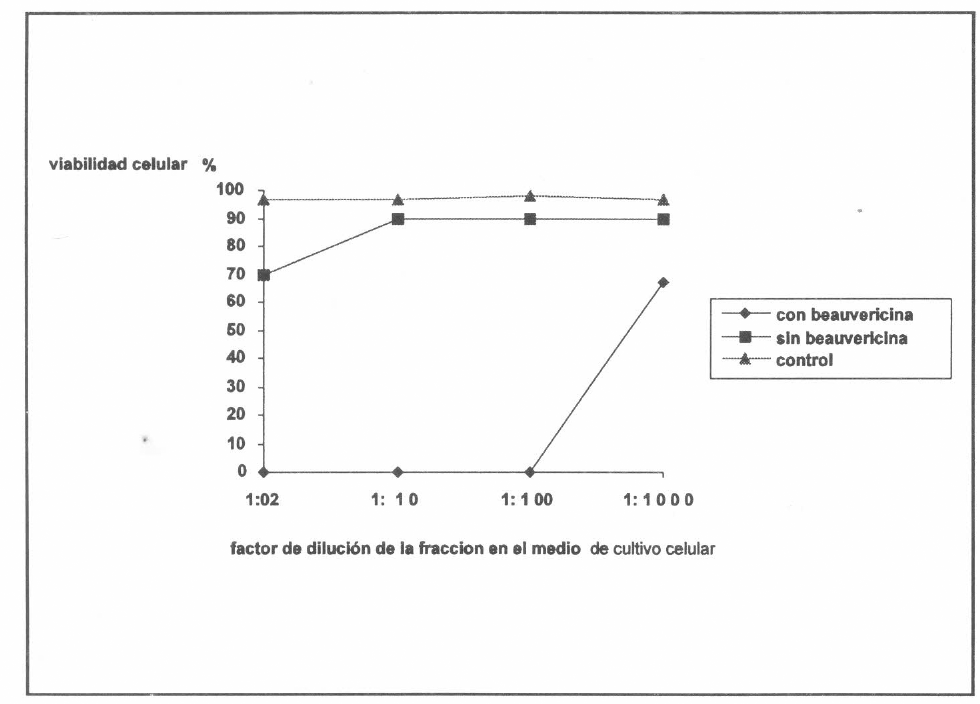
Efecto de la fracción con 10% de beauvericina detectada por HPLC sobre la línea celular C6/36 de Aedes albopictus.
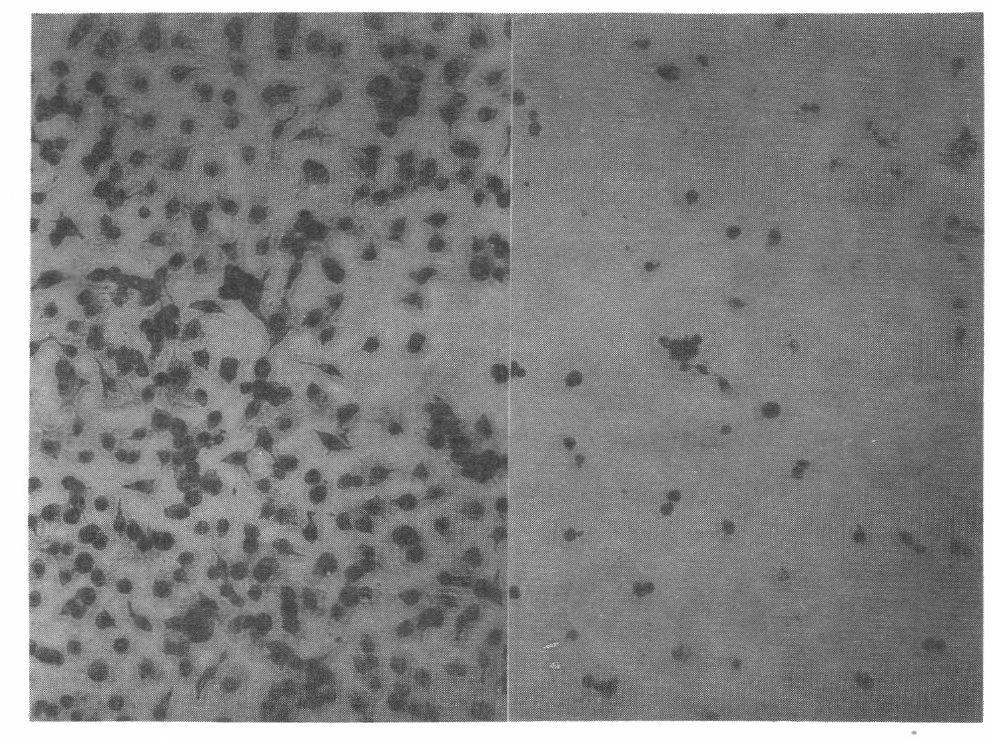
Células C6/36 Aedes albopictus sin tratar y tratadas con beauvericina (0.01 mg/ml) (40X) (microfotografía tomada por Gonzalo R., Laboratorio de Reproducción U. de A.).
En las células tratadas con la fracción con beauvercina, diluída entre 1/2 y 1/100 en el medio de cultivo celular, se observó destrucción y desprendimiento celular a las pocas horas de exposición; por lo tanto, la viabilidad de las células fue cero cuando se estimó con colorante vital eosina observándose algunas células adheridas al fondo del plato y sólo con diluciones de 1/100.
Con dilución de la beauvericina a 1/1000 en el medio de cultivo celular, el contorno de las células se alteró y se presentó retracción de los pseudópodos, observándose globulosas y con marcada granulación del citoplasma.(Figs. 3 y 4).
Estas células son procedentes del intestino del insecto y por lo tanto son una línea epitelial donde la adhesión de las células se da mediante pseudópodos, por ello la retracción de los mismos es considerada como importante señal de citocixidad cuando se utilizan este tipo de células como modelo in vitro para evaluar citotoxicidad (Quiot et al. 1993a; Kopeck y Jegorov 1992).
La dosis letal 50 (DL50) fue estimada como 25 ng/ml, valor que está de acuerdo con el encontrado en ensayos complementarios con la beauvericina estándar 18 ng/ml (datos no mostrados). Lo anterior, sumado a la ausencia de alteraciones en las células usadas como control, permite concluír que la citotoxicidad encontrada en las células tratadas con la fracción seguramente es debida a la beauvericina.
Las alteraciones encontradas en las células tratadas corresponden a las descritas por otros autores como efectos de citotoxicidad causados in vitro por micotoxinas; en el caso de la beauvericina se ha sugerido que ésta actúa como un ionóforo que afecta el transporte de cationes a través de la membrana, lo cual explicaría la destrucción celular (Roberts 1986); las dosis letales 50 (DL 50) de 25 ng encontradas para las células C6/36 sugieren la potente acción de la micotoxina en especial si se tiene en cuenta que micotoxinas como las destruxinas producidas por Metarhizium anisopliae, las cuales poseen similar estructura molecular, solo causaron efectos citotóxicos en la misma línea celular a concentraciones de 50 ug/ml (Kopeck y Jegorov 1992).
Los resultados del presente trabajo donde se confirma la producción in vitro de la micotoxina beauvericina por el aislamiento 9401 de Beauveria bassiana cuya patogenicidad ha sido previamente evaluada in vitro para Lutzomyia sp, Culex sp. y Aedes sp. (Uribe et al. 1994). Sierra et al. (1995) sugieren que probablemente esta micotoxina juega un papel importante en el proceso de patogénesis del hongo hacia estos insectos.
Se ha sugerido que la producción de metabolitos tóxicos por B. bassiana y en especial de beauvericina, no ocurre en todos los aislamientos y que puede ser afectada por factores como la procedencia de los mismos. En el presente estudio la caracterización del aislamiento Bb.9401 como productor de la micotoxina constituye un avance en el proceso de búsqueda y selección de agentes de control microbiológico para disminución de insectos de importancia médica, actividad desarrollada por el Programa de Estudio y Control de Enfermedades Tropicales PECET de la Universidad de Antioquia; sin embargo, para su utilización en el campo deberán realizarse estudios adicionales.
Conclusiones
La extracción de la beauvericina puede realizarse a partir del micelio seco de B. bassiana después de crecer el hongo en medio líquido durante diez días, tiempo que corresponde a la fase de crecimiento activo del hongo.
La extracción de beauvericina a partir del micelio de B. bassiana puede realizarse como sigue:
Secado del micelio a 35°C durante dos horas. Suspensión del micelio en metanol durante una semana Obtención del extracto crudo mediante filtración y eliminación del metanol por rotaevaporación Fraccionamiento del extracto seco por cromatografía de columna y elución de las fracciones con hexano, diclorometano, acetato de etilo en proporciones 8:1.5:0.5 y diclorometano hexano 9.8:2.
La detección y cuantificación de la beauvericina (a partir de fracciones obtenidas de la forma anteriormente descrita) puede realizarse mediante cromatografía líquida de alta performancia HPLC bajo las siguientes condiciones: columna c18-fase reversa, diluyente metanol y fase móvil acetonitrilo-agua en un gradiente lineal de 20 minutos iniciando con 70:30 y terminando 90:10 con un flujo constante de 1 mililitro por minuto.
Bb 9401 produce in vitro la beauvericina y bajo la técnica utilizada tal producción fue estimada como 0.72 mg/gr de micelio seco del hongo.
La beauvericina posee un marcado efecto citotóxico sobre la línea celular de Aedes albopictus con una DL50 de 25ng/ml.
Recomendaciones
Ya que la beauvericina parece ser una micotoxina potente, sería de gran importancia caracterizar los aislamientos utilizados en el campo de acuerdo con su producción y por consiguiente, el uso de aislamientos que la producen, como Bb.9401, deberá ser cuidadosamente evaluado en estudios toxicológicos y ambientales que permitan determinar los riesgos potenciales del hongo y la micotoxina para organismos no blanco incluyendo el hombre.
Es necesario, dada la disponibilidad de una metodología para el aislamiento y purificación de la micotoxina, implementar estudios que permitan entender y precisar su verdadero papel en la patogénesis del hongo.
Footnotes
Agradecimientos
Este trabajo fue realizado gracias a la financiación otorgada por el Comité de Investigaciones de la Universidad de Antioquia (CODI). Al doctor Javier Díaz por el suministro de la línea celular C6/36. A Gustavo Rodríguez, Jhon Dickson, Diana Lorena Muñoz y Consuelo Jaramillo por su asistencia técnica. A los laboratorios especializados de análisis, Leishmaniosis, Virología y Micología de la Universidad de Antioquia por facilitar los equipos necesarios.
