Abstract
With the purpose to standarize the conditions to obtain a biopesticide prototipe useful to the control of the llanera locust Rhammatocerus schistocercoides were established the conditions for Metarhizium spp. massive production, consisting in two methods for fungus inoculation of a sustrate based in steril humid rice contained in high density polietylene bags which were incubated for 15 days at 25°C after inoculation. One methods consisted in the utilization of a liquid preinoculum grown for two days and the other method consisted in the direct inoculation of the rice. In both cases a suspension of 10⁹ spores/ml of the fungus was used as inoculum. The highest level of sporulation was obtained with the last method and was expresed as 30 x 10⁸ u.f.c./g for M. anisopliae and 70 x 10¹³ u.f.c./g for M. flavoviridae. Spores were separated from the substrate and obtained biomass was dried for 24 hours at 25°C. Subsecuently the compatibility between spores and different individual excipients was deteminated and an adherent, a vegetal oil and two solar filters (CBUV01 and CBUV02) were selected in order to obtain a product in powder. This product consisted in spores pelletized with chemical sunscreens and was designed to be reconstituted in a oil in water emulsion (O/W) consisting in sunflower oil, Tween 80, Span 80 and water. In order to determinate the effect of UV radiation against the product bare spores and pelletized spores were exposed to ultraviolet radiation under laboratory conditions at a laboratory radiation of 253,7 nm and under field conditions solar direct exposition at Puerto López, Meta. we demostrated in both cases that excipients used to pelletize spores protected effectively the fungus against ultraviolet radiation adverse effects. Moreover, these excipients did not affect the biocontrol activity of Metarhizium spp. against llanera locust under laboratory conditions.
Introducción
En el año 1994 en la Orinoquía colombiana se observó un incremento alarmante de la población de langostas que fueron identificadas como Rhammatocerus schistocercoides (Rehn 1906).
Los registros actuales han mostrado daños principalmente en praderas nativas, de los que se calcula que por lo menos tres millones de hectáreas han sido afectadas por el insecto. Esta plaga ha llegado hasta los departamento de Vichada, Meta, Casanare y Guaviare y continúa su dispersión por otras regiones del llano (CORPOICA 1995). Sin embargo, de acuerdo a la experiencia brasileña además de afectar praderas nativas, este insecto es capaz de causar daños en cultivos como arroz, soya y sorgo.
Para el control de R. schistocercoides en el Brasil se han utilizado productos químicos clasificados como moderadamente tóxicos y de baja residualidad tales como el malathion y fenithotrion, encontrándose que este último causa la mayor mortalidad tanto en estadios ninfales como en adultos del insecto. El uso de estos productos, además de representar altos costos económicos, podría causar problemas en el delicado equilibrio de los ecosistemas (Cosenza et al. 1990).
Una alternativa promisoria para el control de esta plaga es la utilización del hongo entomopatógeno Metarhizium anisopliae y M. flavoviridae. el cual, en los últimos años ha sido exitosamente utilizado en Africa para el control de la langosta peregrina del desierto Schistocerca gregaria. Sin embargo, una limitante en la utilización de hongos como agentes efectivos de control ha sido el efecto nocivo que sobre ellos tienen factores ambientales tales como humedades relativas bajas, temperaturas altas y la radiación ultravioleta del sol. Las longitudes de onda de la luz UV que van desde 290 hasta 320 nm (UVB) y desde 200 hasta 290 nm (UVC) actúan sobre el hongo como factores mutagénico y germicidas, respectivamente.
Se ha demostrado que la utilización de aceites en la formulaciones mantienen la viabilidad de las esporas ya que evitan la desecación y protegen en cierta medida al hongo de los efectos negativos de la radiación ultravioleta. Teniendo en cuenta estas limitantes, es necesario desarrollar formulaciones cuya combinación de excipientes le permita a las esporas mantener su viabilidad y ejercer efectivamente su actividad biocontroladora.
Por lo tanto, los objetivos del presente trabajo fueron los de generar tecnologías para la producción masiva de los hongos entomopatógenos Metarhizium anisopliae y Metarhizium flavoviridae y de diseñar una preformulación de las conidias de dichos hongos, que le brindara protección contra la radiación ultravioleta aumentando su eficacia.
Revisión de literatura
Generalidades de la langosta brasilera
Rhammatocerus schistocercoides es una langosta nativa del continente americano que ha demostrado hábitos gregarios. Sus poblaciones conforman focos, los cuales se establecen por uno o varios días en sitios para, posteriormente, migrar en relación con la dirección del viento de sur a norte. Esta langosta tiene un ciclo de vida hemimetábolo que comprende cinco estados ninfales y una fase adulta. En la región de Puerto López se ha observado que durante el invierno el insecto se encuentra en estado de huevo y en el mes de marzo comienzan a aparecer los primeros insectos de manera escalonada que pasan por cinco edades o mudas antes de llegar al estado adulto (León 1996). Las ninfas de primer instar constituyen los "mosquitos"; las de segundo y tercer ínstar, las "moscas" y las ninfas de cuarto y quinto ínstar los "saltones" (Cosenza et al. 1990).
En el Brasil se ha establecido que su etapa reproductiva se inicia en la segunda quincena del mes de febrero, cuando ocurren las primeras cópulas entre los individuos y las hembras fértiles comienzan a poner sus huevos (cada hembra puede poner entre 50 y 200 huevos). En el mes de abril comienza el estado ninfal y en el mes de septiembre aparecen los primeros adultos (Cosenza et al. 1990).
En Colombia se han logrado identificar nueve ínstares ninfales que se inician en el mes de abril apareciendo los primeros adultos en el mes de septiembre. Las ninfas recien nacidas miden 6,8 mm aproximadamente y a través de cada estado ninfal su cuerpo va creciendo y cambiando de tonalidades; el último estado ninfal dura en promedio 25 días y los insectos tienen un tamaño aproximado de 31 mm (León 1996).
Generalidades de Metarhizium spp
Dentro de los hongos entomopatógenos pertenecientes a los Deuteromycetes, los del género Metarhizium (Clase Hypomycetes, Subdivisión Deuteromycotina, Orden Moniliales, Familia Stilbellaceae) son los más utilizados con éxito para el control de insectos plaga, el cual fue descubierto por Metschnikov en 1879 (Palacios 1993).
Existen tres especies conocidas de Metarhizium que difieren morfológicamente en el tamaño y color de sus conidias; Metarhizium flavoviridae (W. Gams y Rozypal) presenta esporas elipsoidales, verde grisáceas de 8,0 micrómetros de diámetro y Metarhizium anisopliae (Metschnikov) presenta esporas ovoidales, color verde oliváceo y diámetro entre 10 y 16 micrómetros. Según Tulloch (1976) esta especie comprende dos variedades (anisopliae y major Johnston) que se distinguen por el diámetro de la conidia. M. album (Petch) ha sido la especie menos estudiada (Bridge et al. 1993).
Factores ambientales que afectan la viabilidad de M. anisopliae y M. flavoviridae
El rango de temperatura óptima para el crecimiento y esporulación se encuentra entre 25 y 30°C y la humedad relativa óptima es del 94%. Sin embargo, el hongo es capaz de sobrevivir a una humedad relativa de 45% (Newman y Carner 1975) y su punto termal de muerte oscila entre 55 y 60°C (Avila y Umaña 1988).
Las conidias de M. anisopliae y M. flavoviridae, como las de la mayoría de microorganismos, pierden rápidamente su viabilidad al ser expuestas al sol, que es una de las principales fuentes de luz ultravioleta. Este emite radiaciones de longitudes de onda que van desde 200 hasta 400 nm clasificadas de la siguiente forma:
UVA: de 320 a 400 nm. No es absorbida por el ozono, pero no es considerablemente peligrosa.
UVB: de 290 a 320 nm. Es absorbida por el ADN y otras macromoléculas, induciendo reacciones fotoquímicas que conllevan a mutaciones.
UVC: de 200 a 290 nm. Es absorbida por el ozono atmosférico, por el ADN y otras macromoléculas biológicas induciendo mutaciones en los organismos; además, posee propiedades germicidas.
Las esporas de la mayoría de hongos se ven afectadas principalmente por longitudes de onda inferiores a 320 nm, radiación que puede causar retardo en la germinación o muerte de las conidias debido a la inducción de cambios en la división celular, la actividad enzimática, la permeabilidad de la membrana, el transporte iónico y el metabolismo de los fosfatos (Moore et al. 1993).
Preformulación de bioinsecticidas
La preformulación y formulación son etapas fundamentales en el desarrollo de un bioinsecticida. El objetivo de la formulación es proveer la combinación correcta, de tal manera que el ingrediente activo, para el caso, las conidias de Metarhizium junto con otros materiales formen un producto estable, seguro, efectivo, fácil de aplicar y aceptable para su uso. Para desarrollar un producto, con estas características, es indispensable realizar previamente un estudio de preformulación que revele las propiedades físicas, químicas, microbiológicas, etc., del principio activo (conidias) sólo y en combinación con los auxiliares de formulación que comúnmente se utilizan.
En toda formulación independientemente de su uso final, se distinguen dos clases de componentes: la materia o principio activo, responsable de la actividad insecticida y los excipientes que actúan como vehículos de la materia activa, sean sólidos o líquidos, ayudando al principio activo en el cumplimento de su cometido, aumentando su persistencia en el medio ambiente o mejorando su propia acción. Estos compuestos son inertes frente a los patógenos y permiten:
*Mejorar la estabilidad biológica y física de las formulaciones bajo condiciones razonables de almacenamiento.
*Incrementar la cobertura y adherencia del producto formulado sobre el follaje o la superficie del insecto.
*Usar aditivos para evitar la evaporación, para mejorar la dispersión y suspendibilidad del producto en los tanques de aplicación.
*Incrementar la resistencia a condiciones tales como lluvia y degradación por luz ultravioleta.
*Reducir la pérdida del producto durante la aspersión, exponiéndolo a una variedad de sistemas de aplicación, para establecer las condiciones bajo las cuales el material debe ser aplicado de acuerdo con las diferentes regiones geográficas (Couch 1978).
Materiales y Métodos
Microorganismos y medios de cultivo
En el presente estudio se utilizó la cepa de Metarhizium anisopliae M1 proveniente de Carimagua, Colombia y la cepa de Metarhizium flavoviridae (IMI 330189) proveniente de IIBC de Inglaterra (International Institute of Biological Control).
Con el propósito de mantener el material biológico, cada una de las cepas fue conservada en latencia a 8°C en ampolletas que contenían suelo estéril tamizado. El mantenimiento de las cepas cultivadas en tubo con medio PDA también se hizo a 8°C, en oscuridad.
Producción masiva
Para la producción de las mencionadas cepas de Metarhizium spp. se probaron dos métodos, uno de ellos basado en la utilización de dos fases de cultivo (Jenkins y Lamer 1994) y el otro en una sola fase. El método basado en dos fases de cultivo comprendió la utilización de un medio líquido cuya composición por litro fue de 20 gramos de levadura y 30 gramos de sacarosa. 75 ml de este medio líquido, fueron dispensados en erlenmeyers de 125 ml que posteriormente se esterilizaron. Cada erlenmeyer fue inoculado con 1 ml de una suspensión de conidias de M. anisopliae y M. flavoviridae que contenía 8 x 106 conidias/ml. Estos erlenmeyers se incubaron por 48 horas a 25°C con una agitación constante de l50 rpm. La biomasa obtenida fue utilizada para inocular el medio de cultivo sólido. Este último consistió en arroz humedecido estéril contenido en- bolsas de polietileno de alta densidad a [as que se les acondicionó un tapón de algodón. Las bolsas fueron incubadas a 25°C por un período de 15 días (Jenkins y Prior 1993).
Adicionalmente, se evaluó otro como una alternativa al medio líquido previamente descrito, en el cual se reemplazó la levadura por avena comercial en la misma proporción.
Para evaluar la producción masiva mediante la utilización de una sola fase se obvió la utilización del precultivo líquido y las bolsas que contenían el medio de arroz previamente descrito se inocularon con la mencionada suspensión de esporas del hongo. Las condiciones de temperatura y tiempo de incubación fueron las mismas utilizadas en el ensayo anterior.
Se realizaron tres réplicas de cada método y cada una de ellas fue muestreada por triplicado. A partir de cada muestra se realizaron diluciones sucesivas, de las cuales se sembraron las diluciones 10-8. 10-9, y 10-10 por triplicado. utilizando la técnica de recuento en placa en medio Saboureaud- Rosa de Bengala. para determinar el número de unidades formadoras de colonia producidas por cada gramo de medio de multiplicación masiva.
Separación de las conidias
Las conidias de Metarhizium spp se separaron del arroz mediante lavado con una solución de Tween 80 al 0,1% y agitación vigorosa. La suspensión obtenida se sometió a un procedimiento de filtración al vacío a través de filtro millipore con un tamaño de poro de 0.25 micrórnetros a 30 psi. de presión en condiciones estériles. Las esporas obtenidas fueron secadas en una estufa con corriente de aire continua a 25°C por 24 horas. Para evaluar la pérdida por secado de viabilidad por la técnica de secado se tomó por triplicado una muestra de 0.1 gramo de espora húmeda proveniente del proceso de filtración, se realizaron diluciones sucesivas y se sembraron, por triplicado, las diluciones 10-9, 10-10 10-11 en medio Saboureaud- Rosa de Bengala, para determinar el número de unidades formadoras de colonia. Otras tres muestras de 0.1 gramo de espora húmeda fueron sometidas al proceso de secado anteriormente descrito, y posterior evaluación de su viabilidad con la misma metodología.
Preformulación
Como forma de presentación para el producto se eligió un polvo que contuviera esporas recubiertas con un protector solar. Este debía ser reconstituido en una base autoernulsificable, compuesta por un aceite vegetal y una mezcla de tensioactivos que permitieran emulsionar dicha suspensión en el volumen de agua necesario para su aplicación en campo.
Se probaron los siguientes excipientes que en ensayos preliminares mostraron su inocuidad sobre la viabilidad de las esporas de M. anisopliae y M. flavoviridae: dos filtros ultravioleta (CBUV01 y CBUV02). un agente gelificante, Tween 80 y Span 80.
Para el desarrollo de la pasta cubriente se ensayaron 3 concentraciones del agente gelificante. mezcladas con cada uno de los protectores solares en proporciones l:1, 1:2 y 1:3 P/P. Se evaluó cualitativamente cada una de estas pastas de acuerdo con sus propiedades de fluidez y adherencia, eligiendo la que presentara las mejores características.
Para el recubrimiento de las esporas se mezcló, en mortero de porcelana, la pasta seleccionada con las esporas húmedas recién separadas del arroz esporulado en relaciones 1:25. 1:50 y 1:100 P/P de esporas y pasta, respectivamente.
Cada mezcla obtenida del procedimiento anterior se colocó en una caja de Petri estéril. se cubrió con papel absorbente esterilizado y se sometió a secado en estufa con corriente continua de aire a 25°C por 24 horas.
Después de las 24 horas de secado, las mezclas se trituraron en mortero de porcelana estéril. hasta lograr su completa homogeneidad. Para elegir la preformulación adecuada, se hizo una evaluación microscópica por triplicado de los polvos obtenidos, estableciendo las frecuencias de cada nivel de cubrimiento y se seleccionó la mezcla que contuviera el mayor porcentaje de esporas total y parcialmente cubiertas con los excipientes. De esta mezcla, se determinó la concentración rnicrobial expresada en u.f.c. por cada gramo de producto, tomando tres muestras de 1 gramo de los diferentes productos, a partir de los cuales se prepararon diluciones sucesivas y se sembraron, por triplicado en medio Saboureaud- Rosa de Bengala, las equivalentes a 10-7, 10-8, y 10-9 para cada uno de los productos.
Para determinar la protección frente a la radiación ultravioleta ofrecida por los filtros solares utilizados, se expuso por triplicado un gramo de cada producto y un control compuesto por 0,1 gramo de espora desnuda, durante 30, 60 y 90 minutos, bajo una lámpara germicida G30TR que emite una longitud de onda de 253,7 nm (UVC). Las muestras obtenidas, después de la exposición a dicha lámpara. se sometieron a una evaluación de concentración mediante recuento en placa. Posteriormente, este ensayo fue realizado utilizando la misma metodología, pero exponiendo las muestras directamente a la luz solar en Puerto López (Meta) durante 90 minutos bajo condiciones normales de campo a 32°C de temperatura, entre las 11:30 y 13:00 horas, con una humedad relativa del 80%.
Análisis de resultados. El diseño experimental fue completamente al azar, la unidad de rnuestreo fue un gramo y la variable evaluada fue viabilidad. Se trabajaron todos los tratamientos por triplicado y el análisis estadístico utilizado fue el análisis de varianza.
Resultados y Discusión
Produccion masiva
Mediante el método de inoculación directa de la suspensión de M. anisopliae en arroz se obtuvo una producción de 30 x 10⁹ u.f.c. por gramo, mientras que mediante la técnica de dos fases se obtuvo una producción de 43 x 10⁷ y 15 x 10⁸ u.f.c, por cada gramo de arroz cuando se aplicó como inóculo una biomasa previamente cultivada en los medios líquidos levadura-sacarosa y avena-sacarosa, respectivamente (Tabla 1).
El análisis de varianza (α = 0,05) no registró diferencias significativas entre los tres tratamientos. Sin embargo, se observó una producción ligeramente superior cuando se utilizaron los métodos de inoculación directa y de producción bifásica empleando el precultivo en medio avena-sacarosa. Este resultado podría explicarse por el hecho de que el medio levadura-sacarosa tiene un menor contenido de carbono que los otros dos. El contenido de carbono es directamente proporcional a la duración de la fase de crecimiento exponencial del hongo y su agotamiento determina la iniciación de la fase de decadencia según anota Griffin (1981).
La inoculación directa del sustrato con el hongo fue elegido como el método más adecuado de multiplicación ya que se obtuvieron los mayores niveles de esporulación. Además, los otros dos procedimientos requirieron de un precultivo líquido de 48 horas que aumenta el tiempo total de incubación del cultivo. Para el caso de la inoculación directa éste fue de 15 días mientras que para la técnica de producción en dos fases fue de 17 días. Este precultivo, además de aumentar el tiempo total de la incubación, representa riesgos de contaminación que podrían hacer la técnica poco rentable.
Basados en los resultados anteriores y en la experiencia de producción masiva de M. anisopliae, se probó la producción masiva en medio arroz esterilizado por inoculación directa para M. flavoviridae, obteniéndose una producción de 72 x 10¹³ u.f.c./g.
Secado de las esporas
Metarhizium anisopliae y Metarhizium flavoviridae no mostraron diferencias significativas respecto a la biomasa obtenida. A partir de 100 gramos de arroz inoculados con Metarhizium spp. se obtuvieron 6,3 y 6,7 gramos de espora seca para M. anisopliae y M. flavoviridae, respectivamente.
El análisis de varianza (α = 0,05) permitió concluir que el proceso de secado no causó pérdidas significativas en la viabilidad de las conidias, observándose una pérdida del 1% y del 3% para M. anisopliae y M. flavoviridae, respectivamente.
Preformulación de Metarhizium spp
Al mezclar tres concentraciones del agente gelificante con cada uno de los protectores solares (CBUV01 y CBUV02) en tres diferentes proporciones, se obtuvieron nueve pastas las cuales fueron evaluadas cualitativamente en cuanto a sus características de fluidez y adherencia, seleccionando, tanto para el CBUV01 como para el CBUV02, aquella que presentó las mejores características. Esta última fue mezclada con conidias en relación 1:25, 1:50 y 1:75 P/P conidias: pasta.
Los resultados obtenidos mediante una evaluación microscópica de estas mezclas permitieron establecer que aquella en la que se detectó el mayor número de conidias totalmente cubiertas fue la relación 1:50; además, se observó que al incrementar la cantidad de pasta en la mezcla, el número de esporas totalmente cubiertas decrece (Tablas 2 y 3).
Utilizando la pasta seleccionada con ambas especies se determinó una concentración final de 45 x 10⁷ u.f.c. y 89 x 10⁷ u.f.c. por cada gramo de los productos a base de M. anisopliae preformulados con CBUV01 y CBUV02, respectivamente y de 32 x 10¹⁰ u.f.c. y 58 x 10¹⁰ u.f.c. por cada gramo de los productos a base de M. flavoviridae preformulados con CBUV01 y CBUV02, respectivamente (Tabla 4).
Las conidias de M. anisopliae presentan un tamaño entre 10 y 16 micrómetros, mientras que las esporas de M. flavoviridae tienen un tamaño entre 8 y 10 micrómetros, esto podría explicar el hecho de que un gramo de producto a base de este último hongo presentara una concentración de aproximadamente 1000 veces más que el producto a base de M. anisopliae.
La mayoría de los productos comerciales a base de M. anisopliae existentes en el mercado señalan concentraciones de 10⁸ esporas/gramo de producto. La concentración obtenida para los productos preformulados en el presente trabajo está de acuerdo con las concentraciones utilizadas comúnmente en el mercado.
Evaluación del efecto protector de la preformulación contra la radiación ultavioleta
En condiciones de laboratorio se expusieron a la luz ultravioleta conidias desnudas y preformuladas con los diferentes excipientes.
Concentración de inóculo por gramo de sustrato en el estudio de producción masiva
Porcentajes de recubrimiento de la espora de Metarhizium anisopliae con pastas de CBUV01
Porcentajes de recubrimiento de la espora de Metarhizium anisopliae con pastas de CBUV02
Concentración final de las preformulaciones en u.f.c./g de producto
Se observó una drástica disminución de la viabilidad cuando las conidias fueron expuestas desnudas o suspendidas en aceite de girasol, presentando una pérdida de viabilidad del 29% y del 24%, respectivamente, en comparación con sus testigos no expuestos, en los cuales no se registró disminución de la viabilidad. El análisis de varianza (a = 0,05) de los resultados mostró diferencias significativas entre el número de u.f.c./g encontrados en dichos tratamientos antes y después de 90 minutos de exposición, mientras que no se detectaron diferencias significativas cuando se expusieron las conidias desnudas y cuando éstas se suspendieron en aceite. En ambos casos se determinó una pérdida de viabilidad similar, lo que permite concluir que el aceite de girasol no le brinda ninguna protección a las conidias de Metarhizium spp.
Cuando las conidias se recubrieron con los filtros solares CBUV01 y CBUV02 al ser expuestas a la luz ultravioleta, no registraron pérdida significativa de viabilidad a lo largo del período de exposición ya que las pérdidas no excedieron el 2%, con respecto a los tratamientos testigo (no expuestos a la radiación UV), el cual mantuvo su viabilidad en un 100%, mientras que las conidias desnudas expuestas a la radiación ultravioleta registraron una pérdida de viabilidad del 29%. Estos resultados demostraron que las preformulaciones evaluadas actuaron como efectivos protectores contra los efectos negativos de la luz ultravioleta (Fig. 1).
Cuando se expusieron los mismos productos a la luz directa del sol, en campo (Puerto López, Meta), se observó una dramática pérdida para las conidias desnudas y suspendidas en aceite después de los primeros treinta minutos de exposición (21% y 25%, respectivamente). En contraste, se observó una protección efectiva en las conidias preformuladas con los protectores solares evaluados pues en ambos casos la viabilidad de las conidias se mantuvo constante (Fig. 2).
El análisis de varianza (a = 0,05) demostró que no existen diferencias significativas entre la viabilidad de los preformulados expuestos a la radiación ultravioleta y la viabilidad de los testigos no expuestos, ni entre la protección brindada por cada uno de los filtros solares utilizados CBUV01 y CBUV02. Para todos los tratamientos mencionados la viabilidad de las conidias se mantuvo muy cercana al 100%.
La diferencia encontrada en el comportamiento de la espora desnuda y suspendida en aceite, cuando se exponen a la luz ultravioleta en condiciones de laboratorio y campo, fue probablemente debida a que en condiciones de laboratorio la lámpara utilizada sólo emite una longitud de onda (253,7 nm), mientras que en condiciones de campo las conidias estuvieron expuestas a todo el rango de luz ultravioleta que va desde 200 hasta 400 nm, longitudes de onda que pueden tener efectos germicidas y mutagénicos según lo señalado por Moore et al. (1993). Además, bajo condiciones de campo en Puerto López, las altas temperaturas (32°C) en interacción con la humedad relativa (80%) podría haber ejercido un efecto adverso sobre la viabilidad de las conidias debido a la desecación de éstas, la cual podría haber contribuido al efecto letal.
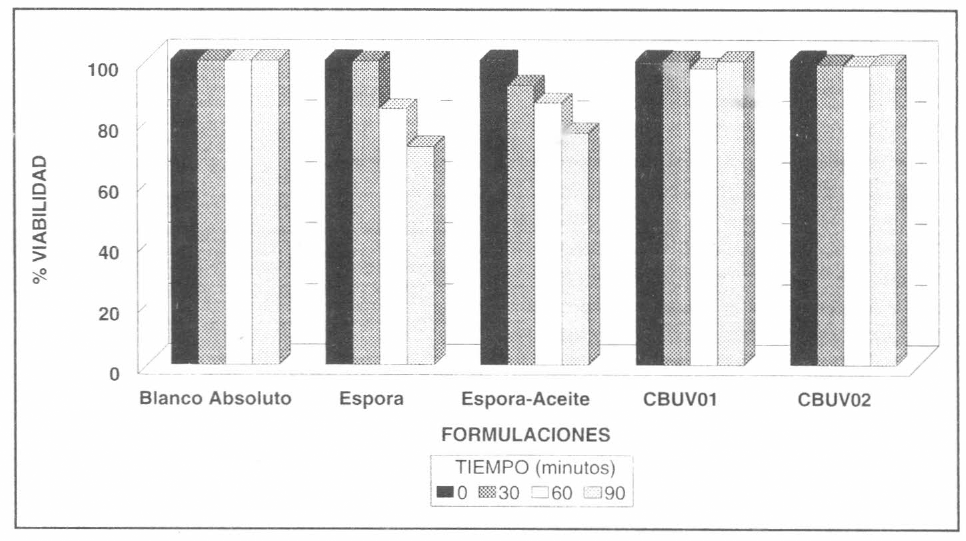
Efecto protector contra la radiación ultravioleta de las preformulaciones de Metarhizium anisopliae después de diferentes tiempos de exposición a una lámpara germicida (253,7 nm.)
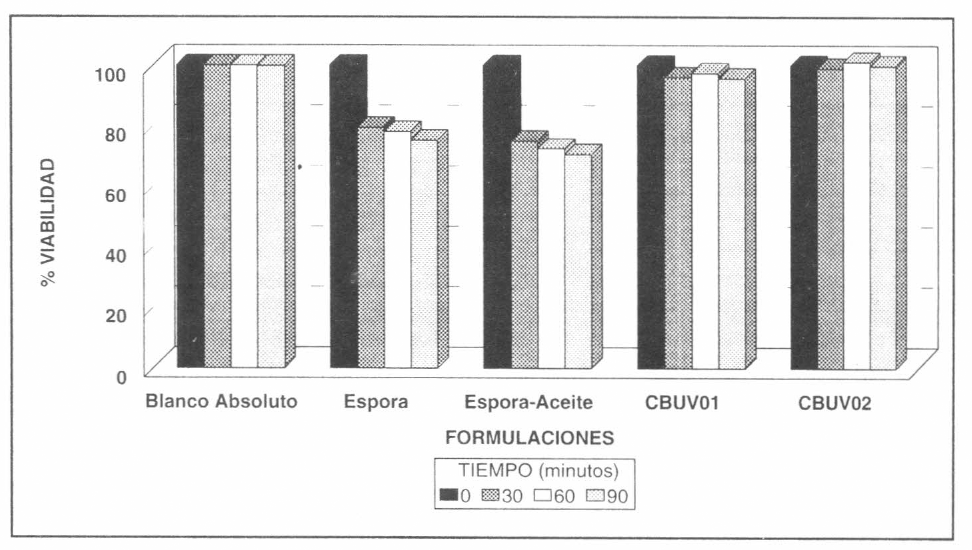
Efecto protector contra la radiación ultravioleta de las preformulaciones de Metarhizium anisopliae después de diferentes tiempos de exposición a la radiación solar directa bajo condiciones de campo en (Puerto López)
El estudio de campo realizado con las preformulaciones presentó un comportamiento similar al obtenido en laboratorio, confirmando la eficiencia de CBUV01 y CBUV02 como protectores contra la luz U.V, lo que los haría recomendables en una formulación en el futuro.
Diseño de la base auto-emulsificable
Para reconstituir el producto preformulado se deseaba obtener una emulsión aceite en agua (O/W), en la cual la fase oleosa representara menos del 10% de la emulsión, lo que significaría la utilización de 10 litros de agua como mínimo para reconstituir un kilogramo de producto. Para lograr ésto, se calculó teóricamente la mezcla de tensioactivos necesaria para alcanzar el HLB requerido por el aceite de girasol (HLB 12); esta relación fue de 72:28 P/P de Tween 80 (HLB 15) y Span 80 (HLB 4,3). Se determinó teóricamente que la máxima cantidad de mezcla de tensioactivos debía ser un peso equivalente a un 10% en peso de la fase oleosa. Sin embargo, el volumen final de agua podría ser aumentado sin perjuicio de la estabilidad de la emulsión de acuerdo con las necesidades técnicas de quien aplique el producto.
Paralelamente a este trabajo se llevó a cabo un estudio en el cual se evaluó bajo condiciones controladas de laboratorio la actividad biocontroladora tanto de las conidias desnudas como de las conidias preformuladas; para este caso, se utilizó la cepa M4 de M. anisopliae la cual había sido previamente seleccionada por su alta actividad entomopatogénica. Los resultados de este estudio mostraron que dicha actividad biocontroladora no presenta diferencias al asperjar, sobre adultos de langosta, la espora desnuda y el producto preformulado, demostrando que los excipientes utilizados para el recubrimiento de las conidias no afectan la actividad entomopatogénica que presenta el hongo contra este insecto (Zamora 1996).
Conclusiones
El método de producción masiva por inoculación directa de las esporas del hongo en arroz presentó un alto rendimiento en la esporulación de M. anisopliae (30 x 10⁸ u.f.c/g de arroz) y M. flavoviridae (72 x 10¹³ u,f,c/g de arroz).
Los excipientes utilizados para las preformulaciones no afectaron la viabilidad de las esporas de M. anisopliae y M. flavoviridae.
Los protectores solares CBUV01 y CBUV02 protegieron efectivamente las esporas de M. anisopliae y M. flavoviridae de los efectos nocivos de la radiación ultravioleta.
