Abstract
The migratory locusts are a group of insects which cause large economic losses to agriculture. When these migratory insects arrive at a place, they can eat all the plant material available especially grasses; they appear in large clouds which can weigh up to 100 tons, and are capable of consuming daily the equivalent to their own weight. The duration of an outbreak can last 4- 5 years. In Colombia in Los LLanos Orientales (Arauca, Casanare, Guaviare, Meta, Vichada), a severe outbreak of Rhammatocerus schistocercoides Rehn (Orthoptera: Acrididae) has been registered since 1993 in pastures over an area estimated at 4 million hectares. An alternative to control this insect is fungal entomopathogens, specially Metarhizium anisopliae (Metschnikoff) Sorokin. This study was planned to develop a bioassay to select highly virulent isolates for further studies to control R. schistocercoides under field conditions. The isolates evaluated were Ma9218 from Teleugryllus comodus (Orthoptera: Gryllidae) isolated in Australia and Ma9236 from an unknown host. A completed randomized design was used to test treatment effects. The experiment had three treatments, the two isolates of M. anisopliae and a control. Isolates were cultivated in Sabouraud Dextrose Agar plus lactic acid at 0.37%. Nymphs of 4th instar collected from Carimagua, were infected by submerging them for 30 seconds in a M. anisopliae suspension containing 1x107 spores/ml. The control treatment was exposed to sterile distilled water. Then the treated nymphs were placed in square plastic cages (17.5x12x7cm) provided with lateral holes covered with nylon cloth for ventilation. Five repetitions were set up for each treatment and five nymphs were deposited in each cage. The experimental units were provided daily with fresh food.
The effect of M. anisopliae on nymphs of R. schistocercoides was evident from the second day after inoculation. At the fifth day, independent of isolate evaluated, the highest daily mortality occurred: 20% for Ma 9218 and 28% for Ma 9236. Significant differences were found (P=0.05) between treatments at the end of evaluation reaching mortalities of 68.0±4.9% for Ma 9218 and 84.0 ± 7.5% for Ma 9236; mortality due to fungus was not observed in the control. Isolate Ma 9236 can be considered a candidate to be evaluated in a control program against this insect under field conditions. Bioassay methodology developed in this study can be used to test further isolates.
Introducción
La langosta migratoria Rhammatocerus schistocercoides Rehn (Orthoptera: Acrididae), conocida como la langosta brasilera debido a que sus ataques se conocieron inicialmente en ese país (Carbonell 1988), se ha detectado desde 1993 en Colombia causando grandes pérdidas a las actividades agrícolas y ganaderas en la zona de los llanos Orientales. Se estima que se ha distribuido en cerca de 4 millones de hectáreas, en los departamentos de Arauca Casanare, Guaviare, Meta y Vichada, arrasando los pastos nativos de esas regiones como la paja llanera, Paspalum pectinatum (León 1996, Jiménez y Jiménez 1996). Este insecto constituye una seria amenaza no solo para las zonas afectadas sino para otras donde potencialmente puede llegar.
La literatura sobre las investigaciones en langostas migratorias ha sido recientemente revisada (Lomer y Prior 1992). Dentro de la familia Acrididae existen alrededor de 18 especies consideradas plagas de importancia económica, ya que causan serios daños en diversos cultivos (Abdalla 1992; Bahana y Byaruhanga 1992; Bani 1992; Coffi 1992; Maiga 1992; Mouhim 1992; Niassy 1992; Zelazny 1992) siendo comunes en Suramérica algunos géneros como Schistocerca, Dicroplus, Staurorhectus y Rhammatocerus. La biología de R. schistocercoides ha sido estudiada en el Brasil (Cosenza 1987; Westin et al. 1994), el insecto presenta un estado de ninfa con una duración de 127 días, tiempo en el cual ocurren de cinco a seis instares con duración media por instar de 26 días y un estado de adulto el cual dura 210 días. Las hembras, colocan sus posturas entre los meses de octubre y noviembre, enterrando su ooteca a 5 cm de profundidad del suelo, la cual contiene de 25 a 30 huevos; cada hembra llega a efectuar hasta 5 posturas. La emergencia de las ninfas ocurre entre noviembre y diciembre; la transformación a adultos entre abril y mayo y la migración de los adultos entre agosto y septiembre; los adultos se aparean entre septiembre y octubre (Cosenza 1987). En Colombia observaciones realizadas por León (1996) indican que la biología de R. schistocercoides es muy similar. El insecto es univoltino, las oviposiciones se observaron a finales de febrero y en marzo en grupos de 30 y demoraron aproximadamente un mes para su eclosión. Las ninfas emergen con las primeras lluvias de abril y se desarrollan durante cinco meses al cabo de los cuales alcanzan el estado adulto. Los adultos de la langosta inician su migración que se prolonga entre septiembre y marzo; la cópula se inicia hacia el mes de febrero.
Estos insectos tienen hábito gregario, formando grupos que alcanzan densidades poblacionales de 500 insectos por mβ. Su movimiento y por ende el daño a los cultivos aumenta a medida que pasa de un instar a otro. Forman nubes de tipo estratiforme, con una longitud hasta de 30 km de largo y una altura de 30 m desde el nivel del suelo. Algunos autores mencionan que el peso de una nube de estas puede alcanzar hasta 100 toneladas, con un consumo por día de materia verde del equivalente a su peso (Cosenza 1987).
Tanto condiciones climáticas como topográficas especialmente baja humedad atmosférica, alta temperatura, bajas altitudes, suelos de textura fina favorecen la dispersión de R. schistocercoides (Ego-Aguirre 1946). Dentro de las preferencias alimenticias se destacan gramíneas, arroz, caña de azúcar, millo, sorgo, soya, frijol, leguminosas, tabaco, pastos, camote, café y plátano (Cosenza 1987; Ego-Aguirre 1946). En Colombia se ha observado alimentándose de pastos nativos y de pastos mejorados como Brachiaria decumbens así como de cultivos de arroz, maíz y sorgo (León 1996; Cortés y Cotes 1996).
Las poblaciones de langostas al igual que otros insectos se caracterizan por tener una gran diversidad de enemigos naturales como son parasitoides (dípteros e himenópteros), predadores (aves) y microorganismos (hongos, bacterias, protozoarios y virus) (Cunningham 1992; Greathead 1992). Algunos de estos organismos pueden ocasionar altas mortalidades como es el caso de la bacteria Coccobacillus acridiorum d'Herelle, causante de serias epidemias naturales (Bierig 1940). En 1946 en la región de Jaén (Perú), se liberó una colonia de la mosca parásita Acridiophaga caridei Bréthes, enemigo natural de la plaga en Argentina, en donde alcanzó un nivel de parasitismo del 50% en un intento para controlar Schistocerca paranensis (Burmeister) (Ego-Aguirre 1946).
En Estados Unidos, Europa, África y Asia se llevan acabo investigaciones para determinar el efecto de algunos agentes de control biológico sobre poblaciones de langostas como son: los protozoarios Nosema locustae Canning y Malamoeba locustae (King y Taylor), algunos parasitoides como Scelio howardi Crawford, Alcimus sp., Ommatius variabilis Engel, Philodicus nigrescens Ricardo (pertenecientes todos a la familia Asilidae), Anisoptera spp. (Odonata), hongos patógenos como Entomophaga grylli (Fresenius) Batko, Beauveria bassiana (Balsamo) Vuillemin, Metarhizium flavoviridae (W. Gams & J. Rozsypel), Sorosporella sp., Aspergillus flavus Link ex Fries, microsporidium Vairimorpha sp. y algunos entomopoxvirus (Cunningham 1992; Krall y Nasseh 1992; Magor 1992; Raina 1992; Zelazny 1992). También se ha probado el efecto de insecticidas de origen vegetal como el Nim, Azadirachta indica (Krall y Nasseh 1992).
Los hongos entomopatógenos pueden jugar un papel importante en el control de langostas; sin embargo, es necesario realizar investigaciones encaminadas a entender la epizootiología del hongo y seleccionar los mejores aislamientos antes que se puedan utilizar satisfactoriamente en el desarrollo de insecticidas microbiales (Goettel 1992; Milner 1992). El desarrollo de un insecticida microbial permitiría eliminar muchos problemas asociados con el uso de insecticidas químicos, especialmente lo relacionado con la polución ambiental y la toxicidad hacia otros organismos (Prior 1992). Actualmente se estudia la preparación de una formulación en aceite de M. flavoridae que se pueda asperjar bajo una tecnología de gotas controladas a bajo volumen para el control de langostas en Africa (Lomer y Prior 1992). En este trabajo se pretende mostrar la potencialidad del uso de M. anisopliae en el control de R. schistocercoides mediante la selección en laboratorio de aislamientos patogénicos.
Materiales y Métodos
Para el presente experimento se utilizaron ninfas de cuarto instar de Rhammatocerus schistocercoides suministradas por el Centro de Investigaciones Carimagua (Meta) de Corpoica. Dos aislamientos de Metarhizium anisopliae se seleccionaron del cepario de la disciplina de Entomología de Cenicafé, los codificados como Ma9218 obtenidas de Teleugryllus comodus (Orthoptera: Gryllidae) originario de Australia y Ma9236 de huésped desconocido. Se utilizó un diseño completamente aleatorio, que constó de tres tratamientos, dos aislamientos de M. anisopliae y un testigo. Por tratamiento se utilizaron cinco repeticiones y cada una estuvo conformada por cinco ninfas. Los aislamientos fueron cultivados en Agar Sabouraud Dextrosa acidificado con ácido láctico al 0,37% (ASDL), en tubos de ensayo de 15 cm de largo por 1,5cm de diámetro.
El inóculo del hongo se preparó suspendiendo las esporas de cada aislamiento en 10 ml de mezcla de Agua Destilada Estéril y Tween 80 al 0,1% (ADET). La concentración de esporas del inóculo por ml, se determinó mediante recuentos en hemocitómetro ajustándola a una concentración de 1x107 para la infección de las ninfas, la cual se realizó por inmersión completa en 50 ml de la suspensión de hongo durante 30 segundos (Vélez et al. 1996). Las ninfas que sirvieron como testigo se sumergieron en agua destilada estéril, en la misma forma. La unidad experimental la conformó una caja plástica de 17,5 x 12 x 7 cm, con orificios en sus paredes laterales, cubiertas con muselina y colocando en su interior cinco ninfas de R. schistocercoides y se utilizaron 5 repeticiones por tratamiento (n= 25). Diariamente se introdujo pasto común que sirvió como fuente de alimento para las langostas. Las evaluaciones se realizaron a los 2, 3, 5, 6, 8 y 9 días después de la inoculación del M. anisopliae sobre las ninfas de la langosta, registrando la mortalidad del hongo sobre las ninfas. La mortalidad causada por el hongo se ratificó colocando las ninfas muertas en cámara húmeda, con el fin de facilitar su manifestación sobre el insecto.
Resultados y Discusión
Los signos de la infección de M. anisopliae en R. schistocercoides son claramente diferenciables, caracterizándose por la aparición de micelio blanco en las membranas intersegmentales del insecto, con el posterior cambio de coloración a verde oliva, indicando de esta forma la esporulación del hongo sobre la ninfa (Fig. 1).
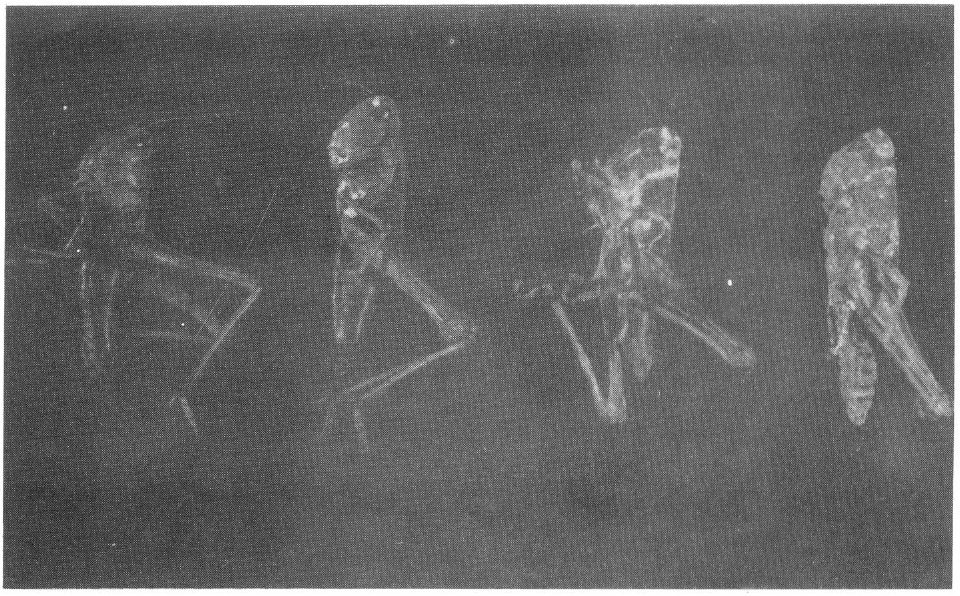
Desarrollo progresivo de M. anisopliae en ninfas de cuarto instar de R. schistocercoides
El efecto de M. anisopliae sobre ninfas de R. schistocercoides se evidencia a partir del segundo día después de la inoculación. En el día quinto, independiente del aislamiento evaluado, se presentó el mayor porcentaje de mortalidad diario, 20% para Ma9218 y 28% para Ma9236 (Fig. 2.). En relación con el porcentaje de mortalidad acumulado, se registra para este mismo tiempo un 36% y un 56% de mortalidad para Ma9218 y Ma9236 respectivamente (Fig. 3), lo que indica que el mayor efecto del hongo sobre ninfas de cuarto instar se logra en los cinco días posteriores a la infección. Lo anterior concuerda con otros trabajos en donde se evaluó el efecto de M. anisopliae, M. flavoviridae y B. bassiana sobre R. schistocercoides, encontrándose los mayores porcentajes de infección entre los 4 y los 7 días después de la infección (Cosenza 1987; León y Rey 1995).
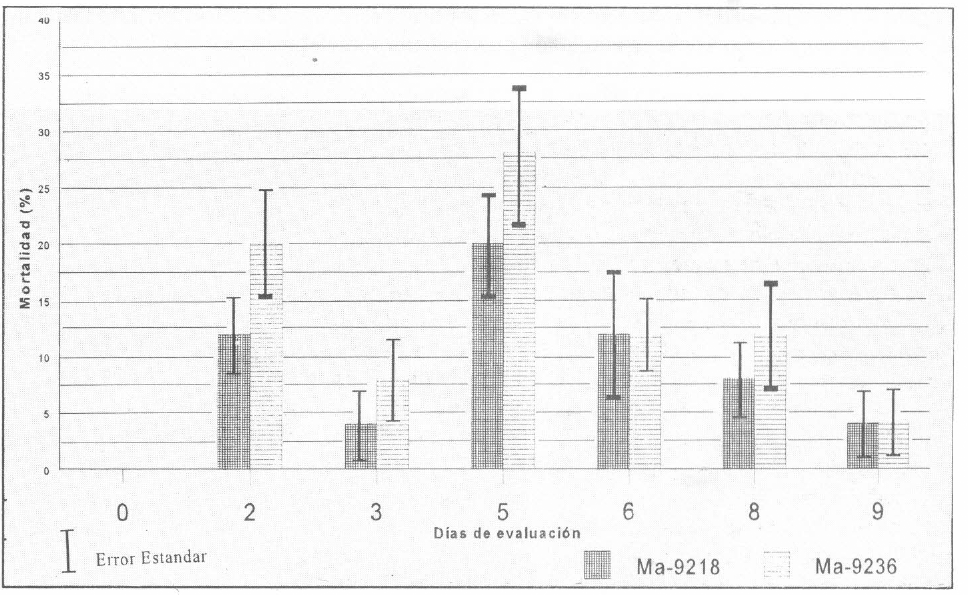
Mortalidad diaria causada por M. anisopliae en ninfas de cuarto instar de R. schistocercoides.
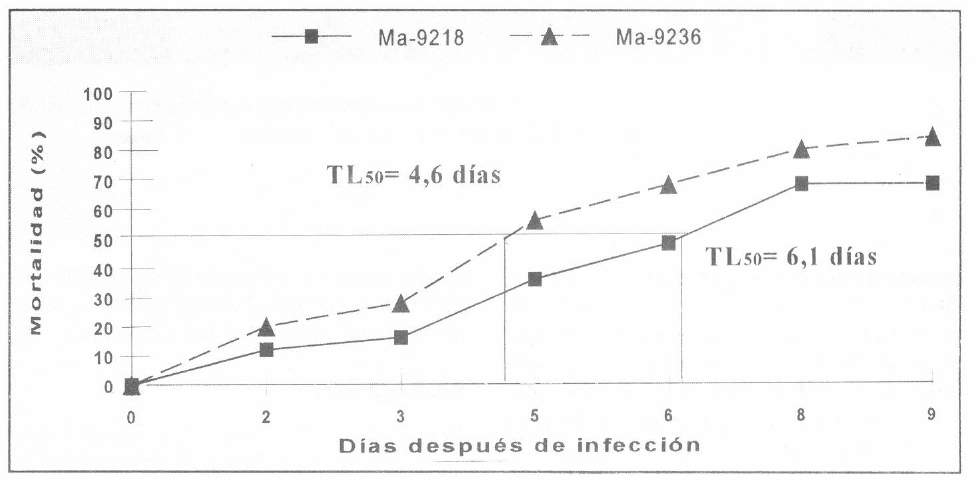
Tiempo letal 50 de ninfas de cuarto instar de R. schistocercoides infectadas con M. anisopliae
Al analizar los resultados mediante análisis de varianza (p=0,05), se encontraron diferencias significativas entre los aislamientos evaluados, presentándose porcentajes de mortalidad (
En relación con la expresión del hongo sobre el insecto, se puede observar que varía según el aislamiento, así Ma9236 presentó crecimiento abundante y pulverulento a diferencia de Ma9218, trayendo como consecuencia alta producción y fácil desprendimiento de las esporas del cuerpo del insecto infectado, lo cual contribuye a asegurar su establecimiento en el campo, favoreciendo el desarrollo de epizootias (Figs. 4 y 5).
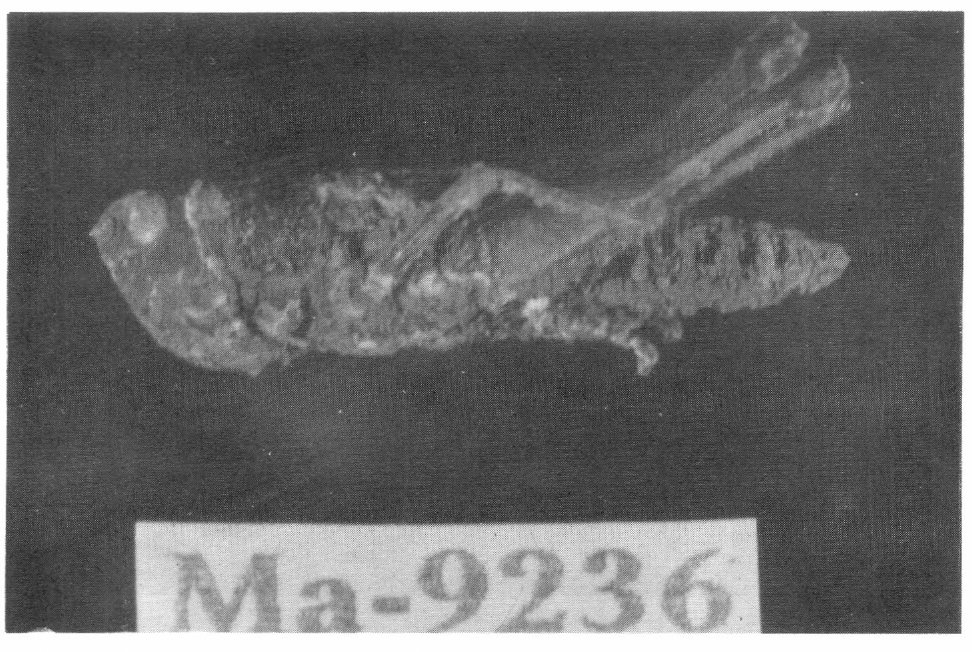
Crecimiento del aislamiento Ma9236 sobre el cuerpo de una ninfa de cuarto instar de R. schistocercoides. Nótese la esporulación pulverulenta sobre el insecto.

Crecimiento del aislamiento Ma9218 sobre el cuerpo de una ninfa de cuarto instar de R. schistocercoides. Nótese el desarrollo poco profuso sobre el insecto.
Conclusiones
Este estudio presenta una metodología para la selección de aislamientos de entomopatógenos, que se debería acoger por todas las organizaciones interesadas en los estudios de control biológico de las langostas en el país, con el fin de realizar comparaciones viables y así llevar a cabo programas de investigación en campo con los mejores organismos. A pesar de que no se evaluaron muchos aislamientos de M. anisopliae, se considera que el codificado como Ma 9236 se puede tener en cuenta para posteriores evaluaciones de campo debido a que bajo condiciones de laboratorio presentó una mayor patogenicidad y producción de esporas sobre el cadáver de las langostas.
