Abstract
From different zones of Colombia (Llanos Orientales, Pacífico, Costa Atlántica y Sabana de Bogotá) 269 strains of sporulated bacilii were isolated. In order to evaluate the toxicity of selected strains, a biological assay against third-instar larvae of Culex quinquefasciatus, Anopheles albimanus and Aedes aegypti was made. Twenty two strains showed 80-100% of mortality between 24 and 72 hours, of which 19 were classified as Bacillus sphaericus and three as B. thuringiensis. For determination of the absence or presence of the plasmidic DNA in these pathogenic strains a plasmid isolation and electrophoresis in agarose gel were made in which it was observed that 20 of 22 strains had large plasmids. To correlate the presence of these plasmids with the toxicity of the 20 strains a treatement of curing using high temperature was undertaken. It was found that four indigenous strains have plasmids linked with toxicity and there is a variability in the stability of plasmids among different strains.
Introduction
Históricamente, la malaria ha sido la enfermedad con mayor mortalidad en la humanidad (Porter et al. 1993). Esta enfermedad es causada por el protozoario parásito Plasmodium falciparum, el cual es transmitido por la picadura de mosquitos del género Anopheles spp. (Diptera: Culicidae), y se encuentra distribuida, principalmente, en Africa, Centro y Sur América, oriente del Mediterráneo y suroriente de Asia (Faust y Russell 1957). Por otra parte, aproximadamente el 90% de la fiebre amarilla, el dengue y la filariasis en el mundo, ocurre en los trópicos, donde las condiciones ambientales favorecen al vector y a los insectos transmisores de éstas enfermedades.
La aplicación del control biológico hacia diferentes especies de mosquitos como Anopheles sp., Culex sp. y Aedes sp. (Diptera: Culicidae), ha arrojado buenos resultados con la utilización de Bacillus sphaericus Nerde y Bacillus thuringiensis Berliner. Estas bacterias entomopatógenas son una buena alternativa por sus características fisiológicas y por su especificidad patogénica. Ambos microorganismos forman esporas, las cuales los hacen resistentes a condiciones adversas, y su patogenicidad es debida a la producción de un complejo de proteínas toxicogénicas durante la esporulación. Estos bacilos esporoformadores son bacterias resistentes a condiciones adversas, especialmente al calor y a la luz ultravioleta (Mc Donald et al. 1983) y tienen determinada capacidad para reciclarse en ciertos hábitats naturales que les confiere una gran ventaja sobre otros microorganismos; por tanto, estas especies de bacilos se convierten en una esperanza para la disminución de la transmisión de las filarias, de los virus del dengue y de la fiebre amarilla y del parásito de la malaria, en las zonas endémicas de Colombia.
El análisis de las toxinas ha revelado la existencia de genes relacionados, los cuales en B. thuringiensis se han localizado a nivel plasmídico, mientras que en B. sphaericus no está claro si estos genes están localizados en el cromosoma o en los plásmidos (Liu et al. 1993; Priest 1992; Singer 1987). El hecho de que estos genes se encuentren localizados en los plásmidos constituye una ventaja para el control de plagas, puesto que una sola célula, al presentar más de una copia plasmídica, puede producir las toxinas en concentraciones más altas con respecto a las cepas con los genes en el ADN cromosomal.
Además de la expresión plasmídica, otro factor importante en el estudio de los plásmidos es la posibilidad de transferir esta información genética a otras células que no la contengan, permitiendo la expresión de toxinas en otros tipos de bacterias y ampliando así el rango de acción. Con base en lo planteado anteriormente, este trabajo tuvo como objetivo principal la caracterización del ADN plasmídico de bacilos nativos útiles en el control biológico de mosquitos.
Materials and Methods
Muestras y selección
Se tomaron muestras de agua, tierra, hojarasca y larvas de diferentes regiones de Colombia (Chocó, Llanos Orientales, Costa Atlántica y Sabana de Bogotá). Estas muestras se homogenizaron y filtraron para luego realizarles un choque térmico a 90°C durante 20 minutos, con el fin de eliminar las bacterias que no poseen esporas. Las muestras procesadas se sembraron en SPC (DIFCO) y se incubaron durante 48 horas.
A partir de las colonias seleccionadas se evaluó la actividad toxicogénica en larvas de tercer instar de Culex quinquefasciatus Say (colonia del CIMIC), Anopheles albimanus Wiedemann y Aedes aegypti (L.) (donadas por la Unidad de Entomología del Instituto Nacional de Salud), utilizando un inóculo de 10e6 células/ml y como controles positivos las cepas B. sphaericus 2362 y B. thuringiensis IPS 82 (donadas por el Instituto Pasteur, Francia). Se evaluó el porcentaje de mortalidad cada 24 horas hasta completar los cinco días.
Identificación y taxonomía
Por observación microscópica con coloración de Gram y verde de malaquita se clasificaron las diferentes cepas aisladas como similares a B. sphaericus o B. thuringiensis acorde con la forma y ubicación de la espora. Para confirmar la especie se realizaron observaciones bioquímicas específicas para bacilos esporulados según el Manual de identificación Bergey.
Aislamiento del ADN plasmídico
La minipreparación de plásmidos se realizó con las cepas aisladas que presentaron más del 70% de mortalidad en larvas de mosquitos. El método de extracción utilizado fue lisis alcalina modificado (Maniatis et al. 1982). La presencia del plásmido se determinó por la visualización de una banda fluorescente en la electroforesis de agarosa al 0,7%.
Curaje con temperatura
Las cepas toxicogénicas que presentaron ADN plasmídico se sometieron a curaje por temperatura a 41°C, con el fin de eliminar los plásmidos. En este tratamiento todas las cepas se sometieron a pases sucesivos en medio fresco (SPC agar) cada 48 horas hasta completar 20 ciclos.
Evaluación de las cepas curadas
Para determinar si las cepas después de 20 ciclos de curaje perdieron el plásmido o no y si éste se encuentra asociado a la toxicidad, se realizaron bioensayos en larvas de tercer instar de C. quinquefasciatus y la extracción de plasmidos a partir de las colonias curadas y de los controles no curados.
Resultados
El bioensayo de la capacidad toxicogénica para larvas de tercer instar de C. quinquefasciatus, A. albimanus y A. aegypti, mostró que de las 269 cepas esporuladas de bacilos, 22 (8,19%) presentaron mortalidad del 80-100% entre las 24 y 72 horas (Fig. 1) y las 247 restantes (91,81%) no patogénicas para mosquitos (Fig. 2).
Larvas de Culex quinquefasciatus, después de 24 horas de inoculación.
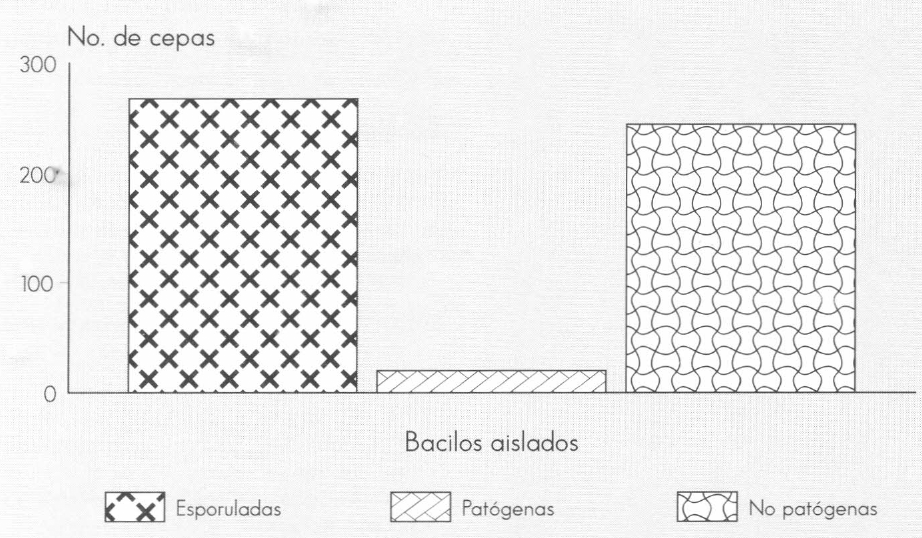
Capacidad toxicogénica de los bacilos esporoformadores según su actividad sobre larvas de mosquitos.
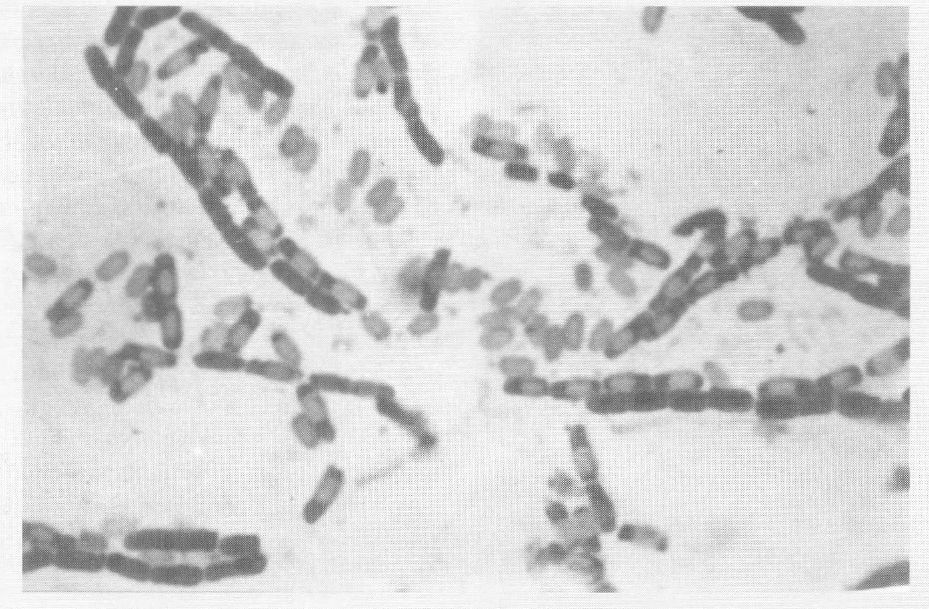
Bacilos esporulados con tinción de verde de malaquita.
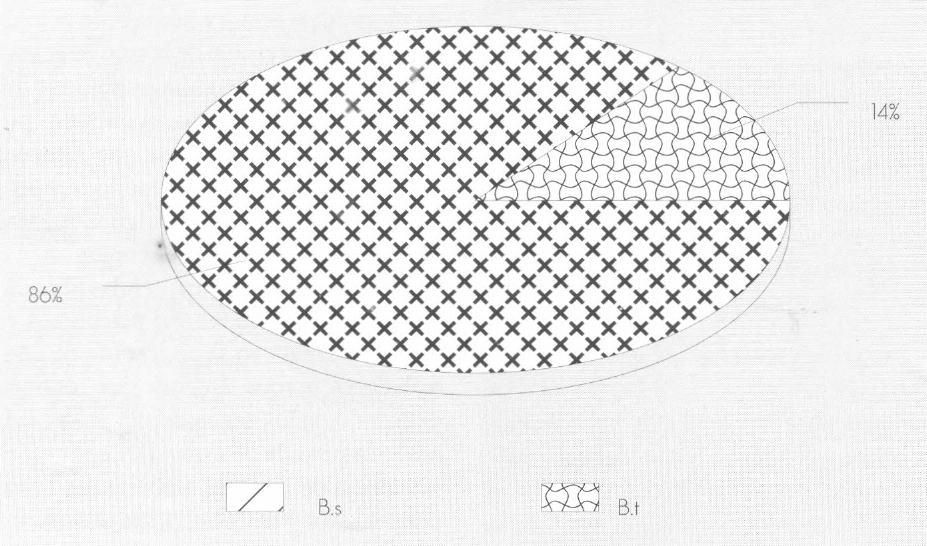
Clasificación de las cepas patógenas según la morfología y posición de la espora.
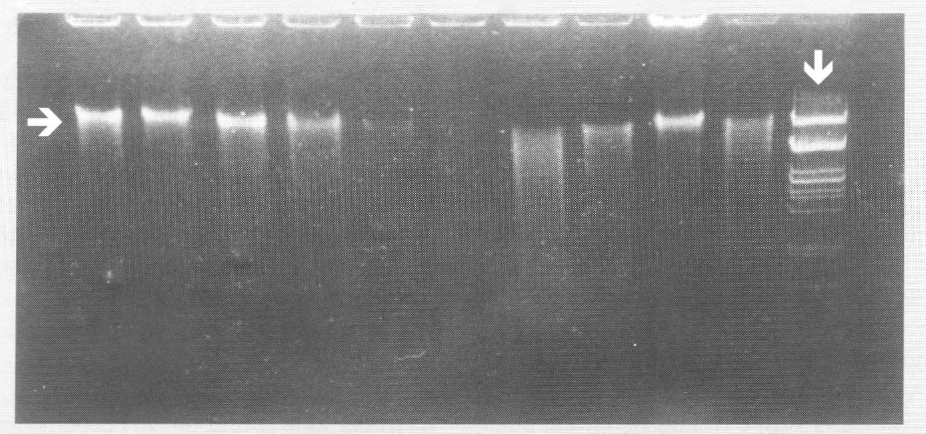
Electroforesis en gel de agarosa de ADN plasmídico aislado de las cepas patógenas. → Banda plasmídica ↓ Patrón de peso molecular de ADN de fago lambda digerido con Pstl
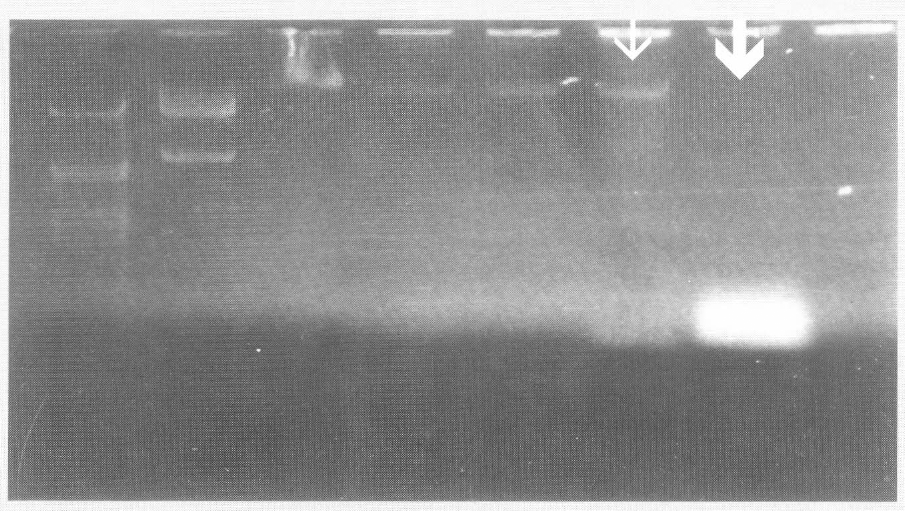
Electroforesis en gel de agarosa de ADN plasmídico de las cepas curadas por temperatura ↓ Cepas curadas con temperatura ↓ Cepas controles no curadas
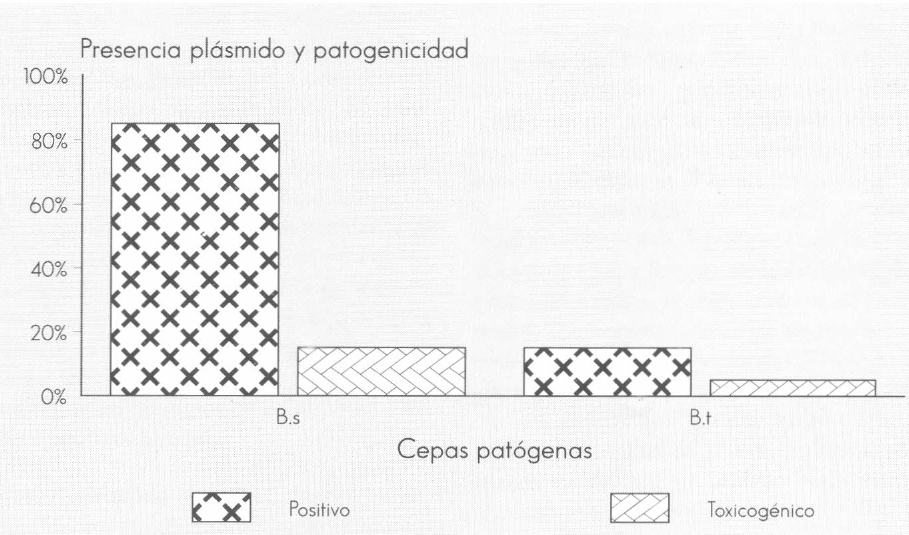
Relación de la presencia del plásmido con la toxicidad de las cepas evaluadas después de 20 ciclos de curaje con temperatura.
Discusión
De los bacilos aislados, sólo una baja proporción (8,19%) presentó actividad larvicida, como era de esperarse, puesto que sólo se han reportado cepas de B. sphaericus y B. thuringiensis como controladores de larvas de mosquitos, además de poseer un rango específico en cuanto a las especies que controlan (Burges 1982; Dumusois et al. 1993; Sattabongkot et al. 1990 y Pantuwatana 1990).
Con relación a la actividad larvicida evaluada de los aislamientos, se observó una alta patogenicidad (80-100%) de diferentes cepas de bacilos hacia larvas de C. quinquefasciatus, A. albimanus y A. aegypti, en un corto tiempo (24-72 horas), lo cual sugiere que estas cepas son candidatas potenciales para evaluar su actividad en el campo.
En cuanto a la distribución de bacilos esporulados, B. sphaericus se recuperó en un número mayor que B. thuringiensis, lo que confirma lo reportado en cuanto a reciclaje y permanencia de estos dos bacilos en la naturaleza (Bernhard et al. 1979; Burges 1982; Dumusois y Priest 1993).
Entre estas dos especies de bacilos se observó diferencia en cuanto al porcentaje de mortalidad en larvas, aunque en todas estuvo por encima del 70%. El título utilizado para los bioensayos fue estándar (10e celulas/ml) con el fin de seleccionar las cepas potencialmente patógenas para el estudio a nivel plasmídico.
Dos de las 22 cepas analizadas no presentaron plásmidos, lo que sugiere que su patogenicidad está codificada por genes que se encuentran en el cromosoma; no obstante, la mayoría de cepas toxicogénicas de B. sphaericus y todas las de B. thuringiensis presentaron plásmidos de alto peso molecular, el cual fue similar entre sí. Estas cepas que contenían plasmidos, se sometieron a un tratamiento de curaje por temperatura, el cual ha sido reportado como efectivo para curar cepas de B. thuringiensis (Miteva et al. 1986); con éste tratamiento se intentó, por pases sucesivos a medio fresco, desestabilizar la replicación del plásmido por un crecimiento acelerado de la bacteria y así obtener células libres de ADN plasmídico.
La respuesta de las cepas al curaje por temperatura fue diferente. Tres cepas perdieron el plásmido sin perder la toxicidad y tres perdieron la actividad larvicida y presentaron una banda muy tenue en la electroforesis, pero después de hacer pases de estas cepas, volvieron a presentar actividad larvicida y ADN plasmídico. Acorde con este resultado se decidió realizar otras veinte rondas de curaje alternando los pases con choques térmicos (90°C por 20 min.), puesto que se ha reportado que en el proceso de esporulación de los bacilos una gran proporción de ADN extracromosomal (plásmidos) se pierde (Cook et al. 1993). Después de este tratamiento se logró obtener y mantener sin actividad larvicida y sin ADN plasmídico a dos cepas, lo que indica que en estas cepas los genes involucrados en la patogenicidad se encuentran ubicados en sus plásmidos, y por lo tanto la información de la toxicidad puede ser transferible a otras bacterias no patógenas que adquieran el plásmido, y esto conlleva a que en la naturaleza se mantenga por más tiempo la acción toxicogénica, debido a una mayor proporción de la población nativa bacteriana portadora de estos plásmidos con capacidad de transferirlo a otras especies de bacilos.
Después del curaje por temperatura en las tres cepas en las que se observó una banda plasmídica tenue y pérdida de la toxicidad, la recuperación de la patogenicidad indica que existe una alta estabilidad del plásmido, con lo cual basta que unas pocas células lo posean para que aumente su número de copias y el bacilo recupere su actividad y tal vez de alguna manera pueda ser transferible (por conjugación o movilización) hacia otras células libres de plásmido; esta estabilidad plasmídica es de gran ventaja en la aplicación de controladores porque asegura una continua expresión de los genes del plásmido, evitando la pérdida de este ADN como consecuencia de factores ambientales como temperatura y radiación ultravioleta.
El hecho que hallan quedado una gran cantidad de cepas sin curar (aprox. 12), es decir que después del tratamiento siguen conservando el plásmido, demuestra que este ADN plasmídico es muy estable en su huésped y posiblemente vital para la célula; y a pesar que la mayoría de estos plásmidos presentó un peso molecular similar, hay diferencias en cuanto a su estabilidad, lo que hace que algunos plásmidos sean más difíciles de curar que otros.
Conclusiones
Es importante anotar que el hecho de haber aislado cepas nativas de B sphaericus y B. thuringiensis con plásmidos muy estables y con actividad larvicida contra tres especies de mosquitos, indica que es promisoria la utilización de estas cepas, y para ello es importante determinar en el laboratorio, por estudios de bioensayos, la LD50 y la dosis letal mínima en la cual presentan alta toxicidad (Burges 1982; Davidson et al. 1993; Lord et al. 1990), como también la producción a gran escala y pruebas en campo, para en un futuro ser implementadas dentro de un manejo integrado de plagas para el control de mosquitos vectores de enfermedades en Colombia.
Footnotes
Agradecimientos
Los autores agradecen a Colciencias por la financiación de la investigación y al Instituto Nacional de Salud (INS), en especial al Dr. Víctor Alberto Olano, Jefe de la Unidad de Entomología, por la asesoría en el montaje de la colonia de Culex quinquefasciatus y por el aporte de larvas de Anopheles albimanus y Aedes aegypti para la realización de los bioensayos.
