Abstract
During field surveys of native natural enemies attacking the coffee berry borer Hypothenemus hampei, carried out by the Entomology Depertament of Cenicafé, the fungus Fusarium sp. was observed in several localities attacking the borer. Samples were purified in culture, coded and sent to IIBC, UK, where they were identified as F. oxysporum and F. solani. Aspects of the biology of the isolate Fu 9401 from El Reflejo (Quindío) were studied in the laboratory, viz. percentage germination, radial growth rate and spore production. This isolate was cultured in acidified Sabouraud-Dextrose-Agar for 30 days and from this a preparation was made of a concentration of 5.4x108 spores/ml consisting of 100% microconidia and used to evaluate pathogenicity of the fungus on adults of H. hampei. The insects were inmersed in the spore suspension for 2 minutes, and 24 hours later offered either a green coffee berry or a parchment coffee bean (40% humidity). The insects of the check (no immersion) were offered parchment beans. Mortalities of 45 ± 17.8% (X + S.D.) were obtained using green berries and 26.3 ± 14.1% with parchment beans. The average time to reach these mortalities was 8.6 ± 2.6 days and 7.9± 3.0 days, respectively. It was not possible to calculate mean lethal time (LT50) from the results. Further tests need to be carried out using higher concentrations of macroconidia and for evaluation of other isolates collected from the field.
Introducción
Desde la llegada de la broca a Colombia, en 1988, se han encontrado, además de Beauveria bassiana (Bals.) Vuill. (Vélez y Benavides 1990), otros hongos entomopatógenos nativos como Metarhizium anisopliae (Metsch.) Sorokin (ICA 1993), Hirsutella eleutheratorum (Posada et al. 1993) y, recientemente, Fusarium sp. en las regiones de Caldas, Huila, Quindío y Risaralda (Pérez y Posada 1995).
El género Fusarium pertenece a la División Eumycota, Subdivisión Deuteromycotina, clase Hyphomycetos, y se caracteriza por la producción de macroconidias, microconidias, y en algunas especies por la producción de clamidosporas y micotoxinas. Crece formando un micelio extenso y algodonoso, a menudo con un pigmento rosado, púrpura o amarillo que varía según la especie y el medio de cultivo utilizado; el crecimiento y la esporulación de Fusarium sp. es altamente dependiente de las condiciones de cultivo, como son: medio de cultivo, condiciones de luz y temperatura (Windels 1993).
Algunas de las especies del género Fusarium son micotoxicogénicas y causan enfermedades oportunistas en humanos y animales (Windels 1993); otras han sido registradas causando enfermedades en plantas, como es el caso de F. oxysporum (Schl.) Snyd. et Hans. f. sp. dianthi, causante del marchitamiento vascular del clavel, el problema más limitante de la floricultura colombiana (Arbeláez et al. 1993) y F. oxysporum f. sp. cubense, responsable de la defoliación del plátano o Mal de Panamá (Ploetz et al. 1992).
Igualmente, otras especies del género Fusarium se han registrado causando patogenicidad en diferentes órdenes de insectos como Coleoptera (Bai y Chen 1991), Diptera (Uribe et al. 1994), Homoptera (Devnath 1987), Lepidoptera (Rodríguez 1984) y Neuroptera (Maharaj y Patil 1986).
Entre las especies entomopatógenas del género Fusarium se encuentra F. oxysporum que ha sido registrado, por diferentes autores, causando mortalidades superiores al 71% en estados inmaduros de poblaciones de mosquitos patógenos y vectores de enfermedades en hombres y animales como Culex fatigans Say y Anopheles stephensi (Diptera: Culicidae) (Balaraman et al. 1979); Aedes detritus y Culex pipiens pipiens L. (Diptera: Culicidae) (Hasan y Vago 1972) y en plagas de cultivos de arroz como Melanitis leda ismene (Lepidoptera: Satyridae), ocasionando mortalidades entre 80-90% (Nayak y Srivastava 1978).
F. moniliforme Schel. var. subglutinans es altamente infectivo a Aulacophora sp. y Mylabris pustulata (Coleoptera: Bruchidae) (Beevi y Jacob 1982); F. semitectum Berk. and Rav. es patogénico a Myzus persicae (Sulzer) y Lipaphis eryzimi (Keltenbach) (Homoptera: Aphididae), plagas de repollo y coliflor (Nagalingam y Jayaraj 1986); F. pallidoroseum (Cooke) Sacc. causante del 100% de mortalidad en adultos de Aphis craccivora Koch (Homoptera: Aphididae), plaga de algunas leguminosas (Hareendranath et al. 1987); F. merismoides var. acetilereum atacando Rhynchites foveipenis (Coleoptera: Curculionidae) (Bai y Chen 1991); F. solani (Mart.) Sacc., patógeno de larvas de Cossus cadambae More (Lepidoptera: Cossidae) (Mathew y Mohamed 1987) y Hemerocampa leucostigma (Smith and Abbott) (Lepidoptera: Lymantriidae) (Maharaj y Patil 1986).
En octubre de 1993, en Quimbaya (Quindío), durante las labores de reconocimiento de enemigos naturales de la broca del café, se registró por primera vez la presencia de Fusarium sp.; a partir de entonces se detectó en otras ocho localidades de la zona cafetera, pertenecientes a cuatro departamentos. Las muestras traídas del campo se codificaron y se aislaron en medio de cultivo Sabouraud-Dextrosa-Agar acidificado con ácido láctico (SDA+a.l.), a partir de los cuales se obtuvieron cultivos puros del hongo. En la actualidad, el cepario de Cenicafé cuenta con nueve aislamientos de Fusarium sp., de los cuales han sido identificadas dos especies F. solani y F. oxysporum por el Dr. Harry C. Evans, del IIBC en Inglaterra (Pérez y Posada 1995).
El hongo ataca los adultos de la broca del café en frutos verdes, maduros y secos; cubre el insecto y el orificio de entrada con una capa gruesa de tejido que corresponde al estroma, el cual presenta diversas coloraciones: blanco, crema, amarillo, rosado, naranja y pardo. En observaciones realizadas bajo el microscopio estereoscópico, la broca infectada con Fusarium sp. presenta un crecimiento difuso, con un micelio que se extiende sobre el cuerpo del insecto, y en algunas ocasiones se destaca la presencia de coloraciones violáceas; las esporas de forma redondeada y cristalinas se observan suspendidas en el micelio como gotas de rocío; al realizar preparaciones en fresco de estos adultos se observaron microconidias escasas y macroconidias en forma de canoa con tres a cinco septas características del genéro Fusarium.
Dada la importancia de este hallazgo, ya que es la primera vez que se registra al género Fusarium infectando de forma natural poblaciones de adultos de H. hampei, se iniciaron estudios tendientes a determinar el porcentaje de germinación, la tasa de crecimiento radial, la producción de esporas en medios de cultivo sintético y en sustratos naturales y la patogenicidad sobre adultos de la broca del café.
Materiales y Métodos
Los estudios se desarrollaron con el aislamiento de Fusarium sp. identificado en el cepario de Cenicafé como Fu 9401, el cual no logró clasificarse debido a que no creció en el medio selectivo Agar-Sucrosa.
Germinación
Los medios de cultivo que se emplearon para determinar el porcentaje de germinación fueron: Papa-Dextrosa-Agar (PDA) y Sabouraud-Dextrosa-Agar (SDA), solos y acidificados con ácido láctico al 0,37% (PDA + a.l., SDA + a.l.), utilizado como un inhibidor bacteriano. Se prepararó una solución madre del hongo y diluciones seriadas hasta 10³; la concentración se ajustó a 1 x 106 esporas/mililitro (e/ml), y se inocularon 5 alícuotas de 5 μl en la caja de petri (unidad experimental) incubadas a 25°C. Las evaluaciones se realizaron a las 6-9-12 - 15 y 18 horas; transcurrido el tiempo de incubación, se adicionó a cada alícuota una gota de azul de lactofenol para detener el crecimiento y se procedió a hacer los recuentos de esporas germinadas y no germinadas, contando 100 esporas por alícuota para un total de 500 esporas por unidad experimental. los tiempos se seleccionaron teniendo en cuenta observaciones preliminares, en las que se obtuvo germinación del 100% a las 24 horas.
El experimento se condujo bajo un diseño completamente aleatorizado en un arreglo factorial 2x2x5 (2 medios de cultivo con y sin inhibidor, 5 tiempos de incubación), con 8 repeticiones cada uno; la variable evaluada fue el porcentaje de germinación.
Crecimiento radial
El centro de cajas de petri, con 10 ml de medio de cultivo, se inocularon 5 μl de una suspensión de esporas en concentración 1 x 106 e/ml; el diámetro de la colonia se midió por el anverso con un noniómetro de precisión (0,02 mm), marca “Mitutoyo”, a partir de las 48 horas de incubación y cada 24 horas hasta completar ocho días. Se utilizó un diseño experimental completamente al azar en arreglo factorial 2 x 2 con 15 repeticiones por tratamiento. La variable evaluada fue la tasa de crecimiento diario de la colonia fúngica medida en cm.
Descripción morfológica
A partir de un cultivo puro en SDA sin acidificar, se determinó el promedio del largo y del ancho de las micro y macroconidias (expresado en micras) y el número de septas, contabilizando 100 y 50 esporas, respectivamente. Para el montaje de las placas al microscopio se tomó un asa recta y se extrajo una muestra seca del hongo, la cual se colocó sobre una lámina portaobjetos con una gota de azul de lactofenol; el tamaño de las esporas se midió utilizando el microscopio de luz, objetivo 40X y con la ayuda de un micrómetro ocular. Igualmente se realizaron observaciones descriptivas como aspecto, color, borde, forma y consistencia de la colonia a los 8, 15, 21 y 30 días de incubación.
Producción de esporas en medio de cultivo artificial
La producción de esporas en PDA y SDA se evaluó en cuatro tiempos de incubación (8, 15, 21 y 30 días), con un diseño experimental completamente al azar en arreglo factorial 2 x 4 con 5 repeticiones, tomando como unidad experimental la caja de petri inoculada con 5 µl de una suspensión de esporas en concentración 1x106 e/ml.
Para determinar el número de esporas/ml se tomó, en los tiempos establecidos, cada una de las cajas de petri y se lavó con 50 ml de agua destilada estéril (ADE); luego se hicieron diluciones seriadas y en cada caja se realizaron conteos en el hemocitometro. El promedio del número de esporas por tratamiento se obtuvo con el recuento de las cinco cajas o unidades experimentales.
Producción de esporas en sustratos naturales
Como sustratos naturales se evaluaron arroz, trigo y papa. Para la preparación del arroz se utilizó la proporción (P/V) de 50 g y 80 ml de agua; se utilizaron 50 g de papa cortada en trozos de ± 1 cmβ sin adicionar agua; el trigo se hidrató y posteriormente se pesaron 50 g. Los sustratos se envasaron en erlenmeyers de vidrio de 500 ml de capacidad y se taparon con algodón; posteriormente se sometieron a esterilización en el autoclave por 15 minutos a 120°C y 15 psi (103,37 kPa); el trigo se sometió a esterilización fraccionada de 20 minutos cada una, para eliminar la flora bacteriana termorresistente presente en el sustrato (Fritsche 1978).
La inoculación se realizó partiendo de una suspensión de esporas del hongo desarrollado en un tubo de ensayo con 30 días de cultivo y de concentración conocida. Se utilizó un diseño experimental completamente al azar con arreglo factorial 3 x 4, correspondiendo a tres sustratos, y cuatro tiempos de desarrollo (8, 15, 21 y 30 días de incubación), y 5 repeticiones; la unidad experimental estuvo constituida por el erlenmeyer.
Para determinar el número de esporas se lavó el sustrato con 300 ml de ADE, y luego se realizaron diluciones seriadas y seis recuentos por repetición en el hemocitómetro. Se determinó el número de esporas por mililitro, para luego llevarlos a número de esporas por gramo.
Patogenicidad sobre adultos de H. hampei
La prueba de patogenicidad se realizó con el aislamiento Fu 9401 cultivado en SDA acidificado con 30 días de desarrollo, en una concentración de 5,4 x 108 e/ml; se emplearon dos tipos de sustrato: fruto verde y grano pergamino seco, siguiendo la metodología estandarizada por González et al. (1993); la exposición al inóculo se realizó por inmersión durante dos minutos. Los insectos utilizados eran recién emergidos y provenían de la unidad de cría de parasitoides de Cenicafé, y previamente se desinfestaron con hipoclorito de sodio al 0,5% por 10 minutos.
La mortalidad de las brocas se evaluó diariamente durante 13 días después de la inoculación, utilizando para ello un microscopio estereoscópico que permitió realizar la disección de los granos sin causar daño al insecto y observar los síntomas y signos de la enfermedad.
Este experimento constó de tres tratamientos (un aislamiento del hongo con dos tipos de sustrato y un testigo sin inóculo) de 80 brocas cada uno, distribuidas en ocho repeticiones de diez individuos.
Resultados y Discusión
Germinación
A las 6 horas de incubación se observó retardo de la germinación en los tratamientos PDA, PDA + a.l y SDA + a.l.. A partir de las 9 horas de incubación, el hongo desarrollado en los medios de cultivo acidificados se recuperó, llegando a tener a las 18 horas porcentajes de germinación iguales o superiores a los observados en los medios de cultivo sin inhibidor (68,8 PDA + a.l; 64,0 PDA; 60,3 SDA + a.l. y 58,1 SDA) (Fig. 1). Para todos los tratamientos se presentaron diferencias estadísticas en los tiempos evaluados, con valores máximos significativos de 3,26% (Tukey 0,05%).
El análisis de varianza para la tasa de germinación no mostró efecto de la interacción medio-adición de inhibidor, lo cual indica que los tratamientos son independientes; sin embargo, para cada tratamiento se presentaron diferencias significativas. La mayor tasa de germinación se encontró para el medio PDA. Estos resultados indican la capacidad que tiene el hongo Fusarium sp. de recuperarse ante condiciones adversas de cultivo, como es la adición de inhibidores bacterianos que modifican el pH.
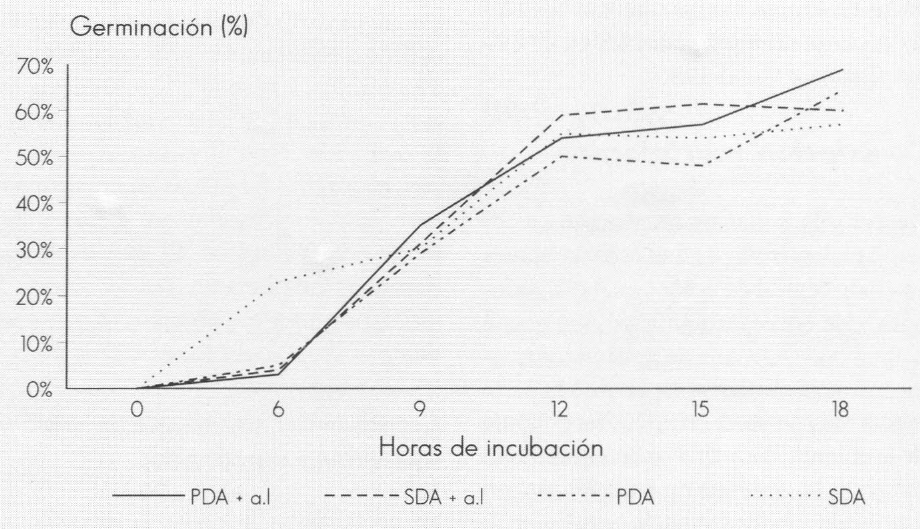
Germinación de Fusarium sp. en medios de cultivo artificial.
Crecimiento radial
El tamaño promedio de la colonia de Fusarium sp., a los 8 días de cultivo, fue de 7,16 cm para SDA, 6,81cm para PDA; 4,71cm y 4,05cm para SDA y PDA acidificados, respectivamente, es decir, los medios de cultivo sin inhibidor facilitan el crecimiento del hongo.
Para la tasa de crecimiento radial de cada tratamiento se calculó la ecuación lineal donde se obtuvieron valores de Rβ entre 0,79 y 0,96 (Fig. 2); la tasa de crecimiento por día fue de 2,42 cm; 1,83 cm; 1,18 cm y 0,61 cm para SDA, PDA, SDA + a.l. y PDA + a.l., respectivamente, con diferencias significativas a favor de los medios sin acidificar (Tukey 0,05%).
Se observó pérdida de la pigmentación del hongo Fusarium sp. cuando éste se desarrolló en presencia del inhibidor (ácido láctico), comprobándose que la formación de pigmentos está directamente relacionada con el medio de cultivo, como lo registra Windels (1993); además, el retardo en el desarrollo de la colonia fúngica se puede atribuir a condiciones adversas de cultivo y a los tiempos prolongados de exposición que afectan la síntesis de los nutrientes presentes en el medio (Lappa y Goral 1986).
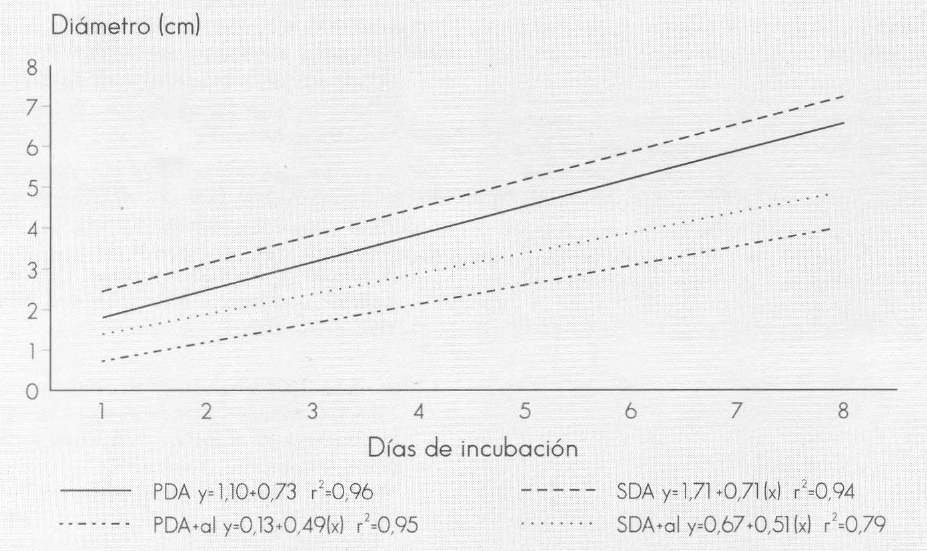
Tasa de crecimiento radial de Fusarium sp. en medios de cultivo sintético.
Descripción morfológica
Después de 8 días de incubación se observó el desarrollo de una colonia blanca con halo central de color violeta, algodonosa y de bordes irregulares, que ocupó la totalidad de la caja de petri; microscópicamente se hallaron esporas en la parte media mas no en el centro ni en el borde de la colonia, dado que su crecimiento es radial, y se observó un micelio hialino vacuolado y la presencia de conidióforos. Las microconidias midieron 5,56 ± 1,54 μ de largo con un valor máximo de 8 μ y mínimo de 3 μ x 1,56 ± 0,51 μ de diámetro; la pigmentación se distribuye en forma homogénea y varía de color dependiendo de la manipulación. Es posible que este cambio en la pigmentación se produzca por un proceso de oxigenación (Arbeláez 1993). Al día 21 de incubación se presentaron escasas macroconidias de 26,52 ± 1,26 μ de largo x 2,05 ± 0,23 μ, significativamente mayores a las observadas en tiempos de incubación menores; el promedio de septas transversales fue de 5, con un mínimo de 4 y máximo de 7; no se observaron variaciones en el aspecto de la colonia.
Pasados 30 días de incubación se encontraron escasas esporas y se había iniciado la formación de clamidosporas, tanto terminales como intercalares, lo que indica un agotamiento de los nutrientes necesarios para el desarrollo del hongo (Windels 1993).
Producción de esporas en medio de cultivo artificial
La producción de esporas para los dos medios artificiales fue muy variable (Fig.. 3). La mayor producción se presentó en SDA el día 15 de incubación (1,59 x 109 e/ml) y en PDA a los 30 días (1,09 x 109 e/ml), indicando que la esporulación es dependiente de la composición del medio de cultivo y que ésta puede ser mayor mientras más pobre sea el medio utilizado (Fisher et al. 1982). En SDA se presentó un descenso en la producción de esporas a partir del día 15 de incubación, debido posiblemente a la presencia de metabolitos, llegando a los 30 días a tener valores de 4,9 x 108 e/ml, contrario a lo que sucedió en el medio PDA, en el cual el desarrollo fue más lento y se mantuvo en forma ascendente a través del tiempo de evaluación. El análisis de varianza mostró diferencias estadísticas significativas entre tratamientos en todos los tiempos evaluados (Tukey 0,05%).
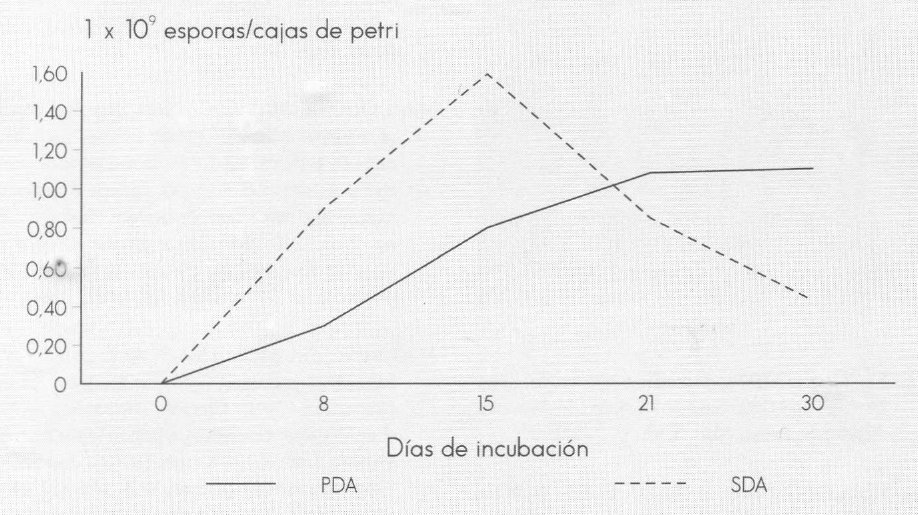
Promedio de la producción de esporas de Fusarium sp. en medio de cultivo sintético.
Producción de esporas en sustratos naturales
Se presentaron diferencias estadísticas significativas a favor del sustrato papa; los picos de producción máxima de esporas variaron con respecto al tiempo de incubación y al sustrato, es decir, a los 8 días fue de 1,11 x 108 e/g en trigo de 1,98 x 108 esporas/g a los 15 días para el sustrato papa y de 1,04 x 108 e/g para el arroz a los 21 días de incubación (Fig. 4). A partir del día 15 de incubación se observó la presencia de macroconidias sólo en el sustrato trigo. La presencia de contaminantes, especialmente levaduras, se vió favorecida en los sustratos arroz y papa. Las diferencias encontradas en la producción de esporas de un aislamiento cuando es cultivado en sustratos diferentes, se deben a la diversidad de los nutrientes aportados por cada medio o pueden ser consideradas como consecuencia de la variabilidad genética particular de cada aislamiento (Paccola y Azevedo 1990).
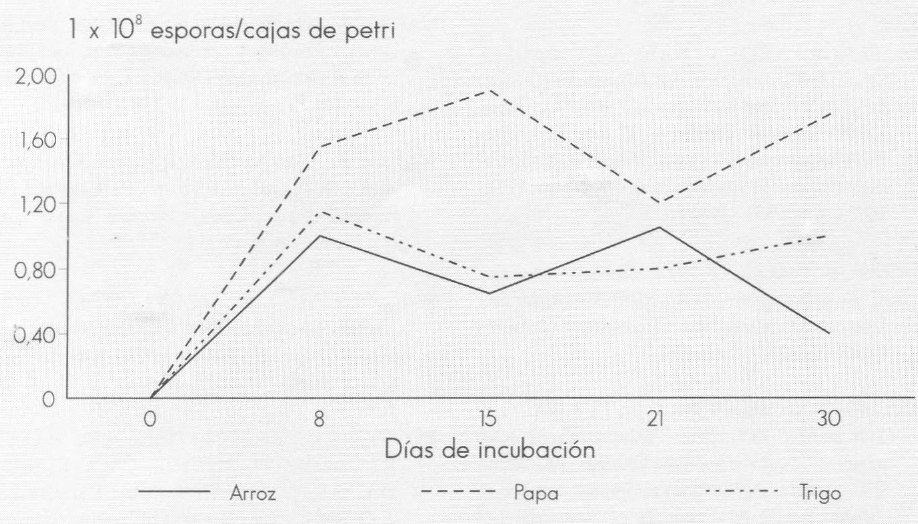
Promedio de la producción de esporas de Fusarium sp. en sustratos naturales.
Patogenicidad sobre adultos de H. hampei
Cuando se utilizó como sustrato el fruto verde se obtuvo un porcentaje de mortalidad de 45 ± 17,75% y de 26,25 ± 14,07 % con grano pergamino seco; el tiempo promedio de mortalidad fue de 8,63 ± 2,58 días y 7,85 ± 3,0 días, respectivamente (Tabla 1). Los resultados no permitieron establecer el tiempo letal medio (TL50) (Tiempo en el cual ocurre la mortalidad del 50% de la población evaluada), ya que ésta sólo alcanzó el 45%. Los datos para el análisis de mortalidad se transformaron a arcoseno ± 0,01.
Porcentaje y tiempo de mortalidad de H. hampei causada por el aislamiento de Fusarium sp. Fu 9401.
*Tukey 0,05%
Durante los primeros 12 días de evaluación no se presentaron diferencias significativas entre los tratamientos fruto verde y grano pergamino; sin embargo, al día 13 hubo diferencias tanto entre los tratamientos como con respecto al testigo. En el tratamiento testigo no se presentó mortalidad del insecto por Fusarium sp.
La distribución de la mortalidad diaria de la broca (Fig. 5) se inició a los 4 días después de la inoculación para los dos tratamientos; los mayores porcentajes (12,5%), para el tratamiento fruto verde, se presentaron los días 7 y 11, y se extendió hasta el día 13; en el tratamiento grano pergamino, el mayor porcentaje de mortalidad (10,0%) se presentó a los 11 días después de la inoculación.
Los porcentajes de mortalidad obtenidos fueron bajos, y esto posiblemente se debió a la utilización de un cultivo en condiciones no aptas para desencadenar el proceso de patogénesis en la broca, como pudieron ser: edad, no reactivación de la cepa, estructuras no infectivas, cultivo atenuado por la edad o el tipo de sustrato; todas ellas, condiciones reportadas en la literatura como causantes de pérdida de virulencia (Dae et al. 1988; Khachatourians 1991; Lane y Trinci 1991; Hayden et al. 1992). Para constatar la mortalidad de los adultos de H. hampei, las brocas infectadas se colocaron en forma individual en tubos de ensayo con medio de cultivo SDA y se incubaron a 25°C por un período de 8 días, verificándose en cultivo y a nivel microscópico que las estructuras presentes correspondian a Fusarium sp.
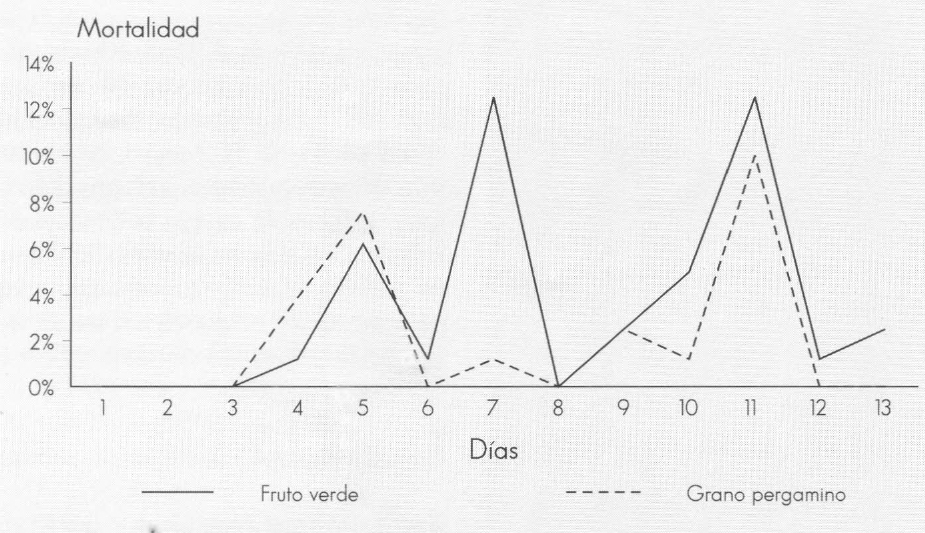
Distribución de la mortalidad diaria de H. hampei causada por Fusarium sp. Fu 9401
Conclusiones
Se concluye que a este nivel, el hongo no tiene un buen potencial como controlador de la broca del café, lo que indica que en campo es más dependiente de las condiciones ambientales que favorecen el desarrollo de epizootias. Se recomienda realizar pruebas de patogenicidad en concentraciones superiores a las evaluadas, utilizando macroconidias y a la vez evaluar la colección de aislamientos que se han recuperado del campo causando mortalidad en poblaciones de H. hampei.
