Abstract
Characterization of the insecticidal and hemolytic activity of solubilized crystal proteins of Bacillus thuringiensis subsp. medellin (Btmed) was performed and compared to solubilized crystal proteins of isolate 1884 of B. thuringiensis subsp. israelensis (Bti) and isolate PG-14 of B. thuringiensis subsp. morrisoni (Btm). In general, at acid pH values, solubilization of the Bt crystalline parasporal inclusions (CPI) was lower than at alkaline pH. The larvicidal activity demonstrated by the CPI of Btmed indicated that optimal solubilization of CPI takes place at a pH value of 11.3, in Bti at pH values from 5.03 to 11.3 and in Btm at pH values from 9.05 to 11.3. Hemolytical activity against sheep red blood cells was mainly found following extraction at pH 11.3 in all Bt strains tested. Polyacrylamide gel electrophoresis under denaturing conditions revealed that optimal solubilization of the CPI in all Bt strains takes place at alkaline pH values from 9.05 to 11.3. An enriched preparation of Btmed crystals was obtained, solubilized crystal proteins were separated on a size exclusion column (Sephacryl S-200). Three main protein peaks were observed on the chromatogram. The first peak had two main proteins that migrate between 90 to 100 kDa. These proteins are apparently not common to other Bt strains isolated to date. The second and third peaks obtained from the size exclusion column yielded polypeptides of 68 and 28-30 kDa, respectively. Each peak independently, showed toxicity against first instar Culex quinquefasciatus larvae. These results suggest that the 94 kDa protein is an important component of the Btmed toxins with the highest potency to kill mosquito larvae. Combinations of the fractions corresponding to the 68 and 30 kDa protein showed an increased toxicity. When crystal proteins of Bti were tested with antisera raised independently against the three main protein fractions of Btmed, the only crystal protein that showed cross reaction was the 28 kDa protein. These data suggest that Btmed could be an alternative bacterium for mosquito control programs in case that mosquito larval resistance emerges to Bti toxic proteins developes.
Introducción
Bacillus thuringiensis (Bt) es un bacilo Gram positivo, utilizado ampliamente en agricultura para el control de insectos plagas durante más de 30 años. Desde el descubrimiento de la primera cepa activa para larvas de mosquitos en 1977, por Goldberg y Margalit, la bacteria ha sido implementada en muchos países del mundo para el control de mosquitos. En años recientes, la búsqueda de nuevas cepas de Bt se ha incrementado con el propósito de descubrir nuevas actividades o cepas más potentes. Las cepas de Bt son tóxicas para insectos lepidópteros, dípteros, coleópteros, himenópteros, homópteros y malófagos (Feitelson et al. 1992; Feitelson 1993; Höfte y Whiteley 1989).
Esta bacteria produce inclusiones cristalinas paraesporales (ICP), usualmente compuestas de una o más subunidades de proteínas, las que al ser ingeridas por insectos susceptibles producen mortalidad. Estas proteínas tienen una variedad de propiedades biológicas y causan citólisis, hemólisis y toxicidad (Aronson et al. 1986; Hofte y Whiteley 1989).
Se conocen muchas variaciones en la estructura primaria de estas proteínas y son las directamente responsables de las diferencias en susceptibilidad de los organismos blanco de cada una de ellas (Hofte y Whiteley 1989). Muchas de las propiedades físico-químicas han sido estudiadas (Huber y Lüthy 1981; Tyrrel et al. 1981; Pfannenstiel et al. 1986; Koller et al. 1992; Du et al. 1994), incluyendo el valor de pH requerido para la solubilización de los cristales, un parámetro muy importante debido a que éste es un paso esencial en la toxicidad en insectos susceptibles. En este artículo se describen las propiedades de solubilización, las inmunológicas y las toxicológicas de las ICP producidas por. B. thuringiensis subsp. medellin descrita por Orduz et al. (1992, 1994) y se reporta el papel de las proteínas individuales y sus mezclas en la toxicidad sobre larvas de Culex quinquefasciatus Say (Diptera: Culicidae).
Materiales y Métodos
Las cepas 1884 de Bt subsp. israelensis (Bti) y PG-14 de Bt subsp. morrisoni (Btm) se obtuvieron de la Unité de Bacteries Entomopathogenes, Institut Pasteur, Paris. La cepa 163-0131 de Bt subsp. medellin (Btmed) fué aislada en Colombia (Orduz et al. 1992). Todas las bacterias se cultivaron en agar LB (triptone 10 g, NaCl 10 g, extracto de levadura 5 g, agar 20 g por litro de agua destilada), y se incubaron por 24 h a 30°C. Los tubos con 5 mI de medio líquido M-l (Proflo 1 g, peptona 5 g, glucosa 3 g, K2HPO4 6 g, sales 10 mI, que contenían 0,02 g de cada uno de los siguientes componentes MgCl2.6H2O, MnCl2.4H2O, FeCl3.6H2O, ZnCl2, y CaCl2.2H2O, buffer de fosfatos 200 mI, en I Ide agua destilada y pH ajustado a 7,2) se inocularon e incubaron por 8 h a 30°C y 200 rpm. Los cultivos bacterianos se transfirieron a 200 mI de M-l y se incubaron a 30°C, 250 rpm en un incubador-agitador ambiental por dos días. El cultivo completo final (CCF) se colectó por centrifugación a 4°C, 9.000 x g durante 30 minoEl botón resultante se trató por 30 min con 1M NaCl, se lavó dos veces con agua destilada y se resuspendió en 1/20 del volumen original y se almacenó a -20°C hasta su utilización. Las larvas de C. quinquefasciatus usadas en estos experimentos se colectaron en el campo, en la vecindad de Medellín, y se mantuvieron bajo condiciones de laboratorio a 30±2°C bajo un fotoperíodo de 12:12.
Para los ensayos de solubilización se empleó un buffer con fuerza iónica constante a los diferentes valores de pH, según la técnica descrita por Koller et al. (1992). Cien microlitros de CCF de Btmed se trataron con las soluciones de pH del sistema buffer con valores entre 2,55 y 11,22, durante 24 h, 30°C a 200 rpm. Las proteínas solubilizadas se dializaron contra un buffer fosfatado y cloruro de sodio (PBS), pH 7,2, (0,32 g NaH2P04, 1,18 g Na2HPO4, 8,58 g NaCl por litro, pH 7,2). El material sólido se concentró por centri fugación y la concentración de proteínas del sobrenadante se midió por el método de Bradford (Bradford 1976). Alícuotas de 400 mI de los sobrenadantes se precipitaron con acetona fría y posteriormente se separaron en un gel de 10% de poliacrilamida con dodecil sulfato de sodio (SDS-PAGE acrilamida bis-N-N' acrilamida) (Laemli 1970).
Una muestra de 12,5 mg del solubilizado de cristales de Btmed se separó en una columna de Sephacryl S-200 (1 x 0,05 m.). La elución de las fracciones se realizó usando el sistema buffer descrito por Thiéry (1987), y se colectaron muestras de 4 mi, a las que se les midió la absorbancia a OD280 nm. Las fracciones colectadas se dializaron contra PBS pH 7,2, y muestras de 400 mI se precipitaron con acetona fría y se separaron en un gel de 10% SDS-PAGE, como se describió anteriormente.
Para la determinación de la actividad hemolítica se colectaron y lavaron tres veces glóbulos rojos de cordero en solución salina (SS) 0,85% y se llevaron a una concentración final de 2,8% en SS. Cien microlitros de las fracciones eluidas de la columna de Sephacryl se mezclaron con volúmenes iguales de la suspensión de glóbulos rojos en platos de microtitulación con fondo en U y se incubaron a 37°C con 5% CO2 por 2 h, después de lo cual se centrifugaron a 500 x g por 10 min y la absorbancia de los sobrenadantes a 540 nm se leyó en un lector de ELISA, marca Multiskan modelo MCC/340.
Las proteínas solubilizadas del cristal de Btmed separadas en la columna de Sephacryl y las proteínas extraidas por el tratamiento en el sistema buffer se evaluaron para encontrar su toxicidad en larvas de primer instar de C. quinquefasciatus. Cinco larvas de C. quinquefasciatus se colocaron en cada uno de 24 pozos con I mI de agua desionizada y se dieron los tratamientos con las diferentes toxinas y mezclas para determinar la concentración letal media (CL50). Cada dosis o extracto de pH se ensayó por duplicado y los experimentos se desarrollaron en cuatro días diferentes. Las interacciones entre las diferentes proteínas se evaluaron según a la fórmula descrita por Tabashnick (1992).
Contra cada una de las proteínas del cristal de Btmed, en ratón, se preparó un suero policlonal administrando inyecciones intraperitoneales semanales a partir de las proteínas separadas en 10% SDS-PAGE. La primera dosis se dió en adjuvante completo de Freund, mientras que las otras se dieron en adjuvante incompleto. Las proteínas del cristal de Btmed y Bti se separaron en un gel de 10% SDS-PAGE y se transfirieron a una membrana de nitrocelulosa. El Western blot con anticuerpos polic\onales se realizó incubando las membranas con los anticuerpos preparados contra las proteínas tóxicas de Btmed de 94, 68, y 30 kDa, diluidas 1:500 e incubadas a 4°C durante toda la noche. Las otras incubaciones se realizaron a temperatura ambiente en TBS pH 7,4, usando 3% de gelatina como agente bloqueador y 0,05% Tween-20. La inmunodetección de las proteínas se realizó por medio de fosfatasa alcalina conjugada a Proteína A, seguido de la incubación con un sistema substrato/color compuesto de naftol fosfato/Fast Red (Sigma Chemical Co.)
Resultados
Se observó una tendencia general, en la que a condiciones alcalinas se pudo extraer más cantidad de proteínas a partir de las ICP en todas las cepas de Bt evaluadas en este estudio. Las ICP de las subespecies de Bt evaluadas en este estudio mostraron actividad hemolítica. Las ICP de Bti, Btm y Btmed, solubilizadas a pH de 11,3 produjeron 100% de hemólisis en glóbulos rojos de cordero, mientras que a valores de pH menos alcalinos se reportó hemólisis entre 0 y 30%. CCF de Bti, Btm y Btmed sin tratar causó 20%, 15% y 10% de hemólisis, respectivamente (Tabla 1).
Concentración de proteínas y ensayos de actividad hemolítica de Bacillus thuringiensis subsp. medellin, B. thuringiensis subsp. morrisoni y B. thuringiensis subsp. israelensis a diferentes valores de pH
Concentración de proteínas medida por el método de Bradford (1976)
Proteínas solubilizadas probadas por duplicado y en dos días diferentes.
Valores de pH en los que se solubilizaron los CPI. El pH se ajustó a 7,2 antes de realizar las pruebas de hemóisis.
Btmed: cepa 163-0131 of B. thuringiensis subsp. medellin, Btm: cepa PG-14 of B. thuringiensis subsp. morrisoni, Bti: cepa 1884 of B. thuringiensis subsp. israelensis.
Cultivo completo final.
Las ICP separadas en 10% SDS-PAGE, mostraron proteínas de 90-100 kDa, bandas multiples a nivel de 80, 70, 67, 68, 40, y 28-30 kDa (Fig. 2A, línea 2). Las ICP a de Bti y Btm mostraron principalmente bandas a nivel de 144, 135, 125, 67, y 28 kDa cuando se solubilizaron a valores de pH entre 9,98 y 11,3 (Figs. 2B, 2C, línea 2). La solubilización óptima de las ICP de Btmed tuvo lugar a un pH de 11,3 (Fig. 2A, línea 12), pero se observaron proteínas a valores de pH entre 4,1 y 9,98 (Fig. 2A, líneas 5 a 11). Cuando en bioensayo se evaluó la actividad tóxica de las muestras correspondientes a las líneas 6 a 11 (Fig. 2A), se observó una mortalidad menor de 62%. De igual manera a Btmed, los cristales de Btm mostraron proteínas solubilizadas a valores de pH entre 4,1 y 11,3 (Fig. 2B, líneas 5 a 12); sin embargo, las proteínas solubilizadas del cristal de Btm causaron menos del 50% de mortalidad en los tratamientos con valores de pH por debajo de 6,01, y más del 80% de mortalidad en los tratamientos con soluciones de pH por encima de 7,04. La mortalidad de las larvas fué de 100% sólo cuando los cristales se solubilizaron a valores de pH entre 9,05 y 11,3 (Fig. 1). En el caso de Bti se observaron proteínas solubilizadas a partir de los cristales, fundamentalmente en los tratamientos con un valor de pH entre 9,05 y 11,3 (Fig. 2C, líneas 10 a 12); sin embargo, se observó más de un 90% de mortalidad de las larvas de C. quinquefasciatus en los tratamiento con valores de pH entre 5,03 y 11,2 (Fig. 1). En Bti y Btm, la proteína de 68 kDa se observó también cuando la solubilización de los cristales se llevó a cabo en los tratamientos con valores de pH de 5,03 y 6,01, respectivamente (Figs 2B y 2C, líneas 6 y 7, respectivamente).
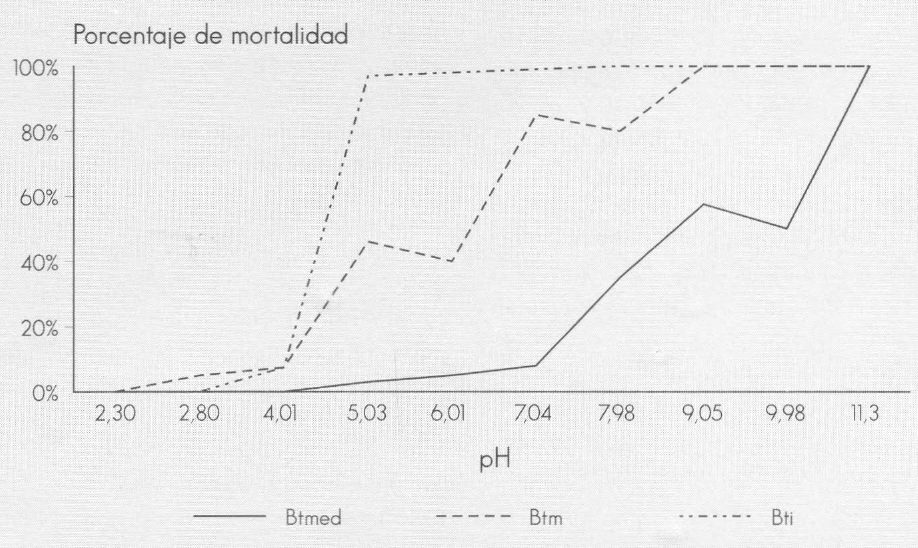
Mortalidad de larvas de primer instar de Culex quinquefasciatus tratadas con proteínas solubilizadas a diferentes valores de pH. Btmed: cepa 163-0131 de Bacillus thuringiensis subsp. medellin; Btm: cepa PG-14 de Bt subsp. morrisoni; Bti: cepa 1884 de Bt subsp. israelensis.
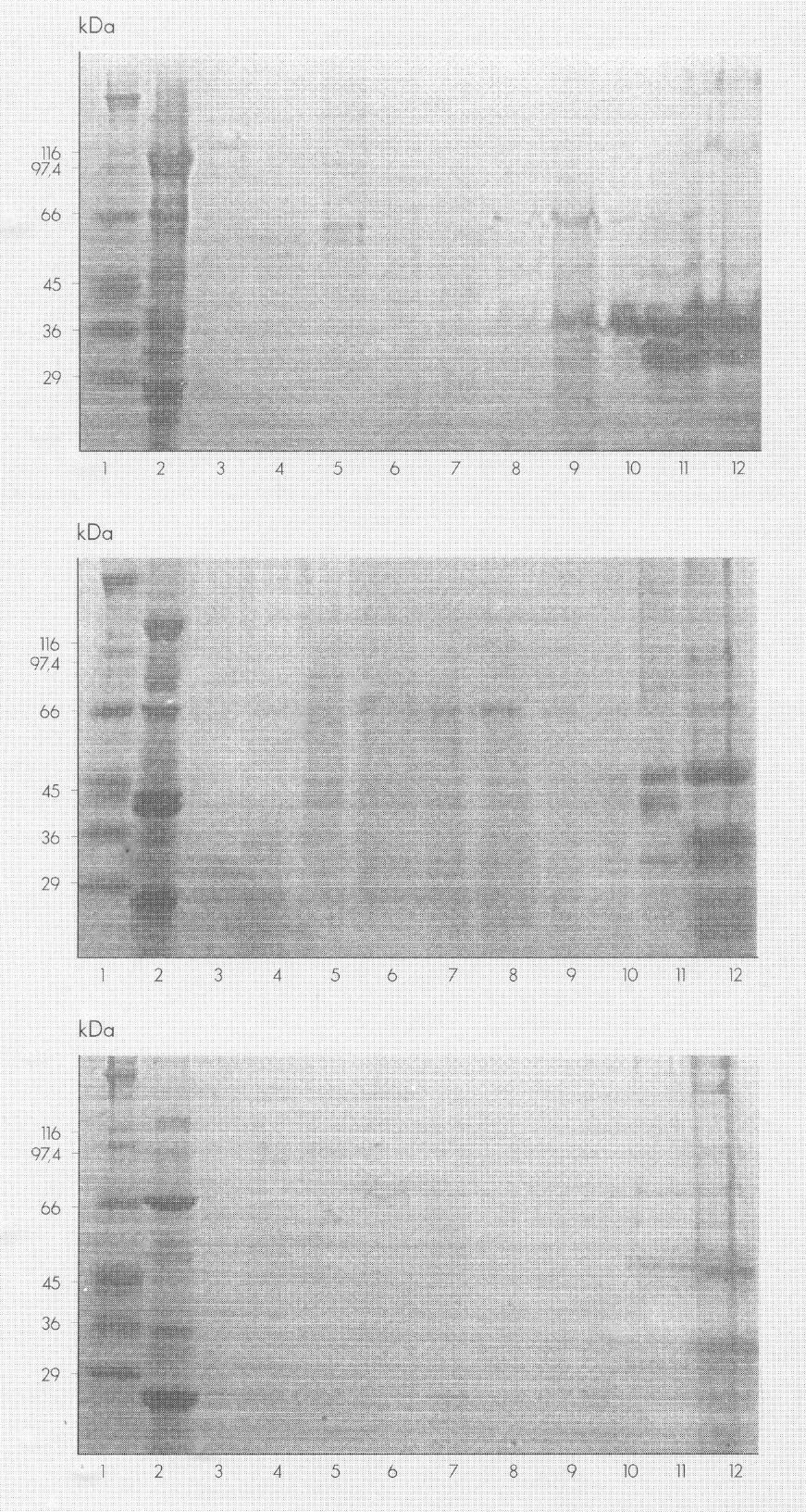
Geles de 10% SDS-PAGE, teñidos con azul de Coomassie (A) Bacillus thuringiensis subsp. medellin, (B) Bt subsp. morrisoni, (C) Bt subsp. israelensis cultivo completo final tratado con diferentes valores de pH. Líneas 1, marcadores de peso molecular indicados en kDa; líneas 2 proteínas del cristal de (A), B. thuringiensis subsp. medellin, (B), Bt subsp. morrisoni, y (C), Bt subsp. israelensis, líneas 3 pH 2,3; líneas 4, pH 3,8, líneas 5, 4,1; líneas 6, pH 5,03; líneas 7, pH 6,01; líneas 8, pH 7,04; líneas 9, pH 7,98; líneas 10, pH 9,05; líneas 11, pH 9,98; líneas 12, pH 11,3.
La separación de las proteínas de Btmed solubilizadas bajo condiciones alcalinas produjo tres picos principales (Fig. 3A). La fracción 23 mostró dos bandas de proteínas cuando se analizó por electroforesis (Fig. 3B, línea 3), las cuales tienen un peso molecular entre 90 y 100 kDa, con el componente predominante situado a nivel de 94 kDa. En los estudios de toxicidad se hace referencia a esta fracción como 94 kDa. La proteína más abundante presente en las fracciones 24 a 30 (líneas 4 y 10) tiene un peso molecular entre 66 y 68 kDa. Las fracciones 32 y 33 (líneas 12 y 13) muestran dos bandas de proteínas de aproximadamente 28 y 30 kDa. La actividad hemolítica fundamentalmente se encontró en estas bandas (Tabla 2).
A: Perfil de elución de las proteínas del cristal de Bacillus thuringiensis subsp. medellin separadas en condiciones alcalinas y separadas en una columna de Sephacryl S-200. B: Gel de 10% SDS-PAGE, teñido con azul de Coomasie Blue de las fracciones de las proteínas de Btmed eluidas de las columna de Sephacryl S-200. Línea 1, marcadores de peso molecular indicados en kDa; línea 2 cultivo completo final de Btmed línea 3 a la línea 12, fracciones 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, y 33 respectivamente. Las fracciones que causaron mortalidad en larvas de mosquito se encuentran indicadas por una línea.
La actividad tóxica obtenida en los tratamientos con las fracciones eluidas de la columna de Sephacryl indica que la proteína de 94 kDa es tal vez el componente más importante de las ICP de Btmed con una CL50 de 82,6 ng de proteína/ml (Tabla 3). Las proteínas de 68 y 30 kDa de Btmed tienen una CL50 de 1.256 y 1.948,5 ng/ml, respectivamente, en larvas de primer instar de C. quinquefasciatus. El efecto de las mezclas de las proteínas de las ICP de Btmed también se evaluó en bioensayos con larvas de mosquito, y los datos se analizaron según la fórmula descrita por Tabashnick (1992). Los resultados indican que la mezcla de proteínas de 94 y 68, y 94 y 30 kDa no presentan una interacción sinérgica, mientras que la mezcla de proteínas de 68 y 30 kDa si proporciona sinergia. La mezcla de las fracciones que contienen las proteínas de 94, 68 y 30 kDa produjo un ligero incremento de toxicidad en comparación con lo esperado, pero este aumento no puede considerarse como una interacción sinérgica (Tabla 3).
Cuando las proteínas de las ICP de Btmed y Bti se evaluaron por Western blot con los anticuerpos preparados independientemente contra cada una de las proteínas de Btmed, se encontró que los anticuerpos preparados contra las proteínas de 94 y 68 kDa de Btmed no reconocieron ninguna de las proteínas de las ICP de Bti mientras que los anticuerpos preparados contra la proteína de 30 kDa de Btmed si reconocieron las proteínas de 28 kDa de Bti.
Porcentaje de hemólisis de glóbulos rojos de cordero causado por las diferentes proteínas de Bacillus thuringiensis subsp. medellin separadas en la columna de Sephacryl S-200
Las proteínas solubilizadas se probaron por duplicado en dos días diferentes.
Mortalidad observada y esperada de larvas de primer instar de Culex quinquefasciatus tratadas con las fracciones enriquecidas de Bacillus thuringiensis subsp. medellin
Calculado según la fórmula descrita por Tabashnick (1992).
Discusión
La mortalidad de larvas de mosquito y la actividad hemolítica de las ICP de las cepas de Bt solubilizadas bajo las diferentes condiciones de pH se correlacionan con la cantidad de proteína extraida de las ICP. Tambien se obervó una tendencia constante, en la que la actividad larvicida y hemolítica de las ICP de Bti se presentó a valores de pH menores que en Btm y Btmed. La hemólisis causada por las proteínas solubilizadas de Btmed sugiere que la mayoría de las cepas de Bt identificadas hasta el momento, contienen proteínas citolíticas (Gill et al. 1987; Thomas & Ellar 1983); además, al menos en las subespecies Bti, Btm, y Btmed, esta actividad biológica es causada por proteínas de bajo peso molecular (25-30 kDa). En todas las subespecies que son activas contra larvas de moquitos a nivel de ng/ml hay una relación inmunológica de las proteínas de bajo peso molecular. Como en el caso de Bti y Btm, se ha demostrado que las proteínas hemolíticas son los componenetes de bajo peso molecular de las ICP. Específicamente se ha podido demostrar que en el caso de Btmed, la proteína de 30 kDa es la responsable de la actividad hemolítica y que la hemólisis parcial causada por las fracciones que contienen la proteína de 68 kDa puede ser debida a contaminación con la proteína de 30 kDa obtenida en los experimentos de purificación por filtración del gel. En los experimentos de solubilzación de las proteinas por tratamientos a diferentes valores de pH, la mortalidad y la actividad hemolítica aparecen a medida que se incrementa el pH, lo que indica que la mayoría de las proteínas de las ICP se solubilizan a pH alcalinos. Contrario a lo que obtuvo Koller et al. (1992), trabajando con las ICP de Bt var san diego, no se detectaron proteínas en los tratamientos ácidos por debajo de un pH de 4,01 en ninguna de las cepas de Bt evaluadas. Gringorten et al. (1992) demostraron que las solubilización de las ICP de Btk requieren un ambiente alcalino para poder retener su actividad total; sin embargo, en los experimentos de toxicidad, la neutralización de los tratamientos de extracción en ambientes alcalinos no evitó la expresión de la actividad tóxica, como se muestra en la Figura 1.
El papel de las cuatro principales proteínas (CryIVA, CryIVB, CryIVD y CytA) de Bti en la toxicidad es controvertido (Wu y Chang 1985; Ibarra y Federici 1986; Pfannenstiel et al. 1986; Visser et al. 1986; Thiéry 1987). Recientemente se ha demostrado que la proteína CytA no es esencial en la toxicidad para larvas de Culex sp. y Aedes sp., y que las proteínas CryIVA and CryIVB son responsables de la mayor parte de la toxicidad en C. pipiens (Delécluse et al. 1991). La sinergia de las proteínas CryIVA y CryIVB ha sido demostrada por Angsuthanasombat et al. (1992) y Delécluse et al. (1993). Sin embargo, el análisis de los resultados obtenidos por Chilcott y Ellar (1988), evaluados por el método de Tabashnick (1992), ha demostrado que la proteína de 27 kDa de Bti interactúa sinérgicamente con las proteínas de 68 y 130 kDa. El efecto de las mezclas de proteínas de Btmed también se evaluó en bioensayos con larvas de mosquito y los resultados se analizaron por medio de la fórmula descrita por Tabashnick (1992). Se hizo claro que únicamente la mezcla de las proteínas de 68 y 30 kDa producía un efecto de sinergia (Tabla 3). La mezclas de las fracciones que contienen las proteínas de 94, 65 y 28-30 kDa produjeron sólo un ligero incremento en la toxicidad. Previamente se ha demostrado que las diferencias en la actividad tóxica entre Btmed, Btm, y Bti contra C. quinquefasciatus, Anopheles albimanus Wiedeman y Aedes aegypti (L.) podría ser debida a la ausencia de las proteínas de 125-135 kDa en Btmed, la presencia de la proteína de 94 kDa en Btmed, la falta de similaridad inmunológica con las cepas PG-14 de Btm y 1884 de Bti o a una combinación de estos factores (Orduz et al. 1992, 1994). La proteína de 94 kDa es el componente más importante de las toxinas de Btmed con una CL50 de 82,6 ng de proteína/ml, en contraste con las observaciones hechas por Chilcott y Ellar (1988), quienes encontraron que el componente más importante de la ICP de Bti fué la proteína de 68 kDa con una CL50 de 4 ng/ml.
La total concordancia inmunológica entre las proteínas de las ICP de Bti y Btm ha sido demostrada (Gill et al. 1987; Thiéry 1987) y la proteína de 27 kDa de estas dos subespecies difieren sólo en una base y un aminoácido (Earp y Ellar 1987; Galjart et al. 1987). En el presente trabajo se encontró una reacción cruzada de la proteína de 30 kDa de Btmed y la proteína CytA de Bti, lo cual concuerda con resultados publicados previamente (Orduz et al. 1994). En otros estudios no se ha podido demostrar relaciones inmunológicas. entre cepas activas para mosquitos como son Bti y las proteínas Bt subsp. fukuokaensis (Yu et al. 1987) y Bt subsp. darmstadiensis (Dobroniewski y Ellar 1989). Sin embargo, anticuerpos preparados contra las proteínas de 135 y 68 kDa de Bti, reconocen proteínas de 70 y 26 kDa de Bt subsp. kyushuensis (Held et al. 1990). De manera contraria, anticuerpos preparados contra las proteínas de las ICP de Bt subsp. kyushuensis reconocen proteínas de las ICP de Bti, cepa PG-14 de Btm y Bt subsp. darmstadiensis (Ishii y Ohba 1992). En el caso reportado por Held et al. (1990), anticuerpos monoclonales preparados contra las proteínas de las ICP de Bti no dan reacción cruzada. Estos datos sugieren que de alguna manera, las cepas de Bt activas para mosquitos comparten epitopes comunes, lo cual podría indicar la presencia de estructuras comunes.
Conclusiones
El papel de la proteína de 94 kDa de Btmed en la toxicidad de las ICP ha sido demostrado. Este estudio también contiene información pertinente sobre las características de las ICP de Btmed. La actividad biológica en esta subespecie de Bt es derivada de proteínas que son inmunologicamente diferentes de aquellas previamente conocidas con actividad para larvas de mosquito. Además, la actividad hemolítica de la proteína de 30kDa de Btmed está de acuerdo al tamaño de las proteínas producidas por Bti y Btm, con las que ha mostrado una relación inmunológica. Estudios posteriores con cepas recombinantes con genes de Btmed y Bti producirá información importante sobre el modo de acción y las relaciones de estas moléculas biológicamente importantes, que podría llevar al desarrollo e implementación de una bacteria con los genes de Btmed en los programas de control de mosquitos.
Footnotes
Agradecimientos
Esta investigación recibió ayuda financiera del Banco Mundial/OMS/TDR, Colciencias y la Corporación para Investigaciones Biológicas (CIB).
