Abstract
In Colombia, the widespread utilization of bioinsecticides such as Bacillus thuringiensis (Bt) has to be supported with products that can compete both in price and availability with chemical pesticides. The objective of this work was to study different nutrients derived from agroindustrial sources, for the production of B. thuringiensis subsp. kurstaki (Btk) and to optimize the process in a 1 liter fermentator. With this purpose, biomass and spores production was followed-up spectrophotometrically and by plating in Luria Bertani medium (LB), respectively. Furthermore, the toxicity of the final product was evaluated on larvae of Spodoptera frugiperda (Lep: Noctuidae) using a diet surface bioassay. The present work allowed the design of a culture medium that yields the following results in a 1 liter fermentator: Biomass 4,03 g/l, spore concentration 21.107 sp/ml, potency 1.284.002 UI/ml, price US$0,03/l. These results are highly promising, because the medium is economic, produces an acceptable quantity of spores and biomass and the latter exhibits high toxicity on lepidoterous larvae.
Introducción
Los genéricamente llamados bioplaguicidas son una alternativa prometedora de los plaguicidas químicos, ya que a diferencia de éstos, los bioplaguicidas son altamente específicos contra la plaga atacada (Deacon 1983), el desarrollo de resistencia por parte de los insectos a estos productos es reducido (Whalon y McGaughey 1993; Siegel y Shadduck 1990) y son inocuos para el medio ambiente, los animales y el hombre (Siegel y Shadduck 1990; Aronson et al. 1993). Entre los bioplaguicidas se destaca la bacteria Bacillus thuringiensis Berliner (Bt) (Eubacteriales: Bacillaceae), cuyos productos representan del 90% al 95% del mercado global de bioplaguicidas (Feitelson et al. 1992). Esta preferencia es debida principalmente a su amplio, pero específico rango de actividad, a la facilidad de producción y a la rapidez de control de la plaga (Deacon 1983).
Las investigaciones realizadas para producir Bt se han encaminado a la búsqueda de substratos económicos y de alta disponibilidad (Burges 1982; Vandekar y Dulmage 1982), al estudio de diferentes métodos de producción (Avignone-Rossa y Mignone 1993; Kang et al. 1992, 1993) y de las variables de operación que afectan el desarrollo de Bt (Avignone-Rossa et al. 1992; Foda et al. 1985). El proceso de producción de Bt pretende la optimización de la producción de esporas, de biomasa y la toxicidad de ésta contra el insecto deseado (Couch y Ross 1980; Kang et al. 1992; Avignone-Rossa y Mignone 1993). Todas estas variables están afectadas tanto por el medio de cultivo como por las condiciones y métodos de producción (Dulmage 1989; Mummigati y Ranghuathan 1990; Salama et al. 1983; Kang et al. 1993; Avignone-Rossa et al. 1992).
Materiales y Métodos
La cepa utilizada en este trabajo es denominada HD1 y fue aislada del producto comercial Dipel 2X de Laboratorios Abbott. Esta cepa corresponde a B. thuringiensis subsp. kurstaki (Btk), la cual presenta toxicidad específica para insectos del orden Lepidoptera.
Para el desarrollo de los inóculos de producción se utilizaron erlenmeyers de 250 ml de capacidad con 125 ml de M1, inoculados al 5% con la suspensión madre de esporas y ampicilina hasta una concentración final de 50 mg/ml. El inóculo de producción se incubó con agitación por 16 h, a 200 rpm y 30°C, y luego se midió la absorbancia a 600 nm y la concentración de esporas. Posteriormente se procedió a inocular, al 5%, cada uno de los medios de cultivo a estudiar y cada uno de los corridos del fermentador.
La suspensión madre de esporas de Btk se obtuvo de 400 ml de un cultivo completo final (CCF) de Btk incubado por 48 h a 200 rpm y 30°C. El CCF se centrifugó a 8.000 rpm y 4°C, por 20 minutos, descartándose el sobrenadante. El sedimento se suspendió en 40 ml de NaCl 1M y se agitó a 125 rpm y 37°C, por 30 minutos y se centrifugó de nuevo bajo las condiciones antes descritas. El sedimento obtenido se suspendió en agua destilada y nuevamente se centrifugó. Este proceso se realizó dos veces. Finalmente, el sedimento obtenido se suspendió en 200 ml de una solución de PBS y glicerol al 20% v/v. Esta suspensión se colocó al baño María, a 80°C por 10 minutos y se almacenó a -70°C hasta el momento de utilizarlo como punto de partida para el desarrollo del inóculo de producción de la totalidad de las fermentaciones.
Como fuente proteica se estudiaron semillas de algodón (Gossypium hirsutum L.), búcaro (Erythrina sp.), carbonero (Calliandra sp.) y guandul (Cajanus indicus (L.) Mills.), además de suero de leche y tortas de carne y de pescado. Como fuente de carbono se utilizó melaza y como fuente de minerales el cloruro de calcio (CaCl₂). La preparación de las soluciones madres de estos nutrientes, con las que se prepararon los medios de cultivo, se realizó de la siguiente manera:
A 50 g de semillas se les añadió 500 ml de agua destilada y esta mezcla se licuó y se filtró. El filtrado se utilizó como medio de cultivo.
A un matraz de un litro se transfirieron 100 g de suero de leche en polvo, se añadió agua y se agitó hasta disolverse. Finalmente se aforó.
En cuanto a las tortas de carne y de pescado, a un matraz de un litro se transfirieron 100 g de torta con 400 ml de agua; esta mezcla se llevó a ebullición por aproximadamente 2 minutos, se aforó y posteriormente se filtró. El filtrado se utilizó posteriormente como medio de cultivo.
Como fuente de carbono se pesaron 100 g de melaza y se completó el volumen a un litro con agua destilada.
Como fuente de minerales se preparó una solución madre de CaCl₂, (20 g/l), y a partir de ésta se realizó la dilución necesaria en la preparación de los medios de cultivo, en los que se utilizó en una concentración de 1 g/l.
Medios de cultivo
La variable composición del medio se definió como la fracción de carbono (Xc), gramos de melaza sobre gramos totales de melaza y fuente proteica. El rango utilizado para esta variable fue desde Xc = 1, melaza como único nutriente, hasta el caso opuesto, Xc = 0, donde el medio poseía únicamente fuente proteica.
La cantidad total de nutrientes se definió como los gramos de melaza y fuente proteica por litro de medio de cultivo. El rango utilizado para esta variable fue desde 25 a 75 g/l.
Fermentador
El rango de temperatura estudiado estuvo entre 28 y 32°C. El sistema fue aireado mediante un Sparger tipo flauta. Las velocidades de aireación, respecto al volumen de medio, correspondían a un rango entre 0,76 a 1,52 vvm.
El rango de agitación utilizado varió entre 250 y 450 rpm. El medio de cultivo se agitó mediante una turbina de seis paletas planas; mejorando la turbulencia del sistema con dos placas deflectoras colocadas a 180°.
Al mezclar los nutrientes, la fuente proteica y la melaza se estudió, por medio de un diseño central compuesto, la influencia de la composición y de la cantidad total de nutrientes del medio de cultivo sobre las variables de respuesta: biomasa total producida y concentración de esporas. Los medios de cultivo, su composición y la cantidad de nutrientes, preparados según este diseño, se detallan en la Tabla 1.
Composición de los medios estudiados
Volumen del medio = 200 ml
pH=7,2 (antes de esterilizar en el autoclave)
Para el estudio del efecto de las variables de interés sobre las diferentes variables de respuesta se utilizó un diseño experimental del tipo 2³ con experimento central. Los valores operacionales de las diferentes variables se muestran para cada una de las fermentaciones en la Tabla 2. Se utilizó un litro de medio de cultivo, pH=7,2, como volumen operacional.
Condiciones de operación de las fermentaciones estudiadas.
Volumen del medio = 1.000 ml
pH=7,2 (antes de esterilizar en el autoclave)
Variables de respuesta y métodos de medición
Para medir la concentración de esporas se tomaron 0,5 ml de cultivo cada 5 horas. De éste se realizaron diluciones seriadas en PBS. Dos de estas diluciones se sembraron por triplicado en LB, teniéndose en cuenta las que, en promedio, más se acercara a 100 UFC.
En el estudio de los medios de cultivo se midió la absorbancia de las diluciones seriadas de la muestra, 1/10 y 1/50, a 600 nm. Con los datos obtenidos se realizaron curvas de crecimiento celular, absorbancia contra tiempo. En la etapa de fermentador se midió la absorbancia de las diluciones seriadas de la muestra, 1/10 y 1/50, a 600 nm y este valor se correlacionó con la biomasa producida mediante una curva de calibración. Con los datos obtenidos se realizaron curvas de crecimiento celular, biomasa contra tiempo.
En el estudio de medios de cultivo, el producto final de la fermentación se pesó por medio del siguiente procedimiento. El CCF se centrifugó por 20 minutos a 8.000 rpm. Al sedimento obtenido se le añadieron 100 ml de agua destilada y se agitó por algunos minutos, procedimiento realizado por duplicado. El sedimento final se suspendió en 40 ml de agua destilada y se transfirió a copas de aluminio previamente pesadas, estas copas se secaron por 72 horas a 75-80°C. El valor de la biomasa producida se infirió de la diferencia de los dos pesos.
Bioensayo de toxicidad contra Spodoptera frugiperda
En laboratorio se estableció una cría masiva del gusano cogollero del maíz, Spodoptera frugiperda (J.E. Smith) (Lepidoptera: Noctuidae), cuyas larvas se alimentaron con una modificación de la dieta artificial de Shorey y Hale (1965), y los adultos se alimentaron con una solución de miel de abejas al 5%.
En la etapa del fermentador, luego de finalizada cada fermentación se realizó el siguiente procedimiento para obtener el ingrediente activo. El CCF se centrifugó por 20 minutos, a 8.000 rpm y 4°C, y el sedimento obtenido se suspendió en 200 ml de NaCl 1M. Esta suspensión se agitó a 125 rpm y 37°C durante 30 minutos. Luego se repitió el proceso de centrifugación, bajo las condiciones antes descritas. El sedimento obtenido se dispersó y centrifugó por dos oportunidades en agua destilada. El sedimento se suspendió en 40 ml de agua destilada, se almacenó por algunas horas a -70°C y posteriormente se liofilizó durante 16 horas.
La metodología utilizada para el bioensayo de superficie fue una modificación de la técnica de Padidam (1992). De los liofilizados obtenidos se pesaron 50 mg y se suspendieron en 4,5 ml de PBS; de dicha suspensión se realizaron diluciones sucesivas también en PBS, en las cuales la concentración de ingrediente activo produjera sobre larvas de primer instar de S. frugiperda una mortalidad entre 0 y 100%. De cada dilución se tomaron cuatro alícuotas de 0,4 ml que se virtieron sobre la dieta artificial utilizada para el cultivo en laboratorio de S. frugiperda.
La superficie de la dieta se dejó secar durante 5 horas a 30°C y luego se depositaron 5 larvas de primer instar de S. frugiperda por copa. La exposición de las larvas a las diferentes dosis se prolongó por 3 días, al cabo de los cuales se contabilizó el número de larvas muertas. Con estos resultados se realizó un análisis Probit para obtener la concentración letal media (LC₅₀), en mg/cmβ de la biomasa obtenida en cada una de las fermentaciones. Este procedimiento se realizó por triplicado y en días diferentes.
Como control negativo se utilizaron 20 larvas de primer instar de S. frugiperda, 5 por copa, alimentadas con dieta artificial sobre cuya superficie se esparcieron 0,4 ml de PBS. Como control positivo se utilizó una preparación de la cepa HD1-S-1980, suministrada por el Instituto Pasteur de París, a la cual arbitrariamente se le ha dado una toxicidad de 18.000 unidades internacionales. Con esta preparación se realizó un procedimiento exactamente igual al indicado para los diferentes liofilizados.
Resultados
Obtención del inóculo de producción
Luego de 16 horas de crecimiento, el inóculo de producción presentó una baja esporulación y valores altos de absorbancia, como se puede apreciar en la Tabla 3. Estas condiciones denotan un inóculo en crecimiento vegetativo, el cual minimiza la fase Lag del cultivo inoculado y aumenta la productividad del mismo (Pearson y Ward 1988a,b; Okafor 1987; Banks 1979). Para obtener el inóculo de producción con las características mencionadas, se utilizó una metodología que permitió el desarrollo del inóculo de producción en un medio de cultivo, M1, con mayor contenido de nitrógeno que de carbono y además en condiciones de baja aireación, condiciones que son adversas al proceso de esporulación (Okafor 1987; Avignone-Rossa et al. 1992, Bernhard y Utz 1993).
Análisis estadístico de las condiciones del inóculo de producción - Etapa del fermentador.
N = 13.
Coeficiente de variación (C.V.) = desviación estándar / valor medio
La poca variabilidad de la absorbancia del inóculo de producción fue otra característica importante observada en el inóculo de producción (Tabla 3). Este resultado permitió asegurar una estabilidad en las condiciones iniciales de cada fermentación, eliminando así esta posible fuente de error. Este resultado se puede atribuir a la utilización de la suspensión madre de esporas, con lo que se aseguró una estabilidad de las condiciones iniciales del inóculo. Además, se aseguró el crecimiento de B.t. en condiciones controladas de agitación, temperatura y por un tiempo fijo de 16 horas.
Medios de cultivo
Cuando se utilizó, como nutriente único de la fermentación, cada una de las fuentes de proteína estudiadas se permitió el adecuado crecimiento de Btk y su posterior esporulación. Además, no se encontraron diferencias significativas en la producción de esporas en cada medio. Por tal motivo, la selección de la fuente proteica se realizó después de analizar otras características deseadas en los medios de producción industrial, como son: la facilidad de consecución en la región, la adecuada composición química del medio y el costo del material, entre otras (Okafor 1987; Bernhard y Utz 1993).
Las semillas de algodón, búcaro, carbonero y guandul se estudiaron como continuación de un trabajo realizado anteriormente en la CIB, en el cual se utilizaron semillas vegetales en su estado natural como substratos para la producción de B. sphaericus (Bs), B.t. subsp. israelensis (Bti) y Bt subsp. medellin (Btm) (Orduz 1993). Estos nutrientes mostraron ser de poca aplicación industrial, debido principalmente a su difícil preparación y, con excepción de la semilla de algodón, a la dificultad de obtenerlos en las cantidades necesarias para la producción a escala industrial.
El suero de leche y las tortas de carne y de pescado son subproductos agroindustriales de fácil consecución en el país y que han sido utilizados con éxito para la producción de Bt en diferentes países (Salama y Morris 1993; Burges 1982). Como parámetro de selección entre estos nutrientes se tomó el factor económico. La comparación del valor en el mercado de estos subproductos favoreció a la torta de carne, $280 por kilogramo.
Como conclusión de esta primera parte del estudio se decidió utilizar la torta de carne como fuente de nitrógeno, la cual se mezcló en diferentes proporciones con melaza, como fuente de carbono, y CaCl₂ en concentración de 1g/l.
Optimización del medio de cultivo basado en la mezcla de melaza y torta de carne
En cuanto al efecto de la composición y la cantidad total de nutrientes del medio de cultivo sobre la producción final de esporas, como se observa en la Figura 1, a mayor fracción de carbono en el medio de cultivo menor fue el tiempo requerido para el comienzo de la esporulación, resultado que está acorde con el metabolismo propuesto para el proceso de esporulación (Pearson y Ward 1988b).
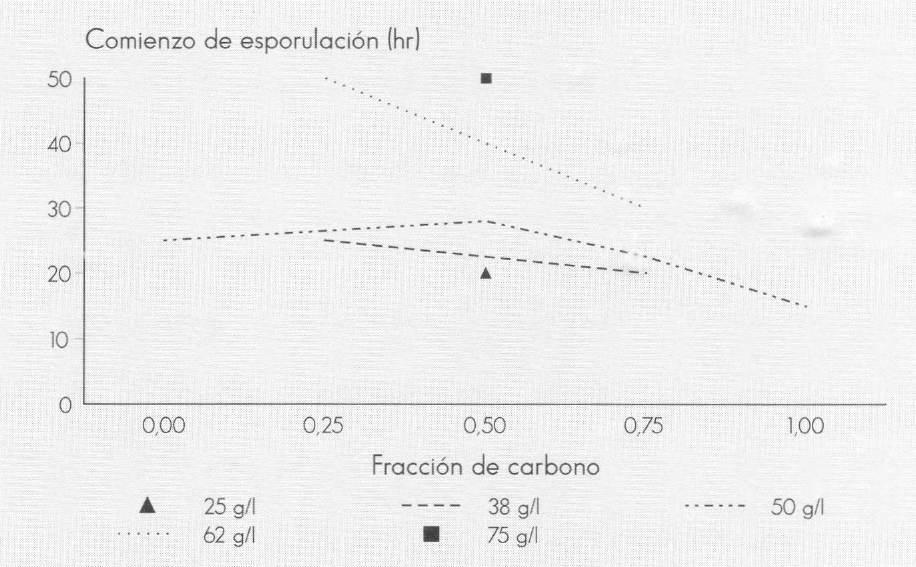
Efecto de la fracción de carbono sobre el tiempo requerido para el comienzo de la esporulación
Al comportamiento mencionado se observa una excepción por parte del medio de cultivo con torta de carne como único nutriente, Xc = 0. En este medio de cultivo, la torta de carne utiliza para soportar el crecimiento del microorganismo, a diferencia de los demás medios donde lo es la melaza. Por esta razón, el consumo de fuente de nitrógeno en este medio es más rápido y al agotarse comienza el proceso de esporulación, según el metabolismo propuesto para el proceso de esporulación de Bt (Pearson y Ward 1988b).
Por otro lado, se notó un ligero aumento en la producción de esporas en los medios de cultivo con mayor cantidad de melaza que de torta de carne (Tabla 4). Además, cuando la cantidad de nutrientes sobrepasó los 50 g/l se afectó, de manera importante, la producción final de esporas (Tabla 4). De manera similar a lo registrado en el presente trabajo, Gangurde y Shetna (1995) y Dharmsthiti et al. (1985) encontraron que luego de sobrepasar cierto limite de concentración total de nutrientes continua el aumento de producción de biomasa, pero la producción de esporas disminuye gradualmente.
Producción de esporas y biomasa en los diferentes medios de cultivo estudiados.
N = 5, coeficiente de variación (C.V.) = 94,5%
N=5, coeficiente de variación (C.V.) = 2,48
El efecto de la composición y la cantidad total de nutrientes en el medio de cultivo sobre la biomasa producida se observa también en la Tabla 4. En general, los medios que poseían una mayor fracción de carbono y los de mayor contenido de nutrientes, produjeron una mayor cantidad de biomasa al final de la fermentación. Sin embargo, al igual que Mummigati y Ranghuathan (1990), se encontró una baja en la esporulación en los medios de cultivo donde se logró una alta producción de biomasa.
Selección de medio de cultivo
En primer término se destacaron los medios de cultivo con baja producción de esporas, cantidad de nutrientes mayor a 50 g/l de nutrientes, y los medios de cultivo con una mayor cantidad de torta de carne que de melaza, ya que producían una menor cantidad de biomasa y demoraron más en comenzar el proceso de esporulación. Además se eliminaron los medios de cultivo con un solo nutriente, sólo melaza o torta de carne, ya que los rendimientos en biomasa fueron más bajos que en cualquiera de los medios de cultivo que tenían mezcla de nutrientes. De esta manera quedaron dos medios de cultivo, los denominados 4 y 7, con una producción de esporas bastante similar. Entre estos medios se escogió el último por producir más biomasa por litro, además de comenzar más rápidamente el proceso de esporulación.
Condiciones de operación del fermentador
Optimización de la productividad del medio de cultivo CIBM7 a nivel del fermentador de un litro de volumen de operación
En cuanto al efecto de las variables de operación sobre la concentración final de esporas, de una manera general se observó un efecto positivo de la velocidad de agitación y la velocidad de aireación sobre la cantidad final de esporas producidas, y un efecto adverso del aumento de temperatura sobre la concentración final de esporas.
El efecto positivo de la velocidad de aireación y la velocidad de agitación están de acuerdo con el metabolismo de Bt. El aumento de estas variables afecta positivamente la tasa de transferencia de oxígeno, lo que se ha comprobado que favorece el proceso de esporulación. Los resultados obtenidos concuerdan con los ya reportados por Foda et al. (1985) y Avignone-Rossa et al. (1992).
El efecto de las variables de operación sobre el tiempo necesario para el comienzo de la esporulación se observa en la Figura 2.
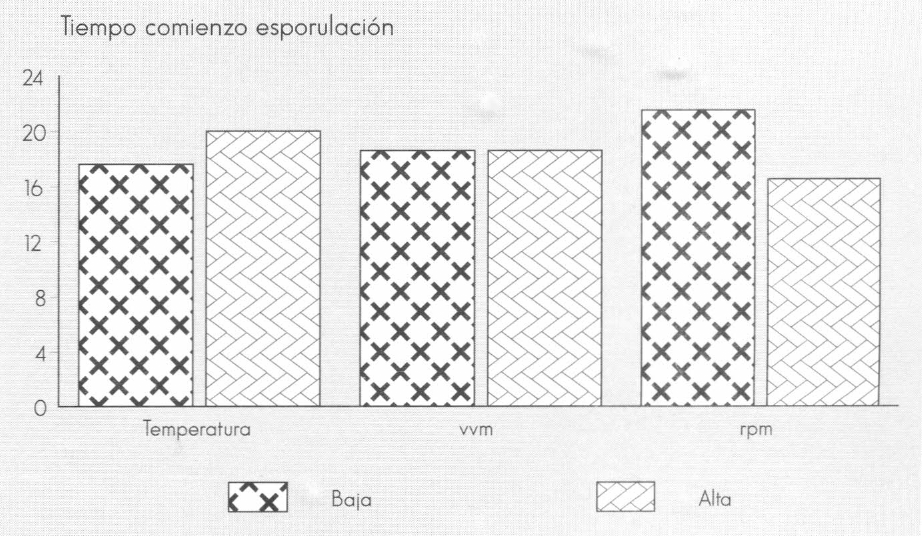
Efecto de las variables de operación sobre el tiempo necesario para el comienzo del proceso de esporulación.
En la Figura 3 se observa el efecto de las variables de operación (temperatura, velocidad de agitación y velocidad de aireación) sobre la biomasa final producida por el medio de cultivo. La velocidad de agitación es la variable de mayor efecto sobre la productividad del medio de cultivo. Avignone-Rossa et al. (1992) reportaron, de forma similar, un aumento en la producción de biomasa al aumentar la velocidad de agitación, manteniendo constantes la velocidad de aireación y la temperatura, hasta alcanzar un tope de 350 rpm.
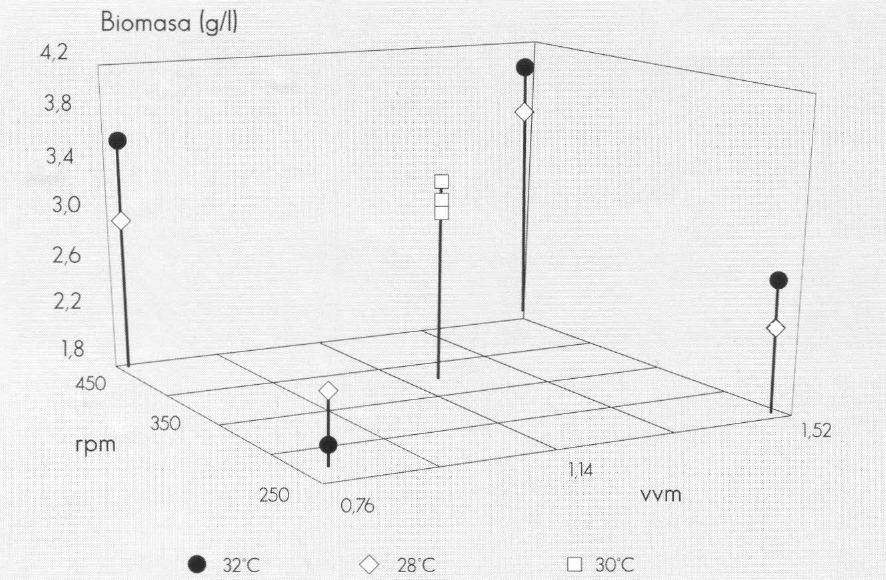
Efecto de las variables de operación sobre la biomasa producida.
El efecto de las diferentes variables de operación sobre la producción de biomasa pudo ser modelado matemáticamente mediante la siguiente ecuación, y cuyo análisis de varianza se muestra en la Tabla 5.
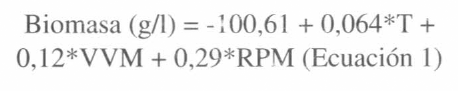
Análisis de varianza de la Ecuación 1.
Con un nivel de significancia de 0,05: F₃,₉ = 3,86, F₅,₄ = 6,26
Los coeficientes de la ecuación propuesta muestran que la producción de biomasa por parte del medio de cultivo se ve afectada positivamente por un aumento en cualquiera de las variables de operación. De estas variables, la velocidad de agitación, en primer lugar, y la velocidad de aireación tuvieron una mayor influencia sobre la productividad del medio de cultivo. Las condiciones de operación óptimas para la producción de biomasa serian entonces 32°C de temperatura, aireación de 1,52 vvm y 450 rpm de agitación.
La toxicidad del producto obtenido, medida con respecto al estándar internacional, estuvo en el rango de 97.000 a 2.320.000 UI/mg, dependiendo de las condiciones de la fermentación (Fig. 4), aunque esta medición demostró tener una alta variabilidad como puede observarse en el valor central de la Figura 4.
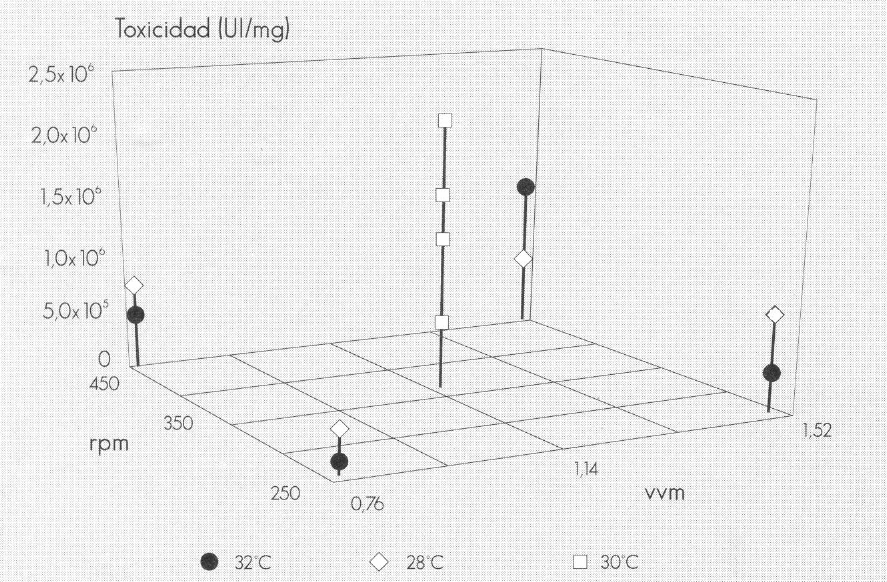
Efecto de las variables de operación sobre la toxicidad de la biomasa producida.
El ingrediente activo del producto comercial, del que se tomó la cepa utilizada, tiene una toxicidad de 500.000 UI/mg. Dadas las condiciones del presente trabajo, la toxicidad del ingrediente activo obtenido en las condiciones de máxima producción de biomasa y de máxima producción de toxicidad son bastante aceptables al compararse con las del producto comercial.
Conclusiones
Los resultados conseguidos con el inóculo de producción obtenido a partir de una solución madre de esporas, demostraron una alta estabilidad según las mediciones de su densidad óptica. La reproducibilidad de estos valores demuestra la eficacia de esta metodología para asegurar que las condiciones iniciales en todas las fermentaciones fueran similares, y por ende se recomienda su utilización para microorganismos que presenten esporulación. Cuando se utiliza como nutriente único, la fuente de carbono permite una mayor producción de biomasa que la fuente de nitrógeno. Sin embargo, cuando se mezclan ambos nutrientes se obtienen mayores rendimientos, siendo lo óptimo la mezcla por partes iguales. Se encontró que los medios con mayor cantidad de fuente de carbohidratos que de proteína comienzan y terminan el proceso de esporulación más rápidamente, además de producir altas concentraciones de biomasa y esporas. Por lo anterior, estos medios son adecuados para la producción de Bt. No así los medios con una relación alta de nitrógeno a carbono, en los cuales se retarda la esporulación. De las variables de operación estudiadas, la velocidad de agitación demostró tener la mayor influencia sobre la productividad del medio de cultivo. Tanto la producción de esporas como la producción de biomasa y la toxicidad de la misma están directamente relacionadas con esta variable. Una buena agitación también demostró reducir el tiempo necesario para el comienzo del proceso de esporulación. La medición de la concentración de esporas no dió resultados confiables durante todo el estudio. Sin embargo, un análisis cualitativo de sus resultados permite identificar otras características importantes en los medios de cultivo como son: el tiempo necesario para comenzar y finalizar el proceso de esporulación y la identificación de posibles causas de una baja toxicidad. La biomasa producida en el medio de cultivo desarrollado tuvo una toxicidad mucho mayor al estándar internacional. Esta toxicidad, aunque no pudo determinarse estadísticamente, parece estar influenciada por las condiciones de operación. El medio de cultivo desarrollado tiene un rendimiento medio para la producción de biomasa, 4,03 g/l, y esporas, alrededor de 21,107 esp/ml. Además, su bajo precio ($30/1) y la alta toxicidad contra S. frugiperda que posee la biomasa producida, del orden de 1.300.000 UI/mg, hace que este medio sea viable industrialmente desde el punto de vista tecnológico o de producción.
Footnotes
Agradecimientos
Esta investigación recibió el apoyo de la Corporación Regional Autónoma de Rionegro y El Río Nare (Cornare) y de la Corporación para Investigaciones Biológicas, CIB.
