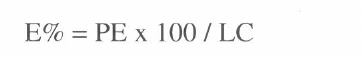Abstract
The Andean weevil Premnotrypes vorax (Hustache) is an important pest of the Colombian potato crops. Nevertheless its importance, few research has been carried out looking for alternatives of control different to the chemical. Based on previous reports, a soil entomopatogenic nematode was isolated and identified from Colombian potatoes fields in Villapinzón, Cundinamarca. Its pathogenicity to the weevil was compared with that of the product EXHIBIT, which active principle is Steinernema carpocapsae strain 25. The new nematode was multiplied in vivo in Galleria mellonella (L). larvae, following Dukty's procedures, and it belongs to the genus Steinernema, and seems to be a new species. By using bioassays the median letal concentration (LC50) to the weevil was established, being 526,43 and 26,30 nematodes /ml for the native nematode and S. carpocapsae, respectively, indicating that S. carpocapsae strain 25 is 20 times more pathogenic to P. vorax than the native nematode.
Introducción
La papa (Solanum tuberosum L.) ocupa mundialmente uno de los primeros lugares en cuanto a producción y consumo. Colombia cuenta con una área total sembrada de 190.000 ha (Fedepapa 1994).
El gusano blanco de la papa, Premnotrypes vorax (Hustache) (Coleoptera: Curculionidae), es uno de los problemas entomológicos más graves que enfrenta la producción de papa en Colombia. El insecto está distribuido en todas las zonas productoras causando pérdidas hasta del 30% en el rendimiento y del 100% en la calidad del producto, cuando no se realiza ningún tipo de control. Aunque se aplican insecticidas carbamatos para su control, las pérdidas ocasionadas por la plaga son aún considerables, y la utilización excesiva de insecticidas se refleja en el aumento de los costos de producción. Además, la probabilidad de generar resistencia a estos productos exige la implementación del manejo integrado del gusano blanco (Paroonagian 1994).
En el presente trabajo se aisló e identificó un nematodo y se evaluó su patogenicidad. El nematodo de la familia Steinernematidae, se encontró parasitando larvas del gusano blanco en zonas productoras de Villapinzón (Cund.), en forma natural.
Los nematodos de los géneros Steinernema y Heterorhabditis son habitantes naturales del suelo y tienen la capacidad de buscar, parasitar y causar la muerte a gran número de insectos plaga.
Para que estos nematodos puedan reproducirse y causar la muerte del insecto hospedante deben estar asociados con una bacteria del género Xenorhabdus. La asociación nematodo-bacteria es importante como factor letal para los insectos, ya que la bacteria es la responsable de la muerte de éstos, pero necesita del nematodo como medio de transporte hacia el insecto hospedante (Kuno y Hernández 1982).
El ciclo de vida de los nematodos entomopatógenos consta de huevo, cuatro estados juveniles infectivos (IJ) y adulto. El tercer estado (IJ3) conserva la cutícula del segundo estado juvenil (IJ2) y lleva la bacteria en su tracto digestivo. Una vez el nematodo encuentra su huésped penetra a través de aberturas naturales como boca, ano y espiráculos, para instalarse en el hemocelo. La bacteria sale del intestino del nematodo y pasa a la hemolinfa, se multiplica y mata al insecto hospedante por septicemia. El nematodo se alimenta de la bacteria y del tejido descompuesto del insecto hospedante, y después emerge a través de la epidermis del insecto como IJ3 (Kaya y Gaugler 1993)
Los nematodos de las familias Steinernematidae y Heterorhabditidae son los de mayor potencial como controladores, ya que se pueden multiplicar masivamente in vivo o in vitro (Poinar y Thomas 1984). En la actualidad, especies de estas familias se están utilizando contra insectos como: Spodoptera sp., Agrotis ipsilon (Hufnagel) (Lepidoptera), Ceratitis capitata (Wiedemann) (Diptera) y los coleópteros Otiorhynchus sulcatus (Fabricius), Diabrotica virgifera Le Conte y varias especies de la familia Scarabaeidae.
Recientemente se han introducido al país productos que tienen como ingrediente activo el nematodo Steinernema carpocapsae Raza 25, y su patogenocidad hacia el gusano blanco de la papa se comparó con la del nematodo nativo mediante bioensayos controlados.
Materiales y Métodos
El trabajo se llevó a cabo en el Laboratorio de Entomología de la Facultad de Agronomía de la Universidad Nacional de Colombia en Santafé de Bogotá. Allí se desarrollaron crías masivas de la polilla de las colmenas, Galleria mellonella (L.) (Lepidoptera: Pyrilidae), y del gusano blanco, sobre las cuales se multiplicaron los nematodos y se realizaron los bioensayos.
Cría y ciclo de vida de gusano blanco de la papa
La cría se inició a partir de individuos traidos de campo y de una cría establecida en el Centro de Investigación «Tibaitatá» del ICA, en Mosquera (Cund.), con las siguientes condiciones: Temperatura máxima 22°C, Temperatura mínima 10°C, Humedad relativa promedia 60%.
En cajas plásticas de 15 x 20 x 30 cm se colocó suelo esterilizado en una autoclave a 121°C, 15 psi durante 15 minutos, hasta una altura de 5 cm; sobre este suelo se colocaron tubérculos de papa criolla (Solanum phureja Juz. et Buk), y huevos del gusano blanco dentro de tallos secos, donde los habían ovipositado los adultos traidos de la cría del ICA. Las cajas se mantuvieron húmedas para favorecer la eclosión de los huevos, y se les adicionó azufre microhomogenizado para controlar la presencia de ácaros y hongos. Los tubérculos se mantuvieron durante dos semanas en estas cajas, hasta la eclosión de los huevos y la penetración de larvas de primer ínstar a los tubérculos, y posteriormente se colocaron en cámara oscura o en bandejas plásticas tapadas con tela, y se esperó hasta la emergencia de las larvas de último ínstar.
Luego, en una caja de acrílico (10x10x5 cm) con una capa de 4 cm de suelo previamente cernido y esterilizado, se colocaron 30 larvas de último instar y se esperó hasta que empuparan. Los adultos emergidos de estas cajas se transfirieron a una bandeja más grande con hojas y tubérculos frescos de papa para su alimentación, y trozos de tallos secos de gramíneas para facilitar la oviposición.
El ciclo de vida de P. vorax se registró en el laboratorio midiendo diariamente el tiempo que dura cada una de las siguientes etapas:
De oviposición a eclosión de los huevos. Huevos de P.vorax se colocaron en la base de cajas de petri con papel de filtro húmedo, y éstas se colocaron en frascos con agua tapados con plástico; se registró el tiempo de incubación.
De larvas de primer instar a larvas de último instar. Larvas recién nacidas se tomaron y colocaron en el interior de tubérculos de papa criolla (10 larvas por tubérculo) con la ayuda de un pincel. Las papas se colocaron en una caja plástica cerrada, y diariamente se hicieron observaciones hasta que salieron las larvas de último ínstar.
De larvas de último ínstar a adulto. En cajas de acrílico se colocarón 30 larvas de último ínstar por caja y se esperó hasta la aparición de adultos. La duración del adulto no se estableció en el laboratorio.
Para establecer la eficiencia del sistema de cría se comparó el número de larvas de último ínstar colocadas en cajas de acrílico y el número de adultos hembras y machos obtenidos, expresándolo en porcentaje. Se tomaron datos de 25 cajas.
Para registrar la oviposición de P. vorax se seleccionaron 14 cajas de las utilizadas para la obtención de adultos y en ellas se colocaron hojas y tubérculos de papa criolla y 10 tallos secos de gramíneas. Se dejaron grupos de 2 a 15 hembras por caja, y diariamente se remplazaron las pajas de cada caja y se registró el número promedio de huevos por hembra.
Cría de Galleria mellonella
Siguiendo la metodología utilizada por Ortiz (1993), quien trabajo con G. mellonella bajo las condiciones de una plantación de palma de aceite en Tumaco (Nar.), se estableció una colonia de este insecto en el Laboratorio de Entomología de la Facultad de Agronomía. Se registró la duración del ciclo de vida y la oviposición por hembra bajo estas condiciones.
El nematodo nativo
Los nematodos entomopatógenos se encuentran frecuentemente asociados con insectos muertos que están sometidos a la acción del medio y de microorganismos. Bedding y Akhurst (1975) obtuvieron parasitismo de nematodos entomopatógenos en el laboratorio, utilizando larvas de G. mellonella como trampa, y colocándolas en muestras de suelo.
Siguiendo esta metodología se trajeron muestras de 5 kg de suelo de diferentes zonas paperas y sobre cada muestra se colocaron 10 larvas de último ínstar de G. mellonella, y se esperó a que se produjera la infección por el nematodo bajo condiciones del laboratorio. Las zonas en donde se tomaron las muestras de suelo fueron: Vereda Riofrío, municipio de Cogua (Cund.), Vereda Casablanca, municipio de Villapinzón (Cund.) y Vereda Huerta Grande, municipio de Ventaquemada (Boy.)
En cada zona se recolectaron larvas, pupas y adultos de gusano blanco. Las larvas y las pupas se dejaron en cámara húmeda con el fin de observar la presencia de algún tipo de afección causada por los nematodos, y los adultos se utilizaron para incrementar la cría.
Las larvas y pupas de gusano blanco traídas del campo, y las larvas de G. mellonella colocadas en las muestras de suelo en el laboratorio que mostraron síntomas de infección por nematodos, se dejaron por separado en cámaras de White, donde se obtuvieron suspensiones iniciales del nematodo nativo.
Aislamiento, multiplicación e identificación del nematodo nativo
De larvas de G. mellonella infectadas se obtuvo el nematodo nativo en una suspensión que contenía simultáneamente nematodos saprófitos e impurezas.
El nematodo nativo se separó mecánicamente utilizando un pincel. Cuando se obtuvo una cantidad considerable del estado IJ3, se infectaron larvas de G. mellonella y con la suspensión resultante se inició un cultivo puro de nematodos.
Para la recolección de los nematodos se esplearon cámaras de White que consisten en una caja de petri de 90 mm de diámetro, dentro de la cual se coloca un tubo de PVC de 1" cortado longitudinalmente (longitud 8,5 cm) y envuelto en un papel de filtro Whatman No 1. A cada caja de se le adicionan 15 ml de agua destilada y formaldehído al 0,3%, y en esta solución se suspenden los nematodos luego de salir del cadáver del huésped
Las suspensiónes de nematodos obtenidos en las cámaras de White se titularon tomando volúmenes de 0,01 ml, los cuales se colocaron en láminas portaobjetos y luego se llevaron al estereoscopio para su observación y conteo. La concentración se expresó en nematodos/ml.
Siguiendo la metodología propuesta por Dutky et al.(1964) para la multiplicación de los nematodos, se utilizaron larvas de último ínstar de G. mellonella, colocando 40 larvas por caja petri de 90 mm de diámetro. Las larvas se colocaron dentro de la caja sobre papel de filtro Whatman No 1, se adicionaron 3 ml de suspensiones de nematodos, y luego se cubrieron con otro papel de filtro. Las cajas se taparon y se colocaron en total oscuridad, cubriéndolas con una tela negra.
Las larvas de G. mellonella muertas se colocaron en cámaras de White, y allí se recuperaron los nematodos y se almacenaron en un botellón de color ámbar, pasándolos por un tamiz de 270 mesh, con el fin de seleccionar únicamente los estados infectivos. El botellón contenía una solución de formaldehído al 0,3%, una gota de Tritón AC, para lubricar las paredes del botellón y evitar que los nematodos se adhirieran a éstas. La suspensión de nematodos se agitó con un oxigenador y así se pudo conservar por tres meses a una temperatura promedia de 19°C.
El nematodo comercial se obtuvo a partir de una muestra del producto EXHIBIT®,* actualmente en estudios preliminares en Colombia por parte de Ciba Geygy. El procedimiento para su multiplicación es igual al del nematodo nativo. Las concentraciones del nematodo nativo y del nematodo comercial se igualaron realizando las diluciones adecuadas.
Marca Registrada de CIBA-GEIGI
Para la identificación del nematodo nativo, éste se recuperó de las cámaras de White y se observó al microscopio para separar las impurezas (nematodos saprófitos del suelo, ácaros y basura). Las características morfológicas se observaron con las referencias de las claves de órdenes, géneros y especies así:
Clave de órdenes de Weiser y Briggs, (1972) que describe aspectos básicos de morfología como: forma del esófago, tamaño del estoma y forma de la cola.
Clave para géneros de Poinar y Thomas, (1984) con la cual se puede establecer otro tipo de características, tales como: Ubicación dentro del huésped, presencia de machos y hembras o de sólo un sexo por generación hembras gigantes en la primera generación, y presencia de estados juveniles.
Con las muestras en el taxón superior se utilizó la clave para identificación de especies propuesta por Nguyen, (1993), de la cual se tomaron los siguientes criterios:
Para tercer estado juvenil (IJ3): Largo del cuerpo, sin tener en cuenta la cutícula exterior, distancia entre el borde anterior y el poro excretor (PE), largo de la cola, distancia comprendida entre el ano y el borde posterior (LC), y se calculó el valor
Para machos adultos de la primera generación se siguieron los criterios: Largo del esófago (LE), el valor D%=PEx100/LE, y el largo de la espícula y largo del gubernáculo.
Otro criterio importante es la relación existente entre las medidas así:
SW = Largo de la espícula / Ancho del cuerpo en la región del ano.
EW = PE / Ancho del cuerpo en la región del poro excretor.
GS = Largo del gubernáculo / largo de la espícula.
Se tomaron medidas de 25 individuos, utilizando un microscopio con ocular micrométrico. Con base en estas medidas y su ubicación en las claves se determinó el orden, la familia, el género y la posible especie del nematodo nativo.
Bioensayos
Para determinar la concentración letal media (CL50) se realizó un bioensayo con tres repeticiones en el tiempo. Se evaluaron concentraciones de 80, 800, 8.000, 80.000, nematodos/ml, tanto del nematodo nativo como del nematodo comercial, sobre grupos de individuos compuestos por 15 larvas de último ínstar de P. vorax por caja de petri (unidad experimental), según un sistema universal establecido para Sterneinematidae y Heterorhabditidae (Woodring y Kaya 1988). Este método consistió en colocar papel de filtro Whatman No.1 en cajas de petri de 90 mm de diámetro y luego esterilizarlas por 15 minutos a 121°C, y 15 psi. Luego el papel de filtro se humedeció con 3 ml de la suspensión de nematodos de cada una de las concentraciones a evaluar. Después se colocaron 15 larvas de último ínstar de P. vorax sobre el papel de filtro y se cubrieron con otro papel de filtro.
A cada caja de petri se le colocó su respectiva tapa, se marcaron y se taparon con una tela negra, y cada 24 horas se registró la mortalidad de las larvas. El estado de muerte o supervivencia de cada individuo se calificó tocándolo tres veces con la cabeza de un alfiler entomológico, y si permanecía inmóvil se consideraba muerto.
Las larvas muertas se lavaron y colocaron en cámara de White, previa confirmación de la presencia de nematodos en su interior. Los bioensayos se llevaron a cabo a partir de los días 11 de julio, 31 de agosto y 15 de septiembre de 1994.
Resultados y Discusión
Ciclo de vida y Cría al gusano blanco
La duración del ciclo total de P. vorax bajo las condiciones del laboratorio de la Universidad Nacional de Colombia (Tabla 1) fue menor que los reportados para la Sabana de Bogotá. Esto posiblemente se debe a la mayor temperatura registrada en el laboratorio, lo que confirma que la temperatura influye significativamente en la duración del ciclo de vida del insecto, lo cual está acorde con los trabajos realizados por Calvache (1986).
Ciclo de vida del gusano blanco de la papa registrado en el laboratorio de la Facultad de Agronomía, Santafé de Bogotá, 1994.
Número de observaciones.
La eficiencia calculada del sistema de cría fue del 58%, lo cual se considera baja. Esto permite concluir que factores como humedad, temperatura, calidad del material y la manipulación deben ser evaluados para mejorar la eficiencia. Factores como el confinamiento y la alimentación pueden también afectar el desarrollo del insecto y sus hábitos de cópula y oviposición. Condiciones no óptimas de cría se reflejan posteriormente en una baja producción de huevos y en la disminución de la longevidad de los adultos.
El promedio de huevos por hembra para la primera oviposición, bajo condiciones de laboratorio, fue de 33,17, lo cual no se había determinado antes. Como las hembras pueden realizar varias cópulas y varias oviposiciones durante su ciclo, se recomienda evaluar la oviposición durante todo éste.
Cría de G. mellonella
El registro se hizo para cada frasco, obteniéndose una duración promedio de 11 días de huevo a larva de primer ínstar. La duración promedio de larva de primer instar a la emergencia de los adultos fue de 49,1 días. Con estos datos se estableció que la duración del ciclo de vida de G. mellonella es de 60,9 días bajo condiciones del laboratorio, lo cual es menor que lo reportado por Ortiz (1993) para las condiciones de Tumaco (Nar.), pero es similar a lo obtenido por Zenner y Posada (1992). El sistema de cría permitió obtener el material para los diferentes ensayos, por lo cual se considera adecuado para los propósitos de este trabajo.
Identificación del nematodo nativo
Nematodos de primera generación. Machos con una longitud promedio de 2,04 mm y hembras con una longitud promedio de 6,22 mm (n = 15).
No se observaron nematodos dentro del tracto digestivo. La hemolinfa del insecto huésped tomó una consistencia espesa y su color cambio a crema oscuro.
Hembras. Con vulva prominente y sin epitigmas, cola redondeada, presencia de miles de huevos y algunos nematodos en formación o de primer ínstar en su interior. Sin espícula ni gubernáculo. Esófago con bulbo medio y bulbo basal, poro excretor conspicuo con abultamiento en el borde, el anillo nervioso no muy visible. Además se observa un mucrón (prolongación de la cola presente en algunas especies de nematodos) como una proyección de la cola de tamaño pequeño.
Machos. Más pequeños que las hembras, con espícula y gubernáculo, presencia de un mucrón muy delgado y alargado, terminado en una punta muy aguda. Las medidas de los adultos machos de la primera generación se presentan en la Tabla 2.
En larvas de G. mellonella de 5 y 6 días de muertas, se observaron nematodos más pequeños (IJ3) dentro de la cutícula del IJ2, en gran cantidad (89.000 nemátodos/ml). Sobre estos nematodos se tomaron las medidas que permitieron la comparación con la clave para la identificación de especies. Las medidas se presentan en la Tabla 3.
Medidas en micras (µ) del nematodo nativo. Machos adultos de la primera generación.
DPE: Distancia del borde anterior al poro excretor; LES: Largo del esófago; APE: Ancho del cuerpo a la altura del poro excretor; LESP: Largo de la espícula; LCO: Largo de la cola (del ano al final posterior); LGU: Largo del gubernáculo; ACO: Ancho del cuerpo en el sitio del ano; D%:Distancia entre el borde anterior y el poro excretor x 100 / Largo del esófago
Los nematodos que se encontraron parasitando pupas de gusano blanco en la vereda Riofrío, son de la familia Heterorhabditidae, lo cual se estableció por la presencia de la bursa o ala caudal en la región de la cola. Estos nematodos no pudieron multiplicarse, ya que el estado infectivo no se encontraba presente.
Los datos obtenidos permiten concluir que el nematodo nativo es del orden Rhabditidae, de la familia Steinernematidae y género Steinernema, y se asemeja a la especie Steinernema feltiae, descrita por Filipjev y Poinar (Nguyen 1993). No obstante, el aspecto del mucrón difiere en tamaño con lo reportado para esta especie, por lo cual es posible que el nematodo pertenezca a una especie que no se ha reportado y que puede ser confirmado por el Dr. George Poinar, Jr. de la Universidad de California Berkeley.
Bioensayos con Gusano blanco
Los resultados de los bioensayos (Tablas 4 y 5 y Fig. 1) permiten concluir que el nematodo del producto comercial EXHIBIT es más patogénico hacia larvas de último ínstar de P. vorax que el nematodo nativo, ya que para tres períodos diferentes después de la infección, la CL50 del nematodo comercial fue menor que la del nematodo nativo. Según los resultados, la ecuación de regresión indica que el incremento en la concentración de nematodos implica una mortalidad en un período menor.
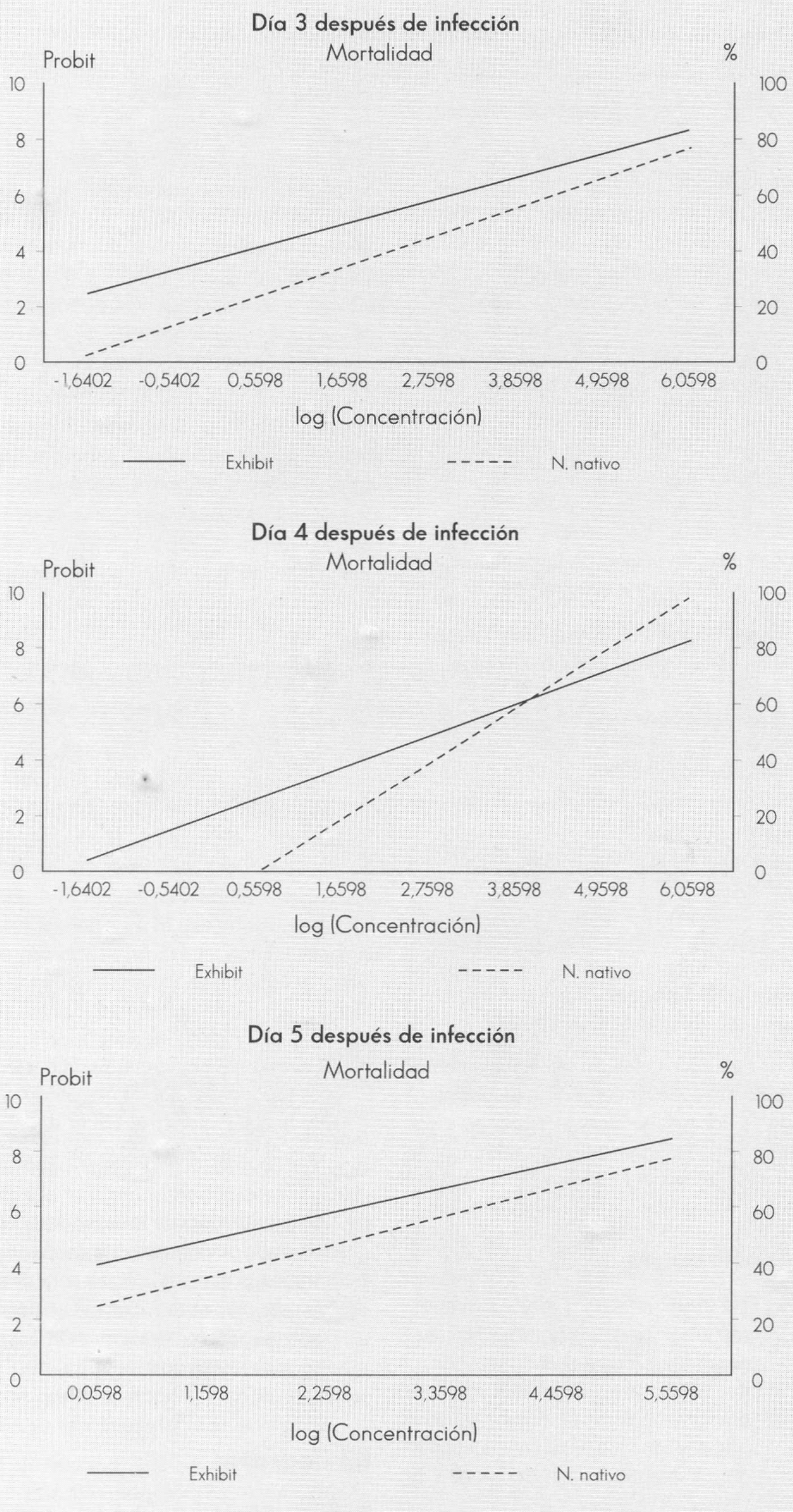
Líneas de regresión, mortalidad Vs Concentración para 3, 4 y 5 días después de la infección.
Medidas en μ del nematodo nativo Estados infectivos juveniles (IJ3).
Patogenicidad del nematodo nativo, sobre larvas de último ínstar de Premnotrypes vorax
DDI: Días después de la infección
Patogenicidad del nematodo Steinernema carpocapsae Raza 25 sobre larvas de último instar de Premnotrypes vorax
DDI = Días después de la infección.
La potencialidad, expresada como la CL50 del nematodo nativo sobre la CL50 de S.carpocapsae, indica que el nematodo comercial fue 3,8 veces más patogénico que el nematodo nativo al tercer día después de la infección, 5,6 veces al cuarto día y 20 veces más al quinto día.
Los resultados indican que ambos nematodos son controladores biológicos potenciales del gusano blanco de la papa y podrían utilizarse como componentes de programas de control biológico de esta plaga.
Conclusiones
En Colombia existen nematodos entomopatógenos de las familias Steinernematidae y Heterorhabditidae que se encuentran presentes en diferentes zonas productoras de papa, y que en alguna proporción están ejerciendo control natural del gusano blanco de la papa, P. vorax.
El nematodo aislado de suelo colombiano y el nematodo comercial resultaron patogénicos hacia el gusano blanco de la papa.
El nematodo comercial fue 3,8 veces más patogénico que el nematodo nativo hacia P. vorax al tercer día, 5,6 veces al cuarto día y 20 veces al quinto día.
La aproximación a la taxonomía del nematodo recuperado de suelos colombianos permitió establecer que se trata de una nueva especie perteneciente al género Steinernema (Rhabditida: Steinernematidae).