Abstract
El Cyrtomenus bergi, la chinche subterránea de las raíces o chinche de la viruela de la yuca, apareció a comienzos de la década del 80 como una nueva plaga del cultivo de la yuca (Manihot esculenta,) en las principales zonas productoras de Colombia. El daño de este insecto afecta directamente la calidad del producto comercial tanto para consumo humano como industrial, aun con bajos niveles de infestación. El reconocimiento de nematodos nativos asociados con C. bergi se realizó como una alternativa al control químico y cultural. De las ocho localidades se obtuvo un 100% de recuperación de nematodos entomopatógenos. En Manizales, Pereira y Santander de Quilichao se identificaron razas geográficas de la especie Heterorhabditis bacteriophora Poinar, recuperadas tanto del suelo como de chinches muertas en el campo, bajo condiciones diversas de clima y características físicas y químicas de suelo. A los nematodos aislados de las localidades restantes se les asignó un código para posteriores referencias mientras se establece su identificación.
Introducción
La chinche subterránea de las raíces, Cyrtomenus bergi Froeshner (Hemiptera: Cydnidae), es considerada como una de las principales plagas del cultivo de la yuca (Manihot esculenta Crantz) en Colombia. Las ninfas y adultos se alimentan introduciendo los estiletes en la epidermis y corteza de la raíz, permitiendo la entrada de microorganismos del suelo, y deteriorando y afectando la calidad (García 1982).
Además de la yuca, la chinche ataca otros cultivos comerciales, tales como: papa (Solanum tuberosum L.); cebolla (Allium cepa L. y A. fistulosum L.); maíz (Zea mays L.); maní (Arachis hypogea L.); sorgo (Sorghum vulgare Pers.); caña de azúcar (Saccharum officinarum L.); café (Coffea arabiga L.); arroz (Oryza sativa L.); espárrago (Asparagus officinalis L.) y pastos (García 1982).
Este insecto tiene una amplia distribución en países de Centro y Sur América, tales como: Costa Rica, Panamá, Cuba, Brasil, Ecuador y Surinam (Riis 1990).
Desde su aparición, a comienzos de la década del 80, se han realizado ensayos de control con variedades tolerantes, con insecticidas aplicados al follaje y al suelo (Vargas et al. 1986) y control cultural con la leguminosa Crotalaria juncea L. (Riis 1990), pero ninguno ha sido implementado por no ajustarse a las exigencias sociales y ambientales.
Como una alternativa de control se presenta el uso de nematodos entomopatógenos de las familias Steinernematidae y Heterorhabditidae (Rhabditida), los cuales son considerados importantes agentes de control biológico de muchos insectos plaga de hábito subterráneo.
Numerosos estudios de reconocimiento y distribucción de estos nematodos se han realizado en el mundo, pero poco se conoce sobre su presencia y distribución en Colombia como posibles enemigos naturales de C. bergi. Por estas razones, el objetivo principal de este estudio fue realizar un reconocimiento de nematodos entomopatógenos nativos asociados con C. bergi.
Materiales y Métodos
Toma de muestras
Las localidades para tomar muestras se seleccionaron por la presencia de C. bergi sobre diversos cultivos, siendo escogidos las siguientes: Santágueda en Manizales (Caldas), La Florida en Pereira (Ris.), Santander de Quilichao (Cauca), Mariquita (Tol.), Ciénaga de Oro (Córd.), Araracuara (Caq.), Mondomo en Santander de Quilichao (Cauca) y Buga (Valle del Cauca).
Las muestras de suelo se tomaron con un barreno sacabocado de 5 cm de diámetro, a 10 cm de profundidad y 10 cm de la base del tallo, si habían plantas. De cada localidad se tomaron muestras por cada lote, con chinche y sin chinche, las cuales se depositaron en bolsas plásticas debidamente rotuladas y conservadas en frigotermos para trasladarlas al laboratorio. Cada muestra contó con la siguiente información: textura y humedad del suelo, cultivo actual o anterior, localidad, altitud, precipitación, contenido de materia orgánica y pH (Tabla 1).
Localización, condiciones ambientales y análisis de suelo de los sitios donde se tomaron las muestras
Recuperación y aislamiento de nematodos
La recuperación de los nematodos del suelo se realizó tomando como referencia la metodología de Bedding y Akurst (1975), utilizando larvas de Galleria mellonella (L.) (Lepidoptera: Pyralidae) como insecto trampa. Las 10 muestras de suelo de cada sitio se mezclaron, y luego se tomaron 30 submuestras de 100 g y se colocaron en vasos plásticos de 7x7x10 cm junto con 10 larvas de G. mellonella, las cuales se dejaron durante 5 días bajo condiciones de laboratorio (T= 23°C; H.R.= 65%), para luego ser retiradas y colocadas sobre una trampa de recuperación, consistente en un papel Kleenex sumergido en una caja petri con agua, durante 24 horas (Fig. 1), tiempo en el cual los nematodos migran al agua, para luego ser recolectados en un beaker y lavados mediante decantaciones sucesivas, para posteriormente inocularlos sobre larvas de G. mellonella de último instar, para comprobar su parasitismo y obtener adultos y estados infectivos para ser enviados al especialista para su identificación. Además, en el campo se recolectaron adultos y ninfas de chinches muertas, los cuales se disectaron para determinar si estaban o no parasitados por nematodos y para aislarlos y reproducirlos sobre larvas de Galleria para su posterior identificación.
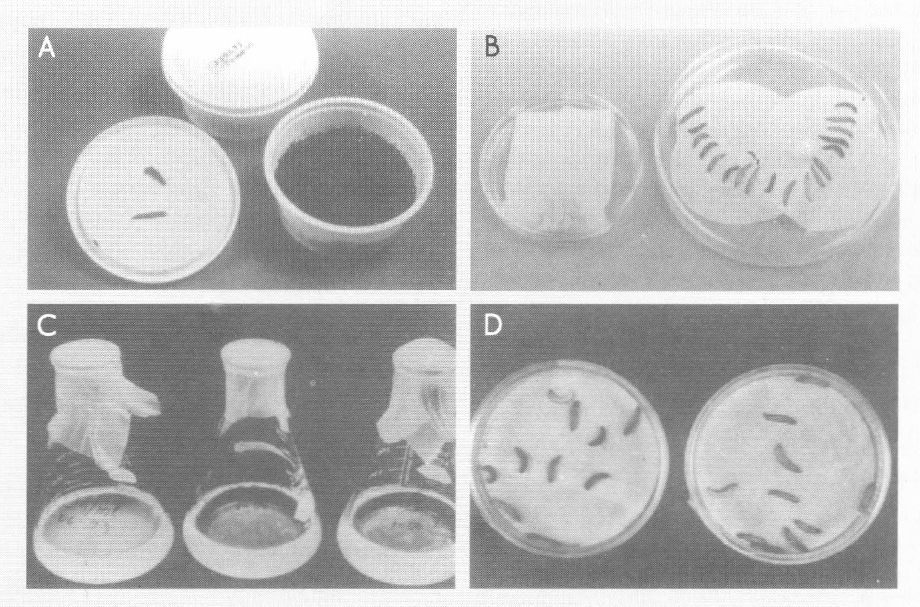
Recuperación y reproducción de nematodos entomopatógenos nativos. A. Submuestra de suelo con larvas de G. mellonella infectadas. B. Trampas de recuperación, papel kleenex (izq.) Trampa White (Der.). C. Larvas de G. mellonella infectadas con nematodos. D. Almacenamiento de nematodos en ADE al 0,1% de formaldehido. (Fotografía de Fernando Pino)
Los nematodos obtenidos de cada sitio muestreado se almacenaron en ADE con 0,1% de formalina a temperatura ambiente, y se reprodujeron en un medio artificial desarrollado por Bedding (1984) a base de menudencias de pollo.
Resultados y Discusión
De las ocho localidades se recolectaron 160 muestras de suelo (Tabla 1), las cuales fueron todas positivas para nematodos entompatógenos, y un 37,3% de los aislamientos correspondieron, según la identificación hecha por el taxónomo G.O. Poinar, Jr., a razas geográficas de la especie Heterorhabditis bacteriophora Poinar (Heterorhabditidae), nombrándolos como H. bacteriophora «SC92» (Santágueda, Caldas 1992) (Fig. 2) y H. bacteriophora «LFR92» (La Florida, Risaralda 1992), los nematodos aislados del suelo y de las chinches de Santander de Quilichao se identificaron por comparación como H. bacteriophora «SQC93» (Santander de Quilichao, Cauca 1993) (Fig. 3).
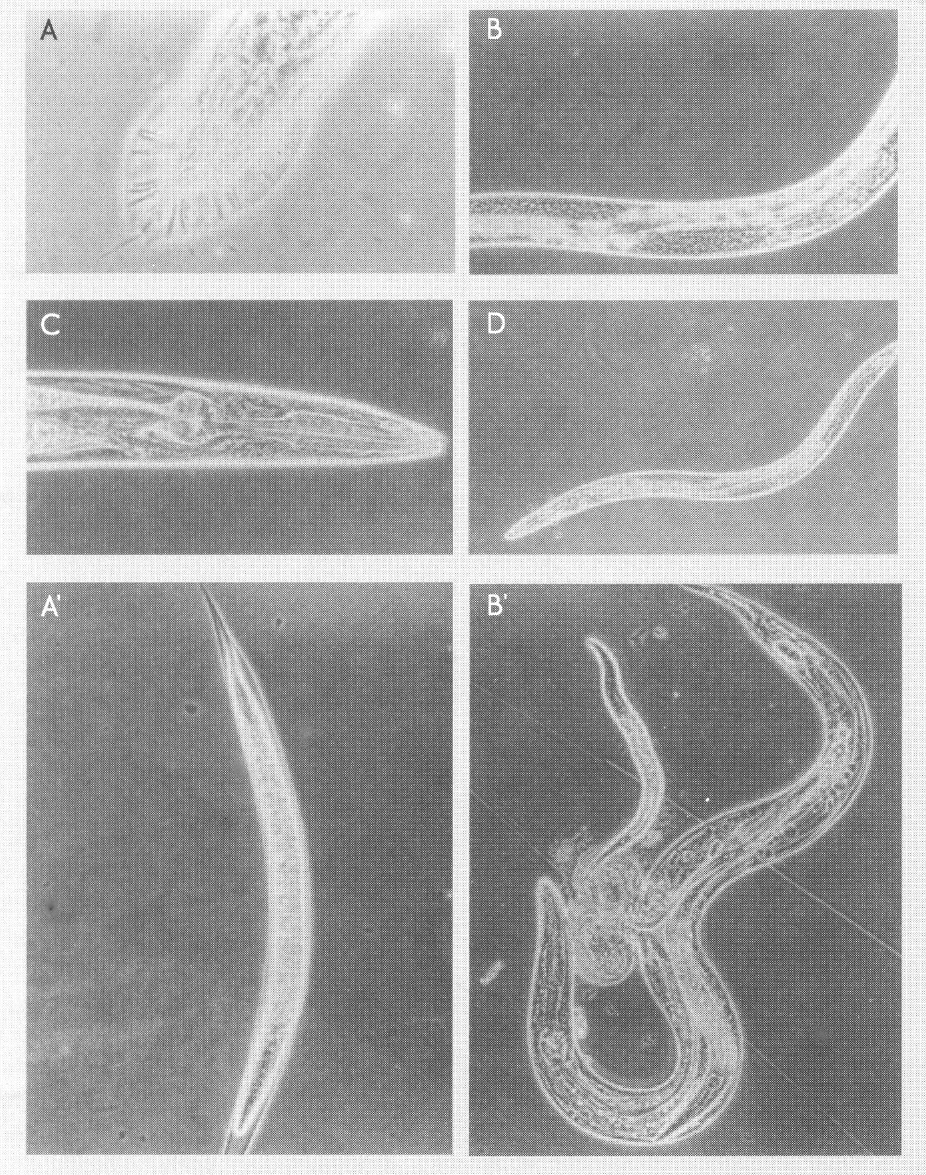
(Arriba). A. Macho completo de H. bacteriophora de Manizales (SC92) 10x. B. Esófago 40x. C. Aparato reproductor masculino 25x. D. Cola con ala caudal 40x; (Abajo).
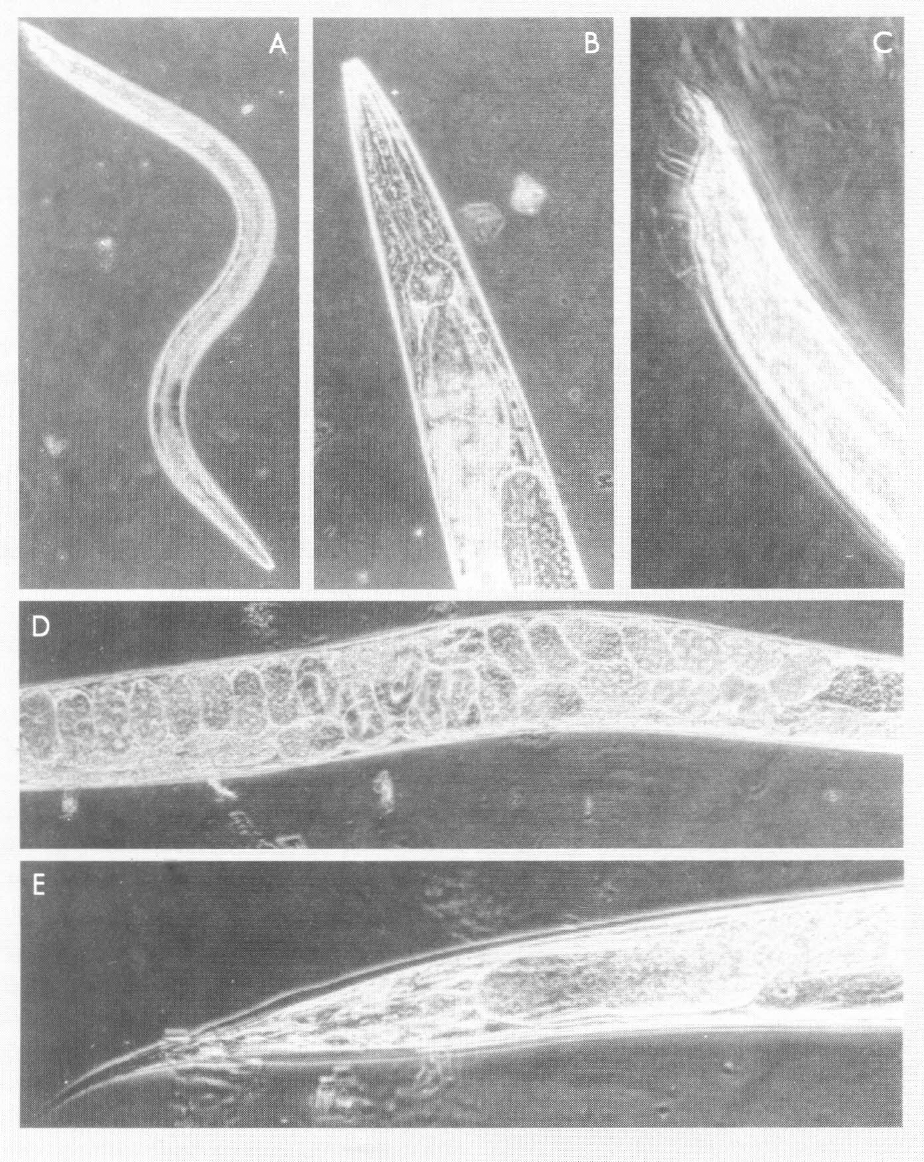
(Arriba). Adulto macho de H. bacteriophora Santander de Quilichao (SQC 92). (Arriba) A. Adulto completo 10x. B. Esófago 40x. C. Cola con ala caudal 40x. (Abajo) D. Hembra con huevos 40x. E. Cola de la hembra 40x. (Microfotografías tomadas por Guillermo Guzmán)
El estado taxonómico de los nematodos aislados de las localidades restantes, como Mariquita, Ciénaga de Oro, Araracuara, Buga y Mondomo, no está definido y por lo tanto se les asignó un nombre y número de accesión para posteriores referencias (Tabla 1).
Según las observaciones morfológicas realizadas, se encontró que tanto el esófago de los adultos como el de los estados juveniles es característico de los nematodos del orden Rhabditida y sólo en las muestras de Manizales, Pereira y Santander de Quilichao se observaron adultos machos que presentaban una estructura en la parte final de la cola, denominada ala caudal, que junto con las rayas músculosensoriales son de gran importancia taxonómica. El ala caudal observada es del tipo «peloderan», la cual rodea y llega hasta la punta terminal de la cola (Maggenti 1991).
Según la descripción de la especie H. bacteriophora hecha por Poinar (1990), se destacan como características de diagnostico la morfología de la cola del macho, la longitud y la posición de la base del esófago del tercer estado juvenil.
A continuación se hace una breve descripción morfológica de los nematodos aislados de Mariquita, Ciénaga de Oro y Araracuara (Fig. 4, 5 y 6). De los nematodos aislados de Buga y en Mondomo, en el momento no se tiene muestra en el laboratorio, ya que al ser almacenados a una temperatura de 13°C murieron.
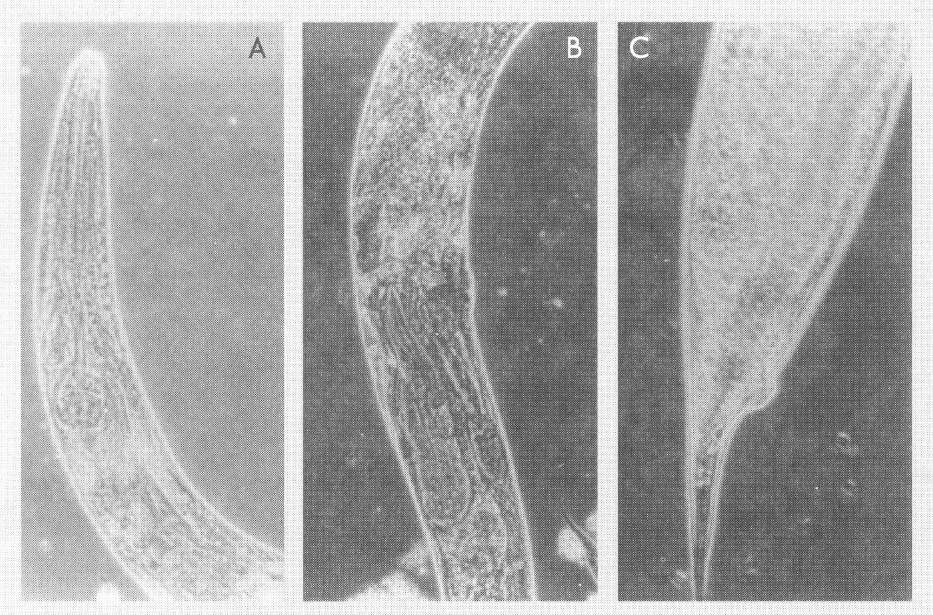
Adulto hembra de Tolima (TM92). A. Esófago 40x. B. Vulva con estados juveniles 40x. C. Cola y ano 40x. (Microfotografías tomadas por Guillermo Guzmán)
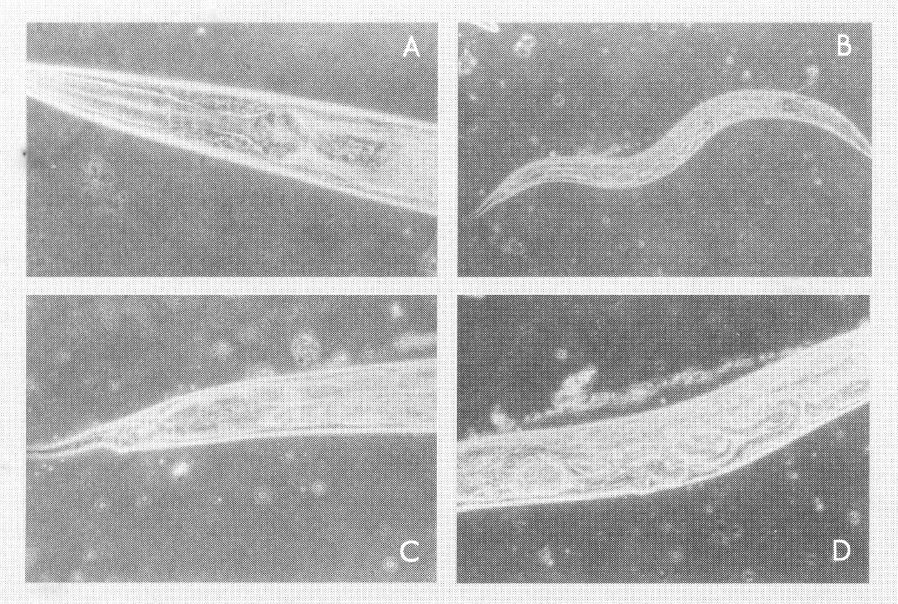
Adulto hembra de Ciénaga de Oro. A. Esófago 40x. B. Hembra completa 10x. C. Cola y ano 40x. D. Vulva y estados juveniles 40x. (Microfotografías tomadas por Guillermo Guzmán.)
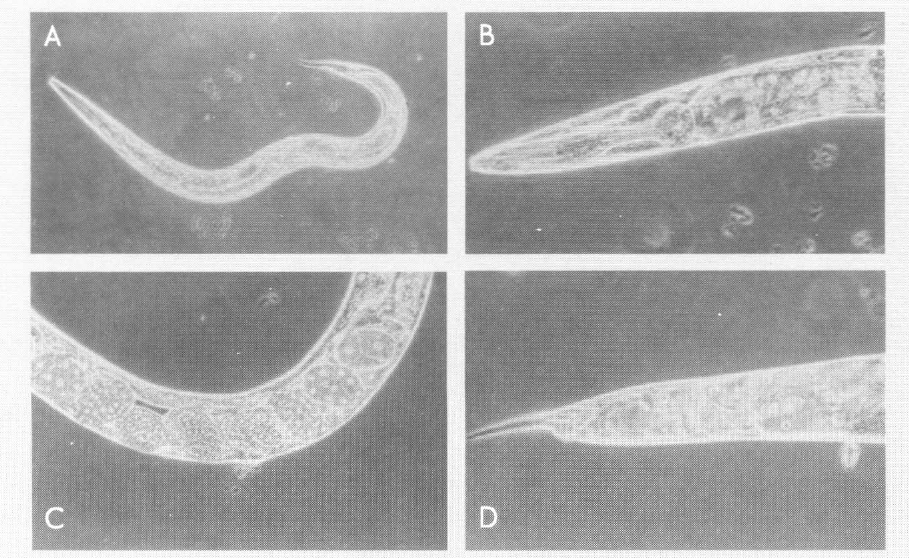
Hembra adulta de Araracuara (AM93). A. Hembra completa 10x. B. Esófago 40x. С. Vulva y huevos en formación 40x. D. Cola y ano 40x. (Microfotografías tomadas por Guillermo Guzman,)
La región esofageal en todos es muy similar, variando en el tamaño y en la ubicación del poro excretor. Así, en las hembras de Mariquita (TM92), el poro excretor se encuentra en la parte media del isthmus, en las hembras de Ciénaga de Oro «COM92» está en la parte final del isthmus, a la altura del bulbo basal, y en las de Araracuara, el poro excretor se encuentra después del bulbo basal. La vulva con labios prominentes se encuentra aproximadamente en el 50% del total, la cola es muy similar en todas las hembras, siendo corta y puntuda con ano prominente. Como característica general son vivíparas; los estados infectivos conservan la cutícula del estado anterior y no se observaron machos en las poblaciones de estas localidades.
Las muestras de suelo positivas para H. bacteriophora no presentaron un tipo de textura predominante, ya que el nematodo se aisló de diversos tipos de textura, tales como: Franco, Franco-Arcillo-Arenoso y Arcilloso. El contenido de materia orgánica fluctuó entre 5 y 12,2%, lo cual es considerado bajo, y el valor más alto se presentó en las muestras de Pereira, en cultivos de cebolla, donde la adición de materia orgánica es una práctica rutinaria para este cultivo.
El pH de las muestras fue ácido, entre 5 y 5,5, lo cual está dentro del rango de pH que no afecta la supervivencia y patogenicidad de los nematodos (Kung et al. 1990).
La precipitación en Pereira, Manizales y Santander de Quilichao se presenta en dos períodos durante el año, con promedios altos para Pereira (2.960 mm) y Manizales (2.301 mm) y el más bajo para Santander de Quilichao de (1.706 mm); la temperatura promedia anual no fluctúa mucho en los tres sitios, con valores entre 19,5 y 23°C, las cuales se encuentran dentro del rango que no afecta la actividad de estos nematodos (Kaya y Gaugler 1990).
El contenido de humedad fue bajo en todas las muestras de suelo tomadas, lo cual, según Molyneux (1984), citado por Kaya y Gaugler (1990), y Poinar (1990), el sitio de origen de las especies de nematodos determina fuertemente la capacidad de adaptación a condiciones de humedad y temperatura y se confirma lo mencionado por Kung, (1990) en cuanto a la capacidad de sobrevivir en suelos con bajo contenido de humedad.
En cuanto a la vegetación asociada con esta especie de nematodo entomopatógeno, se tienen cultivos comerciales hospedantes de C. bergi, tales como: sorgo, maní, cebolla y yuca, a los cuales se les realizan prácticas agronómicas comunes a cada cultivo, incluyendo aplicaciones de plaguicidas, por lo que la recuperación de nematodos nativos en estos hábitats es muy importante y refleja la adaptación de la especie a dichas condiciones.
Según Rueda et al. (1993); se han realizado muchos estudios de reconocimiento y distribución estacional de nematodos entomopatógenos en todo el mundo, incluyendo Australia, Checoslovaquia, Gran Bretaña, Hungría, Irlanda, Suecia, Puerto Rico, Florida, Carolina del Norte y Hawai, donde han sido recuperados de una gran variedad de hábitats, con características de suelo y textura diferentes.
Hara et al. (1991), en su estudio de reconocimiento de nematodos en Hawai, encontraron que predominan los aislamientos de los Heterorhabditidae sobre Steinernematidae, y resultados similares fueron obtenidos por Roman y Beavers (1982), citados por Hara et al. (1991), en Puerto Rico. Estas diferencias en distribución posiblemente reflejan la adaptación a una variedad de huéspedes favorables, vegetación, factores ambientales, tipos de suelo y a diversas prácticas culturales.
Además se confirma lo mencionado por Kaya et al. (1990) en cuanto a la distribución y adaptación de los Heterorhabditidae en el trópico y de los Steinernematidae a climas templados.
El hallazgo de estos nematodos asociados naturalmente con C. bergi en estas localidades del país es muy importante, ya que su ataque es alto en cultivos como maní, yuca y cebolla junca, aunque aparentemente esta especie de nematodo no está ejerciendo un control efectivo de la población, posiblemente por las condiciones de manejo de los cultivos, como es la aplicación indiscriminada de plaguicidas para el control de la chinche, generándose un desequilibrio en la macro y microfauna del suelo.
Se hace necesario realizar estudios básicos para determinar el potencial de las razas geográficas de H. bacteriophora y poderlas incluir dentro de un programa de manejo integrado de C. bergi.
Conclusiones
Se obtuvo un 100% de recuperación de nematodos entomopatógenos, los cuales pueden ser probados sobre un complejo de plagas de cada localidad donde fueron hallados para determinar si pueden ser incluidos en programas de control integrado de plagas.
De las ocho localidades, Manizales, Pereira y Santander de Quilichao, en donde el ataque de C. bergi es severo, se recuperaron razas de la especie H. bacteriophora Poinar asociadas naturalmente con la chinche, bajo condiciones diversas de clima y características físicas y químicas de suelo.
El hallazgo de razas nativas debe tenerse muy en cuenta en la implementación de programas de control integrado para este insecto, ya que pueden jugar un papel muy importante en la regulación de poblaciones, pues con la asociación natural se están dando dos factores importantes que debe cumplir una especie de nematodo para ser considerada como agente potencial de un insecto plaga en particular, que son la adaptación al huésped y la adaptación a las condiciones ambientales del mismo.
