Abstract
Experiments carried out to study the effect of the entomopathogenic fungi Beauveria bassiana (isolate Bb9205) and Metarhizium anisopliae (isolate Ma9101) on Cephalonomia stephanoderis, parasitoid of the coffee berry borer, Hypothenemus hampei, under laboratory conditions (R.H.=90%; T=23.4 ± 1°C) demostrated that both fungi (107 conidia/ ml) applied directly killed 48% and 40% of parasitoids respectively. In subsequent field trials, in the Experimental Station "La Catalina" (1,340 masl; T=21.9°C; R.H.= 80.9%), coffee branches, previously infested artificially in to entomological sleeves, were sprayed with the fungi (7.9 x 10º conidia/tree) according to the following treatments: 21, 14, 7 and 0 days before parasitoid release, and 2, 4, and 7 days after parasitoid release. The highest mortality (24% B. bassiana, 5% M. anisopliae) occurred when the fungi were sprayed on the same day that parasitoids were released. In all other treatments, the mortality was less than 7% and was not significantly different from the control. Results indicate than the fungi are compatible with the adult parasitoid and can be used in an IPM programme though fungal sprays should not be carried out shortly before or after parasitoid release.
Introducción
El mayor limitante fitosanitario de la caficultura colombiana es la broca del café, Hypothenemus hampei (Ferrari) (Coleoptera: Scolytidae), la cual no sólo reduce el rendimiento sino la calidad del grano (Le Pelley 1968; Cárdenas 1991). Para finales de 1994, según la Federación Nacional de Cafeteros de Colombia 1 , se estimaba en 50% el área cafetera infestada por este insecto. Desde su introducción a Colombia en 1988, las investigaciones se han dirigido a desarrollar un programa de manejo integrado, en el cual el control biológico juega un papel importante (Bustillo 1991).
El desarrollo de métodos para la producción masiva de los hongos Beauveria bassiana (Bals.) Vuill. y Metarhizium anisopliae (Metsch.) Sorokin (Hyphomycetos) (Antía et al. 1992; Bernal et al. 1992) y del parasitoide Cephalonomia stephanoderis Betrem (Hymenoptera: Bethylidae) (Orozco y Bustillo 1994) para el control de H. hampei, ha permitido que estos organismos se consideren dentro del manejo integrado de la broca del café. Esta estrategia requiere que antes de recomendar su empleo en campo se conozca la interacción entre estos agentes bióticos en caso de ser utilizados en forma conjunta. En la literatura no se encuentra ningún registro del efecto de los hongos entomopatógenos sobre el parasitoide y, en general, se acepta que los patógenos de los insectos plaga no afectan directamente a los parasitoides (Tanada 1977). Esta investigación tuvo como objetivo determinar el efecto de B. bassiana y M. anisopliae sobre C. stephanoderis, tanto en laboratorio como bajo condiciones de campo.
FEDERACAFE. Gerencia Técnica. 1994. Comunicación Personal. Santafé de Bogotá, D.C., Colombia.
Materiales y Métodos
Las pruebas preliminares y la prueba de patogenicidad se realizaron en el laboratorio de Entomología de Cenicafé en Chinchiná. El experimento de campo se desarrolló en la Subestación Experimental "La Catalina" de Cenicafé, en Pereira (1.340 msnm; T=21,9°C; H.R.=80,9%; 2.100 mm de precipitación).
A partir del modelo de bioensayo propuesto por González et al. (1993) se hicieron varios ensayos para ajustar la metodología a emplear en las pruebas de laboratorio. Los ajustes hechos permitieron mantener una humedad relativa mayor del 90%, necesaria para garantizar el normal desarrollo de los hongos.
Prueba preliminar
Para determinar el efecto de la alimentación y la tapa del recipiente sobre la longevidad del parasitoide, adultos de C. stephanoderis se colocaron individualmente en viales (frascos de antibiótico) estériles, tapados con algodón o con muselina, y se sometieron a tres regímenes alimenticios: 1.) Estados biológicos de broca (EBB); 2.) Solución agua:miel 1:1 y 3.) Ayuno, los cuales se suministraron diariamente. Los EBB se colocaron dentro del vial. En el caso del agua miel, ésta se distribuyó con un pincel sobre la pared del vial cuando la tapa era de algodón, o directamente sobre la tapa en el caso de la muselina.
Los viales se introdujeron en una caja de plástico de 17 x 7 cm, la cual se mantuvo a 24,3 ± 1,2°C y H.R. > 90%. Como el parasitoide era fácilmente atrapado por la humedad condensada en las paredes del vial que los contenía, este riesgo se disminuyó colocando dos tiras de papel toalla en el interior del recipiente para que el insecto caminara sobre ellas.
La duración de C. stephanoderis se obtuvo a partir del registro de mortalidad diaria, y los promedios se analizaron bajo un diseño de clasificación simple con arreglo factorial 3x2 (régimen alimenticio x tipo de tapa) tomando como unidad experimental 10 parasitoides y usando cuatro repeticiones. El tratamiento que mejores condiciones brindara a la avispita sería empleado en la prueba de patogenicidad en laboratorio.
Para los experimentos en el laboratorio y en el campo se emplearon los aislamientos Bb9205 de B. bassiana y Ma9101 de M. anisopliae, recomendados para el control de la broca del café. Los hongos se reactivaron en broca y se cultivaron en el medio Sabouraud-Dextrosa-Agar (SDA) acidificado para el experimento en el laboratorio; para el experimento en campo, los hongos se cultivaron en arroz, según las recomendaciones de Antía et al. (1992). La suspensión final de esporas se preparó siguiendo los procedimientos de la guía de laboratorio de Cenicafé (Vélez et al. 1994).
Efecto de los entomopatógenos sobre C. stephanoderis en el laboratorio
El efecto de B. bassiana y M. anisopliae se evaluó sobre adultos de C. stephanoderis recién emergidos, provenientes de la Unidad de Cría de Parasitoides de Cenicafé. Inicialmente, grupos de 70 especímenes se desinfectaron con una solución de hipoclorito de sodio al 0,3% durante cuatro minutos. Una vez retirado el exceso de humedad, los parasitoides desinfectados se expusieron a cada hongo en concentración de 1x106 y 1x107 esporas/ml empleando los métodos de aspersión directa y de superficie tratada. Para cada método de exposición se tomó un grupo testigo, el cual se trató con agua destilada estéril.
El método de aspersión directa consistió en depositar 2 ml de la suspensión de esporas sobre los parasitoides; por medio de la técnica de colorimetría para determinación de volumen (Florez et al. 1994), se estimó que al emplear las concentraciones 1x10⁶ y 1x10⁷ esporas/ml, se depositaban, en promedio, 16 y 155 esporas por parasitoide, respectivamente. Para el método de superficie tratada se asperjaron 2 ml de la suspensión de esporas sobre una caja petri vacía, en la que se introdujeron los parasitoides una vez evaporado el exceso de agua, según lo recomendado por Folegatti et al. (1990). Las aspersiones se hicieron empleando una Torre de Potter.
De cada grupo tratado se seleccionaron los 40 adultos de C. stephanoderis más activos y se colocaron individualmente en viales estériles con tiras de papel toalla y tapados con muselina. Los viales se colocaron en una caja plástica cubierta con una toalla de papel humedecida y una tapa hermética, y se mantuvieron a 23,4 ± 1°C y una H.R.>90% para garantizar la manifestación de los hongos sobre los insectos (Fig. 1). Los parasitoides se alimentaron con agua miel distribuida sobre la tapa. La mortalidad del parasitoide causada por los hongos se registró diariamente, y los datos se analizaron bajo un diseño de clasificación simple con arreglo factorial 2x2x2+2 (hongos x concentraciones x métodos de exposición + testigo) por cada método de exposición. La unidad experimental constó de 10 parasitoides y se emplearon cuatro repeticiones. Los síntomas y signos de las enfermedades sobre el parasitoide se registraron diariamente.
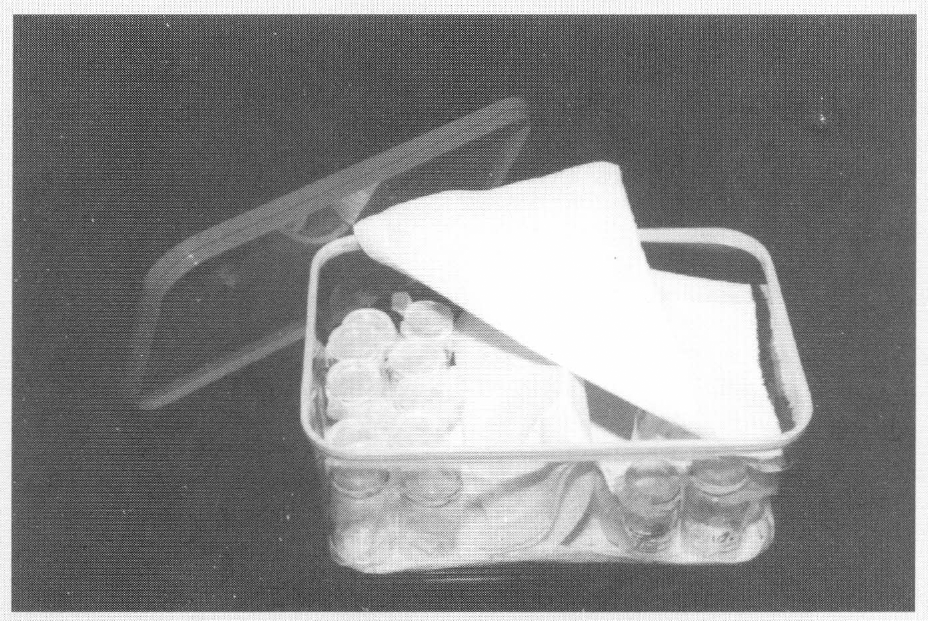
Viales dentro de la caja plástica para mantener la humedad relativa alta. Detalle de dos unidades experimentales del estudio en laboratorio (Foto: Gonzalo Hoyos)
Efecto de los entomopatógenos sobre C. stephanoderis bajo condiciones de campo
La evaluación del efecto de B. bassiana y M. anisopliae sobre el parasitoide bajo condiciones de campo se llevó a cabo en dos etapas: en la primera, los hongos se asperjaron 21, 14 y 7 días antes y el mismo día de la liberación del parasitoide; en la segunda etapa, los hongos se asperjaron 2, 4 y 7 días después de la liberación del parasitoide.
Las parcelas experimentales, compuestas por nueve árboles dispuestos en cuadro, se ubicaron en un lote de café var. Colombia; del árbol central de cada parcela se seleccionó como unidad experimental una rama productiva, la cual se confinó dentro de una manga entomológica y se infestó colocando frutos sobremaduros con adultos de broca (Fig. 2). Los frutos se retiraron al cabo de tres días para obtener una población homogénea.
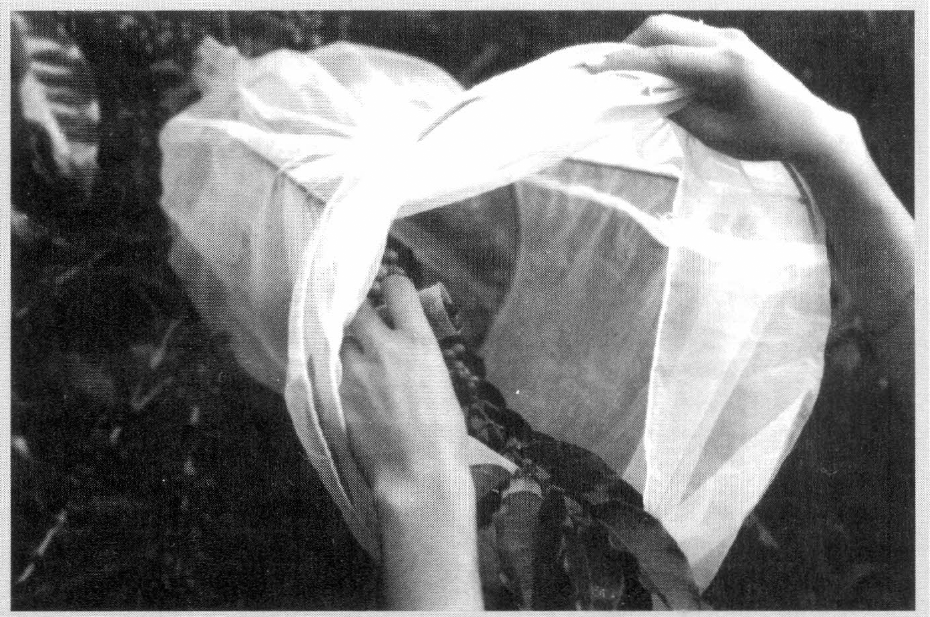
Infestación artificial con frutos de café sobremaduros con adultos de broca. Detalle de la unidad experimental del estudio desarrollado en campo. (Foto: Gilberto Sánchez).
Los hongos B. bassiana y M. anisopliae, producidos en forma artesanal (Antía et al. 1992), se asperjaron sobre la rama seleccionada, usando una dosis de 7,9 x 10⁹ esporas/árbol. La aspersión se hizo con equipos de presión previa retenida, marca "Calimax Experimental" para B. bassiana y marca "Triunfo" para M. anisopliae, calibrados para obtener un flujo de 190cc/min a 40 p.s.i. Los parasitoides se liberaron en el interior de la unidad experimental (Fig. 2) en proporción de uno por cada fruto infestado, y en este momento los frutos tenían en promedio 20 estados inmaduros de broca (32 días después de la infestación).
Ocho días después de las liberaciones, los parasitoides recuperados mediante disección de 30 o más frutos/rama y del interior de las mangas entomológicas se colocaron en cámaras húmedas para que después de su muerte el agente causal se expresara. La confirmación de éste se hizo mediante observación microscópica de las estructuras del hongo y sembrando el insecto en medios de cultivo artificiales (SDA, Agar-agua). Los promedios de mortalidad de C. stephanoderis causada por los hongos se analizaron bajo un diseño de clasificación simple con arreglo factorial 2x4+1 para la primera etapa del experimento y 2x3+1 para la segunda (hongos x intervalos de tiempo + testigo), usando siete repeticiones por tratamiento.
Resultados y Discusión
Los estudios previos sobre longevidad mostraron que la duración de C. stephanoderis bajo las condiciones del experimento, con una humedad relativa mayor de 90%, no superó los 32 días. Esta duración es inferior a la registrada por Barrera et al. (1993), probablemente porque la longevidad del parasitoide en el experimento pudo estar condicionada por factores como la edad, el sexo y la alimentación previa. Además, la alta humedad relativa afectó negativamente a los especímenes, que continuamente quedaban atrapados por el rocío condensado en las paredes del vial.
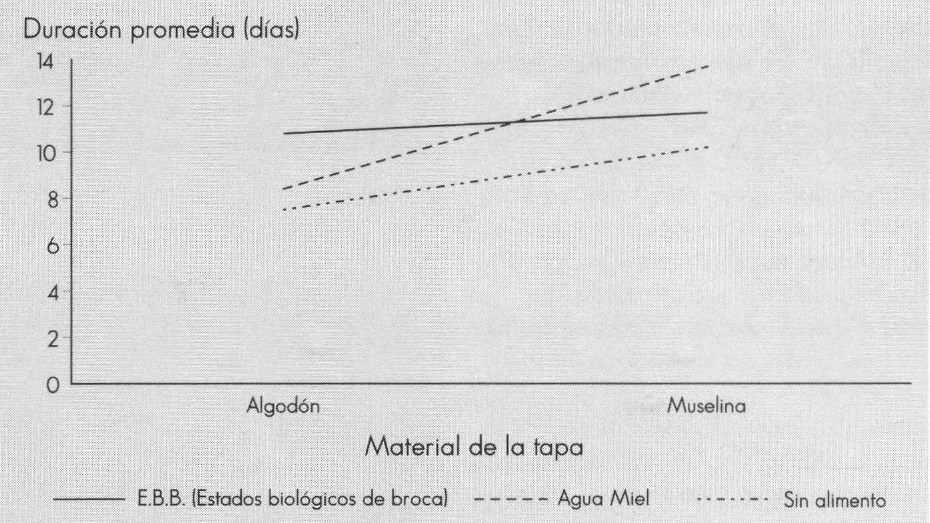
Efecto de tres regímenes alimenticios y dos tipos de tapa sobre la longevidad de adultos de C. stephanoderis en laboratorio (H.R.- 90%; T=24,3±1°C).
Prueba preliminar
La influencia del régimen alimenticio sobre la longevidad del parasitoide fue dependiente del tipo de tapa empleado (Fig. 3). Al tapar el vial con algodón, la longevidad se redujo bien porque los insectos se enredaron entre las fibras de la tapa o porque se pegaron al agua miel localizada en la pared del vial. La tapa de muselina facilitó la ventilación y la colocación del alimento sobre ésta no causó mortalidad a los parasitoides.
Cuando los parasitoides no se alimentaron, la duración promedia fue la más baja: 7,62 ± 2,1 días (tapa de algodón) y 10,17 ± 2,1 días (tapa de muselina). Al alimentarlos con EBB, la longevidad promedio (10,65 ± 3,6 días para tapa algodón y 11,67 ± 4,1 días para tapa muselina) fue aceptable y menos variable; sin embargo, se descartó para la siguiente prueba debido a que alimentar diariamente 400 avispas (individuos para la prueba de patogenicidad) con huevos, larvas y pupas de broca, como lo sugiere Koch (1973), es muy dispendioso y propicia la contaminación. La longevidad de los parasitoides aumentó al ser alimentados con agua miel, corroborando lo registrado por Abraham et al. (1990), acerca de que los carbohidratos influyen en los procesos de longevidad de C. stephanoderis. Para la prueba de patogenicidad se seleccionó el agua miel como alimento y la tapa en muselina, ya que fue el tratamiento con el que se obtuvo mayor longevidad de los parasitoides (13,67 ± 6,4 días).
Efecto de los entomopatógenos sobre C. stephanoderis en el laboratorio
Los hongos B. bassiana y M. anisopliae demostraron ser patogénicos a C. stephanoderis (Tabla 1). Los síntomas de las enfermedades no se diferenciaron entre sí; en general, el parasitoide se tornó lento, redujo el movimiento de sus antenas y, ocasionalmente, presentó temblores. Después de la muerte del insecto se presentaron los signos de los hongos, marcando cinco etapas en el desarrollo de las micosis (Tabla 2). El micelio de los hongos emergió a través de las membranas intersegmentales (Fig. 4a), continuando su desarrollo hasta cubrir el cuerpo del insecto (Fig. 4b). La esporulación tardó de 9 a 11 días desde la inoculación de los hongos y se caracterizó por la presencia de formas redondeadas blancas de B. bassiana (Fig. 5a) y paquetes de esporas color verde oliva sobre el micelio blanco en el caso de M. anisopliae (Fig. 5b), típicas de ambos patógenos (Barnett y Hunter 1972; Gillespie 1988).
Porcentaje promedio de mortalidad de adultos de C. stephanoderis ocasionada por B. bassiana cepa Bb9205 y M. anisopliae cepa Ma9101 en condiciones de laboratorio (23,4±1°C; HR-90%) Cenicafé, Chinchiná.
Mortalidad no atribuible a los hongos evaluados
Agua destilada estéril
Los datos seguidos de la misma letra no son significativamente diferentes (P=0,05) según la prueba de Tukey.
Duración promedio de las etapas de desarrollo de B. bassiana ceра В69205 у М. anisopliae cepa Ma9101 sobre C. stephanoderis bajo condiciones de laboratorio (H.R. 90%; 23,4°C). Cenicafé, Chinchiná.
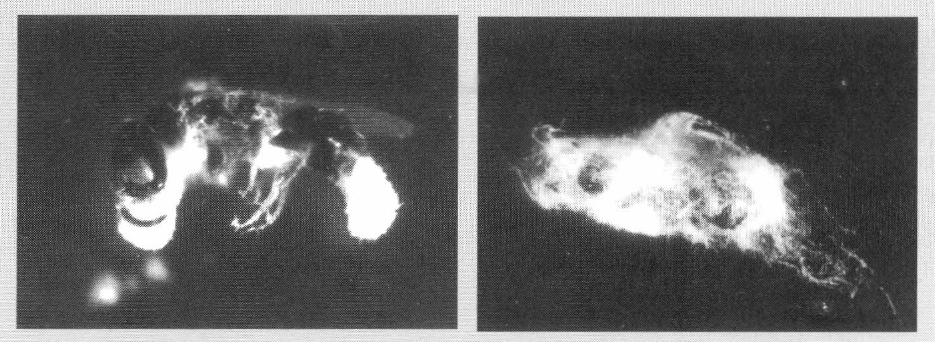
a) Detalle de la emisión de micelio sobre C. stephanoderis. b) Cubrimiento parcial o total del cuerpo del insecto por parte del micelio de los hongos. (Foto: Gonzalo Hoyos).
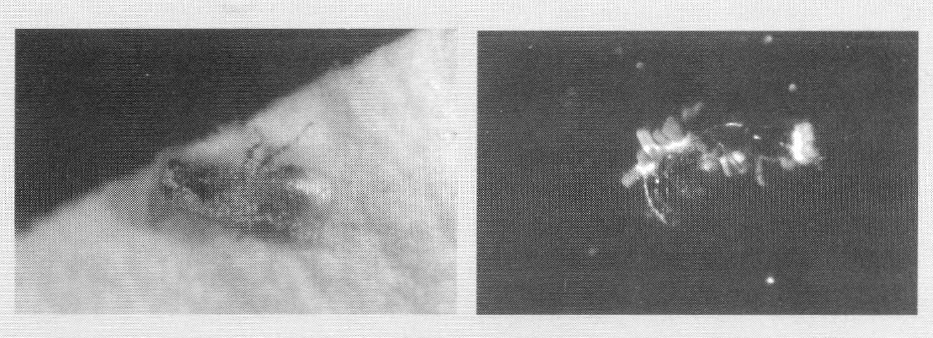
Esporulación sobre C. stephanoderis de a.) B. bassiana con grupos de esporas blancas y b.) M. anisopliae con paquetes de esporas verdes. (Foto: Gonzalo Hoyos).
Con relación al tiempo de mortalidad (Tabla 2), se observó que las avispas tratadas con la concentración alta (1x10⁷ esporas/ml) tardaron menos tiempo en morir que las tratadas con 1x10⁶ esporas/ml. El método de exposición no influyó en el tiempo que tomaron los hongos para producir la muerte del insecto.
Tiempo promedio de mortalidad de C. stephanoderis, ocasionado por B. bassiana y M. anisopliae bajo condiciones de laboratorio (H.R. 90%; 23,4°C). Cenicafé, Chinchina.
n: Número de especímenes muertos por el hongo de un total de 40 individuos evaluados.
A.D.': Aspersión directa; S.T. Superficie tratada
El análisis de varianza de los porcentajes de mortalidad del parasitoide (Tabla 3) indicó que pueden ocurrir diferentes respuestas del insecto al patógeno, en función de los métodos de exposición (P=0,0001) y las concentraciones empleadas (P=0,0029); así mismo, el grado de patogenicidad estuvo determinado por el hongo inoculado (P=0,0001) independientemente de los demás factores. En los tratamientos donde se empleó B. bassiana Bb9205 se presentaron porcentajes de mortalidad más altos que en aquellos tratamientos donde se empleó M. anisopliae Ma9101. La aspersión directa de los hongos sobre las avispitas ocasionó mayor mortalidad que cuando éstas se hicieron caminar sobre una superficie tratada; así mismo, aquéllas que se inocularon con 1x10⁷ esporas/ml presentaron mayores niveles de mortalidad que las tratadas con 1x10⁶ esporas/ml. La mortalidad que se presentó en el testigo fue propiciada por la alta humedad relativa; ningún cadáver en el testigo presentó signos de los hongos.
Efecto de la aspersión de los entomopatógenos sobre C. stephanoderis bajo condiciones de campo
La mortalidad de C. stephanoderis a causa de los hongos asperjados en ambas etapas del experimento fue baja (Tabla 4). Cuando los hongos se aplicaron a los 21, 14 y 7 días antes de la liberación y el mismo día de la liberación de los parasitoides, el análisis de varianza mostró que la mortalidad estuvo determinada por el hongo empleado (P=0,0001) y por el momento de aplicación (P = 0,0002), independientes el uno del otro. En los tratamientos donde se asperjó B. bassiana se presentó mayor mortalidad que en los tratamientos donde se asperjó M. anisopliae. El tratamiento donde el hongo B. bassiana se asperjó el mismo día de la liberación de los parasitoides fue el único estadísticamente diferente de los demás tratamientos (P=0,05), causando 24% de mortalidad.
Mortalidad promedia de C. stephanoderis ocasionada por B. bassiana y M. anisopliae (7,9 x 10º esporas/árbol) asperjados antes y después de la liberación del parasitoide en el campo. Subestación Experimental «La Catalina», Pereira, Risaralda. 1993.
Los datos seguidos de la misma letra no son significativamente diferentes (P=0,05) de acuerdo con la prueba de Tukey.
Parasitoides recuperados de las mangas entomológicas y del interior de los frutos.
En la segunda etapa del experimento, cuando los hongos se asperjaron después de liberar el parasitoide, se presentó menor mortalidad que en la etapa anterior, donde los hongos se asperjaron antes de la liberación. No se presentaron diferencias significativas entre los tratamientos (P=0,05). Lo anterior indica que es más conveniente aplicar los hongos después de liberar los parasitoides. La mortalidad presentó una tendencia similar a la de la etapa anterior, donde B. bassiana fue más patogénico que M. anisopliae.
En general, la mortalidad de C. stephanoderis a causa de los hongos fue menor bajo condiciones de campo que en el laboratorio, a pesar de haber empleado una concentración 79 veces más alta que la recomendada para el control de la broca (1x10⁸ esporas/árbol), permitiendo deducir que los insecticidas microbianos evaluados no interfieren sustancialmente con la acción del parasitoide liberado.
En ambas etapas del experimento se presentó la tendencia a disminuir la mortalidad a medida que el intervalo de tiempo entre la aspersión de los hongos y la liberación del parasitoide aumenta (Tabla 4). Esto se debe probablemente a que en este intervalo de tiempo los factores abióticos como la luz solar, la temperatura, el agua o la humedad relativa influyen sobre la supervivencia de los hongos, disminuyendo la vida media de las esporas o su virulencia a través del tiempo, como lo indica Ferron (1981).
Conclusiones
Los hongos B. bassiana y M. anisopliae fueron patogénicos para adultos de C. stephanoderis. Bajo condiciones de campo, la mortalidad del parasitoide a causa de los hongos fue baja.
Los entomopatógenos B. bassiana y M. anisopliae y la avispa de Costa de Marfil, C. stephanoderis, pueden ser empleados en un programa de manejo integrado de la broca del café, cuando el intervalo de tiempo entre la aplicación de los hongos y la liberación del parasitoide sea mayor de 15 días para disminuir los riesgos de infección en el parasitoide.
La mortalidad de los parasitoides se reduce si éstos se liberan antes de asperjar los hongos.
