Abstract
The viability of B. bassiana evaluated through time (3, 8, 41, 95, 148, 218 days) in artificially contaminated soil with 1 ml (108 con/ml), previously sterilized (SS) or not sterilized (NSS) was investigated under laboratory conditions. The soil was stored in petri dishes at 25 ± 2°C. In order to evaluate the effect of soil type on the fungus, the Colony Forming Units (CFU) was recovered on SDA and on a selective medium (SM) using the soil dilution plate method. The mean number of viable conidia was calculated and then converted to CFU per g of dried soil. On the SM the fungus was recovered at 148 d (9.5 ± 4.0 x 103 cfu/g) and at 218 d (1.7 ± 1.8 x 103 cfu/g) in NSS. In SS at 148 d, 9.8 ± 2.1 x 103 cfu/g and at 218 d, 9.0 ±6.0 x 102 cfu/g of B. bassiana were recovered. The fungus was not recovered on SDA. During the assay the mean number of viable conidia declined through time. However, an unexpected temporary increase in the number of CFU was observed at 41 d (1.67 x 105 cfu/g in SS on SDA and 8.9 x 105 cfu/g in SS on SM) and at 8 d (7.0 x 104 cfu/g in NSS on SDA and 3.0 x 104 cfu/g in NSS on SM). The reasons for this increase are yet unknown.
Introducción
La broca del café, Hypothenemus hampei Ferrari (Coleoptera: Scolytidae), es la plaga de mayor importancia económica en el cultivo del café y su ciclo de vida toma aproximadamente 45 días. Durante este período, la cereza del café puede caer al suelo y permanece allí como fuente de reinfestación después de la cosecha. Cerezas caídas con 30 o más hembras adultas son comunes y, frecuentemente, están casi completamente huecas (Baker et al. 1992).
Como una estrategia dentro del manejo integrado de la broca del café en Colombia, se ha implementando el uso del hongo Beauveria bassiana (Bals.) Vuill. (Hyphomycetos). Este entomopatógeno causa infecciones naturales en muchas especies de insectos, entre las cuales está H. hampei (Bustillo 1991). El empleo de este hongo, como agente benéfico, depende de su habilidad para sobrevivir y mantener su capacidad infectiva contra el insecto plaga por un tiempo relativamente largo y bajo un amplio rango de condiciones físicas y biológicas, como competencia y fungistasis, que son relativamente comunes (Lockwood 1964; Walstad et al. 1970; Lockwood 1977; Groden y Lockwood 1993).
Algunas investigaciones han mostrado que los propágulos de los hongos son afectados por factores biológicos, principalmente en el suelo, por la actividad de microorganismos antagonistas como bacterias (Kenneth y Wilcoxon 1962; Kenneth 1963; Old y Robertson 1970; Jackson y Gay 1976; Fargues y Roberts 1985), actinomycetos (García-Mendoza y Villanueva 1962; Lockwood y Lingappa 1963; Ballesta y Alexander 1972), hongos (Lockwood 1964; Jones y Webley 1967; Jones y Watson 1969) y protozoarios (Old 1977) y factores abióticos como pH, temperatura, humedad, disponibilidad de materia orgánica e inhibidores volátiles, entre los cuales están amonio, metilamina y etilamina (Schippers y Palm 1973; Ko y Chow 1978), monómeros de lignina (Lockwood y Lingappa 1963); incluso, algunos autores señalan un mecanismo de autolisis (Ko y Lockwood 1970; Smith y Grula 1981).
En contraste, otros autores registran que B. bassiana puede permanecer en el suelo por mucho más tiempo (Lingg y Donaldson 1981) debido a su facultad de desarrollar nuevos propágulos en el curso de microciclos de formación de conidias (Fargues y Roberts 1985; Müler-Kögler y Zimmermann 1986).
Doberski y Tribe (1980), a partir de muestras de suelo, aislaron un gran e inesperado número de esporas de B. bassiana, señalando que la conidia está sujeta a fungistasis y que el mayor inóculo está restringido a cadáveres de insectos hospedantes, donde la esporulación puede ser profusa.
Lingg y Donaldson (1981) señalan que la humedad relativa probablemente no es el mayor factor que influya en la supervivencia de las conidias de B. bassiana introducidas para el control de insectos propios del suelo. Excepto en condiciones de extrema sequía, la humedad relativa de la atmósfera del suelo llega a ser hasta aproximadamente del 95-99%. Estos autores, quienes utilizaron un medio selectivo, registraron la inhibición de B. bassiana por Penicillium urticae.
La metodología de inoculación y recuperación del hongo utilizada en el presente experimento ya había sido implementada por diferentes autores en trabajos de laboratorio e invernadero (Storey y Gardner 1987, 1988; Krueger et al. 1992, Villani et al. 1994). El objetivo de este estudio fue determinar la viabilidad y persistencia del hongo en suelo bajo condiciones controladas.
Materiales y Métodos
Para el experimento se utilizaron conidias de B. bassiana Bb9002, aislado de H. hampei, producido en arroz cocido y con una viabilidad superior al 95% a las 48 horas después de la inoculación en Sabouraud-Dextrosa-Agar acidificado con ácido láctico al 0,37% (SDA); este hongo provino de la micoteca del laboratorio de Entomología de Cenicafé. Las conidias se suspendieron en una solución de agua destilada estéril agregando Tween 80 al 0,1% (ADET), obteniéndose una concentración de 1 x 108 conidias/ml.
Las muestras de suelo, Unidad Chinchiná, se tamizaron (Fisher Scientific Company, U.S.A. Standard Testing Sieve) para obtener un tamaño de partícula uniforme con un diámetro de 1 - 1,4 mm (Lingg y Donaldson 1981); éstas se repartieron en 24 cajas de petri, cada una con 10 g. Doce cajas con suelo se esterilizaron a 15 lb de presión, 120°С у 60 min., para obtener suelo estéril, las otras se dejaron sin esterilizar; finalmente, las 24 muestras se inocularon con la suspensión de conidias y se colocaron en agitación en un agitador Orbit Shaker, de Lab Line Instruments Inc., durante 1 hora a 250 rpm, para permitir una mejor distribución del suelo y las conidias, y luego se almacenaron a 23 ± 2°C durante 218 días, con un fotoperíodo de 12 horas.
Para la recuperación del hongo, a partir de las muestras, se prepararon el medio SDA y el medio selectivo descrito por: Rivera y López (1992).
A partir de los 3, 8, 41, 95, 148 y 218 días se hizo un muestreo destructivo para aislar el hongo, haciendo también un seguimiento de los contaminantes. Por cada tiempo evaluado se tomaron dos cajas, poniendo 20 g en matraces con ADET en una proporción 1:9 (asumiendo que las diluciones son hechas en potencia de 10), se agitó durante dos horas a 80 rpm; del sobrenadante se tomó 0,1 ml y se inoculó sobre la superficie en los medios, y la mezcla se distribuyó con un rastrillo bacteriológico.
Las cajas con medios nutritivos se sellaron con parafilm «M» (American National Can, USA) para minimizar la desecación durante el período de incubación (15 días) a una temperatura de 25 ± 2°C, hasta la aparición de las colonias del hongo perfectamente diferenciables; luego se determinó el número de Unidades Formadoras de Colonia (UFC)/g de B. bassiana en suelo seco.
Se utilizó un diseño completamente al azar con arreglo factorial 2 x 2. Los niveles de los factores fueron: suelo estéril y suelo no estéril, el medio de cultivo SDA y el medio selectivo, teniendo como unidad experimental la caja de petri con cada uno de los medios; para cada suelo y para cada tiempo se utilizaron 10 cajas de petri. La variable medida fue el promedio de UFC del hongo B. bassiana procedentes de los diferentes suelos.
Resultados y Discusión
Los promedios encontrados para cada tiempo evaluado están expresados en 103 UFC/g de suelo. Para los suelos se aprecia una disminución gradual de la viabilidad del hongo en el transcurso del tiempo, excepto a los 41 días en suelo estéril y a los 8 días en suelo no estéril (Fig. 1).
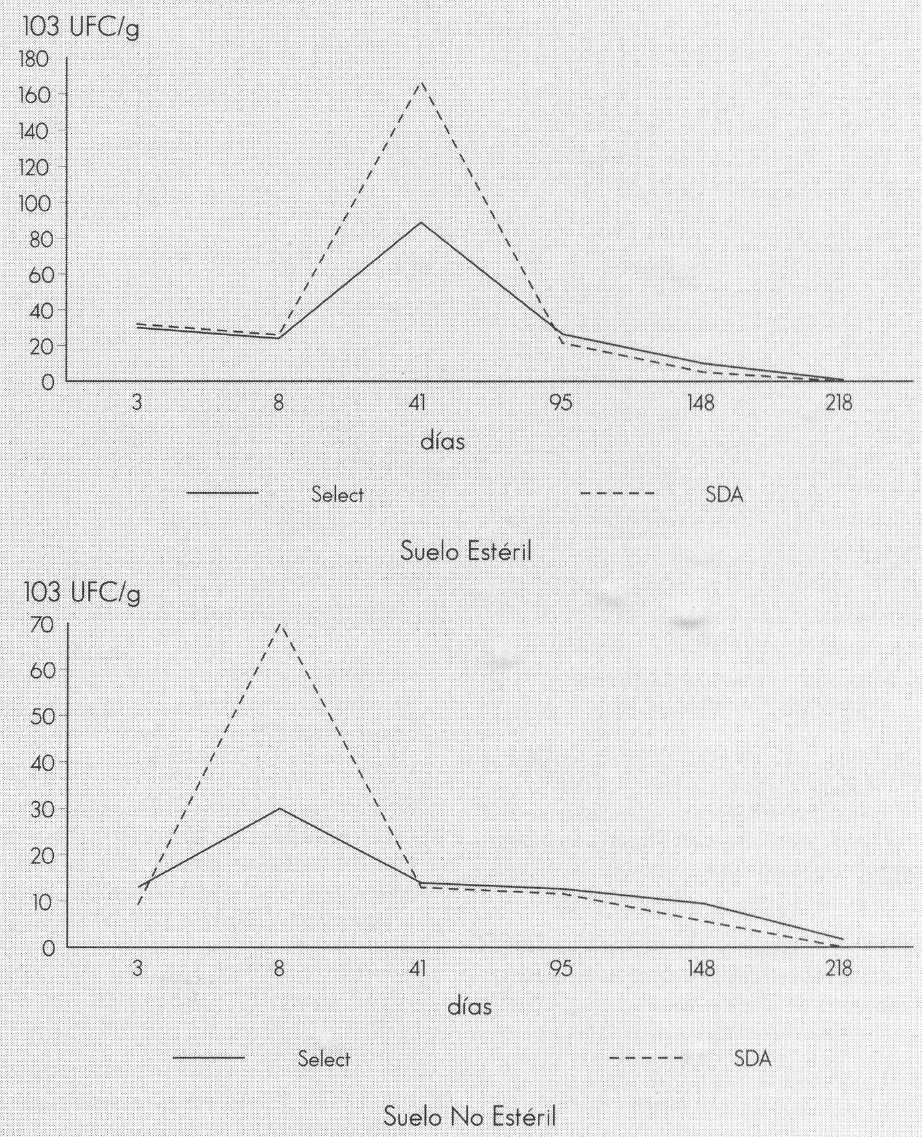
Recuperación de B. bassiana en el tiempo en diferentes medios de cultivo.
Según el comportamiento de la recuperación de UFC en el tiempo (Fig. 1), en ambos medios se observa un aumento temporal inesperado en la recuperación de B. bassiana en suelo estéril a los 41 días; esto explica la interacción (P ≤ 0,01) que se presenta entre los tratamientos y el tiempo, lo cual guarda relación con lo hallado por Müller-Kögler y Zimmermann (1986), quienes explican dicho fenómeno aduciendo la facultad de reproducción a partir de restos de insectos, y Fargues y Roberts (1985), quienes sugieren la presencia de microciclos para producir nuevos propágulos; aunque dichos propágulos parecen disminuir en la siguiente evaluación (95 y 41 días para suelo estéril y no estéril, respectivamente).
La presencia de los microciclos está soportada por el argumento planteado por Sharapov y Kalvish (1984), en el cual señalan que durante la evolución de los hongos entomófagos hacia el parasitismo, el hongo pierde las propiedades necesarias para su crecimiento saprofítico en suelo. Aunque sus esporas son capaces de germinar en suelo, su posterior desarrollo, incluyendo formación de micelio y esporulación, no ha sido observado. En este estado de crecimiento saprofítico se ha observado lisis activa de su micelio por microorganismos que habitan el suelo, y, por tanto, se hace necesario evaluar la existencia y la patogenicidad de estos propágulos.
Al final de la evaluación a los 218 días, en los suelos en SDA no hubo recuperación de B. bassiana y se encontró un aumento de la flora contaminante (Tabla 1). Sin embargo, en el medio selectivo se logró mayor recuperación y una fácil identificación de las colonias de B. bassiana, ya que fue menor la contaminación. Las UFC fueron: para suelo no estéril, 9,5 ± 4 x 103 UFC/g y 1,7 ± 1,8 x 103 UFC/g a los 148 y 218 días, respectivamente, y para suelo estéril, 9,8 ± 2,1 x 103 UFC/g y 9,0 ± 6,0 x 102 UFC/g a los 148 y 218 días, respectivamente.
UFC/g x 10³ de contaminantes* recuperadas a partir de muestras de suelo con diferentes medios.
Aspergillus spp., Geotrichum spp., Penicillium spp., Trichoderma spp., Cladosporium spp., Fusarium spp., Trichothecium spp.
La viabilidad del hongo va disminuyendo en el transcurso del tiempo; esto puede ser atribuido, principalmente, a efectos inhibitorios causados por factores bióticos y, en segundo plano, por factores abióticos. Los inhibidores utilizados en el medio selectivo hacen que se disminuya su desarrollo, alterando también su viabilidad.
El análisis de varianza de los datos transformados a
La respuesta a los medios, aunque no hubo diferencia entre ellos en la recuperación de B. bassiana, expresada en UFC, fue mayor en suelo estéril que en suelo no estéril (Fig. 2); estos aumentos son diferentes en el tiempo, lo cual explica la interacción (P ≤ 0,01) entre suelo y medio.
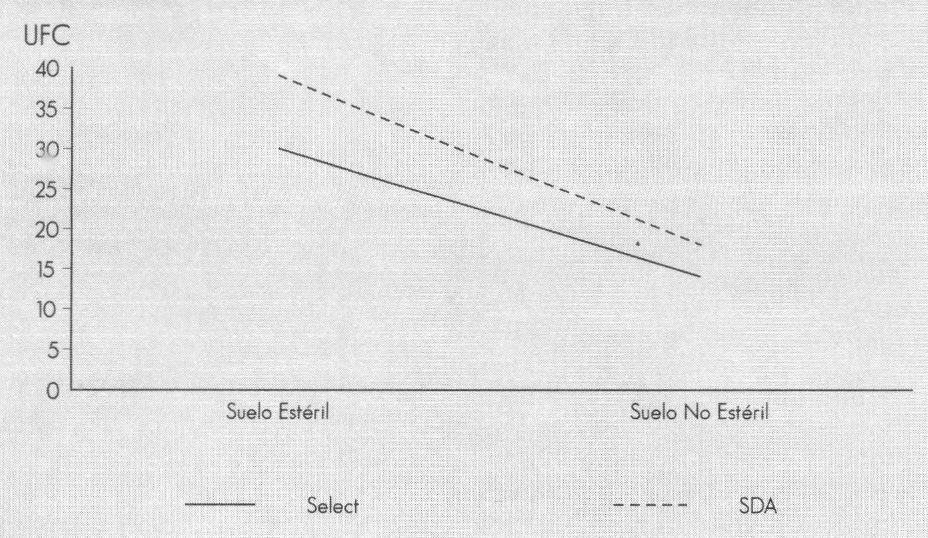
Promedio en UFC (103) de B. bassiana en los diferentes suelos, recuperadas con cada medio.
La diferencia entre los días de aparición de este mecanismo se podría asociar con la presión ejercida por la flora acompañante, aunque, como lo señala Sharapov y Kalvish (1984), este comportamiento es inherente al hongo e inclusive puede existir una potencialidad en el aumento del inóculo en el suelo por este tipo de fenómenos, el cual induciría micosis en subsecuentes emergencias de broca a nivel de suelo, siempre y cuando las condiciones ambientales sean favorables.
