Abstract
Trialeurodes vaporariorum Westwood (Homoptera: Aleyrodidae), the greenhouse whitefly, is considered one of the most important crop pests in the world. At this time in Colombia this pest has been reported in the following departments: Antioquia, Cundinamarca, Valle del Cauca, Tolima and Nariño. In other countries the enthomopathogenic fungus Aschersonia aleyrodis Webber and the parasitoid Encarsia formosa Gahan, natural enemies of this insect pest, have been used with success to control T. vaporariorum. This work shows the results of the infection produce by a native strain of A. aleyrodis, from La Vega (Cund.) that in a previous research showed to be the most effective to control adults of this insect, and from a Netherlands strain; different solutions of spore concentrations and pathogen mycelium were tested on third and fourth instar nymphs. This work also shows the interactions between these isolations and E. formosa. In greenhouse assays on beans plants in pots; with a randomized design, it was tested the interaction between E. formosa, present in the greenhouse due to a previous release, and the following treatments with the pathogen: the low dosages of 2,5 x 104 1 x 104, 1 x 103 spores/ml, mycelium and a check and the treatments with the high dosages of 1,3 x 107, 1 x 106, 1 x 105, 1 x 104 spores / ml, mycelium and a check were tested avoiding the presence of the parasitoid, and for this the plants were placed in individual cages; in both cases observations were made up to the adult emergence. The best low dose for third instar nymphs was 2.5 x 104 conidia / ml. However, this dose is not recommended when E. formosa is not present in the crop. The best high dose tested was 1 x106 conidia / ml. It was proved that insects treated at fourh or third instar are affected by the fungus at the adult stage. It was found that A. aleyrodis is innocuous to E. formosa; according to the Pearson's correlation coefficient between the averages of nymphs affected by the fungus and nymphs parasitized by Encarsia, there is neither competition nor association between the two species.
Introducción
La mosca blanca de los invernaderos, Trialeurodes vaporariorum Westwood (Homoptera: Aleyrodidae), causa daños severos a innumerables cultivos a nivel mundial. Mound y Halsey (1978) registran el insecto en 278 huéspedes diferentes. En países con estaciones, las pérdidas de las cosechas ocasionados por las moscas blancas se atribuyen solamente a T. vaporariorum (Berlinguer 1980). En Colombia, este insecto se considera como plaga de importancia económica, tanto en cultivos en campo abierto como en invernadero, desde 1982 (Saldarriaga y Posada 1993); su distribución incluye zonas de los departamentos de Tolima, Nariño, Cundinamarca, Antioquia y Valle del Cauca (Díaz et al.1990). En el Valle del Cauca afecta cultivos de fríjol (Eichelkraut y Cardona 1989), y además se le encuentra en el valle de Aburrá y el Oriente Antioqueño asociada con el virus del amarillamiento de las venas de la papa (Saldarriaga et al. 1987); en esta misma localidad, Bustillo et al. (1988) registran a T. vaporariorum en cultivos de fríjol. Según Saldarriaga y Posada (1993), este insecto también ha adquirido gran importancia económica en cultivos de flores en varias regiones del país, así como en fríjol y habichuela en la zona de Sumapaz en Cundinamarca.
En otros países se han realizado algunos estudios con hongos del género Aschersonia (Coelomycetos: Sphaeropsidales) como una alternativa de control de diferentes especies de mosca blanca. En Holanda, Estados Unidos y China, A. aleyrodis Webber y A. papilata Petch son usados para el control de T. vaporariorum, Bemisia tabaci (Gennadius) y Dialeurodes citri (Riley y Howard), respectivamente (Fransen 1986, 1987; Gao 1985; Zou-Whane 1988). En Colombia existen registros de A. aleyrodis afectando escamas Coccidae en cítricos y en cafeto de clima medio, bajo condiciones naturales, ocasionando un 100% de control del insecto (Rodríguez 1984a,b).
En 1993 se efectuó el estudio de la biología y patogenicidad de cepas nativas y holandesas de A. aleyrodis contra adultos de T. vaporariorum. Las cepas colombianas fueron aisladas de la cochinilla verde de los cítricos, Coccus viridis (Green) (Homoptera: Coccidae), recolectada de hojas de cafeto y naranjo en las localidades de Chinchiná (Caldas) y La Vega (Cund.), respectivamente. Los resultados de este primer estudio, en Colombia, probaron que las cepas nativas de A. aleyrodis adquieren su óptimo desarrollo en el medio Avena Dextrosa Agar y en arroz precocido con el medio líquido a 28°C, así mismo que en Colombia, este hongo es efectivo para el control de adultos de la mosca blanca de los invernaderos (Vargas 1993; Vargas et al. 1993).
En el presente estudio se determinó la dosis óptima de la cepa de A. aleyrodis de La Vega, que resultó más efectiva, como también de la cepa holandesa, contra ninfas de T. vaporariorum de tercero y cuarto instar desarrolladas en fríjol de invernadero. Se evaluó también el efecto de los tratamientos con micelio del hongo contra los mismos instares del insecto y se determinó la interacción entre el hongo y el insecto benéfico Encarsia formosa Gahan (Hymenoptera: Aphelinidae).
Revisión de Literatura
En Colombia, la mosca blanca de los invernaderos, T. vaporariorum, es una plaga que ocasiona daños de considerable magnitud a innumerables cultivos en diferentes zonas del país; se encuentra principalmente en el Oriente Antioqueño y transmite el virus del amarillamiento de la papa y en Cundinamarca afecta cultivos de habichuela, fríjol y tomate y también ataca cultivos de flores de la Sabana de Bogotá; según Díaz et al. (1990), los departamentos más afectados por este insecto son Antioquia, Valle del Cauca, Tolima, Nariño y Cundinamarca.
La tolerancia de algunos instares del insecto plaga a muchos insecticidas, su preferencia por la parte superior del follaje y su habilidad para vivir en cultivos a campo abierto y luego reinfestar las cosechas de invernadero dificultan su control (Mc Clanahan 1970); los últimos estudios de resistencia de T. vaporariorum a diferentes insecticidas confirmaron que este insecto no es susceptible al dichlorvos, remestrin y bifenthrin (Sanderson y Rousch, 1992); también se ha detectado que el insecto es resistente al dicrotophos y al acephato (Omer et al. 1992). En algunos estudios llevados a cabo en Ohio se probaron diferentes concentraciones de bifenthrin y el insecto es susceptible a este piretroide; ninguno de los tratamientos es considerado como control aceptable cuando la población de la mosca se encuentra en su máximo nivel (Adams et al. 1991).
El control biológico constituye una alternativa al control químico, tiende a minimizar el impacto ambiental sobre ecosistemas aledaños a los de producción y también se traduce en beneficios para el agricultor, al disminuir los costos de los insumos.
Los insectos plagas son atacados por numerosos enemigos naturales, entre los cuales se encuentran virus, bacterias y hongos (Poinar 1984). Las bacterias y los virus si bien pueden infectar al insecto a través de heridas ya existentes, no son tan efectivos como los hongos (Fransen 1990). Según varios autores, los hongos entomopatógenos pueden ser una alternativa de control de moscas blancas, en comparación con los métodos tradicionales de control químico. Existen varios ejemplos de hongos que atacan ninfas de moscas blancas en cultivos de cítricos; los siguientes son los más comúnmente encontrados en Florida: A. aleyrodis, A. goldiana (S&E), Aegerita webberi Faw (Coelomycetes: Sphaeropsidales) y Fusarium aleyrodis Petch (Fawcett 1994).
Las especies de hongos entomopatógenos del género Aschersonia son altamente específicos, ya que parasitan escamas (Homoptera: Coccidae) y moscas blancas (Homoptera: Aleyrodidae);.A. aleyrodis ataca varias especies de moscas blancas, especialmente: Dialeurodes citri Ashmead, D. citrifolii (Morgan), Aleurocanthus woglumi Ashby, Aleurothrixus floccossus (Maskell), Trialeurodes floridensis Quaintance, T. abutiloneus (Haldeman), T. vaporariorum, Bemista tabaci, B. giffardi Kotinsky (Homoptera: Aleyrodidae) (Mains 1959; Fransen 1990).
Según Fawcett (1944), A. aleyrodis es uno de los hongos más utilizados para el control biológico del insecto en Florida; y según este autor, en Estados Unidos se ha desarrollado un método para su multiplicación, y se aplica en cultivos de cítricos atacados por moscas blancas. Recientemente, el hongo también se ha registrado como patógeno de A. woglumi en las zonas citrícolas de Costa Rica (Elizondo y Quezada 1990). Existen registros de varios autores chinos sobre el parasitismo de A. aleyrodis en el control de D. citri y otras especies de moscas blancas (Zou - Wanhe 1988; Gao 1985). Bustillo (1984) anota que A. aleyrodis tiene altos niveles de infestación bajo condiciones favorables de humedad y temperatura, y presenta registros del hongo en Suramérica atacando a A. woglumi, y a las escamas Unaspis citri Comstock y Selenaspidus articulatus (Morgan) (Homoptera: Diaspididae), plagas de importancia económica en cítricos. En Colombia se presenta en forma natural sobre C. viridis en cítricos y en cafeto, en localidades de Antioquia, Cundinamarca y Caldas; existen también registros sobre Coccus sp. en mango y sobre U. citri, en cítricos en Sevilla-Ciénaga (Mag.) (Rodríguez 1984b).
Según Fransen (1990), A. aleyrodis es eficiente en el control de T. vaporariorum. El proceso de infección del hongo en el insecto se realiza por la germinación de las picnidiosporas sobre la superficie del integumento de las moscas blancas; las picnidiosporas deben permanecer en contacto con la cutícula para iniciar su geminación y penetracion, dependiendo de las condiciones favorables para esto. Durante esta fase se forma el tubo germinal que penetra directamente en la cutícula o por medio de un aprehensorio que produce las enzimas, proteasas, lipasas y quitinasas. La formación del aprehensorio sobre la ninfa de la mosca blanca de los invernaderos ocurre uno a dos días después de la penetración del tubo germinal del hongo en la cutícula del insecto; antes de formar el micelio se producen varias estructuras, que en conjunto se denominan cuerpos hifales, los cuales circulan en la hemolinfa. Los hongos entomopatógenos pueden vencer a sus huéspedes antes de que la invasión se extienda a sus órganos, por lo cual se presume que las toxinas producidas por estos hongos son las responsables de la muerte del huésped. Es difícil realizar un cálculo del tiempo exacto de la muerte del insecto antes de que aparezcan los primeros síntomas de infección por el entomopatógeno. Un decrecimiento de la producción de mielecilla producida por la mosca blanca, cuando ésta se alimenta en la planta, puede significar una interrupción del metabolismo del huésped; posteriornente, el insecto muere. Cuando el micelio invade los órganos de T. vaporariorum, se reconoce porque adquiere un color anaranjado brillante; este cambio de coloración de blanco opaco a naranja brillante se considera como el primer síntoma de infección. Cuando el insecto en este estado se encuentra bajo condiciones de alta humedad relativa, el micelio se proyecta fuera del cuerpo. El micelio de A. aleyrodis es blanco, crece desde el borde del insecto y lo cubre completamente; luego se producen nuevamente masas de esporas en picnidios, las cuales requieren de agua para su infección (Fransen 1990). Aunque los síntomas de infección de T. vaporariorum por A. aleyrodis pueden ser muy claros, en algunos casos se ha observado que las aplicaciones del hongo hechas sobre plantas pequeñas aisladas producen síntornas diferentes a los obtenidos de las aplicaciones efectuadas sobre cultivos bien desarrollados; en plantas pequeñas, el hongo tiende a estar dentro del cuerpo del insecto, y sólo se observa una coloración amarillenta, y los insectos mueren sin producir gotas de color anaranjado. La inspección microscópica muestra abundante micelio y escasas conidias en el exterior del insecto muerto (Ramarkers y Samson 1984).
Según Fransen (1990), existe escasa literatura que proporcione datos confiables acerca de la mortalidad diferida de T. vaporariorum por infección con hongos; a menudo, la información se basa sólo en observaciones de campo poco representativas, puesto que algunos instares se reconocen más fácilmente que otros cuando están infectados. Sin embargo, este mismo autor, en 1987, presenta resultados de un estudio en el cual se evaluó la mortalidad diferencial de instares de la mosca blanca T. vaporariorum ocasionados por A. aleyrodis, y según los resultados obtenidos en dicho trabajo, la infección va decreciendo a medida que las moscas blancas aumentan su edad, por lo cual el tratamiento a adultos resulta poco efectivo. Los resultados de Fransen también muestran que los primeros síntomas aparecen cuatro días después de contaminadas las ninfas y que el período de incubación puede ser de 10 a 14 días. El estudio concluye que A. aleyrodis es efectivo para el control del primero, segundo y tercer instares ninfales; pero que las pupas y los adultos son menos susceptibles debido posiblemente a un cambio en la composición de la cutícula o tal vez a la producción de sustancias fungicidas que inhiben los procesos de germinación y penetración del hongo.
La especie E. formosa fue descrita en 1924, en Ohio, como parasitoide de moscas blancas; en esa época también se encontró naturalmente en Inglaterra y Canadá. En estos países se liberaron altas poblaciones de este benéfico en cultivos bajo invernadero y se encontró que el control biológico con este insecto reemplazó las peligrosas fumigaciones de cianídricos, sin embargo, el uso de E. formosa como único elemento de control del insecto plaga no resultó satisfactorio (Mc Clanahan 1970).
Van Lenternen y Nell (1980), en un estudio que determinó las relaciones entre E. formosa y T. vaporariorum, describen el comportamiento de oviposición del parasitoide en relación con la selección y discriminación del huésped. Según estos autores, E. formosa siempre utiliza sus antenas para realizar el primer contacto con las ninfas de T. vaporariorum, en esta fase, el benéfico se «asegura» de que el huésped se encuentre en un estado adecuado para ser parasitado; los estados muy jóvenes como primero y segundo instares y los muy viejos como las pupas, son rechazados; así mismo ocurre con las ninfas ya parasitadas; las ninfas sanas de tercero y cuarto instar y las prepupas son seleccionadas.
E. formosa posiblemente discrimina las ninfas ya parasitadas o las afectadas por otros enemigos naturales como A. aleyrodis, debido posiblemente a sus patrones de comportamiento. Este insecto sólo oviposita un huevo en cada ninfa de su huésped, para que el desarrollo de sus larvas sea óptimo y también para disminuir la competencia intraespecífica; únicamente en raros casos, cuando la población de mosca blanca es baja y esto se constituye en un factor de presión, se pueden encontrar dos larvas de E. formosa en cada ninfa de T. vaporariorum.
En planes de manejo integrado de moscas blancas en muchos cultivos de hortalizas, el parasitoide E. formosa se usa con éxito; la introducción de este insecto benéfico en cultivos de plantas ornamentales se encuentra todavía en etapa experimental. El uso del parasitoide y de A. aleyrodis puede producir mejores resultados que el uso E. formosa solo; las poblaciones del insecto benéfico sobreviven después de aplicaciones del entomopatógeno A. aleyrodis cuando en el cultivo se encuentran presentes suficientes huéspedes sanos. Por otro lado, las especies de Aschersonia son altamente selectivas e incapaces de infectar otras especies de insectos diferentes a los de las familias Aleyrodidae y Coccidae (Fransen 1990).
Materiales y Métodos
Los ensayos de patogenicidad de dos cepas del hongo A. aleyrodis, cepa La Vega (Cund.) * y otra holandesa ** , se efectuaron en los invernaderos del Centro Nacional de Investigaciones "Tibaitatá" en Mosquera (Cund.). La cría de T. vaporariorum se estableció en plantas de fríjol de tres semanas de edad, desarrolladas en materos de 14 cm de diametro por 13 cm de alto; en las plantas se eliminaron las hojas bajeras para obtener poblaciones homogéneas del insecto. Las plantas se expusieron a adultos de la mosca blanca de los invernaderos durante 48 horas, para que ovipositaran sobre ellas; luego se retiraron cuidadosamente los insectos adultos usando agua a presión y las plantas se guardaron en una casa de malla, y cuando la población ninfal de la mosca alcanzó el tercer instar, se seleccionaron 3 hojas de cada matero con poblaciones altas del insecto, las cuales constituyeron las unidades experimentales.
Aislamiento efectuado de escamas Coccidae atacadas por el hongo en cítricos; muestra gentilmente enviada por Reinaldo Cárdenas de CENICAFE. Chinchiná (Caldas).
Aislamiento enviado gentilmente por el Dr. Harry Evans del International Institute of Biological Control. Silwood Park, Ascot Berks S15 7PY U.K.
Para determinar las dosis efectivas de las cepas del hongo y la interacción de éste con el insecto benéfico E. formosa se usó en la cría del insecto, que se estableció como consecuencia de liberaciones anteriores del parasitoide en el invernadero. Se usó un diseño completamente al azar con tres repeticiones y 5 tratamientos: 3 dosis (2,5 x 104, 1 x 104, 1 x 103 esporas/ml.), micelio y un testigo con agua. Se contaminaron plantas con ninfas de T. vaporariorum de tercero y cuarto instar. En los mismos instares del insecto se probaron dosis mayores del hongo y se colocaron jaulas individuales de tul fino en cada matero con el fin de evitar la presencia de E. formosa. Estos experimentos se realizaron bajo el mismo diseño estadístico que el anterior, y los tratamientos fueron 4 dosis del hongo (1,3 x 107, 1 x 106, 1 x 105,1 x 104 esporas/ml), micelio y un testigo con agua. En ambos ensayos se hicieron lecturas de mortalidad diaria del insecto en una superficie de la hoja de 3 x 3 cm, marcada previamente. Las lecturas de mortalidad por el hongo y por otras causas se tomaron diariamente, durante diez días y se observaron los tratamientos hasta la emergencia de los adultos. Con los promedios de mortalidad diaria y total se efectuaron los análisis de varianza, la diferencia mínima significativa (DMS), los análisis de regresión y el coeficiente de correlación de Pearson. Se estableció la dosis efectiva del hongo contra el insecto, el estado del insecto más susceptible al patógeno, el tiempo de acción de A aleyrodis y la interaccion del hongo con el parasitoide E. formosa.
Para confirmar los datos tomados en el invernadero, en el laboratorio se hicieron minuciosas observaciones bajo un estereomicroscopio; también fue necesario realizar frotis y coloraciones varias (azul de metileno, verde de malaquita y safranina) a ninfas que no mostraban producción de mielecilla y presentaban una coloración diferente a la característica de ninfas sanas, pero que no concordaba con los síntomas típicos de infección por A. aleyrodis citados en la literatura.
Para la obtención del inóculo, el hongo se sembró en cajas de Petri con medio Avena Dextrosa Agar con Extracto de Levadura y se mantuvo a 28°C; 10 días después se recuperaron las colonias en agua destilada, estéril; se filtró la suspensión y se tituló a las concentraciones requeridas para el ensayo; en la misma forma se procedió con las colonias multiplicadas masivamente en arroz precocido estéril más el medio líquido.
Resultados
Para realizar el análisis de varianza (Anava), que permitió determinar el efecto de las dosis de A. aleyrodis, cepas La Vega y holandesa, y del tiempo de muestreo, lo mismo que las interacciones entre éstos, se analizaron las variables: ninfas con micosis, es decir, todas aquellas ninfas que en una primera observación mostraron síntomas claros de infección por el hongo y la variable ninfas aplanadas, que son todas aquellas que requirieron de observaciones más detalladas y de frotis con coloraciones específicas para confirmar la presencia del patógeno dentro del cuerpo del insecto. El análisis de la variable ninfas parasitadas por E. formosa, permitió establecer las interacciones del parasitoide con A. aleyrodis. El análisis de varianza para estos datos se presenta en la Tabla 1.
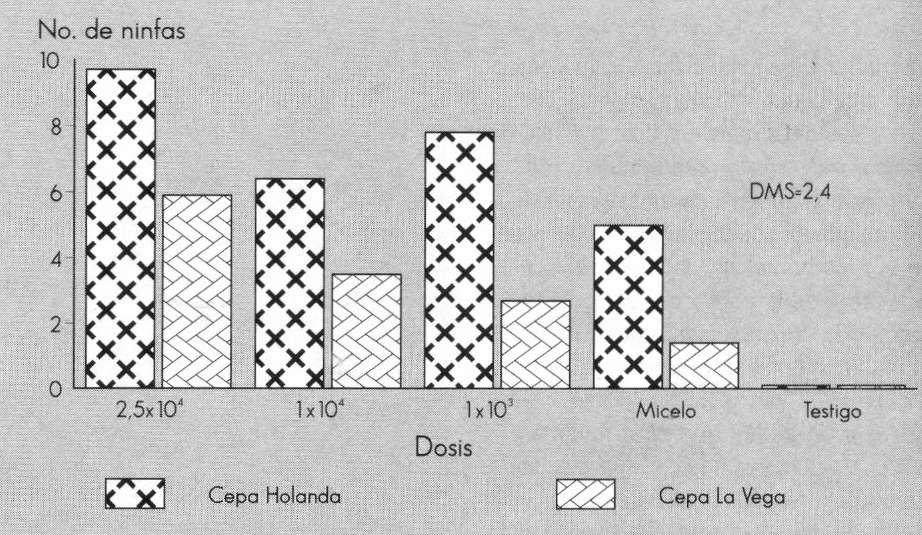
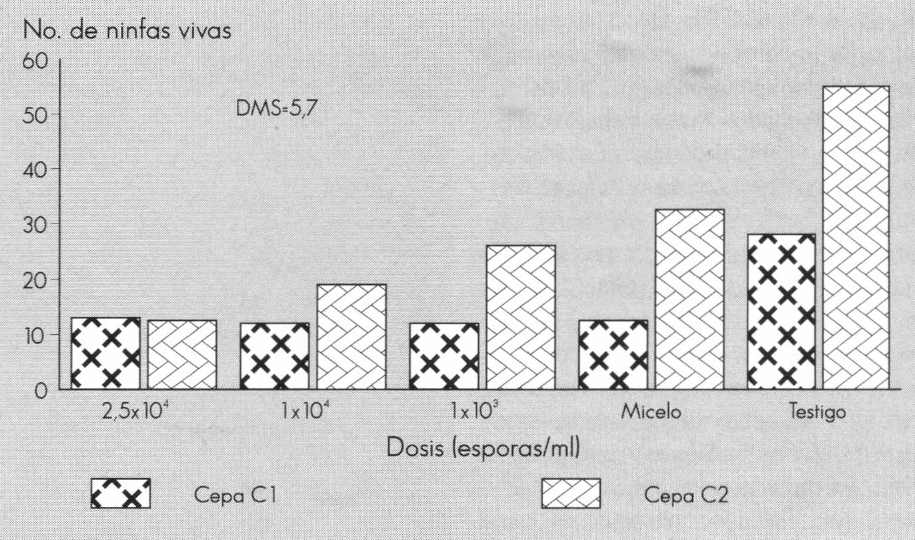
En el primer ensayo de invernadero, en el que se contaminaron ninfas de T. vaporariorum en plantas de fríjol con las dosis de 2,5 x104, 1 x 104, 1 x 103 esporas/ml de A. aleyrodis y se registró la presencia de E. formosa, la variable número de ninfas con micosis mostró diferencias significativas para las interacciones tratamiento por cepa y tratamiento por tiempo de muestreo, lo cual indica que A. aleyrodis se comporta diferente según la dosis y la cepa utilizadas; la mortalidad producida por el hongo en el insecto es diferente con todas las dosis de cada una de las cepas a los distintos tiempos del muestreo. Los promedios del efecto de difererentes dosis de dos cepas de A. aleyrodis contra ninfas de tercero y cuarto instar de T. vaporariorum se presentan en la Figura 1.
Análisis de varianza para la evaluación de ninfas de tercero y cuarto instar de T. vaporariorum infectadas con A. aleyrodis a dosis de 2,5 x 104, 1 x 104, 1 x 103 esporas/ml y micelio cuando se presenta E. formosa en el invernadero.
Variable transformada para el análisis de varianza
Diferencia significativa (α=0,05)
Diferencia altamente significativa (α=0,01)
Para todos los tratamientos se confirma que la cepa de A. aleyrodis procedente de Holanda afecta un número de ninfas significativamente superior a las afectadas por la cepa La Vega. En la Figura 1 también se observa que la mortalidad por micosis producida con la cepa holandesa a las dosis 2,5 x104 y 1 x 103 esporas/ml en las ninfas de T. vaporariorum es igual; sin embargo, las diferencias son significativas comparando estas dosis y el tratamiento con micelio de la misma cepa. Con el aislamiento de La Vega se obtiene el mayor porcentaje de mortalidad con la dosis más alta de 2,5 x104 esporas/ml.
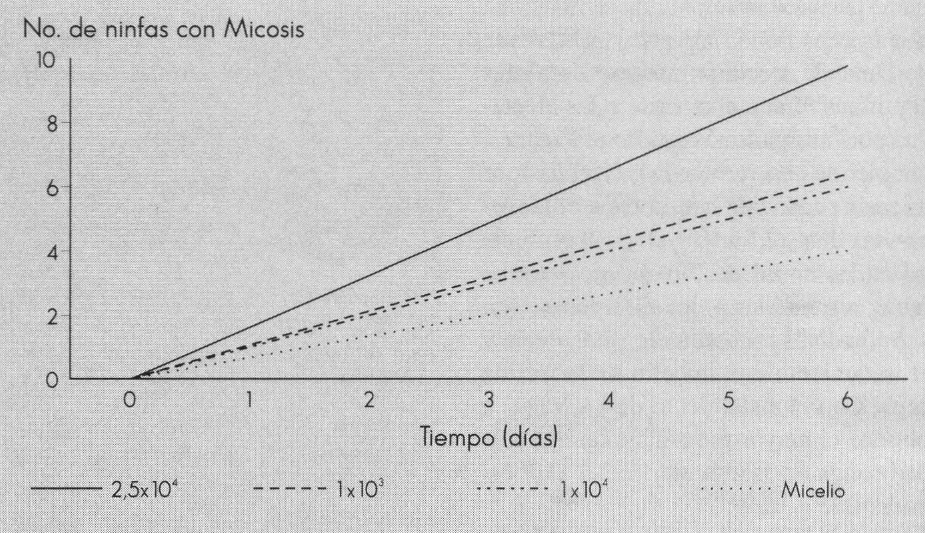
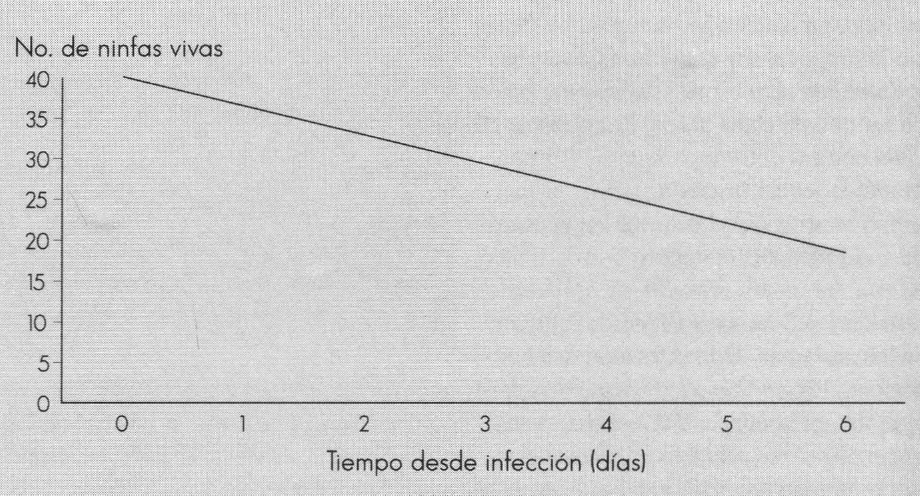
Para analizar la interacción significativa encontrada entre los tratamientos y el tiempo de acción de estos en el insecto, se ajustaron modelos de regresión para el número de ninfas con micosis en función del tiempo transcurrido después de la infección, para cada uno de los tratamientos (Fig. 2). Las líneas de regresión permiten apreciar la evolución de la infección en la poblacion de ninfas de tercero y cuarto instar de mosca blanca. La dosis. 2,5 x 104 esporas/ml presenta la mayor pendiente, lo cual indica una mayor velocidad de acción del hongo en el insecto, produciendo una rápida aparición de micelio sobre las ninfas muertas. En este ensayo las pendientes de los otros tratamientos no son apreciablemente diferentes.
El análisis de regresión confirma una vez más que en el primer ensayo la mejor dosis de los dos aislamientos de A. aleyrodis para el control de ninfas de tercero y cuarto instar de T. vaporariorum es 2,5 x 104 esporas/ml. Según la gráfica de la Figura 2, el desarrollo de micelio obtenido con este tratamiento es significativamente superior a los 4, 5 y 6 días después de la infección y es significativamente superior al obtenido con suspensiones de los hongos a 1 x 104 esporas/ml y 1 x 103 esporas/ml a los 5 y 6 días después de la infección.
El análisis del número de ninfas parasitadas por E. formosa (Tabla 1) mostró diferencias significativas para la interacción tratamientos por cepa. En otras palabras, E. formosa alcanza diferentes niveles de parasitismo cuando interactúa con cada uno de los tratamientos de A. aleyrodis a las diferentes dosis (Fig. 3). Los resultados de ninfas de mosca blanca parasitadas por E. formosa son significativamente superiores cuando se usó la cepa La Vega a 2,5 x 104 esporas/ml en comparación con la cepa holandesa a la misma dosis (DMS = 2,1); sin embargo, no existen diferencias significativas entre el parasitismo de E. formosa cuando interactúa con A. aleyrodis a las dosis de 1 x 104 esporas/ml y 1 x 103 esporas/mly micelio. En las Figuras 1 y 2 se aprecia una tendencia a la asociación de niveles bajos de micosis producidas por A. aleyrodis con niveles altos de ninfas parasitadas por E. formosa; las ninfas tratadas con la cepa La Vega presentan niveles bajos de micosis y alto parasitismo por E. formosa.
El coeficiente de correlación de Pearson, con niveles de significancia de 0,09 y proveniente de 30 pares de las variables ninfas con micosis y ninfas parasitadas por E. formosa, a los seis días de la aplicación de los tratamientos, corrobora la relación inversa que se presenta entre estas variables. La correlación obtenida entre los dos agentes biocontroladores es positiva, con un nivel de significancia observado de 0,66 y n = 18, cuando la infección de las ninfas se realiza con micelio de A. aleyrodis (Tabla 2).
Número de ninfas de tercero y cuarto instar de T. vaporariorum muertas y con desarrollo de micosis de A. aleyrodis, cepas Holanda y La Vega a diferentes dosis.
Estimación de ninfas de T. vaporariorum con micosis de A. aleyrodis a diferentes tiempos después de la contaminación.
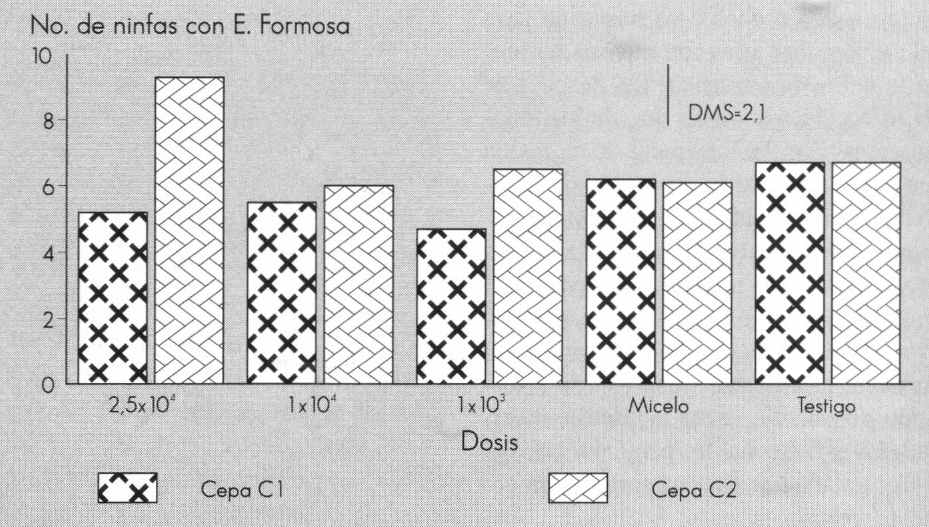
Parasitismo natural de E. formosa en ninfas de T. vaporariorum encontrado en los tratamientos de dos cepas de A. aleyrodis a diferentes dosis, en condiciones de invernadero.
En el análisis de varianza para el número de ninfas parasitadas con E. formosa interactuando con A. aleyrodis se encontró que el efecto del tiempo de parasitación del benéfico fue altamente significativo. La Figura 4 muestra que los promedios de mortalidad obtenidos en los cinco tratamientos de las dos cepas aumentan significativamente con el tiempo a una tasa promedio de 1,15 ninfas parasitadas por día. El mismo análisis, efectuado con la variable ninfas vivas, muestra que éstas decrecieron a una tasa de 3,77 por día (Fig. 6); en este caso se ve el efecto de los dos agentes controladores.
La matriz de correlación (Tabla 2) permite establecer varias relaciones de interés; el coeficiente de correlación de Pearson negativo y altamente significativo entre el número de ninfas con micosis y el número de ninfas vivas comprueba la efectividad de A. aleurodis en la reducción de la población de T. vaporariorun. Existe correlación positiva y significativa entre el número de ninfas aplanadas y el número de ninfas con micosis, lo cual indica que el aplanamiento de las ninfas es síntoma de la infección micótica producida por A. aleyrodis y que este aplanamiento está asociado con la reducción de la población de T. vaporariorum en fríjol de invernadero. Por frotis y coloraciones específicas de estas ninfas se confirmó la presencia de picnidiosporas triseptadas y hialinas en los extremos, características de A. aleyrodis.
Coeficientes de correlación entre el número de ninfas vivas, aplanadas y con E. formosa y el número de ninfas con micosis.
Coeficiente de correlación de Pearson
Nivel de significancia observado
Tamaño de la muestra
Coeficiente de correlación de Spearman
Los resultados del segundo ensayo, sin presencia de E. formosa, realizado con A. aleyrodis cepa La Vega (Tabla 3) muestra que existen diferencias altamente significativas en la mortalidad de ninfas de cuarto instar tratadas con las dosis de 1,3 x 107, 1 x 106, 1 x 105, 1 x 104 esporas/ml y micelio de A. aleyrodis a los 5 y 9 días después de la aplicación del hongo, bajo condiciones de invernadero. Los promedios (Tabla 4, Fig. 7 y 8) y el cálculo de las DMS (Tabla 5) confirman este resultado.
Según la Tabla 4, la mayor mortalidad en ninfas de cuarto estado y de adultos emergidos de éstas, se obtienen con la dosis 1 x 106 esporas/ml, a los cinco días después del tratamiento.
Los resultados de las DMS de los promedios de mortalidad obtenidos con A. aleyrodis (cepa La Vega) a diferentes dosis, muestran que a los 9 días después del tratamiento, las ninfas de cuarto instar presentaron una mayor mortalidad con las dosis 1 x 106 y 1 x 107 esporas/ml; por otra parte no hay diferencias significativas entre estos dos tratamientos. Se observa un mayor número de adultos afectados por el hongo emergidos de pupas originadas de ninfas de cuarto instar en plantas tratadas con 1,3 x 107 esporas/ml (Tabla 4).
Discusión
Los resultados obtenidos en las pruebas de patogenicidad de A. aleyrodis, cepas La Vega y Holanda, en ninfas de tercero y cuarto instar de T. vaporariorum, efectuadas en el invernadero, muestran que al usar las cepas mencionadas a dosis 2,5 x 104 esporas/ml se produjo el mayor número de ninfas con micosis (Fig. 9); además se comprobó que una sola aplicación del patógeno en fríjol de invernadero a dosis bajas del hongo no alcanza a controlar totalmente la plaga; la población del parasitoide E. formosa, presente en el invernadero por liberaciones anteriores, complementó el control de T. vaporariorum.
Las ninfas de cuarto instar son más susceptibles a la infección de A. aleyrodis, aunque Fransen (1987) afirma que estas ninfas y las pupas del insecto son menos susceptibles al hongo; sin embargo, en las condiciones del ensayo se comprobó lo contrario, debido posiblemente a factores ambientales favorables o al mayor grado de patogenicidad de las cepas probadas. Con respecto a la poca susceptibilidad de ninfas de cuarto instar y de pupas encontrado por Fransen (1987), el autor no atribuye este fenómeno a una respuesta inmunológica del insecto a la penetración de un cuerpo extraño; según Zahedi et al. (1992), las respuestas de los insectos a cuerpos extraños no son tan complejas como las de los vertebrados, pero son igualmente eficientes. Según estos autores, los insectos son capaces de responder a un amplio rango de compuestos externos; estos pueden ser reconocidos por sus diferencias físicas; la respuesta inmediata es la encapsulación del cuerpo extraño y su síntoma externo es la presencia de áreas melanizadas en el insecto. En los ensayos de invernadero se encontraron ninfas con síntomas de melanización (Fig. 10); estos datos no se tuvieron en cuenta para las lecturas, por presentarse esporádicamente.
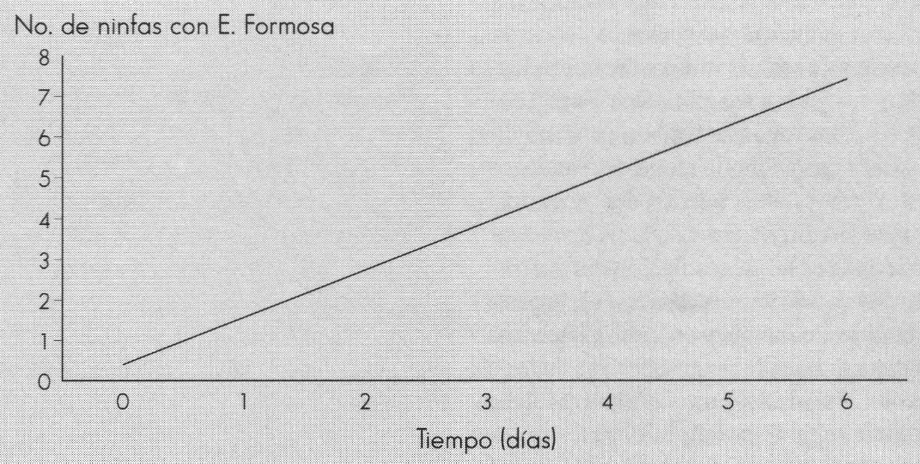
Efecto del tiempo transcurrido desde la aplicación del tratamiento sobre el número de ninfas de T. vaporariorum parasitadas por E. formosa.
Promedio de ninfas vivas de T. vaporariorum en los tratamientos de dos cepas de A. aleyrodis a diferentes dosis.
Efecto del tiempo transcurrido entre la contaminación de ninfas de T. vaporariorum con dos cepas de A. aleyrodis sobre el número de ninfas vivas de T. vaporariorum.
Las esporas de los entomopatógenos son las responsables de la infección del insecto; por lo tanto, los tratamientos con micelio de hongos generalmente no se usan. Los resultados de este trabajo muestran que es posible producir infección en ninfas de tercero y cuarto instar con tratamientos de micelio de A. aleyrodis; sin embargo, resulta difícil determinar las concentraciones de micelio en la suspensión fungosa; la infección de las ninfas con micelio del hongo se debe posiblemente a que éste encuentra sobre el integumento del insecto un medio adecuado para su desarrollo. Según Alexopoulus (1962), en muchos casos los Deuteromycetes, bajo condiciones particulares, producen estructuras reproductivas asexuales como las esporas a partir de fragmentos miceliales; sin embargo, este autor también afirma que este fenómeno se oberva raramente en los hongos que forman las esporas en estructuras complejas como los picnidios. A. aleyrodis podría ser uno de estos casos. Por otra parte, los hongos entomopatógenos forman elementos levuriformes a partir del micelio, o blastosporas que también causan infección en los insectos.
Ramakers y Samson (1984) concluyen que los síntomas de la infección ocasionada por el hongo no son fácilmente distinguibles en las ninfas del insecto, cuando se realizan los estudios en plantas que crecen en materos aislados, bajo condiciones de invernadero, debido a que las ninfas mueren sin producir coloración anaranjada; sólo se aprecia una coloración amarillenta y en la observación microscópica se encuentra micelio dentro de las ninfas muertas. En este trabajo, realizado en las condiciones mencionadas por el autor, fue difícil observar la sintomatología de las ninfas enfermas. Algunas mueren y generalmente tienden a deshidratarse sin presentar desarrollo micelial al exterior del cuerpo, ni coloración anaranjada como la presenta el hongo en el medio de cultivo, otras son color carmelito oscuro y al deshidratarse dejan una mancha en el sitio de la hoja en donde se encuentran; las ninfas que no presentan síntomas típicos de infección con A. aleyrodis aparecen generalmente comprimidas (ninfas aplanadas); en los frotis de ninfas de color carmelito y comprimidas observados al microscopio se encontraron picnidiosporas típicas de A. aleyrodis.
Resumen del ANAVA para los promedios de ninfas de cuarto instar y adultos con micosis originados de estas ninfas contaminados en invernadero.
Diferencia significativa (α=0,1)
Diferencia altamente significativa (α=0,01)
Promedios de la mortalidad de ninfas de cuarto instar contaminadas con A. aleyrodis y de adultos obtenidos de estas ninfas, en condiciones de invernadero en plantas de fríjol a los cinco y nueve días del tratamiento, sin presencia de E. formosa.
En cada columna, promedios con letras iguales no son significativamente diferentes al nivel del 5%.
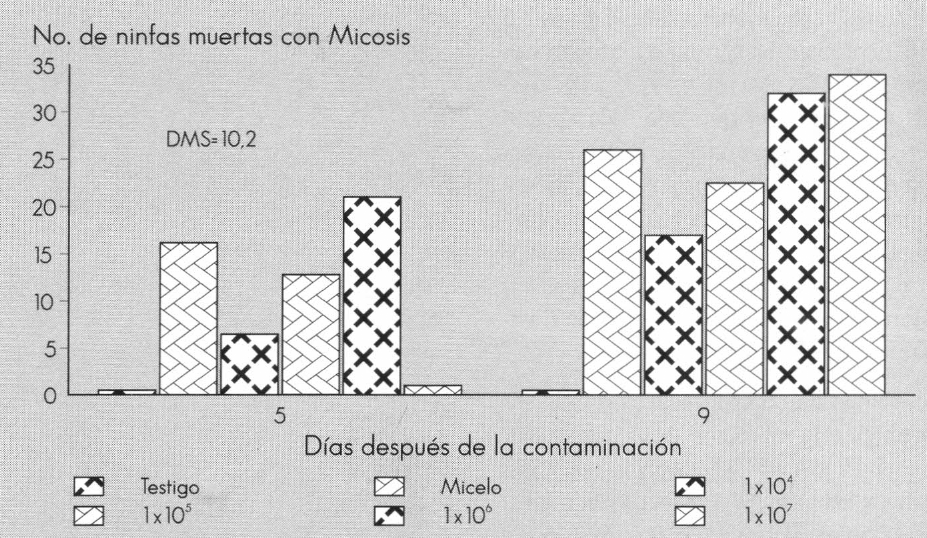
Mortalidad de ninfas de T. vaporariorum con desarrollo de micosis de dos cepas de A. aleyrodis a diferentes dosis, sin presencia del parasitoide E. formosa.
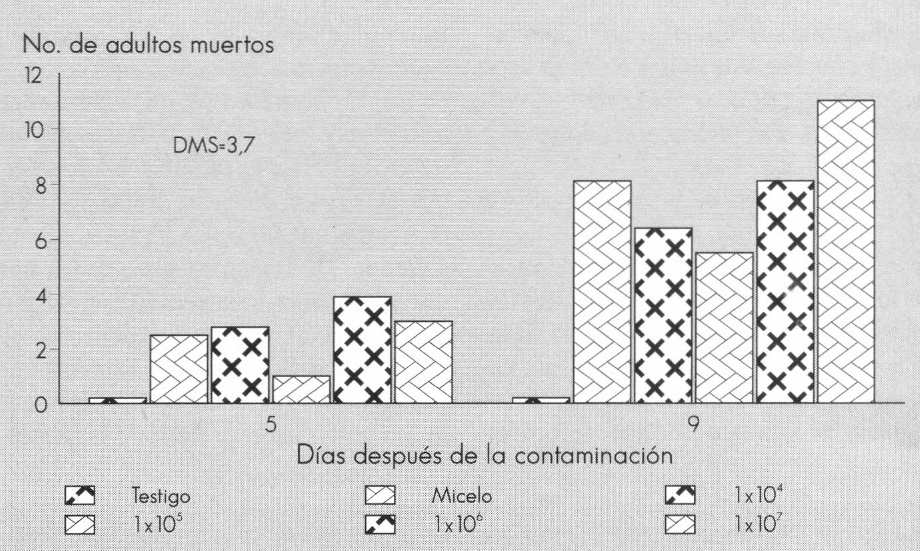
Mortalidad de adultos de T. vaporariorum con desarrollo de micosis de dos cepas de A. aleyrodis a diferentes dosis, sin presencia del parasitoide E. formosa.
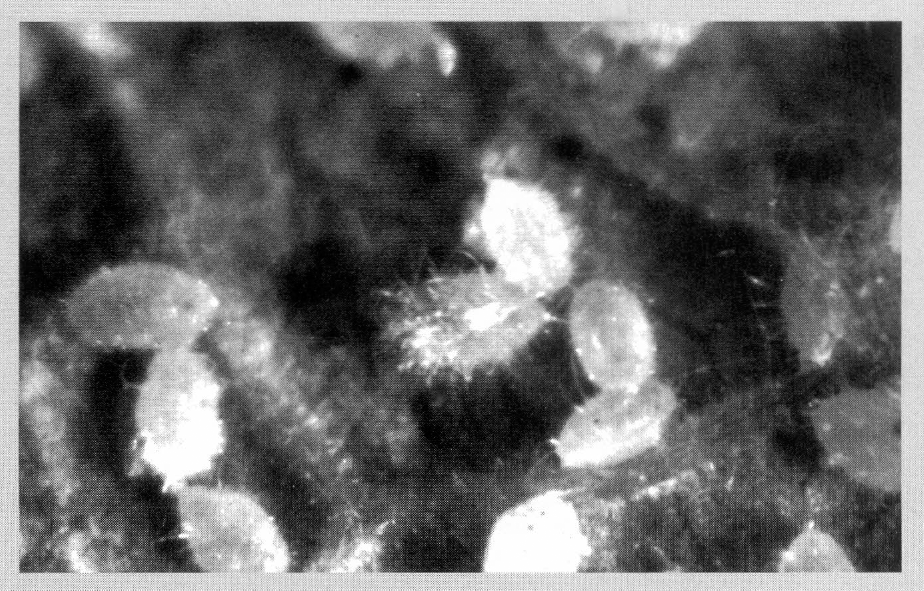
Micosis externa en ninfa de T. vaporariorum afectada por A. aleyrodis. (Foto: Aristóbulo López-Avila)

Areas melanizadas producidas en las ninfas de T. vaporariorum como reacción a la infección por A. aleyrodis. (Foto: Aristóbulo López-Avila)
En las ninfas de cuarto instar y en los adultos emergidos de pupas provenientes de ninfas tratadas en este instar, las micosis se aprecian más frecuentemente que en las ninfas tratadas en el tercer instar. Se registraron también adultos deformes muertos al tratar de salir de pupas de ninfas contaminadas en cuarto instar; los adultos presentaban excresiones cerosas, en forma de filamentos, en la parte ventral del abdomen (Fig. 11). Hussey (1958) realizó una revisión de trabajos sobre control de T. vaporariorum con el hongo Cladosporium sphaerospermun Penzig y cita a Webber (1931), quien describe los síntomas mencionados anteriormente; según este último autor, las excresiones cerosas son el producto del daño ocasionado por el hongo a las glándulas de cera del insecto. En este trabajo se constató la presencia de picnidiosporas de A. aleyrodis por medio de observaciones al microscopio tanto en los filamentos cerosos como en el abdomen del insecto; esto demuestra que la deformación y posterior muerte de los adultos se debe a la infección ocasionada por el hongo.
Por otra parte, las observaciones de los tratamientos con A. aleyrodis (cepa La Vega) en ninfas de cuarto instar y su seguimiento hasta la emergencia de los adultos, permitieron establecer que los síntomas característicos de la enfermedad producida por el hongo no se presentan siempre en el estado tratado (Fig. 12); Fransen (1987) asegura que los síntomas de infección por el hongo pueden aparecer en la prepupa, aun cuando las ninfas hayan sido tratadas en los primeros instares ninfales. Otros autores han demostrado el mismo efecto en insectos Lepidoptera y Coleoptera, y lo han identificado como mortalidad diferida en el tiempo de desarrollo del insecto contaminado (Fargues et al. 1973; Farguez y Rodríguez 1980).
DMS con los promedios de las evaluaciones de la mortalidad en los diferentes tratamientos con las dos cepas de A. aleyrodis con presencia de E. formosa, en invernadero. Primer ensayo.
†: Tiempo de evaluación 4, 5 y 6 días después del tratamiento
T: Tratamiento 1-2,5 x 104; 2=1 x 104; 3= 1x 103; 4= micelio; 5- Testigo
NM: Ninfas con micosis; NE: Ninfas con Encarsia; NV: Ninfas vivas; NA: Ninfas aplanadas
** En los tiempos 4 y 5 las ninfas son de 3° instar y en el tiempo 6 las ninfas son de 4° instar
En este estudio se observó que en cultivos puros de A. aleyrodis, en cajas de petri, se obtiene un promedio de 104 esporas/ml, mientras en colonias desarrolladas en granos de arroz se obtienen hasta 107 esporas/ml; estas dosis corresponden al primer y segundo ensayo de invernadero respectivamente. Según Ramakers y Samson (1984), la cantidad de conidias producidas en medios sólidos en cajas de Petri es mucho menor que la cantidad de conidas obtenidas de hongos sembrados en arroz.
Se confirmó que A. aleyrodis no es patogénico a E. formosa. El coeficiente de correlación de Pearson obtenido en este trabajo para los datos de ninfas atacadas con A. aleyrodis y ninfas parasitadas por E. formosa resultó negativo; lo que sugiere que no existe competencia o asociación entre las dos especies (Fig. 13), lo cual coincide con lo encontrado por Ramakers (1983), quien sostiene que las aplicaciones del hongo no tienen influencia en el parasitismo de E. formosa.
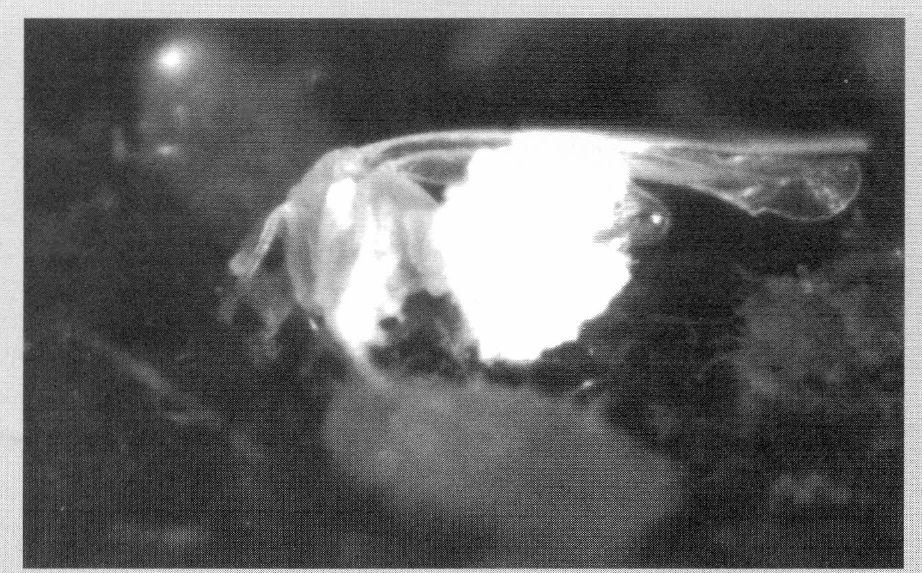
Adulto de T. vaporariorum afectado por el patógeno, tratado en su cuarto instar ninfal con A. aleyrodis. Obsérvense las secreciones cerosas del abdomen producidas como reacción a la infección por A. aleyrodis. (Foto: Aristóbulo López-Avila)
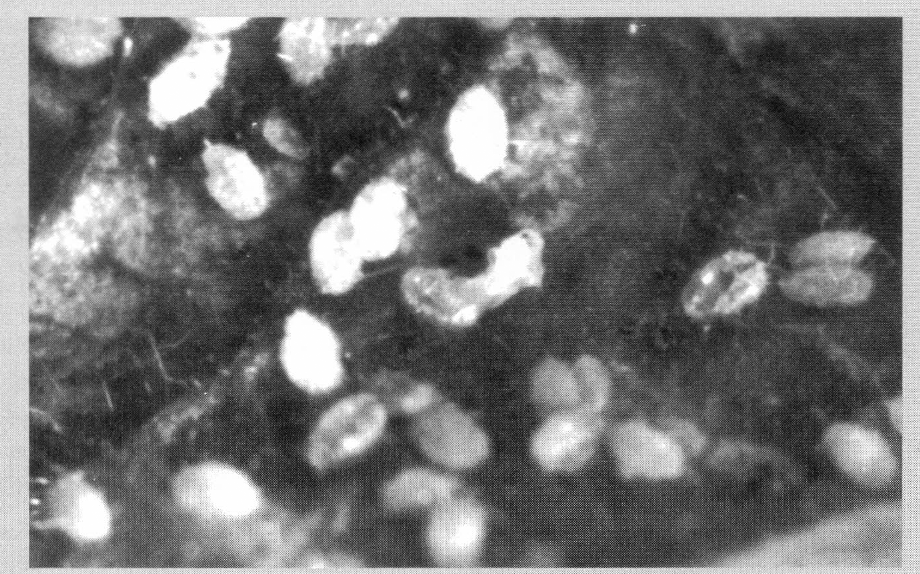
Adulto deforme y muerto de T. vaporariorum, emergiendo de pupas provenientes de ninfas tratadas con A. aleyrodis en el tercer instar. (Foto: Aristóbulo López-Avila)
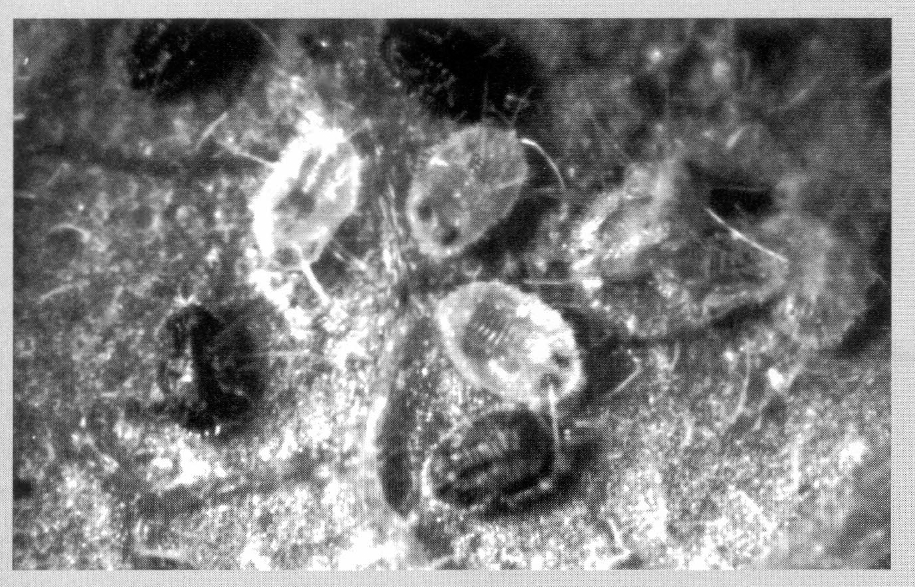
Ninfas de cuarto instar de T. vaporariorum parasitadas por A. aleyrodis (ninfas naranjas) y E. formosa (ninfas negras). (Foto: Aristóbulo López-Avila)
Conclusiones
El parasitismo de Encarsia formosa registrado en ninfas de tercero y cuarto instar de Trialeurodes vaporariorum en plantas de fríjol contaminadas con Aschersonia aleyrodis es altamente significativo en todos los tratamientos del hongo. A. aleyrodis no compite, ni se asocia con el parasitoide y es compatible con éste, para el control de T. vaporariorum. En las pruebas de patogenicidad de A. aleyrodis (cepa La Vega) realizadas en el invernadero de "Tibaitatá", se encontró que el cuarto instar ninfal es más susceptible a la infección del patógeno que el tercero. Para lograr un control eficiente de las ninfas de tercero y cuarto instar de T. vaporariorum se necesitan dosis de A. aleyrodis superiores a 1,3 x 107 esporas/ml. La población de adultos vivos aumenta proporcionalmente a medida que disminuyen las dosis. Los síntomas de infección por A. aleyrodis no resultan muy evidentes en las ninfas y adultos criados en plantas en invernadero. Se aprecian ninfas atacadas por el hongo que no presentan crecimiento micelial; sin embargo, son de color carmelito y generalmente se deshidratan dejando manchas del mismo color en el sitio donde se encuentran. Los frotis de estas ninfas observados al microscopio presentan picnidiosporas de A. aleyrodis. La acción de la enfermedad producida por A. aleyrodis en T. vaporariorum continúa en los estados de desarrollo subsiguientes al estado del insecto contaminado con el hongo.
