Abstract
Three trypsin inhibitors (T9003, T9253, T9378), two Chitinases (C1650, C6137) and a chymotrypsin-trypsin inhibitor (T9777) in two doses (1.0 and 0.1%) were evaluated on a random design with factorial arrangement of 6x2+2. Each treatment consist of 200 eggs of Hypothenemus hampei. The experimental unit was four eggs placed in 1 cmβ of an artificial diet with 50 repetitions per treatment. The evaluations were made from the eggs hatch until adult emergence (T=28 °C and R.H.= 75%). With the T9003, T9253 and T9378 (1.0 %), the insect life cycle had a mean half life (± SD) of 20.81 ± 1.64, 21.71 ± 1.93 and 22.57 ± 1.35 days and the mean mortality was 47.69, 57.66 and 60.66%, respectively; for the concentration 0.1% was 21.75 ± 2.11, 23.60 ± 2.59 and 22.23 ± 1.85 days, and the mean mortality was 37.50, 43.0 and 39.33%, respectively. The control allowed the complete life cycle duration, 22.08 ± 1.55 days, and a mean mortality of 10.50%. With the chitinases (1.0%), the mean half life was 20.36 ± 2.51 and 20.37 ± 2.98 days, the mean mortality was 43.25 and 51.40%; for 0.1% the mean half life was 20.62 ± 2.03 and 20.25 ± 2.33 days, and the mortality was 42.57 and 44.84%, respectively. With the chymotrypsin-tripsin inhibitor in 1.0%, the mean half life was 20.92 ± 2.44 days and the mean mortality was 33.29%; for 0.1% the mean half life was 20.89 ± 3.07 days and the mean mortality was 25.61%. The control for the two latter treatments exhibited a complete life cycle duration of 22.21 ± 1.47 days and the mean mortality was 15.43%. In relation with the insect life cycle, there were not significative differences among treatments and the control; in contrast, the mean mortality showed differences, however, this mortality was less than 65%. It is important to continue testing other commercial inhibitors.
Introducción
Animales, plantas y microorganismos sintetizan proteínas específicas capaces de inactivar enzimas seleccionadas por medio de la formación de complejos estables enzima-inhibidor que han sido denominadas con el nombre genérico de inhibidores de proteínas (Samac et al. 1990; Whitaker 1980; Wolfson y Murdock 1987). Hasta el momento se han descrito cuatro tipos mayores de enzimas proteolíticas con base en la presencia de aminoácidos esenciales en el sitio activo o en el mecanismo de acción (Birk 1987; Whitaker 1980), estos grupos son: las serin-proteinasas, entre las que están las proteínas inhibidoras de tripsina, quimotripsina, elastasa y plasmina; las tiol-proteinasas, entre las que están los inhibidores de la papaína, la proteinasa streptococcal y la xathepsina B; las metalo-proteinasas como inhibidores de las carboxipeptidasas A y B y las aminopeptidasas; y las proteinasas ácidas que inhiben la pepsina, la renina y la penicilopepsina (Whitaker 1980).
Muchos tejidos de plantas pueden sintetizar diferentes tipos de inhibidores de proteínas. Los tubérculos de papa, por ejemplo, contienen al menos seis diferentes tipos de inhibidores de proteínas. Estos compuestos son termo-estables y pH-estables, en especial los de bajo peso molecular, y algunos son glicoproteínas (Whitaker 1980). Muchos de los inhibidores de proteínas mejor estudiados pertenecen al grupo de las serin-proteínas; estos interactúan con las enzimas por un mecanismo común denominado el mecanismo estándar (Birk 1987).
Se ha demostrado que heridas en las hojas de las plantas causadas mecánicamente o por un insecto, llevan a un incremento masivo en los niveles de inhibidores de proteinasas en el sitio de la herida y en los tejidos adyacentes (Birk 1987).
Algunas semillas, como soya y trigo, contienen inhibidores de crecimiento y de proteasas intestinales larvales, los cuales se han encontrado en insectos como Tribolium sp. y Tenebrio sp. (Coleoptera: Tenebrionidae), sugiriendo la posibilidad de que estos inhibidores están implicados en los mecanismos de defensa de las plantas contra los insectos (Applebaum y Birk 1972; Birk 1987). Las enzimas tripsina y quimotripsina han sido detectadas y parcialmente purificadas a partir de extractos del intestino medio de algunos insectos coleópteros, con propiedades muy similares a las que presentan estas enzimas en mamíferos (Crowson 1981).
Para demostrar que los inhibidores de proteinasas restringen el crecimiento y desarrollo de diversos géneros de insectos se han utilizados dietas artificiales que contienen los diferentes inhibidores de proteínas, y en las cuales se colocan a alimentar larvas del insecto (Christeller y Shaw 1989; Wolfson y Murdock 1987).
Al igual que con el gen de la 8-endotoxina del Bacillus thuringiensis Berliner, genes que codifican para un inhibidor de tripsina aislado a partir de fríjol y que es activo contra un amplio rango de insectos coleópteros y lepidópteros (Boulter et al. 1989), han sido utilizados para transformar plantas de tabaco, protegiéndolas contra el ataque de larvas del gusano de las yemas y otros insectos (Christeller y Shaw 1989; Hilder et al. 1987; McIntosh et al. 1990).
Muchas enzimas que posiblemente se encargan de disolver la cutícula de algunos insectos han sido aisladas de hongos entomopatógenos (St. Leger et al. 1986). Entre estas enzimas se encuentran las quitin-hidrolasas, las endo-quitinasas y la B-N-acetil-glucosaminidasa (exoquitinasa o quitobiasa) (El-Sayed et al. 1989). La quitinasa es una enzima que se ha demostrado es sintetizada por algunas especies de hongos, bacterias y plantas (Huber et al. 1991; Rodríguez-Kabana et al. 1983; Samac et al. 1990).
En el hongo Nomuraea rileyi (Farlow) Samson (Hyphomycetos) se lograron detectar altos niveles de actividad endo- y exo-quitinasa en dos aislamientos virulentos, pero no en un aislamiento avirulento donde los niveles de actividad fueron bajos (El-Sayed et al. 1989). En el hongo Beauveria bassiana (Bals.) Vuill. (Hyphomycetos) se ha logrado determinar que la quitinasa es una enzima inducible.
Otra forma en que pueden actuar las quitinasas sobre los insectos es por ingestión. El intestino de muchos insectos se encuentra recubierto por una membrana denominada membrana peritrófica, la cual está constituida principalmente por quitina (Brandt et al. 1978; Crowson 1981; Dow 1986; Wigglesworth 1972). Se ha demostrado que la membrana peritrófica del mosquito transmisor de la malaria es digerida por quitinasa aislada de la bacteria Serratia marcescens (Huber et al. 1991).
La adición de quitinasa en diversos ensayos ha aumentado la patogenicidad de diversos entomopatógenos como el baculovirus de la mariposa gitana, Lymantria dispar (L.) (Shapiro et al. 1987), y también de B. thuringiensis (Smirnoff 1971).
El objetivo a largo plazo es transformar plantas con el gen de la quitinasa para obtener plantas con resistencia total o parcial a la broca del café, Hypothenemus hampei (Ferrari) (Coleoptera: Scolytidae) (Vaeck et al. 1987). Plantas de tabaco ya han sido transformadas con el gen de la quitinasa aislado de fríjol, lográndose plantas resistentes al hongo patógeno Rhizoctonia solani Kuehm (Broglie et al. 1991).
Las dietas artificiales para la cría de insectos son importantes para desarrollar bioensayos con agentes químicos o biológicos que puedan ser usados para su control (Bustillo 1979). Mediante el uso de dietas artificiales es posible controlar la dosis del producto a evaluar, el tiempo de mortalidad de los insectos y la cantidad de producto ingerido por cada individuo.
El uso de dietas artificiales (Rexrode y Krause 1968; Schmidt 1966; Bautista-Martínez y Atkinson-Martín 1988; Villacorta y Barrera 1993) ofrece diferentes alternativas en la investigación sobre la broca del café tales como:
Conocimiento de la biología. Producción de parasitoides y depredadores. Ensayos de patogenicidad con entomopatógenos. Estudios fisiológicos para la selección de insecticidas, atrayentes y esterilizantes. Evaluación de productos promisorios para el control de la broca del café con inhibidores de proteinasas y quitinasas, endotoxinas de B. thuringiensis para la posible obtención por transformación de plantas resistentes a esta plaga (Smirnoff 1971).
Por medio de la biotecnología se han desarrollado metodologías orientadas a la incorporación de genes de resistencia dentro del genoma de varias especies vegetales (Weising et al. 1988). Algunos de dichos genes codifican para la síntesis de compuestos inhibitorios de proteasas como tripsina y quimotripsina, los cuales actuan a nivel del tracto digestivo degradando las proteínas, como parte del proceso alimenticio vital para su supervivencia. El efecto de los inhibidores de proteinasas sobre el crecimiento y desarrollo de los insectos se ha estudiado usando dietas artificiales. La biotecnología provee una herramienta adicional para el control de la broca del café y otras plagas de importancia comercial.
En este trabajo se estudió el efecto de inhibidores de proteinasas comerciales (Sigma) sobre el desarrollo de la broca del café criada en dieta artificial para seleccionar compuestos con actividad para un programa de transformación genética de la planta de café.
Materiales y Métodos
Se evaluaron tres inhibidores de tripsina (T9003, T9253, T9378), dos quitinasas (C1650, C6137) y un inhibidor tripsinaquimotripsina (T9777) en dosis de 1,0% y 0,1% (Tabla 1), en un diseño completamente al azar con un arreglo factorial 6x2+2. Se utilizaron huevos de la broca del café extraídos de café pergamino infestado. Cada tratamiento constó de 200 huevos. La unidad experimental la constituyó cuatro huevos colocados en 1 cmβ de dieta artificial con 50 repeticiones por tratamiento. La evaluación se realizó desde el momento de la eclosión del huevo hasta la emergencia del adulto a una temperatura de 28 ± 1°C y una humedad relativa entre 70-80%.
Con tal propósito se utilizaron dos recipientes diferentes: en uno se colocaron regletas de 25 cm de largo x 1 cm de ancho, dividida en compartimientos cada centímetro, en donde se ubicaron 4 huevos de H. hampei. Con esta metodología se evaluaron los tres inhibidores de tripsina con su respectivo testigo. Para los tratamientos con quitinasas y el inhibidor tripsina-quimotripsina se usaron vasos plásticos de 4 cm de alto y 3 cm de ancho, donde se colocaron dos discos de dieta por recipiente, cada uno con cinco huevos.
Resultados y Discusión
En la Tabla 2 se presenta la duración promedia del ciclo de vida de H. hampei para los inhibidores de quitinasa y el inhibidor tripsina-quimotripsina evaluados. Para obtener estas duraciones totales sólo se tuvieron en cuenta los insectos que llegaron al estado adulto y fueran hembras, las cuales presentan dos instares larvales.
Inhibidores comerciales (Sigma) evaluados por medio de su incorporación a una dieta artificial.
Duración de huevo a adulto de H. hampei para los inhibidores de quitina y el inhibidor de tripsina-quimotripsina evaluados con respecto al testigo.
* Promedios seguidos por la misma letra no difieren significativamente según la Prueba de Tukey al 5%.
Duración promedia de huevo a adulto de H. hampei para los inhibidores de tripsina evaluados con respecto al testigo.
* Promedios seguidos por la misma letra no difieren significativamente según la Prueba de Tukey al 5%.
En la Tabla 3 se presentan los resultados para los inhibidores de tripsina evaluados.
En cuanto a la duración del ciclo de vida de la broca del café no se presentaron diferencias significativas de los tratamientos en comparación con el testigo para las quitinasas y el inhibidor Bowman-Birk (T9771). Se encontró un mayor número de individuos sobrevivientes en los tratamientos evaluados en los recipientes plásticos (las quitinasas y el inhibidor Bowman-Birk) que con los inhibidores de tripsina evaluados en las cámaras de cría.
En cuanto a la duración de cada instar, igualmente se encontró que no habían diferencias entre los diferentes tratamientos. La Tabla 4 muestra la duración promedia para cada estado de H. hampei sometido a los diferentes tratamientos.
En la Figura 1 se presentan las mortalidades promedias de H. hampei con los inhibidores de quitinasa y el inhibidor tripsina-quimotripsina evaluados. A medida que aumenta la dosis, la mortalidad es mayor. Los incrementos en el porcentaje de mortalidad para estos tratamientos, entre la dosis 0,1 y el 1,0%, fue inferior al 10%. La mayor mortalidad se obtuvo con la quitinasa C6137 al 1,0% (51,40%), seguida por C1650 al 1,0% (43,25%) y para T9777 al 1,0% fue de 33,29%. En la dosis del 0,1%, los porcentajes de mortalidad fueron de 44,84, 42,57 y 25,61% para C6137, C1650 y T9777, respectivamente.
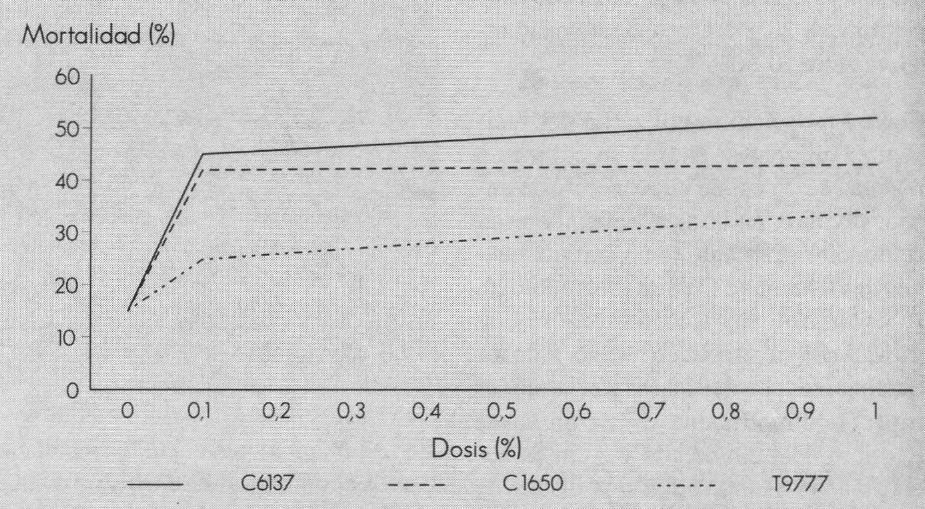
Mortalidad promedia de H. hampei obtenida con los inhibidores de quitinasa y el inhibidor tripsina-quimotripsina evaluados.
El análisis de varianza mostró que existen diferencias significativas entre los productos y las dosis empleadas en los diferentes tratamientos evaluados en el recipiente plástico.
La Figura 2 muestra las mortalidades promedias de H. hampei obtenidas con los inhibidores de tripsina evaluados (T9003, T9253, T9378). De igual forma, a medida que aumenta la dosis mayor es la mortalidad. Los incrementos en el porcentaje de mortalidad entre las dosis 0,1 y 1,0%, para estos tratamientos, oscilaron entre 10,19 y 21,33%. Con la dosis 1,0%, las mortalidades promedias fueron de 60,66, 57,66 y 47,69% para T9378, T9253 y T9003, respectivamente. Con 0,1%, los porcentajes de mortalidad fueron de 39,33, 43,00 y 37,50 para T9378, T9253 y T9003, respectivamente.
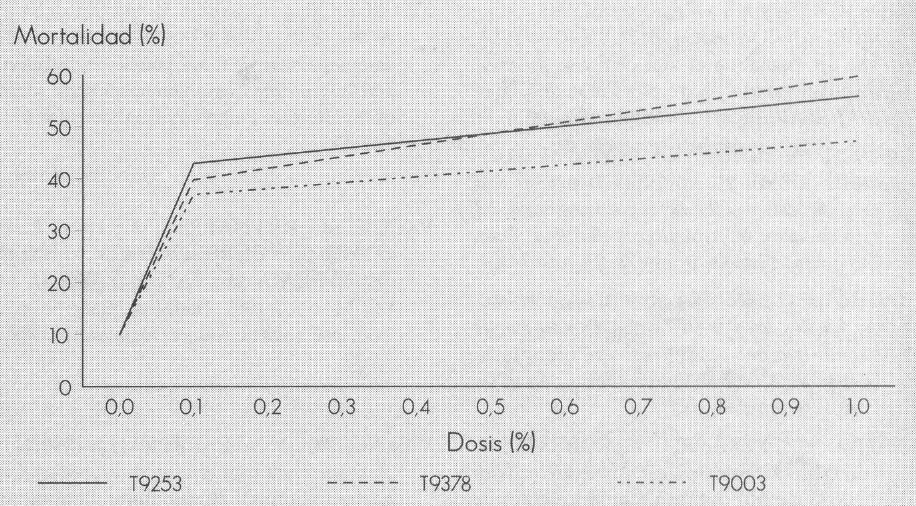
Mortalidad promedio de H. hampei obtenida con los inhibidores de tripsina evaluados.
El porcentaje de mortalidad para el testigo de los tratamientos evaluados en el recipiente plástico fue de 15,43% y para el testigo, evaluado en la cámara de cría, fue de 10,50%.
Por medio de una prueba de contrastes se compararon los porcentajes de mortalidad de todos los tratamientos con su respectivo testigo, encontrando diferencias para los tratamientos C1650, C6137, T9777, T9003 en ambas dosis y para T9378 al 0,1%, en comparación con su respectivo testigo.
En la Figura 3 se aprecia como no hay diferencias en cuanto a las dosis para los tratamientos con quitinasas. La mayor mortalidad se obtuvo con el inhibidor de tripsina T9378, con una mortalidad del 60,66% para 1,0%, seguida del producto T9253 con 57,66%.
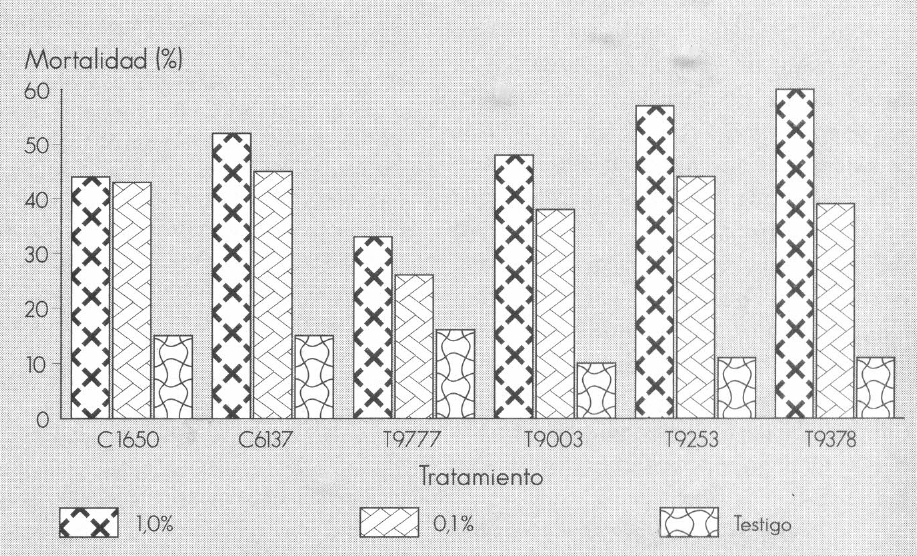
Mortalidad acumulada de H. hampei obtenida con los diferentes inhibidores comerciales evaluados.
Duración promedia de cada uno de los estados de la broca del café, H. hampei, sometidos a los tratamientos evaluados.
D.E. = Desviación estándar
Es importante evaluar otros inhibidores de diferente procedencia que pueden llegar a ser más eficaces y realizar la obtención de dichos inhibidores en plantas del trópico.
Footnotes
Agradecimientos
Los autores presentan sus agradecimientos a la Dra. Roxanne Broadway, Departamento de Bioquímica de la Universidad de Cornell, por el suministro de algunos inhibidores de proteinasas y al Dr. Bernardo Chaves, Disciplina de Biometría de CENICAFE por el análisis estadístico de los datos.
