Abstract
In the insects, odorant signals play an important role in the survival of the species. Cockroaches are gregarious insects. The approach of groups is assured by a gregarious pheromone which is secreted (in some species) by the jaw glands. These insects secret sexual pheromones which ensure the approach of both sexes and play an aphrodisiac role. In E. floridana, it's the male which emites a sexual pheromone exposing a caracteristic calling posture. This sexual pheromone emition by tergal glands allow the approach of both sexes: male and female touching their antennae, the male perceive, sometimes, a sexual contact pheromone present in the genital part of female or in her cuticular wax. The males exposes the tergal glands of abdominal tergites 2, 7 and 8. It shakes its body side to side. The mature female approaches the male and opens her genitalia. She mounts on the male and backs to lick the tergal secretions emited on tergite 1, where a tuft of setae can be seen. Finally, the male underneath the female, moves backwards, thrusting upward his abdomen and protuding its phallomere to make connection with the genitalia of the female. Histological studies of different glandular regions showed that glands which produce the pheromone are of type III. The structure of tuft of setae seems to be complex. The chemical identification reveals the presence of three principal compounds in the tergite 8: (2R-3R)-(-)butanediol, dodecanol and benzyl-2-hydroxybenzoate); and a principal compound in the tergite 7 the 2,2-dimethyl-4-hydroxy-3(2H)-furanone "furaneol". No compounds were identified in the tergite 2.
Introducción
Frecuentemente, las señales químicas guían al insecto hacia el sitio de oviposición o hacia las fuentes de nutrición. Igualmente, ciertas moléculas en suspensión en el medio ambiente permiten al insecto detectar su pareja, localizar sus depredadores o identificar sus congéneres. Según la extención de esta capacidad de detección, los insectos se dividen en dos grandes grupos. El primero esta contituido por insectos muy especializados en sus relaciones químicas con el medio ambiente: los insectos especialistas, como es el caso particular de los Lepidoptera.
El segundo gran grupo de insectos que poseen una sensibilidad química mucho más diversificada: son los insectos generalistas. Ejemplo: Los insectos sociales : (abejas, hormigas, termitas) y como las cucarachas que han conservado un modo de vida gregario similar en ciertos aspectos a la vida en sociedad organizada. Estas especies tienen generalmente una duración de vida larga (meses o años), mientras que los insectos especialistas viven menos tiempo (horas o días) (Masson y Brossut 1981).
Las cucarachas constituyen un ejemplo particularmente interesante de insectos con comunicaciones químicas múltiples y que al mismo tiempo conservan una alta sensibilidad hacia ciertas sustancias específicas. Estos insectos reconocen varias señales olfativas. Por ejemplo: las feromonas que aseguran la cohesión de los grupos, las feromonas gregarias, como en el caso de Blaberus craniifer, donde la feromona gregaria es una mezcla de undecano y de tetradecano (Tokro 1984). Otras son las feromonas que aseguran el acercamiento de los sexos, las feromonas sexuales, caso de Blatella germanica (L.), donde la feromona sexual es la 3,11-dimethyl-2-nonacosanone) (Tokro 1984; Abed et al. 1993), y éstas son responsables del aislamiento geográfico de las especies.
De otra parte, y según la especie, los métodos de defensa contra los depredadores son diferentes. Ciertas especies utilizan sustancias fuertemente repulsivas y tóxicas como es el caso de Eurycotis floridana Walker (Dyctyoptera: Blattidae) que posee una glándula esternal defensiva muy desarrollada que secreta (E)-2-hexenal con olor de chinche aplastada (Stay 1957) y que puede ser incluso alérgico para los humanos (Roth y Alsop 1978).
Parece ser que en las cucarachas, el gregarismo es una estrategia en la cual la comunicación química juega un papel fundamental. Todo ocurre como si el mantenimiento de una cierta cohesión de grupo las hubiera protegido contra el empobrecimiento de los sistemas de reconocimiento químico, favoreciendo la diversidad de intercambios. Seguramente por ello, aparecieron primero que el hombre, en el cuaternario, y seguirán existiendo cuando la vida humana se haya extinguido en el planeta.
Por esta razón, las cucarachas constituyen un útil material experimental que permite un análisis paralelo y comparado del reconocimiento de señales olfativas específicas y no específicas.
La escogencia de E. floridana, en este estudio, se hizo esencialmente porque esta especie posee glándulas exocrinas muy desarrolladas asociadas a sus tergitos abdominales y resulta un insecto ideal para el estudio de la química de los productos secretados y también para el estudio del comportamiento sexual.
Revisión de Literatura
E. floridana pertenece a la sub-familia Polyzosteriinae que cuentan con 181 especies repartidas en cinco géneros: Eurycotis, Methana, Polyzosteria, Platyzosteria, Melazosteria (Cornwell 1968).
E. floridana, conocida en inglés como Florida woodroach, es originaria de las regiones tropicales del sur de los Estados Unidos, y vive también en los estados de Georgia y Mississippi. En estas regiones constituye un verdadero insecto dañino, ya que se ha adaptado a la vida en las casas y apartamentos (Barth 1968).
Es una cucaracha aptera, gregaria, que mide entre 30 y 40 mm de largo y 10 mm de ancho; de color rojizo-marrón (David-Henriet 1993). Esta especie vive en pequeños grupos en madera seca (Stay 1957), en las fibras de palmeras, bajo las hojas en descomposición, en las cavidades de rocas calcáreas y también en interiores domésticos.
E. floridana presenta siete instares ninfales en los machos y ocho en las hembras. La duración de cada instar es de 3 a 4 meses según las condiciones de cría. La hembra es ovípara y la ooteca se queda en la cavidad incubatriz durante una semana antes de la oviposición. La eclosión de 18 a 20 ninfas se efectua 2 a 3 meses más tarde. Las condiciones de cría juegan un papel importante sobre la reproduccción y la duración del desarrollo (David-Henriet 1993).
Materiales y Métodos
Las cucarachas se criaron en acuarios de vidrio (40 X 25 X 25 cm). El alimento fue bizcochos para perro, los cuales se suministran en un algodón húmedo; y cajas de huevos sirvieron como abrigo. La temperatura de cría fue de 28+ 2°C, la humedad relativa osciló entre 70 y 80% y el fotoperíodo fue 12:12.
Con el fín de observar los orificios glandulares y determinar el número presente sobre los tergitos, las cucarachas se disecaron y luego se trataron por 24 horas con una solución de potasa al 20% hasta la eliminación completa de los músculos y del cuerpo graso. Las piezas fueron enseguida deshidratadas con baños progresivos de etanol (de 70° hasta 100°) durante 24 horas. Después de 2 baños de tolueno por 2 horas, las piezas se montaron en placas con bálsamo de Canadá.
Para las observaciones en un microscopio electrónico JSM-35CF scanning, microscope JEOL, los tergitos se disecaron e introdujeron en etanol; luego se limpiaron al ultrasonido durante 5 minutos, se deshidrataron y después se pegaron sobre una platina de aluminio. Estas fueron luego recubiertas de una fina capa de oro por sublimación al vacío.
Para los estudios histológicos, los tergitos de los machos fijados al Bouin alcohólico o Duboscq-Brasil (Gabe 1968), se trataron por los métodos clásicos de la histología (Martoja y Martoja Pierson 1967). Los pedazos fueron inmediatamente incluidos en parafina (3 baños de 24 horas a 56°C). Se realizaron cortes de 7 um de espesor con la ayuda de un microtomo.
La coloración utilizada fue el tricromo de Masson, variante de Goldner. Después de la deshidratación (etanol a 95°, 100° y tolueno), los cortes se montaron en placas usando bálsamo de Canadá. Se efectuaron diferentes medidas sobre los epitelios glandulares con la ayuda de un microscopio dotado de un micrómetro.
Pruebas de comportamiento
Todas las pruebas biológicas se efectuaron bajo luz roja en las primeras horas de la escotofase, bajo una temperatura constante de 28° ± 1°C. Se estableció una humedad relativa cercana al 70%. Así, en este recinto cerrado, y con el fín de probar el efecto etológico de la feromona del macho sobre la hembra, se depositaron diferentes concentraciones de la feromona con una microjeringa Hamilton sobre un papel de filtro de 2 cm2. Después de la evaporación del solvente, se colocó el papel de filtro en un sitio opuesto a aquel donde se encontraba el insecto. El testigo estuvo constituido por papeles de filtro tratados con el solvente (1 µl de CH2Cl2 solvente / testigo).
Los diferentes estímulos químicos fueron los principales constituyentes de la feromona sintética del macho. Estos extractos correspondieron a concentraciones de: 10−11,10−10, 10−9, 5 X 10−9, 10−8, 5 X 10−8, 2 X 10−7, 10−7, 5 X 10−7, 10−6 de (2R3R)-(-)-butanediol, dodecanol y 2,5-dimethyl-4-hydroxy3(2H)-furanone («fureneol»)
El parámetro más importante medido fue el «tiempo de contacto» o sea el tiempo utilizado por el insecto macho o hembra al tocar con sus antenas el papel impregnado de la muestra.
Con el fin de describir las diferentes secuencias del comportamiento sexual, en un recinto privado se introdujo un macho virgen, 10 minutos antes del comienzo de la observación. Una hembra virgen se introdujo luego en el mismo recinto. Se anotó el comportamiento del macho y de la hembra durante 15 minutos. Se observaron 300 machos, y se les impidió la cópula con el fín de guardar los individuos vírgenes, y 500 hembras. Para detallar las fases de comportamiento se recurrió a la CCTV Cámara Hitachi con el fín de volver a observar las secuencia en cámara lenta y a partir de estas observaciones describir un etograma.
Este ensayo sirvio igualmente para conocer el comienzo de la madurez sexual de los individuos machos y hembras, y a partir de las observaciones se pudieron definir las edades exactas durante las cuales aparecen las posiciones precopulatorias características de la hembra y del macho. Estas posiciones indicaron la madurez y la receptividad sexual de cada individuo.
Se observó el comportamiento de llamada de los machos aislados desde la muda imaginal, repitiendo el experimento dos veces durante 24 horas. Se utilizaron 73 machos de edades diferentes. Las edades variaron de 9 a 71 días. Los individuos aislados se observaron cada media hora.
Feromona sexual del macho
Para la preparación de los extractos, los individuos se anestesiaron el frío (-20°C) y se disecaron rápidamente. Los tergitos abdominales 2, 7 y 8 se sumergieron en un frasco con diclorometano destilado. Después de una hora de maceración, a temperatura ambiente, los extractos se filtraron en lana de vidrio con el fín de eliminar todas las partículas sólidas.
Los extractos se concentraron por microdestilación, según el método Kudernat-Danish (Marquardt y Luce 1961), y después se llevaron a un volumen conocido por evaporación bajo flujo de nitrógeno con el fín de conocer la concentración de los extractos probados. Se estimó el equivalente tergito (Eq T) o sea la secreción feromonal contenida en los tergitos evaluados en el macho. Por razones prácticas, poca cantidad de insectos disponibles, en los ensayos biológicos se utilizaron solamente los productos equivalentes de origen industrial (feromonas sintéticas).
Las muestras de los extractos se analizaron por cromatografía en fase gaseosa. El cromatógrafo utilizado fue un PACKARD 437A equipado con una columna capilar en silicio fundido de tipo polar CPWax 58 CB (25 m x mm de diámetro interno, Crompack). La temperatura del horno estuvo programada de la manera siguiente: 40°C durante 2 minutos, permaneciendo a 20°C durante 1 minuto, después 2°C/ min hasta llegar a 220°C. La temperatura del inyector y del detector fueron de 270°C y de 290°C, respectivamente. El gas vector fue hidrógeno (3ml / min). La inyeccción es en split-splitless (escape cerrado durante 30 segundos, después de la inyección). La señal se grabó en un micro-computador SHIIMADZU CR 4A. La técnica de captura de diferentes compuestos estudiados se utilizó con el fín de determinar la naturaleza química del 5-methyl-4hydroxy-3(2H) furanone, aunque aquí sólo se describe la respuesta etológica de los insectos al otro tautomero: el 2,5-dimethyl-4-hydroxy-3(2H) furanone («furaneol»), que presenta un fuerte olor a caramelo y que se puede encontrar de manera sintética en el mercado.
Resultados
Morfología de las glándulas Exocrinas tergales
Durante el comportamiento sexual del macho de E. floridiana intervienen glándulas tergales: las glándulas tergales situadas sobre la parte medial del tergito abdominal 1 y las situadas sobre la parte anterior de los tergitos abdominales 2, 7 y 8. Las glándulas de los tergitos 8 y 1 son específicas al macho, mientras que las glándulas tergales 2 y 7 están presentes también en las hembras.
Glándula del tergito 1
La región anterior de la parte central del tergo 1 esta ocupada por un montículo sobre el cual se observa un mechón de setas (Fig. 1). Esta formación había sido observada por Brossut y Roth (1977).

Vista general del montículo con setas situado en el centro de la primera tergito. Escala: 200 µm.
Se observó que el montículo tiene un diámetro de 500 µm en la base. Las setas son muy numerosas (casi 2.000), y están espaciadas a una distancia mediana de 12 μm (Fig. 2).
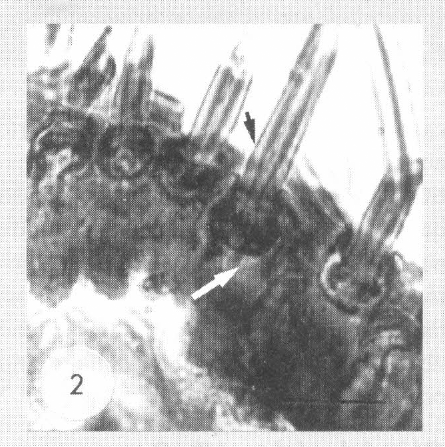
Corte histológico de la base de las setas articuladas. Cada seta penetra en una cúpula articular (pequeña flecha negra). Un canal atraviesa toda la cutícula (flecha blanca). Escala : 25 μm.
La histología y la microscopía electrónica muestran que estas setas son articuladas. El aspecto de las setas hace pensar en mecanoreceptores.
En el trabajo de histología se observó, debajo de la cutícula, un macizo espeso pluriestratificado de células glándulares. Este tiene un espesor de 300 µm. El montículo tiene una superficie de 0,25 mm2. Las células glandulares presentan numerosas vesículas claras y todas poseen una canalícula. Estas células son unidades glandulares de tipo III, compuestas de una célula de canal y de una célula glandular que tiene un aparato terminal (Noirot y Quennedey 1974; 1991).
Los cortes longitudinales muestran la existencia de dos regiones histológicamente diferentes: una constituida de células glandulares y vesículas claras, en la cual las canalículas salen por haces en la parte anterior del montículo, y otra región constituida por células con citoplasma denso que podrían ser el cuerpo celular de neuronas asociadas a los mecanoreceptores. Las Figuras 3 y 4 muestran la importancia y, al mismo tiempo, la complejidad de las estructuras asociadas al montículo con mechón de setas.
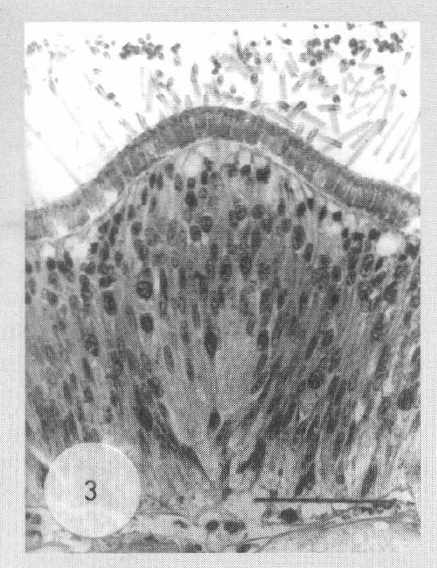
Detalle del montículo con setas. El epitelio glandular es estratificado. Escala: 40 µm.
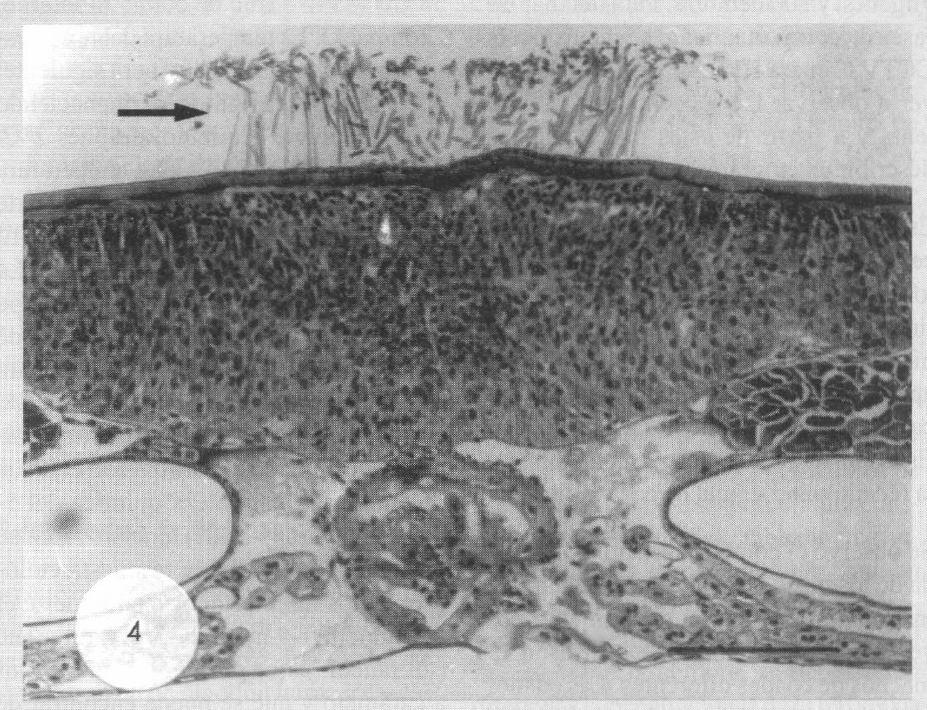
Corte transversal del tergito 1, donde la zona glandular es la más gruesa (parte trasera del montículo). Las setas son todavía visibles (flecha negra). Escala: 100 µm.
Glándula del tergito 2
Esta glándula forma una capa uniestratificada (células de tipo III). En la base se observan células con citoplasma más denso, que son enocitos epidérmicos. Bajo la cutícula, de más o menos 30 µm de espesor, se observan pequeños núcleos correspondientes a aquellos de las células epidérmicas achatadas y de las células de canalícula (Fig. 5).
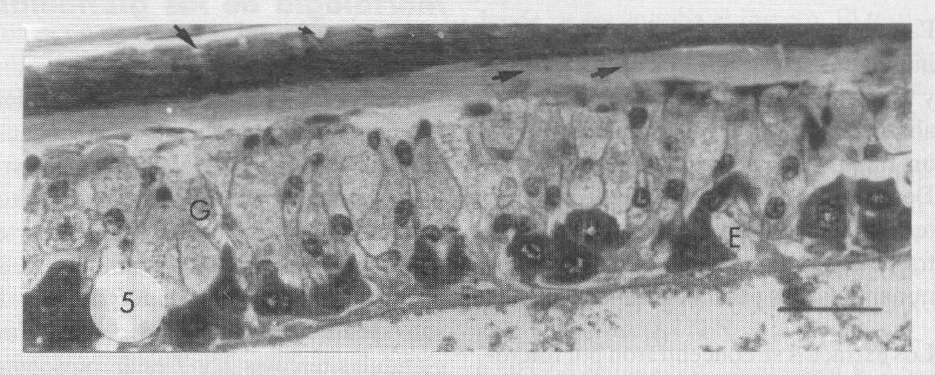
Epitelio glandular del tergito 2. La cutícula presenta numerosos orificios glandulares (pequeñas flechas negras en la parte superior de la foto). Se observa una capa de células glandulares (G) con citoplasma claro. Los canalículos conductores son visibles (pequeñas flechas negras) a nivel de la cuticula post-exuvial más clara. Las células basales con citoplasma denso y núcleos gruesos corresponden a los enocitos (E). Escala: 25 μm.
Glándula del tergito 7
En la región anterior del séptimo tergito se observan cuatro zonas cubiertas, correspondientes a dos regiones glandulares. Dos zonas cubiertas, donde las depresiones cuticulares son menos densas (6.000 por mm2) están situadas de una y otra parte del eje del cuerpo, y dos zonas cubiertas más alargadas, situadas lateralmente, con una densidad de depresiones cuticulares más densa (13.000 por mm2). La microscopia electrónica muestra que del fondo de cada depresión salen, en promedio, tres células glandulares (Fig. 6).
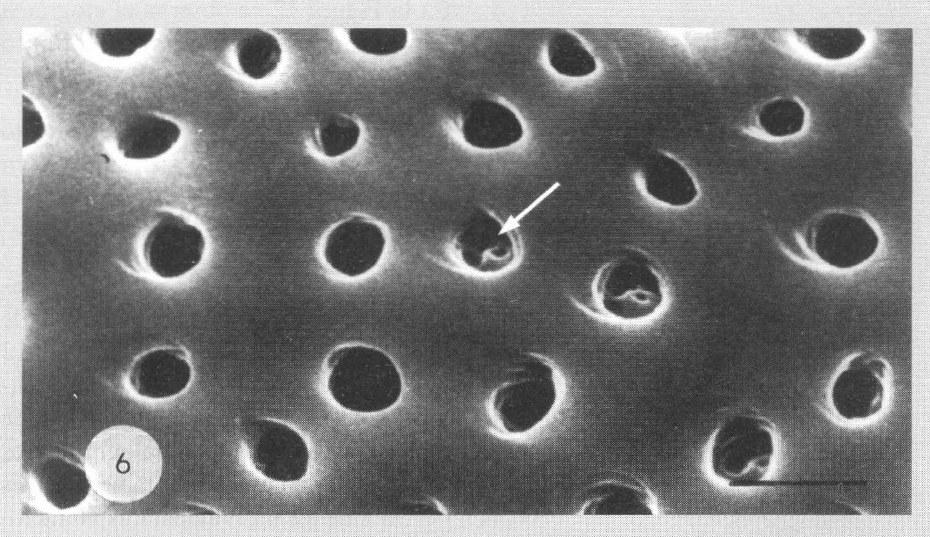
Depresiones cuticulares sobre el tergito 7. En cada depresión salen en promedio 3 orificios glandulares (flecha blanca). Escala: 10 μm.
Glándula del tergito 8
Esta glándula presenta la misma histología del tergito 7. El epitelio glandular es grueso: 300 µm (Fig. 7). La glándula no forma una capa uniestratificada, pero al contrario un montón donde las células están repartidas sobre numerosos estratos a causa de su abundancia. El citoplasma presenta un aspecto floculento y las canalículas receptoras son visibles. La cutícula presenta cavidades redondas correspondientes a las depresiones observadas en microscopía electrónica y parecidas a las que se observan sobre los tergitos 2 y 7 (Fig. 8).
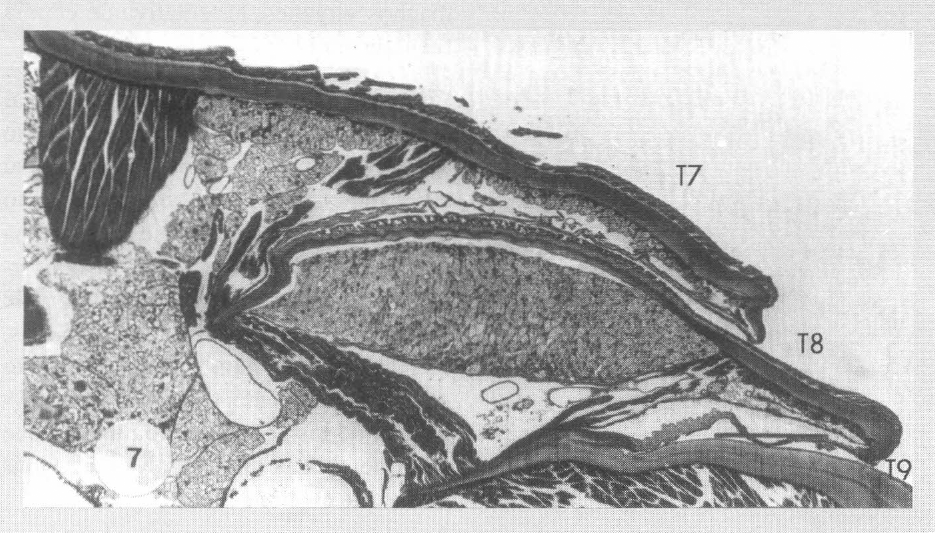
Corte longitudinal de la extremidad abdominal mostrando los tergitos 7 (T7), 8 (T8) y 9 (19) imbricados el uno en el otro. La glándula del tergito 8 está recubierta enteramente por el tergito 7. Escala: 200 µm.
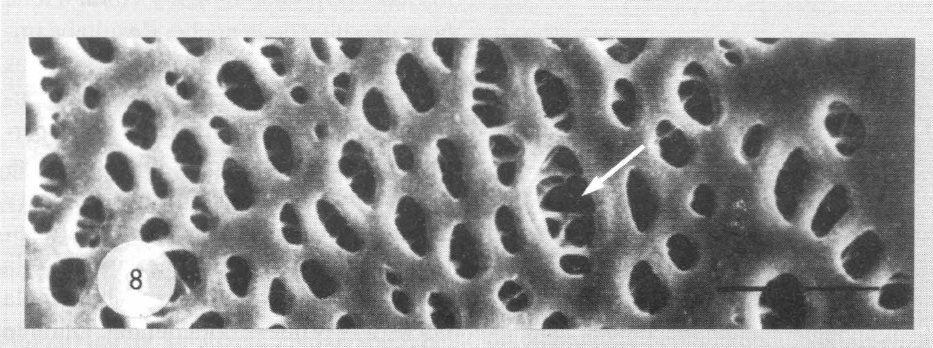
En el tergito 8 se observa en el microscopio electrónico, que al fondo de las depresiones cuticulares (flecha blanca), salen de 3 a 8 orificios de los canalículos de las glándulas secretroras. Escala : 20 µm.
Comportamiento Sexual
En E. floridiana es el macho el que inicia el comportamiento sexual. Atrae a la hembra adoptando una posición de llamada característica, exponiendo el abdomen y mostrando las partes anteriores de los tergitos 2 y 8 (Fig 9).
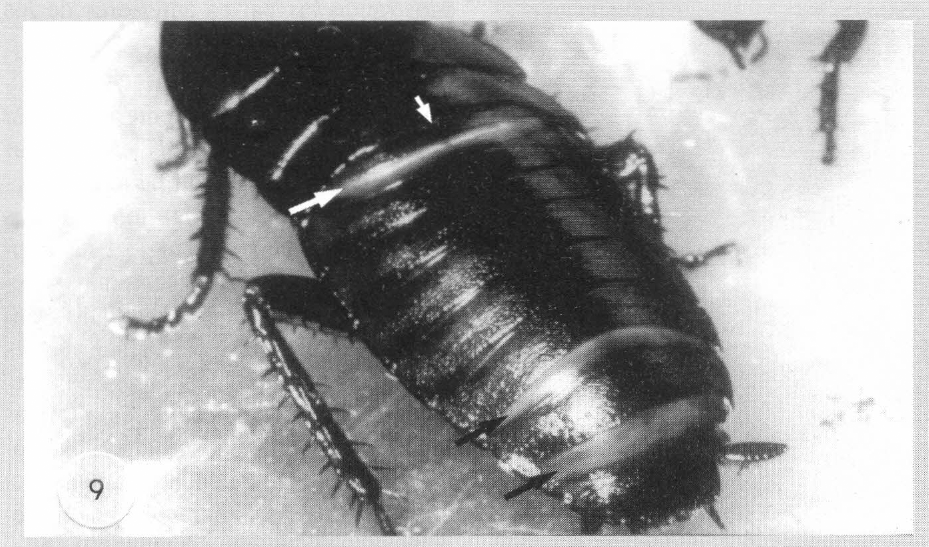
Durante el comportamiento de llamada el macho muestra, sobretodo, la parte anterior de los tergitos 2 y 8 (flechas negras). Si la hembra se demora en responder, la excitación del macho aumenta y éste muestra igualmente la parte anterior del tergito 7 (flecha negra). Cuando el macho ha percibido la presencia de una hembra, éste adopta la posición de parada, el abdomen completamente estirado, hace aparecer el montículo con setas situadas en el centro del tergito 1 (pequeña flecha negra).
La hembra receptiva se siente atraída por el macho. Esta atracción se expresa por un comportamiento exploratorio más activo y un aumento de los movimientos antenales («antennal fencing»). Esta adopta simultáneamente una postura característica: su atrio genital se abre y las glándulas, normalmente incluidas, son visibles (glándulas atriales). Esta posición sugiere la producción de mediadores químicos en la hembra como respuesta a la percepción del macho. La hembra mantendrá el atrio genital abierto durante todas las secuencias precopulatorias (Fig. 10).
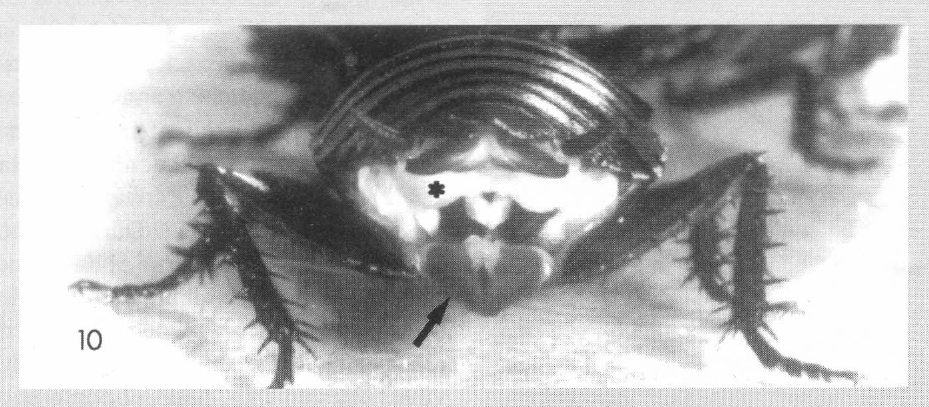
Cuando la hembra percibe la feromona sexual del macho, ésta abre ampliamente sus válvulas genitales (flecha negra). Las glándulas atriales se vuelven visibles (asterisco). La hembra conservara esta posición durante toda la duración del comportamiento precopulatorio.
Estas secuencias parecen una verdadera comunicación química: el macho emite primero una feromona sexual y la hembra responde a este estímulo liberando su feromona.
El macho identifica la presencia de la hembra después del contacto antenal. Expone de nuevo sus glándulas tergales y dirige la extremidad de su abdomen hacia la cabeza de la hembra. Este comportamiento se llama: "la parada". Durante este comportamento, el tergito 7 es bien visible y es posible percibir un fuerte olor de caramelo. El macho puede quedarse en esta posición más de una hora y puede vibrar lateralmente, hasta el punto que estas vibraciones adquieren un ritmo.
La hembra monta sobre el macho (Fig. 11) y comienza a lamer las secreciones tergales, yendo de la parte posterior hacia la parte anterior del abdomen; mientras tanto su atrio genital continúa abierto. La hembra termina de lamer al macho a nivel del tergito 1, en el medio del cual se encuentran los pelos del mechón. Este comportamiento aumenta la excitación del macho que saca su falomero y engancha los genitales de la hembra. Esta efectua una rotación de 180°C y el acoplamiento se realiza y se continúa en posición opuesta. La cópula finaliza cuando el macho ha depositado su espermatoforo en la espermateca de la hembra. El acoplamiento puede durar entre 1 hora y media y 2 horas.

El macho exhibe su comportamiento de parada y la hembra monta sobre su abdomen para lamer las secreciones tergales.
En la Figura 12 se observa el etograma correspondiente al comportamiento sexual de esta especie.
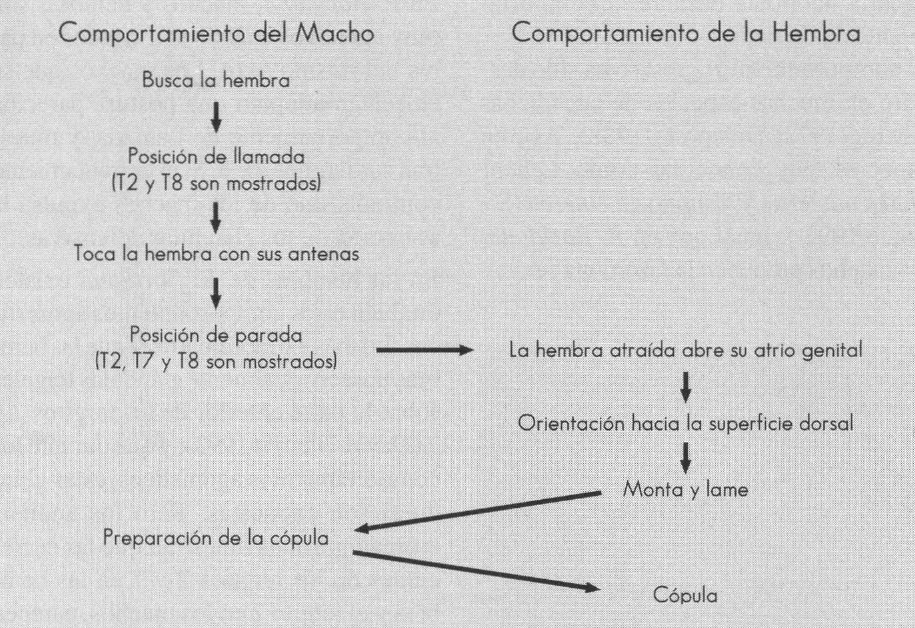
Etograma correspondiente al comportamiento sexual de Eurycotes floridiana.
Las observaciones del comportamiento sexual permitieron precisar la edad (en días) en la cual la madurez sexual del macho y de la hembra aparece.
La Figura 13 muestra que desde el octavo día de la muda imaginal, el 50% de machos exponen su tergito 8. El tergito 2 es expuesto por más del 50% de los individuos siete días después de la muda imaginal. La exposición del tergito 7 es muy variable y concierne raramente a más del 30% de los individuos. Las vibraciones aparecen desde el cuarto día de la muda imaginal. Diez días después de la muda imaginal, el 50% de los machos intenta copular (con el fín de conservar los machos virgenes, la tentativa de cópula fue interrumpida).
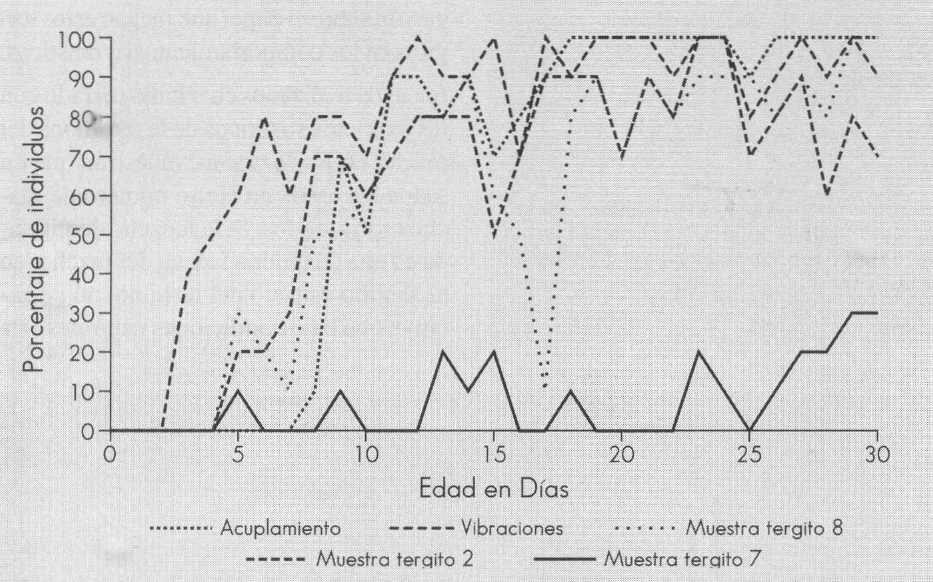
Respuesta de los machos delante de las hembras antes y después de la aparición de la madurez sexual. En el eje de la variable X, se encuentra la edad de los machos y en el eje de la variable Y, el porcentaje de machos que exponen sus glándulas presentes en los tergitos 7, 2 y 8, y también el porcentaje de machos que vibran. Al mismo tiempo se observan el porcentaje de machos que intentan copular.
En lo que se refiere a la madurez sexual de la hembra (Fig.14), desde el noveno día, el 50% de las hembras puede abrir su atrio genital, pero este comportamiento no es sistemático y no está seguido de una tentativa de cópula (con el fín de conservar las hembras virgenes la tentativa de cópula fue interrumpida). Al los 25 días, el 100% de las hembras abre su atrio genital y el 70% intenta copular y el 100% a partir de los 26 días. Esto muestra que en la hembra la madurez sexual es más tardía que en el macho.
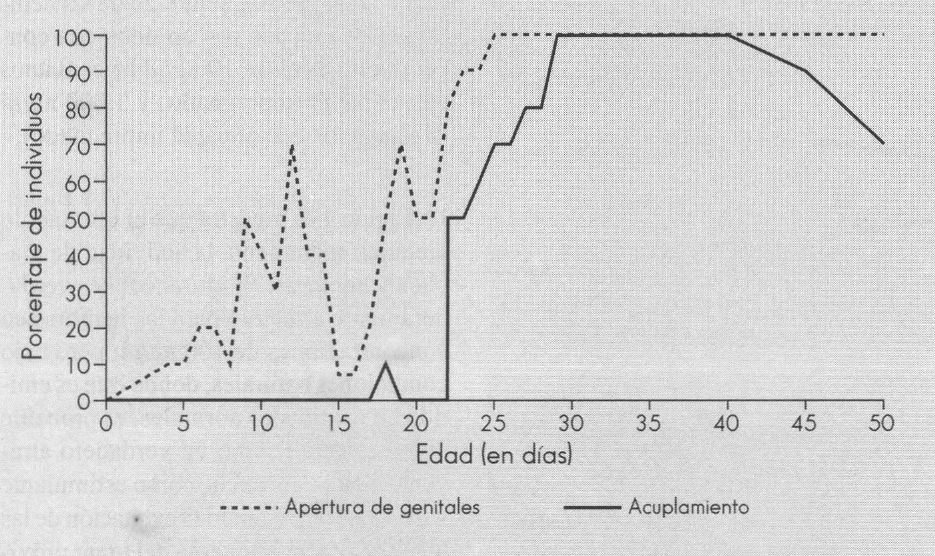
Respuesta de las hembras delante de los machos antes y después de la aparición de la madurez sexual. En el eje de la variable X, se encuentra la edad de las hembras y en el el eje de la variable Y, el porcentaje de hembras que exponen su atrio genital y también el porcentaje de hembras que intentan copular.
Comportamiento de Llamada
En observaciones preliminares se vió que los machos podían llamar y vibrar a toda hora del día y de la noche. Resultaba importante entonces determinar si estos comportamientos seguían un ciclo regular. Observaciones durante 24 horas permitieron constatar que los machos llamaban, sobretodo durante la escotofase (y al principio de la fotofase), particularmente durante dos períodos: de la sexta a la octava hora y de la undécima hora de la noche a la primera hora del día. Durante estos dos períodos, más del 50% de los machos presentaba el comportamiento de llamada. A partir de la sexta hora de la noche y hasta la vigésima hora del día se observan siempre el 40% de los machos en posición de llamada. El 20% de los machos permanece todo el tiempo en posición de llamada (Fig. 15).
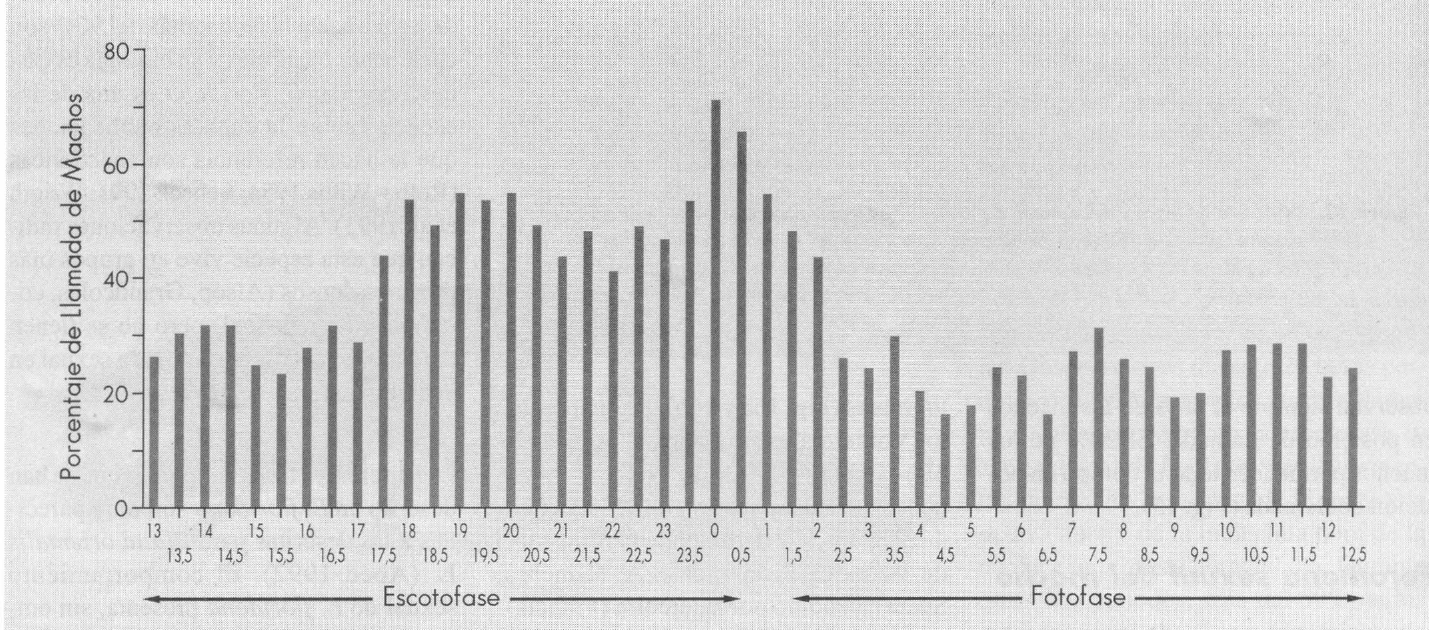
Comportamiento de llamada de 71 machos de Eurycotis floridana durante 24 horas. Se observan dos picos de actividad durante el período de la noche (escotofase).
Feromona sexual del macho
Los análisis de los productos volátiles secretados por los diferentes tergitos de los machos mostró los siguientes cromatogramas (Fig. 16a y 16b). Los compuestos comerciales probados fueron: (2R3R)-(-)butanediol de la Pfaltz y Bauer, dodecanol de Interchim y el 2,5-dimethyl-4-hydroxy-3(2H)-furanone («furaneol») de la marca Firmenich S.A. (Ginebra, Suiza), vendido por Interchim (Francia). Los resultados obtenidos con estos compuestos se indican en las Figuras 17a, 17b y 17c.
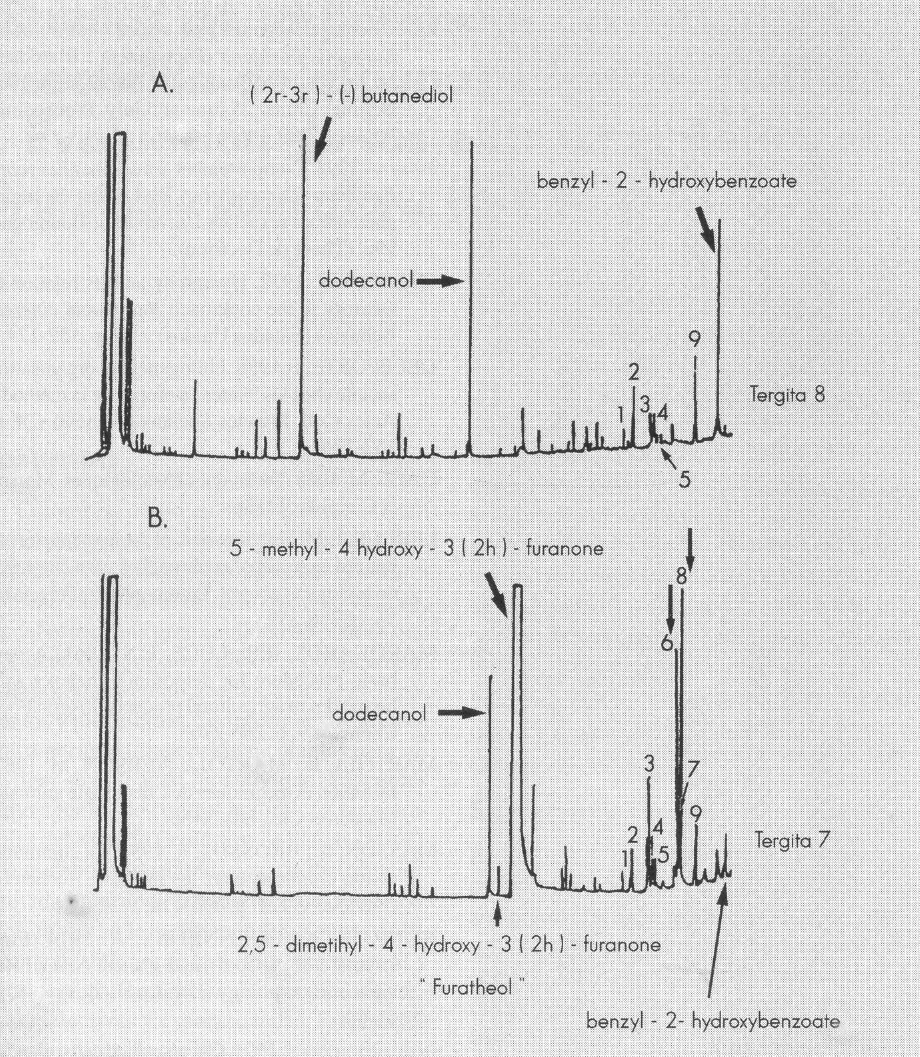
Cromatogramas obtenidos a partir de extractos de los tergitos 7 y 8 de machos de Eurycotis floridana. Condiciones :columna capilar en silicio fundido CP Wax 58 CB (25m X 0,25mm de diámetro). Temperatura: 4-22°(2°c/min). Gas vector: Hidrógeno. Figura 16a: Productos volátiles más importantes secretados por el tergito 8 del macho. Figura 16b: Productos volátiles más importantes secretados por el tergito 7 del macho.
Como lo muestra la Figura 17a, los ensayos efectuados con diferentes concentraciones de dodecanol sintético disminuyen la actividad de los machos, pero incrementa la actividad de las hembras (que tocan con sus antenas el papel filtro impregnado).
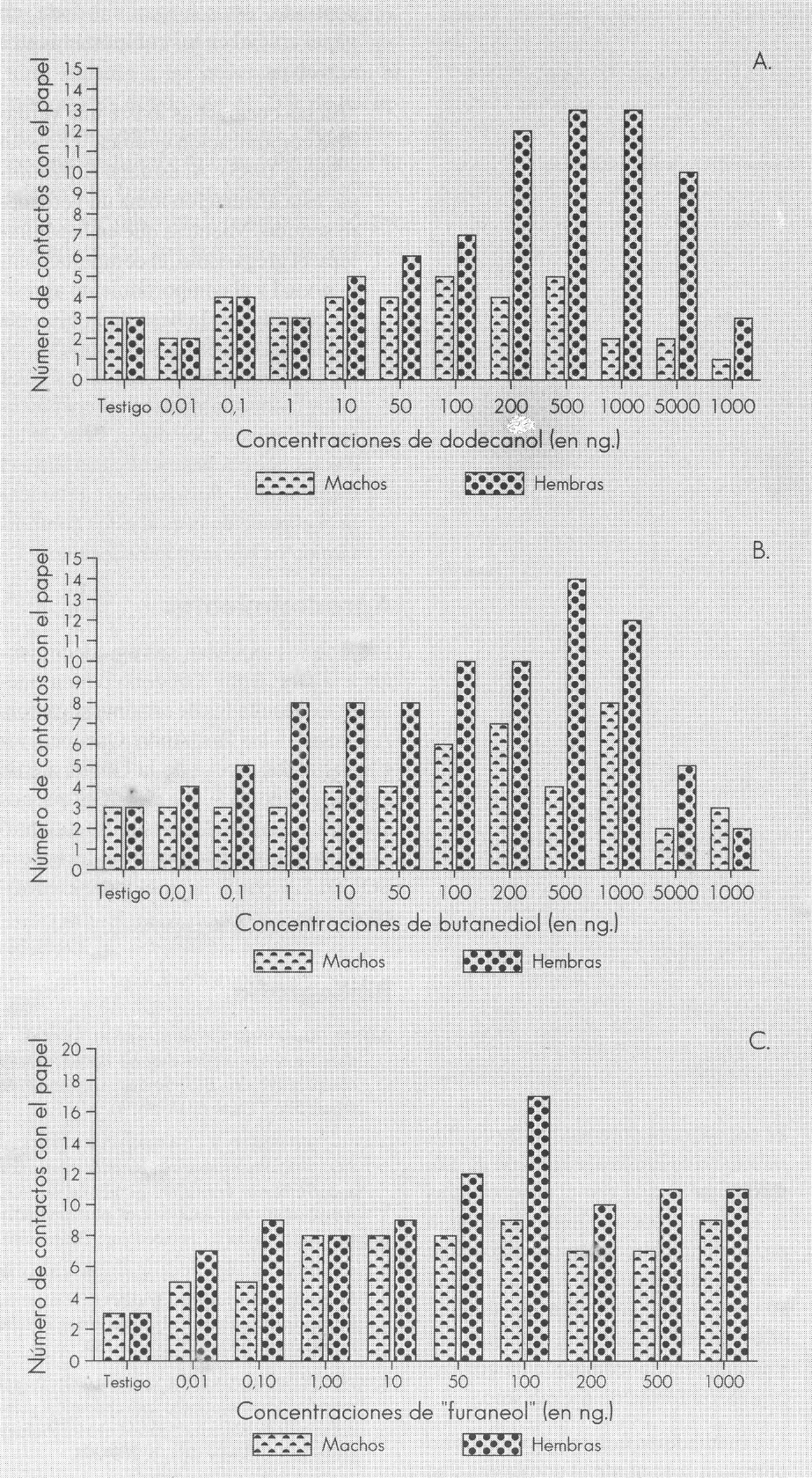
Resultados obtenidos con los compuestos sintéticos de la feromona sexual macho. Figura 17a: Actividad del dodecanol sintético, probado sobre machos y hembras. Figura 17b Actividad del (2R-3R)-(-)-butanediol sintético, probado sobre machos y hembras. Figura 17c: Actividad del 2,5-dimethyl-4-hydroxy3(2H)-furanone «furaneol» sintético, probado sobre machos y hembras.
En la Figura 17b, las diferentes concentraciones de (2R-3R)(-)-butanediol sintético incrementan la actividad de las hembras. Los machos son atraídos con concentraciones entre 10 ng/µl (4 contactos con el papel impregnado) y 1.000 ng/µl (8 contactos con el papel impregnado).
La Figura 17c muestra que el «furaneol» sintético incrementa la actividad de machos y hembras. El «furaneol» es verdaderamente atractivo para las hembras en concentraciones de 100 ng/ul; pero bajo condiciones naturales, donde este es emitido en cantidades normales, es probable que éste actue como un verdadero atrayente a corta distancia, como estimulante sexual, incrementando la excitación de las hembras y previniéndola del lugar próximo donde se encuentra el macho.
Discusión
Sobre las 4.000 especies de cucarachas descritas hasta la fecha, más del 90% son cucarachas tropicales y su biología es casi desconocida. E. floridana es una de las especies sobre la cual las publicaciones que le hacen referencia son anecdóticas (Roth y Willis 1954; Lebeck 1991; Wrigth et al. 1991). Algunas observaciones indican que esta especie vive en grupos más o menos densos (Alsop, Grandcolas, comunicación personal) pero no se tienen datos sobre el comportamiento sexual en el medio natural.
Las diferentes fases etológicas que se han descrito en E. floridana son muy parecidas a las descritas para Blatta orientalis L. (Abed 1992). El comportamiento sexual de E. floridana presenta, sin embargo, aspectos que no se encuentran en otras especies estudiadas (David-Henriet y Farine 1992).
La falta de observaciones sobre el comportamiento de llamada en un medio natural sumado a las observaciones en el laboratorio, donde casi el 25% de los individuos observados llaman a todas horas, queda difícil explicar, solamente si se admite que frente a un ambiente artificial éstos desarrollan una hiperagresividad que se traduce por una postura comparable a aquélla adoptada durante el comportamiento de llamada.
El comportamiento agresivo ha sido descrito en muchas especies de cucarachas (Ewing 1972; Deleporte 1988). Así, en especies muy conocidas como Leucophaea maderae y Nauphoeta cinerea (Sirugue 1992), igual que en E. floridana, los machos producen la feromona sexual. En E. floridana, machos y hembras son muy agresivos cuando son criados en pares del mismo sexo. Los machos que se enfrentan adoptan una postura parecida al comportamiento de llamada, y muestran sus tergitos 2 y 8. Si el enfrentamiento continúa, uno de los machos expulsa la secreción de sus glandulas defensivas.
En las hembras de E. floridana existen también estos comportamientos agonísticos. Lo más extraordinario es que las hembras poseen igualmente glándulas tergales sobre la parte anterior de los tergitos 2 y 7 (David-Henriet 1993), y que durante los comportamientos agonísticos, estas glándulas son expuestas. Pero los análisis cromatográficos muestran que las secreciones de los tergitos 2 y 7 en las hembras y el tergito 2 en los machos, parecen desprovistas de todo producto volátil en el sentido cromatográfico del término. Existe entonces un gran punto de interrogación sobre el papel que juegan estos tergitos en los comportamientos agonísticos.
Ensayos realizados en recinto cerrado con los extractos sintéticos de la feromona del macho de E. floridana, muestran que en todos los casos un cierto número de machos son atraídos. Si la mezcla identificada es una feromona sexual del macho, en el sentido estricto del término, no se excluye que bajo condiciones naturales esta feromona pueda tener dos acciones sucesivas: primero como feromona gregaria y luego como feromona sexual,
Conclusiones
El caso de E. floridana confirma que contrariamente a muchos otro grupos de insectos como los lepidópteros, donde las feromonas sexuales están compuestas de mezclas de moléculas vecinas (alcoholes, acetatos, esteres) o donde el porcentaje respectivo de cada constituyente dentro de la mezcla es el que asegura la especificidad, las cucarachas fabrican moléculas originales y complejas.
El comportamiento sexual de E. floridana no se limita a la emisión de una feromona sexual por el macho, pues la hembra responde inmediatamente produciendo otra feromona sexual. Si las feromonas emitidas por el macho son productos que le son específicos, ellos atraen igualmente a otros machos y promueven la formación de grupos, una cierta forma de gregarismo.
Los mediadores químicos volátiles no permiten solamente el comienzo y el control de los comportamientos observados, son los mediadores químicos no volátiles, percibidos únicamente por contacto, que van a permitir al macho reconocer el congenere reencontrado, estos juegan sin duda, un papel crucial en los comportamientos agresivos.
En las cucarachas existe una verdadera comunicación química" (Brossut y Sreng 1985). Al estudiar E. floridana, esta afirmación toma un verdadero sentido. Mientras que en la naturaleza, el gregarismo, el comportamiento sexual y el comportamiento agresivo constituyen la base de la biología de las cucarachas y son simultaneas; en el laboratorio es posible estudiar estos comportamientos independientes los unos de los otros. Pero de todas las cucarachas estudiadas hasta el día de hoy, E. floridana es ciertamente la especie en la cual estos comportamientos son muy indisociables.
Footnotes
Agradecimientos
Los autores expresan sus agradecimientos a la Dra. Ruby Londono por su interés en los resultados de esta investigación. Así mismo a los Drs. Andre Quennedey y Christian Bordereau de la Université de Bourgogne por la ayuda científica que nos aportaron durante los tres años que duró nuestra investigación. Igualmente a SOCOLEN por aceptar el valor científico de este trabajo.
