Abstract
The fungus Metarhizium anisopliae has been found attacking white grubs (Coleoptera: Scarabaeidae) under natural conditions in Antioquia, Colombia. This fungus has a great potential as a biological control of the white grubs, because it attacks all the developmental stages of the insect. Its easy multiplication on rice allows its production at the farm level. However, its survivorship capacity when it has to compete with the most comnon agrochemicals used in the region is unknown. For this reason, an experiment was carried out in order to evaluate the effect that over the growth and sporulation of the fungus M. anisopliae have some fungicides (fentin hidroxide, cymoxanil-mancozeb), insecticides (clorpirifos, diazinon), herbicide (Round-up), and fertilizers (manure, urea, 10-30-10, CaCO3), using three different concentrations of each product (50, 5, and 0.5 ppm). The treatments were applied at the culture medium (SDA) in petri dishes. The fungus was sowed in the center of each petri dish, and the growth was annotated. In this experiment a randomized complete block disign was used, with 28 treatments and 3 replications. Clorpirifos and fentin hidroxide inhibited the fungus growth 9, 15 and 18 days after sowing, with a concentration of 50 ppm. Sporulation days fluctuated between 6 and 8, being the highest for cymoxanil-mancozeb and clorpirifos, because these completely avoided fungus sporulation, even until 36 days after sowing in SDA.
Introducción
Como un importante control biológico de las chisas o mojojoyes (Coleoptera: Scarabaeidae) se viene utilizando, en el departamento de Antioquia, el hongo Metarhizium anisopliae (Metsch.) Sorokin (Hyphomycetos), debido a su relativa facilidad de manejo, su gran capacidad de esporulación y su persistencia en el campo. Sin embargo, se desconoce la acción que ejercen los agroquímicos más usados por los agricultores en el departamento, sobre el crecimiento micelial y la esporulación del hongo, cuando estos se aplican con el fin de obtener más altos rendimientos.
Entonces se hace necesario evaluar el efecto que sobre el crecimiento y la esporulación del hongo M. anisopliae tienen algunos fungicidas, insecticidas, herbicidas y fertilizantes, para así, disminuir el disturbio ecológico y potenciar la acción del control biológico natural en los ecosistemas. El objetivo de esta investigación fue establecer la compatibilidad del hongo M. anisopliae, medida por el crecimiento micelial y la esporulación, con la aplicación de agroquímicos.
Revisión de Literatura
Entre las especies de hongos patógenos de insectos se destaca M. anisopliae, el cual se encuentra dentro de la familia Tuberculariaceae, orden Moniliales, clase Hyphomycetes, división Deuteromycota (Tulloch et al., citado por Hernández y Rodríguez 1992).
Este hongo fue descubierto por Metschnikoff en 1879, atacando larvas del escarabajo del trigo, Anisoplia austriaca (Herbst), en Rusia, denominándolo inicialmente Entomopthora anisopliae; más tarde, Sorokin, en 1883, describió el género Metarhizium, y llamó a este hongo M. anisopliae (Arango 1984).
El género Metarhizium se caracteriza por presentar conidióforos que forman una capa de esporas; las fiálidas pueden ser solas, en pares o en manojos, y de ellas se forman las conidias en cadena. Las conidias presentan diferentes tonalidades de verde; son ovoides o cilíndricas y unicelulares (Barnett y Hunter, citado por Bustillo 1987). Este género tiene dos especies: M. anisopliae y M. flavoviridae Grams y Rozsypal. Del M. anisopliae existen dos variedades:
M. anisopliae var. anisopliae: Es la más común; forma conidias esféricas u ovales de 3,5 - 9,0 μ de longitud, generalmente de 5,0 a 8,0 μ y 1,5 a 2,5 µ de ancho.
M. anisopliae var. major (Johnston): Agrupa las formas de conidias largas de 10 a 14 u de longitud por 1,8 a 4,0 μ de ancho (Tulloch 1976, citado por Rodríguez 1984).
La especie M. flavoviridae forma conidias elipsoidales de tamaño intermedio entre las dos variedades de M. anisopliae. Sus colonias toman coloraciones desde verde grisáceo hasta oliva (Rodríguez 1984).
Dentro de los reportes de control natural se le ha visto atacando a más de 200 especies de insectos en todo el mundo. En Colombia se han registrado 24 especies de insectos atacadas por este hongo, pertenecientes, en su mayoría, a los órdenes Coleoptera, Homoptera, Lepidoptera y Hemiptera (Tabla 1).
Reportes de especies de insectos hospedantes de M. anisopliae registradas en Colombia hasta 1991.
H: Huevo; L: Larva; P: Pupa; A: Adulto
Tomado de Bustillo (1987); Posada (1983); Posada y García (1976); Rodríguez (1984).
En el departamento de Antioquia se han registrado ataques de M. anisopliae en chisa o mojojoy en los municipios de San Vicente, El Carmen, El Santuario, La Ceja, El Retiro, Marinilla, Rionegro, Envigado, Medellín (Santa Elena) y Bello. Hasta ahora se han hecho 17 aislamientos del hongo (Londoño 1992), los cuales se mantienen en medios artificiales en el cepario de la colección del Centro de Investigación «Tulio Ospina» del ICA, Sección Entomología, Medellín, codificados según el lugar de procedencia, el cultivo, la fecha del aislamiento y la clase de chiza (Londoño, 1993).
Se conocen algunos estudios con respecto a la compatibilidad del M. anisopliae con los plaguicidas. En cuanto a los fungicidas, se estudió el efecto in vitro de algunos de ellos sobre la germinación y crecimiento de M. anisopliae, contando el número de esporas germinadas y no germinadas por campo óptico 40x; se encontró que fungicidas protectantes de ámplio espectro como mancozeb, captafol, fentin hidróxido, fentin acetato, mancozeb + carbendazin, redujeron la germinación entre un 75 y 100%, mientras que fungicidas sistémicos específicos como triziclazol, edifenfos, benomyl afectaron la germinación en un 40%, lo que posibilita su uso cuando se prevee utilizar M. anisopliae como control biológico (Albornoz y Parada 1984).
En otro estudio se encontró que el fungicida pentacloronitrobenceno (PCNB), a una concentración de 5 ppm, no afecta el crecimiento de los hongos M. anisopliae, Beauveria bassiana (Bals.) Vuill., Nomuroea rileyi (Farlow) Samson y Verticillium sp.; y contrarresta la contaminación por hongos mucoráceos cuando se adiciona 1 mg por cada gramo de salvado de trigo como sustrato (Olmert y Kenneth 1974).
También se ha evaluado la compatibilidad de los herbicidas más usados en los pastos brasileros con el hongo M. anisopliae. Los estudios fueron realizados in vitro y se observó que todos los productos son altamente tóxicos al hongo. El orden decreciente de toxicidad fué el siguiente: dicamba + 2,4 D; 2,4 D y picloram + 2,4 D (Paiva Castro 1981).
Materiales y Métodos
El hongo M. anisopliae utilizado en esta investigación fué aislado de larvas de chisa, procedentes de la parte alta del municipio de Bello (Ant.), en la vereda Llano de Ovejas. La cepa codificada en el ICA como Ma-11, presenta una coloración de conidias verde oscuro típico, diferente al de otros aislamientos procedentes del Oriente antioqueño. El hongo fué multiplicado en arroz. y luego se pasó al medio de cultivo comercial Sabourad-Dextrosa-Agar (SDA), en el cual se suministraron los tratamientos respectivos.
El trabajo experimental se realizó en el laboratorio de Entomología del Centro de Investigación «Tulio Ospina» del ICA, en Medellín, localizado a 1.440 msnm, con una temperatura promedio de 24,6±1,7°C y humedad relativa de 73,4±8,1%. La variación diaria de temperatura y la humedad relativa entre el día y la noche fluctuó en los rangos de 23,3 a 25,8°C y de 79,6 a 69,9%, respectivamente.
Se evaluaron algunos de los agroquímicos de mayor uso en los cultivos de fríjol y papa en el departamento de Antioquia. Para hacer una muestra representativa de los mismos, se escogieron fertilizantes, fungicidas, insecticidas y herbicidas. Se utilizó un diseño de bloques al azar, con 28 tratamientos y tres repeticiones. La unidad experimental fué la caja de petri, con el tratamiento químico aplicado al medio de cultivo (SDA) y debidamente sembrada con el hongo. Los agroquímicos evaluados fueron: los fungicidas Brestanid (fentin hidróxido, trifenil hidróxido de estaño) y Curzate (cymoxanil-mancozeb); los insecticidas, Lorsban (clorpirifos) y Basudin (diazinon); un herbicida, Round Up (glifosato); y los fertilizantes: Gallinaza, Urea, el compuesto 10-30-10 y un correctivo, Cal (CaCO3). Como testigo se incluyó un tratamiento en el cual sólo se adicionó agua destilada estéril.
Las cantidades probadas de cada producto fueron medidas en partes por millón (ppm); para esto se preparó una solución madre de 1.000 ppm de ingrediente activo, y de ésta se obtuvieron diluciones de 100 y 10 ppm, utilizando para ello erlenmeyers con agua destilada estéril. De cada una de las concentraciones así obtenidas se mezcló 1 ml con 20 ml del medio de cultivo SDA al 4%, en cajas de petri de 9 cm de diámetro, a una temperatura de 45°C. Las cajas vertidas se dejaron reposar hasta que solidificara el medio, teniendo cuidado de marcar debidamente cada una con el agroquímico y la concentración utilizados. Los tratamientos así establecidos quedaron a una concentración de 50, 5 y 0,5 ppm.
Una vez preparadas las cajas de petri con los tratamientos se procedió a inocularlos con M. anisopliae. Esta parte se llevó a cabo en la cámara de aislamiento, la cual fue previamente desinfectada con alcohol industrial.
Para facilitar la siembra, se tomaron granos de arroz con hongo esporulado y se colocaron en una caja de petri estéril. De allí se tomó consecutivamente, colocando un grano en el centro de cada caja. Una vez inoculados los medios con el hongo, se sellaron las cajas con plástico adhesivo transparente y se colocaron a temperatura ambiente (23 - 25°C), con suministro diario de luz por 21 días.
Las variables medidas fueron: el crecimiento micelial y los días a esporulación. Para calcular el crecimiento micelial, se midió el largo y el ancho de la colonia fungosa que creció alrededor del grano de arroz a los 3, 6, 9, 12, 15 y 18 días después de sembrado. Posteriormente se promediaron estas medidas y se calculó el área del círculo mediante la fórmula A = π/4×r2. Con los datos así obtenidos se realizó el análisis de varianza y se compararon los promedios mediante la prueba de Rangos Múltiples de Duncan (Little y Hills 1979).
A los datos sobre días a esporulación se les hizo una transformación
Resultados y Discusión
Para evaluar el efecto que los diferentes agroquímicos ejercieron sobre el crecimiento y esporulación del hongo M. anisopliae se analizaron dos criterios importantes. Estos fueron la inhibición en el crecimiento y los días a esporulación. El análisis se hizo con los datos obtenidos a los 9, 15 y 18 días después de la siembra del hongo; estos datos permitieron comparar la evolución del crecimiento micelial entre los diferentes tratamientos.
Inhibición en el Crecimiento
A una concentración de 0,5 ppm de cada uno de los productos evaluados, el crecimiento del hongo M. anisopliae, en cm2, no fué afectado en relación con el testigo, nueve días después de sembrado en el medio de cultivo. Quince días después de la inoculación se empezaron a observar algunas diferencias entre los tratamientos cal y glifosato con respecto al testigo, pero no alcanzaron una valoración estadística. Estos dos tratamientos se igualaron con el testigo a los 18 días (Fig. 1).
Durante todo el período de evaluación se nota un estímulo del crecimiento de M. anisopliae a la concentración 0,5 ppm, especialmente en los tratamientos úrea, gallinaza, 10-30-10, fentin hidróxido, diazinon y clorpirifos, situación que puede observarse en la Figura 1; siendo éstos estadísticamente diferentes al testigo el día 18.
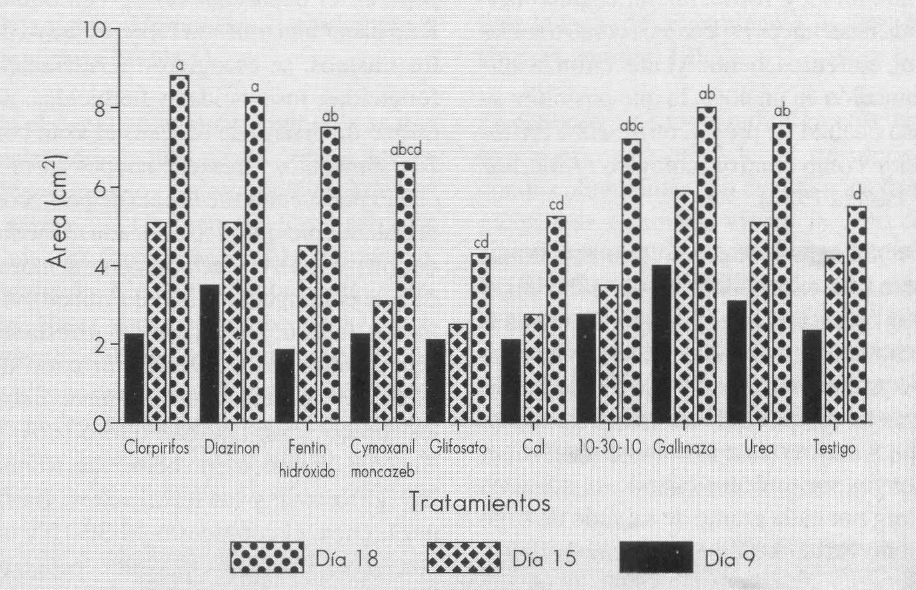
Crecimiento del hongo M. anisopliae bajo diferentes tratamientos, en una concentración de 0,5 ppm.
Cuando la concentración de los diferentes componentes se aumenta a 5 ppm, se empieza a mostrar la inhibición del fentin hidróxido y del clorpirifos, la cual se mantiene desde los nueve hasta los 18 días (Fig. 2); sin embargo, estos tratamientos no difieren estadísticamente del testigo a un nivel de significancia de α = 0,05. A concentraciones de 50 ppm, a los 9, 15 y 18 días después de sembrado el hongo, el análisis estadístico (α = 0,05) muestra más claramente la inhibición de los productos fentin hidróxido y clorpirifos. Es interesante destacar el efecto promotor del crecimiento del hongo a esta concentración, de los productos urea y glifosato, cuando se le compara con el testigo; efecto que sólo es estadísticamente diferente para la urea a los 18 días (Fig. 3).
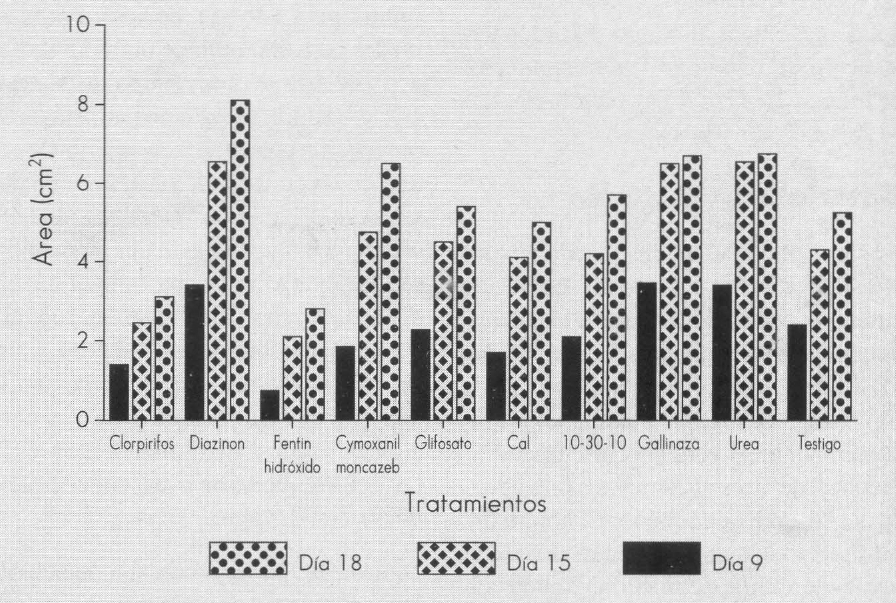
Crecimiento del hongo M. anisopliae bajo diferentes tratamientos, en una concentración de 5 ppm.
Según los resultados obtenidos, es necesario establecer si las dosificaciones recomendadas de ingrediente activo de cada uno de los tratamientos en estudio afectan el crecimiento micelial del hongo M. anisopliae, comparadas con las dosificaciones evaluadas en el trabajo, para así utilizar adecuadamente los agroquímicos sin que se afecte el control biólogico, que en este caso se utiliza para disminuir el ataque de la chisa en los cultivos.
La dosis comercial del insecticida clorpirifos es de 150 g/l, lo cual representa 1.500 ppm del producto en cada aplicación. Considerando que la formulación del producto es al 2,5% de i.a., se estarían aplicando 37,5 ppm de clorpirifos en un litro de agua. Dicha dosis se encuentra en el rango de 5 y 50 ppm evaluadas en este trabajo, en el cual se observó que concentraciones de 5 ppm no inhibieron el crecimiento del hongo mientras que las de 50 ppm si lo hicieron. Por lo tanto, se presume que puede manifestarse un efecto inhibitorio en el crecimiento del hongo a la dosis recomendada. Esta situación hace necesario continuar con investigaciones en este sentido, ampliando el rango de concentraciones entre 5 y 50 ppm, aumentando, además, el número de repeticiones, para esclarecer aún más la respuesta. Cuando al aplicar M. anisopliae para el control de la chisa se requiera adicionar clorpirifos para el control de otra plaga, podría recomendarse la aplicación del hongo incorporado al momento de la siembra y la del clorpirifos 30 días después. Con esto se dá un tiempo prudencial al agente de control biólogico de crecer y esporular, si encuentra su huésped, antes de entrar en competencia con el producto químico.
Para el caso de fentin hidróxido, la dosis comercial es de 0,6 cm3/l, equivalente a 3 ppm de i.a. en cada aplicación. Esto indica que la dosis comúnmente aplicada en el campo no afecta el desarrollo de M. anisopliae, ya que para alcanzar una inhibición se requiere una concentración de 50 ppm. Además, este producto es aplicado sobre el follaje y la mayor parte del producto quedará sobre él. Por esto se considera que sólo una mínima parte del químico cae al suelo, siendo menor el riesgo para el M. anisopliae.
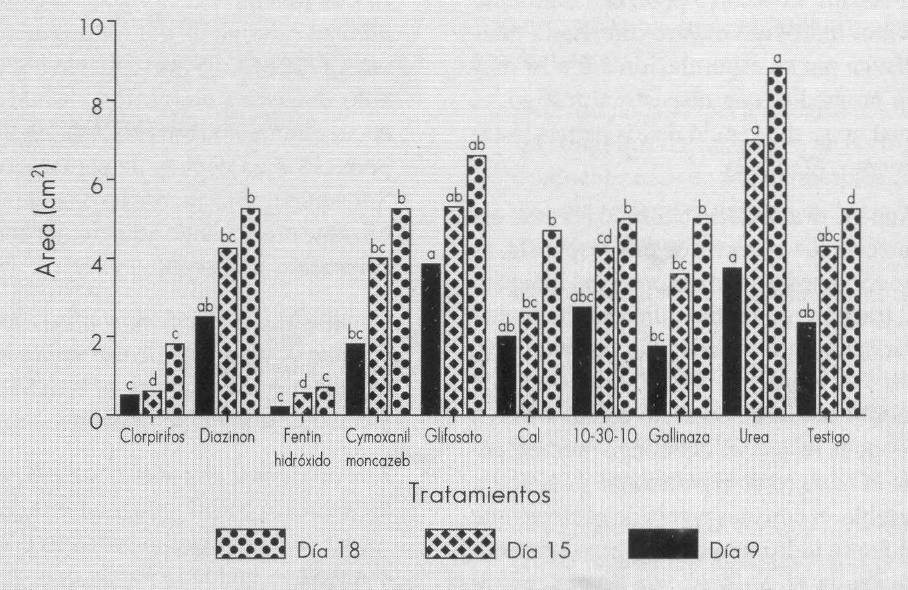
Crecimiento del hongo M. anisopliae bajo diferentes tratamientos, en una concentración de 50 ppm.
Para los productos glifosato, cymoxanil-mancozeb y diazinon, que no presentaron inhibición en el crecimiento del hongo bajo ninguna de las concentraciones utilizadas (50, 5 y 0,5 ppm), se estima que las dosis comerciales de i.a. tampoco causarían inhibición en el desarrollo del mismo, ya que se encuentran por debajo de 50 ppm (38,4, 18 y 20 ppm, respectivamente).
La gallinaza, el compuesto 10-30-10, la urea y la cal son productos que se aplican directamente al suelo a las concentraciones que vienen los productos comerciales. En la presente investigación se usaron dosis máximas de 50 ppm procurando comparar todos los productos a un mismo nivel. Todos estos agroquímicos se aplican a concentraciones superiores a las evaluadas y por lo tanto no se puede inferir el efecto que podrían tener en el campo. Por este motivo, vale la pena evaluar concentraciones superiores a 50 ppm, procurando acercarse a las aplicaciones de campo.
Días de Esporulación
Bajo condiciones de laboratorio y con iluminación permanente, M. anisopliae esporula a los seis días de sembrado en SDA. Los días a esporulación en los diferentes tratamientos probados variaron entre seis y 18.
A una concentración de 50 ppm se observó que clorpirifos y cymoxanil-mancozeb evitaron completamente la esporulación del hongo, incluso hasta los 36 días de sembrado. Estos dos tratamientos fueron significativamante diferentes al testigo (α = 0,05), el cual esporuló a los seis días (Tabla 2). Esto no indica que la esporulación haya sido evitada totalmente, pues es posible que el hongo lo haga después; por lo tanto es conveniente verificar hasta qué día se mantiene esta inhibición. Por otra parte, en fentin hidróxido, a la misma concentración, el hongo esporuló a los 18 días en una sola de las repeticiones, en la otras dos repeticiones no se presentó esporulación después de 36 días de observación. Este hecho hizo que el tratamiento fuera significativamente diferente del testigo. Los tratamientos diazinon, glifosato, 10-30-10, gallinaza, cal y urea se igualaron al testigo para esta variable.
Días a esporulación del hongo M. anisopliae en el medio de cultivo SDA con diferentes agroquímicos, a concentraciones de 50, 5 y 0,5 ppm.
Promedios seguidos por la misma letra, dentro de cada concentración, no difieren significativamente, según la Prueba de Duncan al 5%.
A la concentración 5 ppm, el tratamiento fentin-hidróxido mostró diferencia estadística por su esporulación a los 14 días en promedio, con respecto al testigo, el cual no se diferenció de los demás tratamientos (Tabla 2).
Aunque el análisis estadístico permite establecer la tendencia de una respuesta, es importante hacer la observación que para el tratamiento fentin hidróxido hubo una variación entre repeticiones que pudo forzar la valoración estadística. Por este motivo se hace necesario estudiar más a fondo la respuesta del hongo, aumentando el número de repeticiones para poder establecer con más precisión el efecto que el fentin hidróxido tiene sobre la esporulación de M. anisopliae a las concentraciones 50 y 5 ppm.
A concentraciones de 0,5 ppm no hubo diferencia entre los tratamientos, igualándose al testigo. M. anisopliae bajo estas condiciones esporuló a los seis días en todos los tratamientos, a excepción de fentin hidróxido, en donde esporuló en un promedio de siete días (Tabla 2).
Conclusiones
Los productos fentin hidróxido y clorpirifos, a una concentración de 50 ppm, causan inhibición en el crecimiento micelial del hongo M. anisopliae a los 9, 15 y 18 días de sembrado en el medio de cultivo SDA.
El crecimiento del hongo M. anisopliae es estimulado por los productos urea, gallinaza, 10-30-10, fentin hidróxido, diazinon y clorpirifos, cuando se encuentran a concentraciones de 0,5 ppm, 18 días depués de sembrados. Situación que se mantiene con el fertilizante urea cuando aumenta su concentración a 50 ppm.
La cepa Ma-11 de M. anisopliae, procedente de Bello (Ant.), esporula a los seis días después de sembrada en SDA y con iluminación permanente.
Los productos clorpirifos y cymoxanil-mancozeb a 50 ppm inhiben totalmente la esporulación del hongo M. anisopliae, incluso a los 36 días después de sembrado.
