Abstract
The potential for the control of Cyrtomenus bergi by the entomopathogenic nematode, Steinernema carpocapsae in the laboratory was evaluated. Three methodologies, using all instars of C. bergi, were evaluated: a) Petri dishes (100×15mm) with filter paper and with unsterilized soil, with one insect per unit and one doses of 6.788.800 nematodes/ml. Results confirmed that C. bergi was infected by S. carpocapsae at 5 and 8 days after exposure; b) the second experiment used plastic cups (7×7×10cm) containing unsterilized soil in petri dishes containing 10 insects of the same stage of development and doses of 2.000, 4.000, and 6.000 nematodes/ml. No clear tendency in parasitism was observed 2 and 8 days after exposure; c) the third experiment used plastic cups (3.5×4×5cm) containing 10 g of sterile sand with 3% RH and one insect per cup, with 2.000, 4.000, 6.000, 8.000 and 10.000 nematodes/ml. Results showed that the adult stage is the most sensitive at all doses with 58.6% parasitism after 10 days; the least sensitive are the first and second instars with 17 and 31% parasitism, respectively. An additional experiment using the afore described methodology evaluated the six nematode doses with adults. A Probit analysis showed that an average dose of 192 nematodes/ml is required to obtain 50% parasitism, 10 days after inoculation. Plastic cups with sterile soil was the most successful experiment unit. Results showed that S. carpocapsae is a potential biological control agent of C. bergi.
Introducción
El Cyrtomenus bergi Froeschner (Hemiptera: Cydnidae), es una chinche subterránea de las raíces que apareció a comienzos de la década del 80 como una nueva plaga del cultivo de la yuca, (Manihot esculenta Crantz) en algunas de las principales zonas productoras de Colombia. El daño lo causan las ninfas y los adultos, al introducir el estilete en la epidermis y corteza de la raíz, permitiendo la entrada de microorganismos del suelo, que deterioran y afectan la calidad de la yuca (García 1982).
Además de la yuca, esta chinche ataca otros cultivos comerciales tales como: papa, Solanum tuberosum ssp. andigena (J. G. Hawkes); cebolla, Allium cepa L.; cebolla junca; A. fistulosum L.; maíz, Zea mays L.; maní, Arachis hipogaea L.; sorgo, Sorghum vulgare Pers.; caña de azúcar, Saccharum officinarum L.; café, Coffea arabiga L.; arroz, Oryza sativa L.; espárrago, Asparagus officinalis L. y pastos (García 1982; cp. Bellotti). El insecto se encuentra distribuido en otros países de Centro y Sur América tales como: Costa Rica, Panamá, Cuba, Brasil, Ecuador y Surinam (Riis 1990).
En el Centro Internacional de Agricultura Tropical-CIAT se han realizado estudios básicos sobre este insecto, tales como biología, comportamiento y fluctuación poblacional, preferencia alimenticia y ensayos de control químico y cultural con la leguminosa Crotalaria juncea L. El uso de insecticidas químicos no es recomendado, no sólo por los costos, sino también por la destrucción de los enemigos naturales que controlan las poblaciones de otras plagas de la yuca. El control con la leguminosa no fue implementado por la disminución en el rendimiento. Como una alternativa de control se presenta el uso del nematodo parásito de insectos Steinernema carpocapsae Weiser (Rhabditida: Steinernematidae), el cual está asociado mutualísticamente con una bacteria del género Xenorhabdus y parasita en condiciones de laboratorio, cerca de 250 especies de insectos de 10 órdenes, destacándose por su alto parasitismo y capacidad de búsqueda, amplio rango de huéspedes y su economía por ser fácil y seguro de producir (Gaugler 1981).
El objetivo general de este trabajo fue evaluar el potencial del nematodo S. carpocapsae como agente de control biológico de C. bergi, y los objetivos específicos fueron: - Probar metodologías para evaluar el parasitismo de S. carpocapsae sobre C. bergi bajo condiciones de laboratorio y evaluar la susceptibilidad de los diferentes estados de C. bergi a S. carpocapsae en laboratorio.
Revisión de Literatura
Taxonomía
Según Poinar (1990), la familia Steinernematidae contiene sólo el género Steinernema con diez especies reconocidas hasta el momento. En el año de 1923, Steiner describió la primera especie hallada en Alemania como Aplectana kraussei. En 1927, Travassos erigió el nuevo género Steinernema, y en 1929, Steiner nombró un nuevo género Neoaplectana, no estableciendo claras diferencias para separarlos, pero en 1934, Filipjev notó la semejanza entre los dos géneros y los colocó en la subfamilia Steinernematinae, siendo erigida a nivel de familia por Chitwood & Chitwood. Estos cambios taxonómicos a nivel de género y especie han generado una confusión en la literatura, siendo aceptado el género Steinernema, por estar mejor definido.
Biología
Los nematodos tienen un ciclo de vida simple que incluye, huevo, cuatro estados juveniles (separados por mudas) y adulto. El tercer estado es el infectivo, el cual conserva la cutícula del estado anterior, y es el que contiene las células de la bacteria Xenorhabdus en su tracto digestivo. Una vez se localiza en el huésped, los estados infectivos lo penetran a través de las aperturas naturales (boca, ano, espiráculos) o posiblemente por alguna herida hasta alcanzar el hemocelo y libera la bacteria, la cual le causa septicemia y mata al huésped generalmente en 48 horas; los estados infectivos se alimentan de los nutrientes que las bacteria degradan; se aparean produciendo de dos a tres generaciones, de las cuales sólo el tercer estado sobrevive e inicia nuevamente el ciclo. La bacteria aprovecha al nematodo para la penetración al hemocelo del huésped y protegerse contra las condiciones ambientales adversas. El tercer estado está adaptado morfológica y fisiológicamente para permanecer en el medio ambiente por períodos prolongados sin tomar alimentos (Kaya y Gaugler 1993; Woodring y Kaya 1998).
Ecología y Comportamiento
El hábitat natural de los nematodos entomógenos es el suelo, el cual varía en composición química y estructura física (Gaugler 1981; Kaya 1990).
Los factores que gobiernan la distribución, localización y además limitan su uso como agentes de control biológico son los de orden físico, como la humedad, la temperatura, el tamaño de los poros, el agua, la aireación, la química de la solución del suelo y las raíces de las plantas, siendo la humedad el más importante, ya que ellos se alimentan y movilizan en una película de agua. Otros factores que pueden ser limitantes son el fotoperíodo, la radiación solar y la salinidad (Gaugler 1981; Burges y Hussey 1979; Wouts 1992; Kaya 1990).
Schroeder & Beavers (1987) hallaron que Neoaplectana glaseri se mueve más fácilmente en un suelo arenoso que las especies Heterorhabditis heliothidis, H. bacteriophora y N. carpocapsae. Según Georgis y Gaugler (1991), el parasitismo de S. glaseri y S. carpocapsae fue menor en un suelo con alto contenido de arcilla que en un suelo arenoso.
Los rangos de temperatura para que los nematodos causen infección están dados por la especie o raza de nematodos, dependiendo de su sitio de origen, y para que sean efectivos como agentes de control biológico debe utilizarse la especie mejor adaptada a la plaga y a las condiciones ambientales de la misma (Kaya 1990).
Las raíces de las plantas pueden afectar la dispersión de los nematodos por la respuesta de éstos a la acumulación de CO₂ alrededor de las raíces, pudiendo entrar en contacto con el huésped que se alimente en dicha zona (Kaya y Gaugler 1993).
Materiales y Métodos
El trabajo se realizó en el laboratorio del Programa de Entomología de Yuca del CIAT, en Palmira (Valle), con una temperatura promedio de 23°C y una humedad relativa de 65%.
La especie de nematodo evaluada, S. carpocapsae, se obtuvo de la casa comercial Biosys (Palo Alto, California, USA). Los estados de la chinche, seis en total, fueron tomados de la colonia ya establecida en el laboratorio.
Inicialmente se realizó una prueba preliminar con una dosis alta de nematodos para determinar si C. bergi era susceptible a los nematodos, ya que hasta el momento no se tenía ningún registro de ello. Se utilizaron cajas petri con papel filtro y con 10 g de suelo de textura franco-arenoso sin esterilizar, con 20 individuos de cada estado de la chinche, confinados individualmente, con la suspensión de nematodos en una concentración de 6'788.800 nematodos/ml. Al testigo se le adicionó solamente agua.
La evaluación se realizó a los 5 y 8 días después de inoculados. Tanto los insectos vivos como muertos se disectaron en una caja Petri de vidrio con agujas de disección y 0,1 ml de agua para facilitar la observación de los nematodos bajo el microscopio y estereoscópio, y se registró el número de nematodos presente por chinche.
Los datos obtenidos se sometieron a un análisis de varianza en un modelo de bloques completos al azar con estructura factorial, como fuentes de variación: Estados (instares ninfales I, II, III, IV, V y adulto), Tiempo (5 y 8 días), Ambiente (Papel filtro y Suelo) y Concentración (6'788.800n/ml). Se generó una variable binaria indicando la infección o no de la chinche que permitió estimar, con el total de las repeticiones, un porcentaje de parasitismo por estado.
En una segunda prueba se evaluaron tres concentraciones de nematodos, 2.000, 4.000 y 6.000 nematodos/ml, y se incrementó el número de insectos por unidad experimental a 10 individuos. Se utilizaron cajas petri con papel filtro y vasos plásticos (7×7×10cm) con 20 g de suelo de textura franco-arenoso sin esterilizar, un ml de la suspensión de nematodos según el tratamiento y un ml de agua. Al testigo se le adicionó agua solamente. Esta prueba contó con dos repeticiones.
La evaluación se realizó a los 2 y 8 días después de inoculados, de la forma antes descrita. Los datos obtenidos se analizaron de igual forma que en el ensayo anterior y se totalizaron para obtener el porcentaje de parasitismo de cada estado.
En un tercer ensayo se utilizó otro tipo de unidad experimental para determinar la susceptibilidad de los diferentes estados de la chinche con cinco concentraciones de nematodos, 2.000, 4.000, 6.000, 8.000 y 10.000 nematodos/ml en vasos plásticos (3,5x4x4,5cm) con 10 g de arena estéril, con un contenido estándar de humedad del 3%, un sólo insecto por vaso y un ml de la suspensión de nematodos según el tratamiento. Al testigo se le adicionó agua solamente. Se definió como repetición, el conjunto de diez vasos (10 insectos) por dosis replicándose seis veces.
La evaluación se realizó a los 10 días después de inoculados, de la forma antes descrita. Los datos obtenidos se sometieron a un análisis de varianza y a una prueba Duncan con la transformación del tipo arcoseno cuando se encontraron diferencias significativas.
Con base en los resultados del ensayo anterior se realizó un último ensayo con el estado adulto de la chinche y seis concentraciones, 200, 500, 1.000, 2.000, 4.000 y 10.000 nematodos/ml, y se utilizó la misma unidad experimental del ensayo anterior con el mismo número de insectos por tratamiento y el mismo número de repeticiones. La evaluación se realizó a los 10 días. Los datos obtenidos se sometieron a un análisis Probit para calcular la dosis letal media (LD50). Este análisis es el utilizado para la evaluación de insecticidas químicos, y el objetivo principal es estimar la dosis suficiente para causar la muerte (o un nivel particular de intoxicación) a una población dada de insectos. Para realizar este tipo de análisis con nematodos entomógenos se asume que todos los individuos son igualmente infectivos.
Resultados y Discusión
Los resultados obtenidos en la primera prueba preliminar indican que S. carpocapsae es capaz de parasitar a C. bergi en todas las interacciones evaluadas: medios (papel filtro y suelo sin esterilizar), estados y tiempos de evaluación (5 y 8 días), no observándose un estado más susceptible que otro, ni un medio ni un tiempo más efectivo.
Sin embargo, en los tratamientos con papel filtro, con las ninfas de II Y III instar se obtuvo un 100% de parasitismo a los 5 y 8 días después de inoculados, y los menores porcentajes con las ninfas de V instar, con sólo 20% a los 5 días, en las de IV instar con un 66,3% a los 8 días. En el suelo, los mayores porcentajes de parasitismo se presentaron en el estado adulto con un 70% y 60% a los 5 y 8 días después de inoculados, y los menores se obtuvieron con las ninfas de IV instar con un 0% a los 5 días, y a los 8 días, las ninfas de III y V instar presentaron el 10% de parasitismo (Tabla 1).
Porcentaje de parasitismo de C. bergi expuesto a una sola dosis de S. carpocapsae. (6'788.800 nematodos/ml.).
= Número de insectos
= Días de evaluación
En la segunda prueba preliminar tampoco se presentó una tendencia clara sugerida por las dosis, tiempos, medios y estados evaluados, pero se observó, al igual que en la prueba anterior, los mayores porcentajes de parasitismo en los tratamientos con papel filtro en ambos tiempos de evaluación, con rangos entre 0-80% y 0-40% para 2.000 nematodos/ml, de 0-90 y 30-100% con 4.000 nematodos/ml y con la dosis de 6.000 nematodos/ml los rangos fueron 0-70% y 0-66% a los 2 y 8 días, respectivamente (Tablas 2 y 3).
Con el ensayo en el cual se utilizó arena estéril con un contenido estándar de humedad del 3%, un sólo insecto por vaso y cinco dosis de nematodos sí se logró obtener un comportamiento más definido de S. carpocapsae sobre todos los estados de C. bergi, presentándose el estado adulto como el más susceptible a todas las dosis de nematodos evaluadas (Fig. 1 y 2), con un rango de parasitismo entre el 55-80% y en promedio de 58,6%, los menos susceptibles resultaron ser los dos primeros instares ninfales, con un promedio de 17 y 30,8%, respectivamente, no presentándose diferencias significativas entre los demás estados.
Con los datos obtenidos no se pudo establecer la dosis suficiente para causar la muerte, por no ajustarse adecuadamente al modelo Probit, pero mediante la prueba de rangos múltiples de Duncan, con transformación de los datos al tipo arcoseno y con una probabilidad ≤ 0,05, se estableció que el parasitismo más bajo se presentó con la menor dosis de nematodos evaluada (2.000 nematodos/ml), con un promedio de 31,1%, entre las otras cuatro dosis probadas no hubo diferencias significativas, con un rango promedio entre 45 y 52% (Fig. 3).
Porcentaje de parasitismo de C. bergi expuesto a tres dosis de S. carpocapsae en papel filtro.
= Número de insectos
= Días de evaluación
= Dosis, nematodos por mililitro
Porcentaje de parasitismo de C. bergi expuesto a tres dosis de S. carpocapsae en suelo.
= Número de insectos
= Días de evaluación
= Dosis, nematodos por mililitro
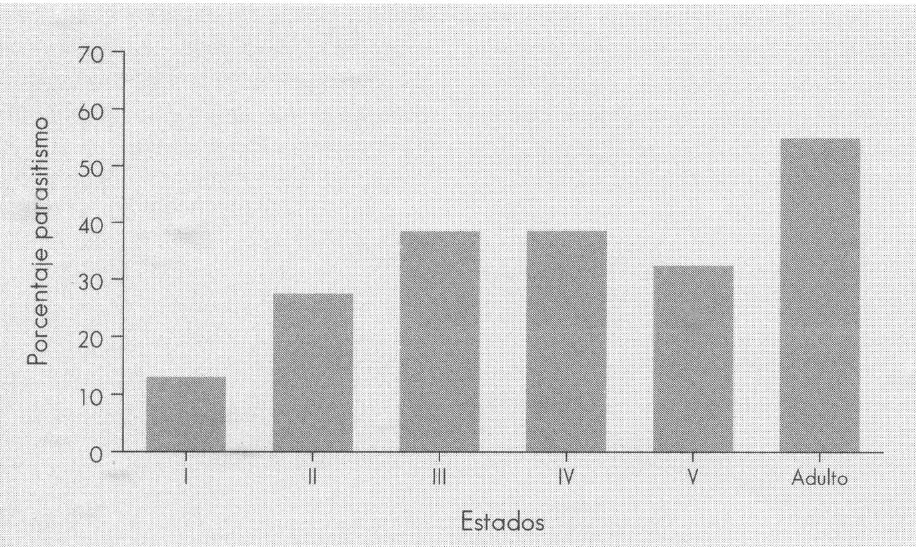
Porcentaje de parasitismo de S. carpocapsae sobre C. bergi.
En el último ensayo se confirmó la susceptibilidad del estado adulto de la chinche a los nematodos, incrementándose el parasitismo con el aumento en la dosis, así para las dosis de 200 y 500 nematodos/ml, el porcentaje de parasitismo fue de 55 y 73,3% y a partir de 1.000 nematodos/ml fue del 100%. Al someter estos datos al análisis Probit, los cuales se ajustaron adecuadamente (Tabla 4), se obtuvo una dosis letal media (DL50) con sólo 193 nematodos/ml y una LD90 con 641 nematodos/ml, con un intervalo de confianza entre 7,6 y 403 nematodos/ml, entendiéndose éstos valores como el número de nematodos necesarios para causar el 50% y el 90% de parasitismo sobre C. bergi.
Con los resultados obtenidos en estas pruebas se descartó el uso de las cajas Petri como unidades experimentales para la evaluación de nematodos entomógenos sobre C. bergi, ya que no fue posible obtener una tendencia definida en el parasitismo y, según Bedding (1990), el uso de las cajas Petri no es recomendado para la evaluación de nematodos sobre insectos del suelo porque se alejan en alto grado de su hábitat natural.
Entre los factores que pudieron influir el comportamiento de los nematodos tanto en las cajas Petri con papel filtro como en los tratamientos con suelo sin esterilizar se encuentran los factores bióticos, tales como: hongos y bacterias, los cuales son considerados como los principales enemigos de los nematodos, tanto en condiciones naturales como en artificiales (Poinar 1979).
Los factores físicos, tales como la textura y la humedad del suelo, también pudieron influir los bajos porcentajes de parasitismo obtenidos en los tratamientos con suelo de textura franco-arenoso con un contenido de humedad no estandarizado, los cuales en el momento de la evaluación presentaban exceso o falta de humedad, pudo afectar el comportamiento de los nematodos, disminuyendo la capacidad de hallar e infectar al huésped, como lo menciona Kaya (1990). Además, según Kung et al. (1990), la infectividad es dependiente del contenido de humedad del suelo, por lo que un cierto contenido es necesario para que ocurra.
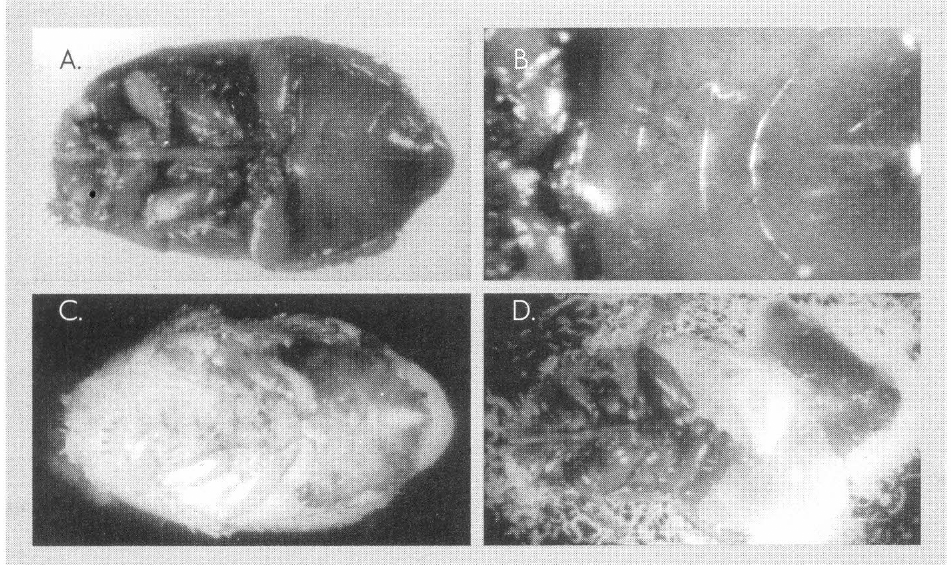
Secuencia del estado adulto de C. bergi parasitado por S. carpocapsae.
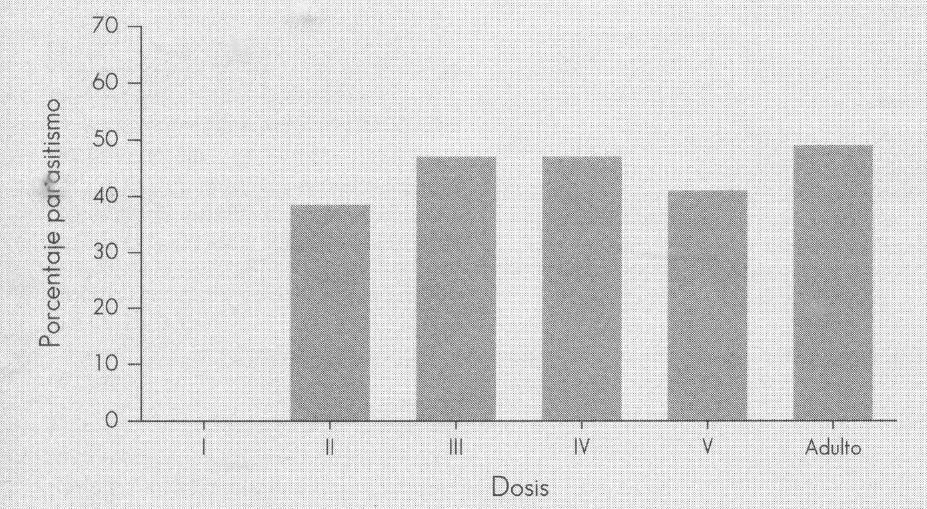
Porcentaje de parasitismo de C. bergi con cinco dosis de S. carpocapsae.
Dosis de S. carpocapsae necesarias para causar el 50% y el 90% de parasitismo al estado adulto de C. bergi.
= Número de insectos
= Número de nematodos/ml para obtener el 50% de parasitismo
= Número de nematodos/ml para obtener el 90% de parasitismo
= pendiente de la recta obtenida
Otro factor que pudo afectar el parasitismo fue el confinamiento de los insectos de un mismo estado por unidad experimental, como se realizó en la segunda prueba preliminar, ya que según Bedding (1990), esto conlleva a una variabilidad en la respuesta por la atracción y susceptibilidad entre insectos de la misma especie, por lo tanto recomienda el uso de un tipo de arena con un contenido estándar de humedad, un sólo insecto por vaso y mínimo cinco concentraciones de nematodos para obtener un comportamiento definido y determinar la dosis suficiente para causar la mortalidad.
Debido a las diferencias de comportamiento e infectividad entre especies y razas de nematodos, no es posible establecer un tipo de bioensayo universal que pronostique los niveles de control bajo diversas condiciones ambientales. Por lo tanto es necesario realizar los bioensayos bajo condiciones ambientales particulares como por ejemplo, temperatura y tipo de suelo, dependiendo de la especie de nematodo y del insecto en particular (Hominick y Reid 1990, citados por Wouts 1992).
También es necesario destacar que en los tiempos evaluados, 2, 5, 8 y 10 días, S. carpocapsae no le causó el 100% de mortalidad a C. bergi, pero sí el 100% de parasitismo, condición por la cual se observaron cambios en su comportamiento, permaneciendo en la superficie del suelo; sin embargo, sería conveniente determinar el tiempo de mortalidad con la dosis de 193 nematodos/ml, ya que después de estar parasitados sólo cuenta el tiempo de multiplicación de la bacteria y de reproducción del nematodo dentro del huésped para causar la muerte.
Conclusiones
El nematodo S. carpocapsae parasitó a la chinche C. bergi en los medios y tiempos evaluados, utilizando una unidad experimental compuesta de arena estéril con un contenido estándar de humedad del 3% y un sólo insecto, la más adecuada para la realización de ensayos de parasitismo de nematodos entomógenos sobre C. bergi, bajo condiciones de laboratorio.
Las cajas Petri con papel filtro y suelo sin esterilizar no fueron las unidades más adecuadas para evaluar el parasitismo de S. carpocapsae sobre C. bergi.
El estado adulto de la chinche fue el más susceptible a todas las dosis de nematodos evaluadas, con un promedio de 58,6% de parasitismo. Los menos susceptibles fueron los dos primeros estados ninfales con 17 y 30% de parasitismo, en promedio, después de 10 días de inoculados.
El menor porcentaje de parasitismo en todos los estados de C. bergi se presentó con la menor dosis (2.000 nematodos/ml), con un 31,1%, en promedio. Con 4.000, 6.000, 8.000 y 10.000 nematodos/ml el parasitismo estuvo entre 45 y 52%, en promedio, después de 10 días de inoculados.
Las dosis necesarias de S. carpocapsae para causar el 50 y el 90 % de parasitismo sobre el estado adulto de C. bergi, que fue el más susceptible de todos los estados, fueron de 193 y 641 nematodos/ml, después de 10 días de inoculados.
Los resultados obtenidos en el presente trabajo permiten concluir que S. carpocapsae puede ser considerado como un agente potencial de control biológico para incorporarlo dentro de un programa de control integrado de la chinche C. bergi.
