Abstract
The population of the white grubs has increased lately in Antioquia, Colombia. The insect has been reported cutting roots and stems of beans, corn, grasses, potatoes, vegetables, fruits and forest crops. In order to identify the natural enemies of the insect, a collection of larvae was made in some towns of the eastern part of the department. Each larva was placed in a plastic container with soil from the same place of collection. The natural biological control caused a 44% of mortality of white grubs. The most common regulator factor was the disease caused by Bacillus popilliae, which was the best enemy and was found in all the sites sampled. Rhabditid and Mermithid nematodes as well as the entomogenous fungi Metarhizium anisopliae and Beauveria bassiana were detected causing parasitic action. Insect parasitoids were found in less amount; two of them exerting an ectoparasitic action (Hymenoptera: Tiphiidae and Scoliidae), and other as endoparasite (Diptera: Tachinidae).
Introducción
Hace unos años, la chisa, gallina ciega o mojojoy pasaba desapercibida o su presencia era esporádica en los campos; hoy en día son insectos comunes en varias regiones de Colombia y otros países de Centro América (Posada et al. 1976; King y Saunders 1984).
Los cambios en el medio ambiente han favorecido la aparición de ciertas plagas que al ver deteriodado el entorno para sus enemigos naturales o agentes naturales de control, encuentran el momento oportuno para su multiplicación. La chisa es uno de estos insectos, a los cuales el medio ambiente les es favorable hoy. Antiguamente se le encontraba en áreas boscosas, donde la alta humedad relativa favorecía a los hongos, bacterias y otros microorganismos entomógenos, los cuales regulaban las poblaciones de estos insectos. La tala de los bosques, el sobrecalentamiento de la tierra, la disminución del agua superficial y de la precipitación y el uso indiscriminado de agroquímicos, entre otros factores, han limitado las poblaciones de los enemigos naturales de la chisa, con el consecuente surgimiento del insecto como plaga de importancia económica. Es necesario, por lo tanto, buscar e identificar los factores de mortalidad que tiene la chisa y buscar métodos económicos para la multiplicación de los agentes de control biológico (Velásquez 1993; Londoño 1993).
Revisión de Literatura
El manejo de las diferentes especies de chisa ha tenido un gran apoyo en el uso de agroquímicos. Para Eutheola bidentata (Burmeister), King y Saunders (1984) recomiendan la aplicación de insecticidas granulares al sitio de siembra. Jiménez y Lobatón (1986) sugieren la aplicación de insecticidas piretroides. No obstante, el control químico de estos insectos ha sido deficiente, ya que requiere grandes volúmenes de agua para lograr que el producto químico se ponga en contacto con la larva o el adulto que está dentro del suelo, a profundidades que varían entre 25 y 79 cm. En un trabajo de campo realizado por Rivera y Posada (1991) se pudo constatar la baja eficiencia de los productos clorpirifos, trizofos, lindano, diazinon y carborufan en el control de chisas en maíz, tanto en monocultivo como en asocio. En fríjol en asocio, de los insecticidas anteriormente mencionados, sólo el carbofuran permitió rendimientos superiores al 80% respecto al testigo, ya que en monocultivo la eficiencia no superó el 73%.
Las especies de Scarabaeidae registradas haciendo daño en Colombia son diversas y sus daños son de diferente magnitud según el cultivo y la región. E. bidentata es una especie que se encuentra haciendo daño en cultivos jóvenes de maíz, arroz y sorgo en los Llanos Orientales, la Costa Atlántica y la zona de Urabá en el departamento de Antioquia; en este caso, el estado dañino del insecto es el adulto, el cual troza las plantas a nivel de la superficie o ligeramente por debajo de éste (Jiménez y Lobatón 1986; Londoño 1993). En las zonas fría se observa a Ancognatha scarabaeoides Erichson como las especie predominante, atacando cultivos de papa, maíz, fríjol, pastos, cereales menores y hortalizas (Ruíz y Posada 1985; Hernández y Rodríguez 1992). En el clima frío moderado, donde están comprendidos la mayoría de los municipios del Oriente antioqueño, se encuentra un variado número de especies, con frecuencias diferentes en cada uno de ellos (Londoño 1993).
En un reconocimiento de especies de chisa realizado en cuatro municipios del oriente antioqueño (La Ceja, La Unión, Guarne y Carmen de Viboral) se detectó la presencia de más de 20 especies, donde figuran: A. scarabaeoides, A. sp. pos. nigriventris Otoya, A. sp. pos. humeralis Burmeister, Cyclocephala sp., C. sp. pos lucida Burmeister, C. gregaria Arrow, C. sp. pos. lunata Burmeister, C. sp. pos. signata Fabricius, Heterogomphus sp. y Golofa sp. como representantes de la subfamilia Dynastinae; Phyllophaga spp., Plectris sp., Pseudoserica sp., Macrodactylus sp. y Faula sp. de la subfamilia Melolonthinae; Anomala sp. (con dos posibles especies), Strigoderna sp. y Leucothyreus sp. de la subfamilia Rutelinae (Nanclares y Ramírez 1992).
Las especies de la subfamilia Dynastinae hacen daño tanto en el estado larval trozando raíces, como en el estado adulto masticando follaje, flores o haciendo roeduras en los frutos. De este modo se les ha visto en mora de castilla (Rubus glaucus Benth.), tomate de árbol (Cyphomandra betacea (Car.) Sendt.), uchuva (Physalis peruvianus L.), además de los cultivos ya mencionados para A. scarabaeoides (Posada et al. 1976; Nanclares y Ramírez 1992; Londoño 1993). La subfamilia Melolonthinae se ha observado principalmente en cultivos de maíz, fríjol, lulo (Solanum quitoense Lam.), granadilla (Passiflora edulis Sims.), jardines ornamentales, gramas de canchas deportivas, mora, guayaba y eucaliptus (Nanclares y Ramírez 1992; Londoño 1993).
Como agentes de control biológico de las chisas del género Phyllophaga se han identificado en Centro América los ectoparasitos Campsomeris dorsata Fabricius, Ellis sp. y Tiphia sp. (Hymenoptera: Scoliidae), vertebrados depredadores que atacan tanto larvas como adultos y patógenos microbiales, probablemente del tipo Micrococcus nigrofasciens Northrup (King y Saunders 1984).
La bacteria Bacillus popilliae Dutky, causante de la enfermedad lechosa, ha sido usada en el control biológico del cucarrón japonés, Popillia japonica Newman, en los Estados Unidos de Norte América por más de 50 años (Stahly y Klein 1992). Este mismo microrganismo se ha encontrado atacando larvas de Cyclocephala hirta LeConte en pastisales de California (Thurston et al. 1993).
Los nemátodos entomógenos han sido reportados atacando larvas de Scarabaeidae en distintas ocasiones, y numerosos trabajos de investigación se han realizado con ellos. Las especies de nematodos más comúnmente registradas son: Steinerne-ma feltiae, S. glaseri, S. carpocapsae, Heterorhabditis heliothidis y H. bacteriophora (Villani y Wrigth 1988).
Jiménez y Lobatón (1986), Rivera y Posada (1991) y Hernández y Rodríguez (1992) han encontrado el hongo entomógeno Metarhizium anisopliae (Metch.) Sorokin atacando diferentes estados de desarrollo de las chisas en Colombia.
Materiales y Métodos
Este trabajo se realizó en varios municipios del Oriente antioqueño, los cuales se localizan en una zona montañosa, con temperaturas que oscilan entre 6-20°C, con un promedio aproximado de 17°C. En el área de muestreo se registran dos climas. El clima frío de las zonas paperas altas, correspondiente a los municipios de Santuario y Medellín (corregimiento de Santa Elena); el municipio de Santa Rosa de Osos, aunque pertenece a la zona norte de Antioquia, también está incluido en este clima. En el clima frío moderado están comprendidos la mayoría de los municipios muestreados, los cuales son: San Vicente, El Retiro, Rionegro, Carmen de Viboral, Marinilla, Guarne y La Ceja.
Muestreo de Campo
Durante el primer semestre de 1992, en zonas con evidencia de daño de chisa se tomaron muestras de suelo y larvas, las cuales se introdujeron en bolsas plásticas obscuras o en costales de fibra sintética. En el muestreo colaboraron instituciones como CORNARE, Secretaría de Agricultura de Antioquia, las unidades CRECED del ICA y agricultores particulares, quienes siguieron un instructivo diseñado para tal fin (Londoño 1992).
Las muestras se identificaron con el lugar de procedencia (vereda y municipio), fecha, cultivo y propietario, y se remitieron al Centro de Investigación «La Selva», ubicado en la vereda Llano Grande del municipio de Rionegro, con una temperatura promedia de 17°C.
Manejo del Material Biológico
Las larvas de chisa recibidas se colocaron individualmente en vasos plásticos desechables, con suelo del lugar de procedencia de la muestra, el cual cubría más de la mitad de capacidad del recipiente. A cada sitio de muestreo se le asignó un código, seguido por el número consecutivo que identificaba la larva. Los vasos así marcados se taparon y se colocaron en una mesa dentro de una casa de malla, donde estuvieron sometidos a la temperatura y humedad relativa ambientales.
Semanalmente se revisó todo el material, anotando cualquier cambio en el insecto y registrando la mortalidad ocurrida. En cada revisión se adicionó agua al suelo, utilizando un atomizador manual para no causar impacto sobre las larvas ni inundación.
Las larvas con síntomas de enfermedad se llevaron al laboratorio para facilitar su observación. Al detectar crecimiento micelial se retiró la larva del suelo y se colocó en una cámara húmeda para facilitar la esporulación del hongo. Una vez se obtuvieron las conidias, se hicieron observaciones al microscopio compuesto, tanto en agua como en azul de lactofenol. Para la identificación de los hongos entomógenos se utilizó la clave Barnett y Hunter (1981). Otros microorganismos causantes de mortalidad se identificaron con la colaboración del personal técnico de la Corporación de Investigaciones Biológicas, CIB, en Medellín.
Se anotaron tanto las características típicas de la muerte de los insectos por cada agente de mortalidad, como el número de larvas muertas por la acción de cada uno. Estos datos se analizaron estadísticamente utilizando los rangos de Friedman (Siegel 1956).
Resultados y Discusión
Durante el período comprendido entre julio de 1992 y marzo de 1993 se llevaron a cabo las observaciones sobre el material biológico recogido en 1992, proveniente de 21 muestras de diferentes localidades.
Dada la complejidad de la taxonomía en estado larval y ante la dificultad de hacer identificaciones rápidas de este tipo de insectos en el país, se hizo un seguimiento a todos los insectos colectados con el fin de obtener información sobre la biología, hábitos y factores de mortalidad, que permitieran establecer algunas pautas de manejo.
Las chisas pasan la mayor parte de su vida en el suelo. Los huevos son blancos y globosos inicialmente; a medida que aumenta su desarrollo embrionario se tornan más redondos. Miden en promedio 2 mm de diámetro. Se les encuentra en el suelo en los primeros 30 cm de profundidad.
La larva es de tipo scarabaeiforme, con su característica forma de C; su cuerpo es de color blanco cremoso, con la cabeza bien esclerotizada, cuyo color varía de amarillo a café-marrón según la especie. Tiene tres pares de patas torácicas de color café y no posee seudopatas. Presenta una zona traslúcida en la parte posterior del cuerpo que deja ver el contenido interno de color oscuro. Durante el estado larval, las chisas se encuentran en el suelo a distintas profundidades dependiendo de la humedad. En la zona de estudio, durante los meses de mayo a octubre se localizan en la zona de raíces de las plantas nospedantes y la profundidad varía según el tipo de cultivo. En papa, maíz, fríjol, hortalizas y flores se ubican en los primeros 30 cm; en potreros entre 10 y 15 cm y en árboles frutales a profundidades que varían entre 25-60 cm. Durante los meses de noviembre a febrero permanecen a profundidades entre 70 cm y un metro, donde se convierten en pupa. Durante este último estado, el insecto está incluido dentro de una cámara pupal, elaborada con tierra y con el producto de sus excrementos. Allí permanece hasta la llegada de las lluvias en marzo, cuando la humedad debilita la cámara pupal y el adulto sale a la superficie.
Bajo condiciones de laboratorio se ha observado que en suelos con humedad permanente, el adulto emerge en 25-30 días después de empupar. Esta observación indica que la humedad del suelo, generada por la llegada de las lluvias en el mes de marzo, es la que está favoreciendo la emergencia de los adultos. Cuando las lluvias se retrasan, como ocurrió en 1992 que el período de lluvias comenzó en abril, los adultos emergieron sólo hasta este mes (Londoño 1993).
De un total de 1.314 larvas evaluadas, 571 murieron, lo cual corresponde a un 44% de mortalidad, con un promedio de 3,1 factores de mortalidad por sitio de muestreo (Tabla 1).
Mortalidad total observada sobre chisas en diferentes localidades de Antioquia. 1992
Dentro de los controladores naturales se destaca la «enfermedad lechosa» causada por la bacteria B. popilliae. En los aislamientos realizados para su identificación, siempre se le encontró con B. lentimorbus, bacteria que se reporta en las producciones comerciales de este agente de control biológico. Los síntomas que se aprecian sobre las larvas enfermas son: debilidad, movimientos lentos y una acumulación de masas blancas gelatinosas en la parte caudal que simulan leche cuajada (Fig. 1). Estas acumulaciones de color blanco mate, corresponden a las esporas de ambos microrganismos. La larva infectada muere y se desintegra, liberando las esporas en el suelo. La bacteria B. popilliae fue aislada en medio de cultivo Agar Yousten, donde tardó 20 días en crecer. Mediante tinción con safranina y verde de malaquita, se pudieron observar las características propias de la espora, la cual es deformadora de la estructura bacilar. La enfermedad lechosa se encontró actuando en 20 localidades (Tabla 2), y puede afectar tanto las larvas como las pupas.

Chisa afectada por Bacillus popilliae Dutky
Factores de mortalidad en chisas (Col: Scarabaeidae) y su importancia relativa en cada localidad de muestreo. Oriente Antioqueño 1992.
Secundarios: ataca larvas débiles; Ma: Metarhizium anisopliae; O.C. Otras causas; Bb: Beauveria bassiana; Pa.: Parasitoides; Rhabditida; Mermithidae.
En distintas localidades se encontraron dos nematodos parasíticos causando la muerte a las larvas. Uno de ellos, del orden Rhabditida, está presente en 13 sitios de muestreo. La larva atacada por este nematodo se debilita y torna de color café, y después de la muerte toma una coloración gris. De la larva muerta emerge una gran cantidad de larvas del nematodo en busca de otro huésped (Fig. 2). El otro nematodo pertenece a la familia Mermithidae, y mide aproximadamente 11 cm de longitud. Se encuentra más comúnmente en chisas provenientes de potreros. Cuando la larva es atacada por un mermítido, se vuelve muy lenta, y a veces se puede apreciar la presencia del nematodo en el interior del insecto, principalmente hacia la zona caudal (Fig. 3). Los mermítidos penetran a la chisa por vía oral, y cuando son de tamaño grande pueden causar la muerte de la larva en 24-48 horas. El síntoma de la chisa muerta es igual que en el caso de los Rhabditida.
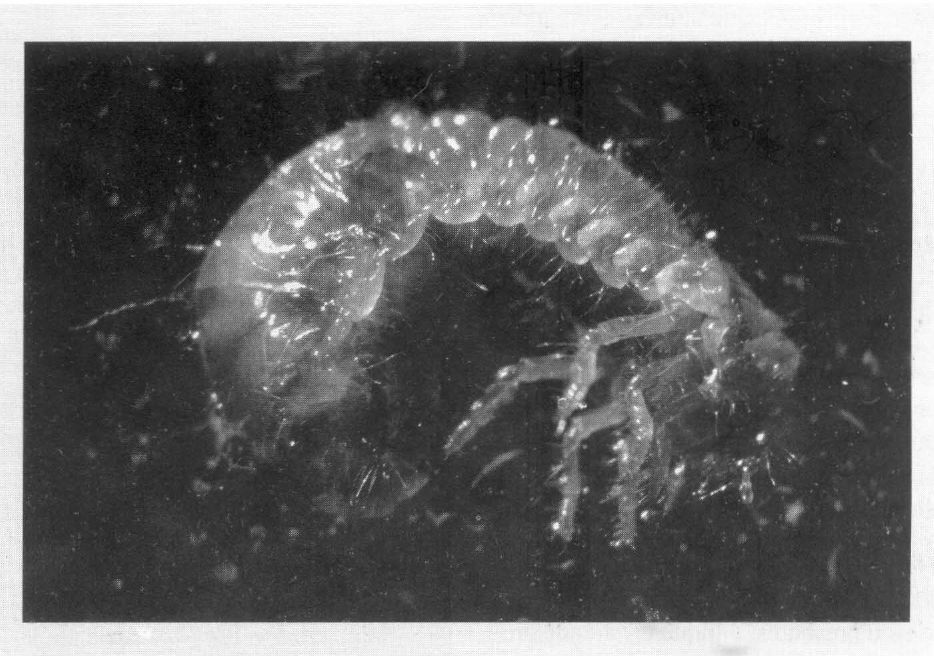
Chisa rodeada de nematodos (Rhabditida) que han salido de su cuerpo después de causar la muerte.

Nematodo (Mermithidae) acomodado en la zona caudal interna de una chisa.
Los hongos entomógenos M. anisopliae y B. bassiana atacan los cuatro estados de desarrollo de la chisa. En 14 de las localidades muestreadas se encontró el hongo M. anisopliae y en tres B. bassiana. Al tener en cuenta la variabilidad de especies de chisa existentes en el Oriente antioqueño y los reportes de Hernández y Rodríguez (1992) sobre la especificidad de M. anisopliae, se hicieron aislamientos en forma separada para cada sitio de muestreo, asignando un código según el lugar de procedencia. La mayoría de los aislamientos fueron de larvas y por el mismo motivo no se sabe la especie de insecto atacada. Sin embargo, se tienen cinco aislamientos de adulto, obtenidos de las especies A. scarabaeoides, Phyllophagasp., Plectris sp. Cyclocephala sp. pos. lucida.
Las chisas atacadas por M. anisopliae presentan un punto de penetración del hongo, el cual se observa como una quemazón hecha con cigarrillo. Estos puntos de penetración son oscuros y de tamaño variable y se pueden localizar en cualquier parte del cuerpo. Cuando el hongo penetra por una o varias de las patas causa una digestión de las mismas deformándolas o haciéndolas incluso desaparecer. Posteriormente ocurre el crecimiento micelial dentro del insecto, el cual pierde movimiento y muere momificado. En este momento, el hongo empieza a emerger por el integumento, cubriendo de un micelio blanco toda la larva. La espoluración es de color verde (Fig. 4), con tonos que varían del claro al oscuro, según el aislamiento. Uno de los dos aislamientos procedentes de Ancognatha presenta conidias alargadas, de paredes gruesas, que podrían corresponder a la variedad «major», según la descripción de Tulloch, citado por Hernández y Rodríguez (1992).
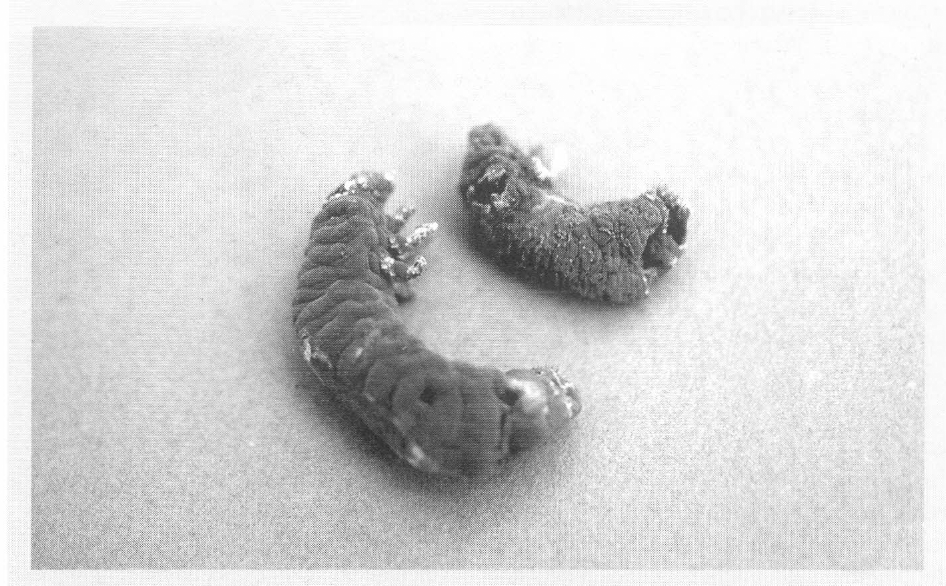
Larvas de Ancognatha scarabaeiodes afectadas por Metarhizium anisopliae. Hongo completamente esporulado sobre el insecto muerto.
El hongo B. bassiana se aisló en tres localidades, y sólo uno de los aislamientos procede de un adulto de Cyclocephala sp., sobre el cual hubo una abundante producción de conidias (Fig. 5). Las larvas atacadas por B. bassiana presentan deformaciones de su conformación, observándose encogidas. En ellas se puede apreciar un crecimiento micelial blanco, que semeja copos de algodón discontinuos.
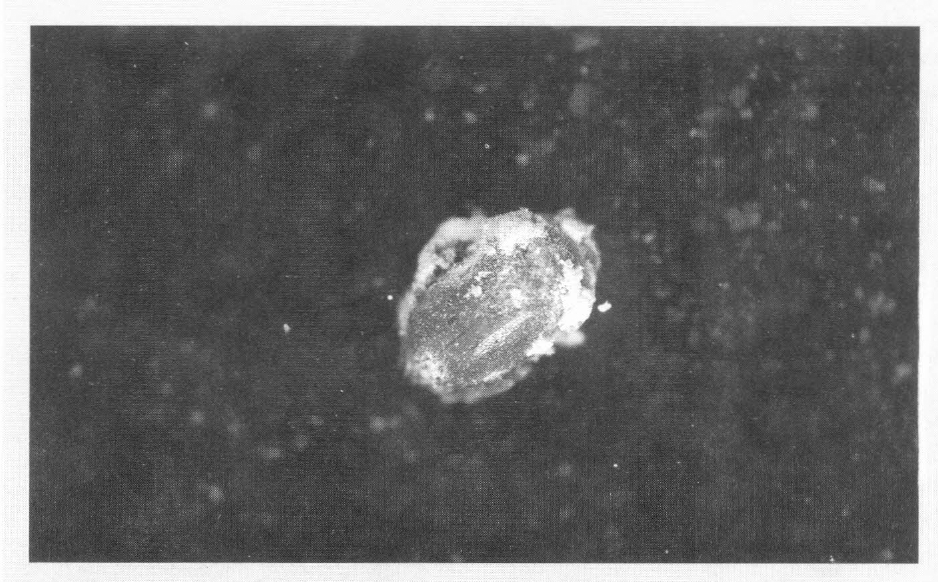
Beauveria bassiana afectando adultos de Cyclocephala sp. pos. lucida.
Himenópteros ectoparásitos de las familias Scoliidae y Tiphiidae también se hicieron presentes, aunque en menor proporción que los microrganismos entomógenos. Los más comunes son las avispas de la familia Scoliidae, las cuales son corpulentas y de color amarillo y negro vistoso (Fig. 6). Estas avispas se les observa volando cerca del suelo en las mañanas soleadas y se profundizan en el suelo buscando larvas hospedantes y se han encontrado hasta 28 cm de profundidad. Las avispas ovipositan sobre el dorso de la larva, detrás de la cabeza (meso-noto), donde eclosiona y se desarrolla la larva, succionando el contenido interno y causando la muerte de la larva de chisa, dejando las paredes del integumento unidas. La pupa se desarrolla dentro de un cocoon algodonoso de color café claro, el cual se encuentra a profundidades entre 30 y 50 cm.

Avispas Scoliidae, ectoparasitos de larvas de Scarabaeidae.
En la muestra procedente de San Vicente se observó la acción endoparasítica de moscas de la familia Tachinidae. Estas moscas consumen todo el contenido interno de la larva de chisa y rajan lateralmente el integumento para salir. Empupan por fuera del insecto.
Al comparar los factores de mortalidad mediante los rangos de Friedman, se detectan dos grandes grupos. Uno donde se destaca la enfermedad lechosa y el nematodo entomógeno del orden Rhabditida, como los agentes más importantes de control biológico, teniendo ambos un aporte estadísticamente igual en el control de la chisa (Tabla 3). Dentro de este mismo grupo se detecta una mortalidad alta, con igual valoración estadística que las anteriores denominada «otras causas». En este factor se acumula probablemente un número de chisas con síntomas terminales de la enfermedad lechosa (obscuras y descompuestas).
Comparación estadística de los factores de mortalidad en larvas de Scarabaeidae. Oriente Antioqueño. 1992.
DMS = 21
Otras causas - enfermedad lechosa = Acaros = Nematodo nato > M. anisopliae = Parasitoide = Mermitidae = B. bassiana
Un segundo grupo dentro de los factores de mortalidad de la chisa incluye los hongos entomógenos M. anisopliae, B. bassiana, los parasitoides y los nematodos de la familia Mermithidae; todos ellos, iguales entre sí, tienen un menor efecto en el control natural. Este resultado no indica que tengan menor importancia, ya que en un momento dado podrían ser más efectivos si las condiciones les fueran favorables. El alto uso de agroquímicos, en especial de fungicidas, puede estar limitando el crecimiento o la esporulación de los hongos patógenos (Hernández y Rodríguez 1992).
Conclusiones
En el Oriente antioqueño, las chisas tienen varios agentes de control biológico que afectan sus poblaciones en un 44%. En forma natural aparecen en casi todas las localidades muestreadas las bacterias B. popilliae + B. lentimorbus afectando larvas y pupas del insecto. Los nemátodos parasíticos del orden Rhabditida son también comunes y causan mortalidad sobre el estado larval.
Los hongos entomógenos M. anisopliae y B. bassiana son comunes, especialmente el primero, del cual se tienen 14 aislamientos codificados según la localidad de recolección.
Se encontraron parasitoides de las familias Scoliidae, Tiphiidae (Hymenoptera) y Tachinidae (Diptera) atacando larvas de chisa, pero su incidencia sobre la población es baja.
