Abstract
El propósito del trabajo fue el de determinar el comportamiento y la dinámica de la infección de la filaria Dipetalonema viteae en su vector, la garrapata blanda Ornithodoros tartakowskyi así como el de analizar el comportamiento de este argásido en el laboratorio. En los estudios histológicos de los vectores infectados se encontró, que en las garrapatas, que no se les permitió picar después de la infección, las larvas se distribuyeron en grupos por el hemocelo, especialmente en la base de las patas, en la base del capítulo, alrededor del orificio genital (al nivel del cerebro), alrededor del poro anal y en los espacios hemocelómicos laterales y posteriores. Durante la picadura de los ácaros, las larvas mostraron una marcada migración hacia el extremo anterior, congregándose especialmente en el capítulo. Durante la transmisión, las larvas penetraron algunas estructuras del aparato digestivo anterior, para entrar a la cavidad bucal, de donde son transmitidas a su huésped vertebrado; esto lo realizan a través de cuatro posibles vías: 1) la unión de la faringe con la cavidad bucal; 2) el esófago; 3) los conductos salivares, y 4) el techo del hipostoma. Las garrapatas eliminaron microfilarias en el líquido coxal, hecho que podría interpretarse como un mecanismo que previene hiperinfecciones, que comprometen la vida de los vectores. Esta especie de ácaro exhibió un hábito canibalístico, siendo capaz de adquirir y transmitir la infección de garrapata a garrapata, comportamiento que ayudaría a conservar esta especie de filaria en la naturaleza.
Introduccion
Las filarias son parásitos altamente especializados que se diferencian por algunas características morfológicas y detalles de su ciclo de vida que son únicos entre los nemátodos. El período más crítico de su vida es el que pasan en el huésped intermediario, el cual a su vez está sujeto a la acción del micro y macro clima, cuyos factores regulan el desarrollo de las larvas dentro del vector. La constante aparición en el hombre de casos de zoonosis por filarias relieva la necesidad de obtener información sobre los ciclos de vida y modos de transmisión de las filarias de animales. Se ha demostrado que filarias, que eran consideradas parásitos exclusivos de animales, son en realidad responsables de infecciones importantes en el hombre (Danaraj y Schacher, 1957; Buckley, 1958; Nelson, 1965; Beaver y Orihel, 1965).
El descubrimiento por Chabaud (1952) de la filaria Dipetalonema viteae en el teiido subcutáneo del roedor de los desiertos Meriones libycus y el subsiguiente establecimiento de la infección en el laboratorio en garrapatas de la especie Ornithodoros tartakowskyi por Baltazard (1953), abrieron nuevos campos de investigación en la filariasis experimental. Este modelo ha sido señalado como uno de los más ventajosos para el estudio de diferentes aspectos biológicos de las infecciones por filarias (Baltazard et al., 1953; Worms et al., 1961; Weiss, 1970). Sin embargo pocos estudios se han publicado acerca del comportamiento de los parásitos dentro de sus huéspedes intermediarios. Se sabe por ejemplo, que las larvas de filarias en desarrollo, y la migración de las mismas, destruyen los tejidos de los mosquitos y moscas, afectando sus actividades y la transmisión de la infección (Townson, 1970; Beckett y Boothroyd, 1970; Lavoipierre, 1958).
De otra parte, la alimentación de ciertos artrópodos sobre miembros de la misma especie o especies diferentes ha sido descrita por varios autores; este comportamiento, sin embargo, no ha sido clarificado en los argásidos. Observaciones previas en el laboratorio habían demostrado. que las garrapatás jóvenes presentaban una gran tendencia a montarse sobre otras recién alimentadas y trataban de picarlas; además es poco lo que se conoce sobre el comportamiento de esta filaria dentro de su vector. Por los hechos anteriormente mencionados se consideró importante estudiar la dinámica de la población de larvas de esta filaria en su vector con el fin de obtener una mejor comprensión de los aspectos de transmisión, y de estudiar el comportamiento de las garrapatas en el laboratorio. Los propósitos primordiales de la presente investigación fueron:
Describir el comportamiento migratorio de las larvas infectantes de la filaria D. viteae y determinar la correlación de las estructuras internas del vector y la trayectoria seguida por las larvas desde el sitio de su desarrollo hasta los sitios por los cuales son transmitidas a los huéspedes definitivos.
Determinar la posibilidad de canibalismo entre los individuos de la garrapata de la especie O. tartakowskyi y estudiar la posible transmisión de la infección de garrapata a garrapata.
Materiales Y Metodos
En la presente investigación se utilizó el modelo experimental formado por la filaria D. viteae (KrepKogorskaya, 1933) (Chabaud, 1957), el roedor Meriones unguiculatus (Milne-Eduards, 1867) y la garrapata O. tartakowskyi.
Estudios Histologicos
La distribución y comportamiento de las larvas del D. viteae dentro de las garrapatas fueron estudiados en cortes histológicos de este último. Dicho comportamiento se comparó con aquel exhibido por las larvas en garrapatas infectadas, pero estando en estado de reposo, es decir, aquellas que no se les permitió picar un huésped después de la infección.
Garrapatas con más de 30 días de infección se pusieron a picar a un roedor y se fueron despegando a intervalos de cinco minutos durante una hora. Los argásidos se mataron por inmersión en agua caliente a 65°C, y después se cortaron transversalmente en dos y se fijaron en diferentes sustancias. Los fijadores utilizados fueron los siguientes: una modificación del fijador de Carnoy por DeGiusti y Ezman (1955), líquido de Zanker, Formol-alcohol-ácido acético (AFA) y formol neutro al 10%. Después de la fijación las garrapatas se deshidrataron en éter-etilen-glycol (cellosolve) con el fin de evitar el endurecimiento y luego en butanol. Los teiidos se embebieron en parafina de 57-60 grados de punto de fusión, y de cada garrapata se hicieron cortes seriados de cinco a seis micras de espesor, los cuales se colorearon con hematoxilina eosina.
Los cortes se estudiaron al microscopio compuesto y se tomaron microfotografías.
Para estudiar el canibalismo entre los individuos de esta especie de argásidos y la posible transmisión de la infección de garrapata a garrapata se realizaron varios experimentos:
Canibalismo e infección de garrapatas con microfilaria
En primer lugar para determinar si las garrapatas ingerían microfilarias de otras, grupos de 80 a 100 garrapatas se infectaron con microfilarias de D. viteae dejándolas ingerir sangre hasta repleción completa de un M. unguiculatus infectado. Los roedores fueron anestesiados con una inyección intraperitoneal de Nembutal a la dosis de 0.1 ml por 100 g de peso. Después de la alimentación las garrapatas se separaron en grupos de 10, y a cada grupo se le agregó varias ninfas hambrientas, las cuales se dejaron por espacio de una hora; al cabo de este tiempo las ninfas que mostraron haber picado a una garrapata nodriza e ingerido algo de sangre se separaron; algunas de ellas se disectaron en solución salina al 8.85% y otras se mantuvieron en el laboratorio por espacio de un mes para determinar el desarrollo de las microfilarias.
Transmisión de larvas infectantes de garrapata a garrapata
En este experimento se realizaron varias pruebas que consistieron básicamente en colocar por separado en platos de Syracuse pequeños una garrapata con más de 30 días de infección y hambrienta, junto con una recién alimentada pero no infecta; después de dos horas de estar en contacto se disectaron las garrapatas nodrizas para determinar la transferencia de larvas infectantes hacia éstas. Los platos de Syracuse con las dos garrapatas se cubrieron con una laminilla para evitar su escape y tratar de mantenerlas en la mayor vecindad posible.
Eliminación de microfilarias en el líquido coxal
En el tercer experimento se estudió la eliminación de microfilarias en el líquido coxal. En este caso se alimentaron garrapatas sin infección sobre M. unguiculatus infectadas con microfilarias de D. viteae. Después de alimentarse, cada garrapata se colocó en un plato de Syracuse pequeño y se cubrió con laminilla; luego, los recipientes se colocaron en una cámara húmeda y se observaron constantemente durante las 10 primeras horas después de la alimentación. Cuando alguna de ellas excretó el líquido coxal, inmediatamente se añadió una gota de solución salina fisiológica con el fin de evitar la desecación. Los líquidos se examinaron bajo un microscopio compuesto a 4X y 10X, y se llevó el registro del número de microfilarias eliminadas.
Resultados
Hallazgos histológicos
El estudio de las secciones de las garrapatas en estado de reposo mostraron que las larvas de la filaria se encontraban distribuidas en todo el hemocelo pero con una mayor concentración en los espacios hemocelómicos posteriores y alrededor de los sacos rectales (Figuras 1 y 2); sin embargo, pocas larvas se encontraron en el capítulo (Figuras 3, 4 y 5), y en esta región los órganos exhibieron una estructura completamente normal en ausencia de larvas. En contraste con lo anterior, en las garrapatas a las cuales se permitió picar un huésped, la actividad de las larvas produjo desplazamiento y desorganización de los músculos y otras estructuras internas (Figuras 6 y 7). Una de las características de la distribución de las larvas fue el hecho de que casi invariablemente se observaron en grupos, y casi nunca aisladas.
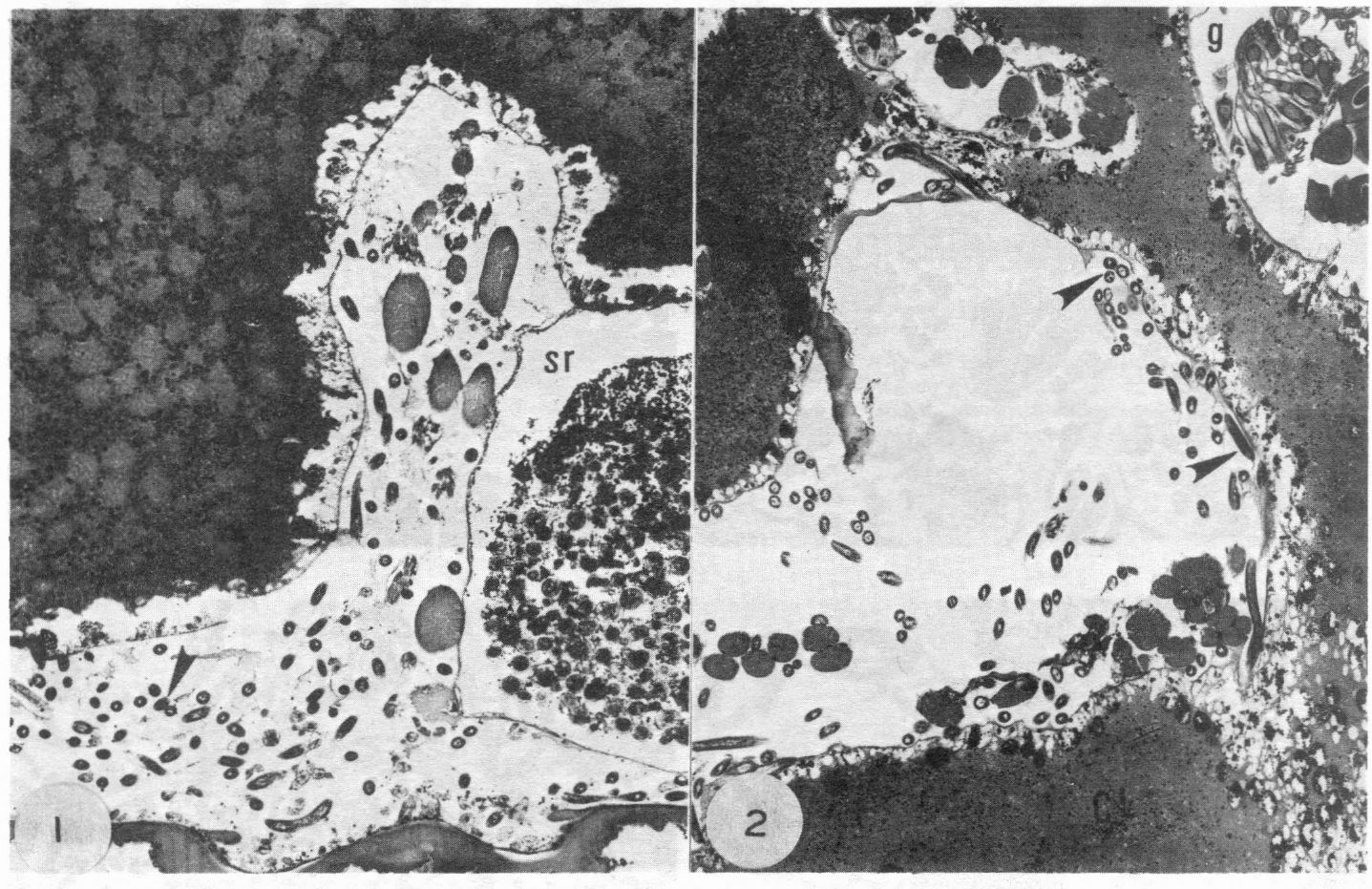
Secciones frontales de la región posterior de garrapatas infectadas a las que no se les permitió picar después de la infección. 97Χ.
Sección a nivel de los sacos rectales (sr) mostrando grupos de larvas en los espacios hemocelómicos comprendidos entre los dos lóbulos postero-centrales del estómago.
Sección a nivel de las gónadas (g) mostrando grupos de larvas en el espacio entre los lóbulos postero-centrales del estómago. Note las larvas recostadas sobre la pared epitelial del cecum (flechas). Algunas larvas logran penetrar la pared, para luego encapsularse y morir en la luz del estómago.
Secciones frontales de la región anterior de garrapatas infectadas, a las que no se les permitió picar después de la infección. 97X.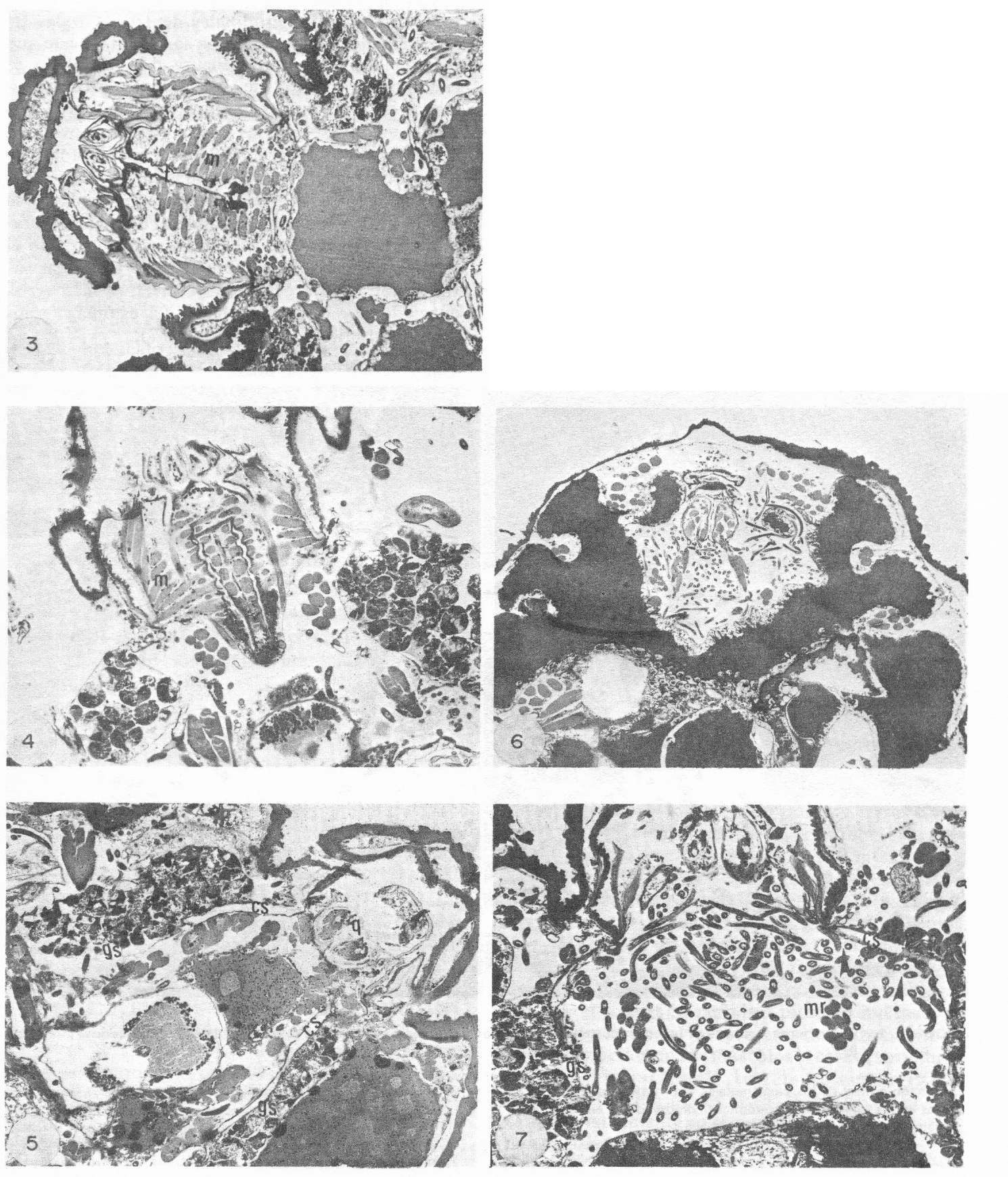
Corte del capítulo con la faringe bien definida (f), la cual muestra las comunicaciones claras con la cavidad bucal y el esófago. Los músculos (m) exhiben una perfecta organización. Note la ausencia de larvas en esta área.
Corte mostrando la configuración del capítulo y sus músculos (m). A pesar de la infección no se observan larvas en el capítulo ni en las áreas cercanas.
Corte a nivel de las glándulas salivares (gs) y región media de los queliceros (q), mostrando una excelente configuración de las glándulas con sus conductos salivares (cs). Al igual que en las figuras anteriores no se observan larvas en la región capitular, ni en el espacio hemocelómico central.
Secciones frontales de una garrapata infectada, sacrificada y fijada inmediatamente después de 55 minutos de estar picando a un huésped.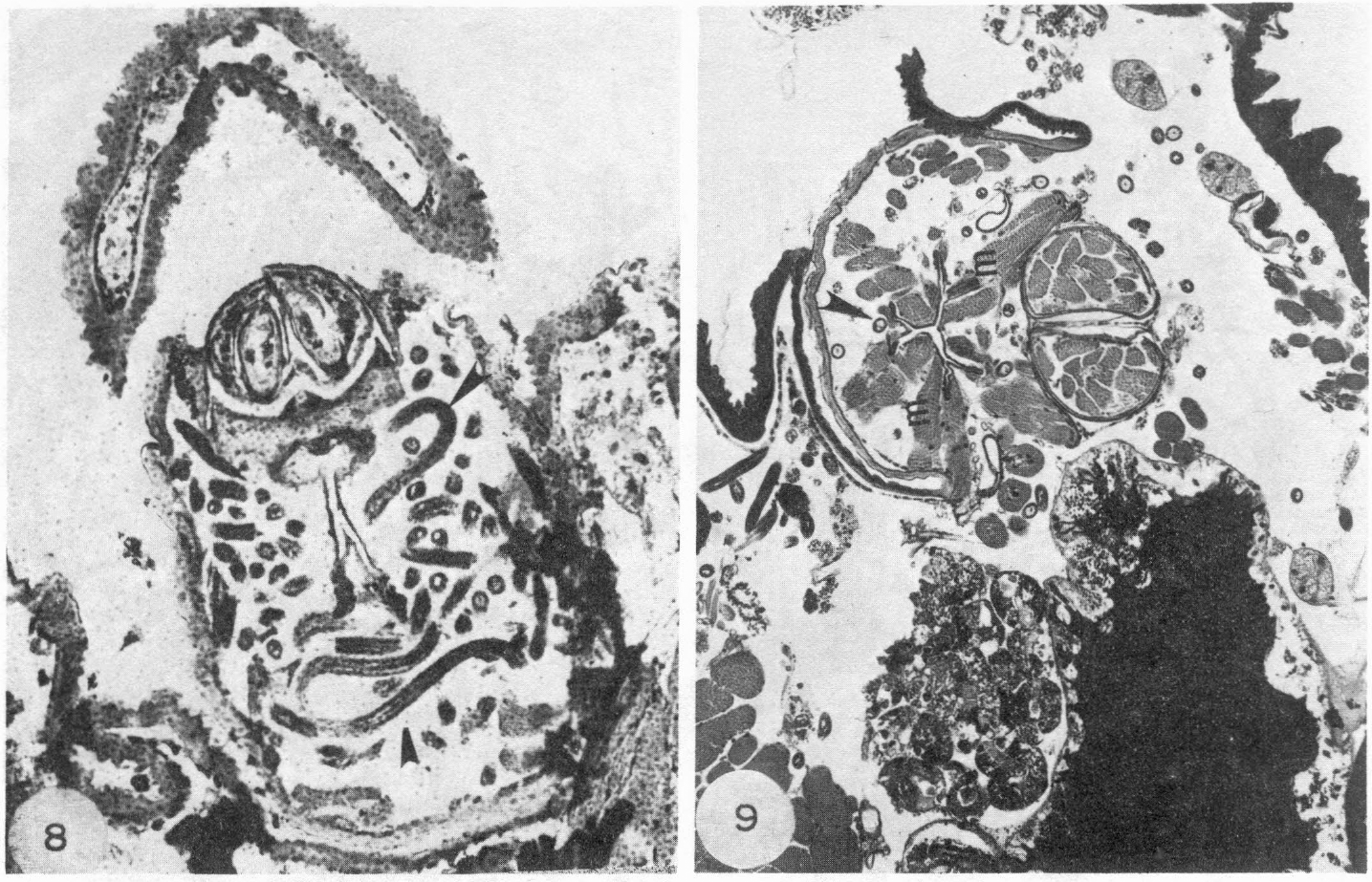
Corte a nivel del camerostoma y porción basal de los queliceros, mostrando concentración de larvas en el espacio hemocelómico central cónico. Note la ausencia de larvas en los espacios postero-laterales. 39X.
Corte a nivel de las glándulas salivares (gs) y la unión entre el esófago y el proventrículo. Las larvas (flechas) se ponen en contacto con la superficie interna de las glándulas en la región media de los conductos salivares (cs). Not la completa desorganización de los músculos retractores (mr) de los queliceros. 97X.
El acto de la picadura estimuló la migración de las larvas hacia el extremo anterior, resultando este hecho en una excesiva concentración de larvas en el espacio hemocelómico central de la región del capítulo, donde se vieron rodeando el proventrículo, el esófago, las glándulas salivares, la faringe y las partes bucales. La migración fue progresiva, observándose que a los pocos minutos de comenzada la picadura de las garrapatas, las larvas empezaron a concentrarse alrededor de la faringe (Figura 8). A medida que pasó el tiempo, éstas se movieron hacia el capítulo, localizándose entre los queliceros y la faringe (Figuras 9 y 10), para llegar luego al foramen del capítulo (Figura 11). Las larvas se agruparon especialmente en la unión de la faringe con la cavidad bucal, sitio en el cual la pared es muy delgada y altamente susceptible a la perforación por parte de las larvas. Estas fueron capaces de moverse a lugares aún más anteriores y localizarse en el hemocelo del hipostoma, introduciéndose por el estrecho espacio que queda entre el surco y la pared externa de dicha estructura (Figura 12).
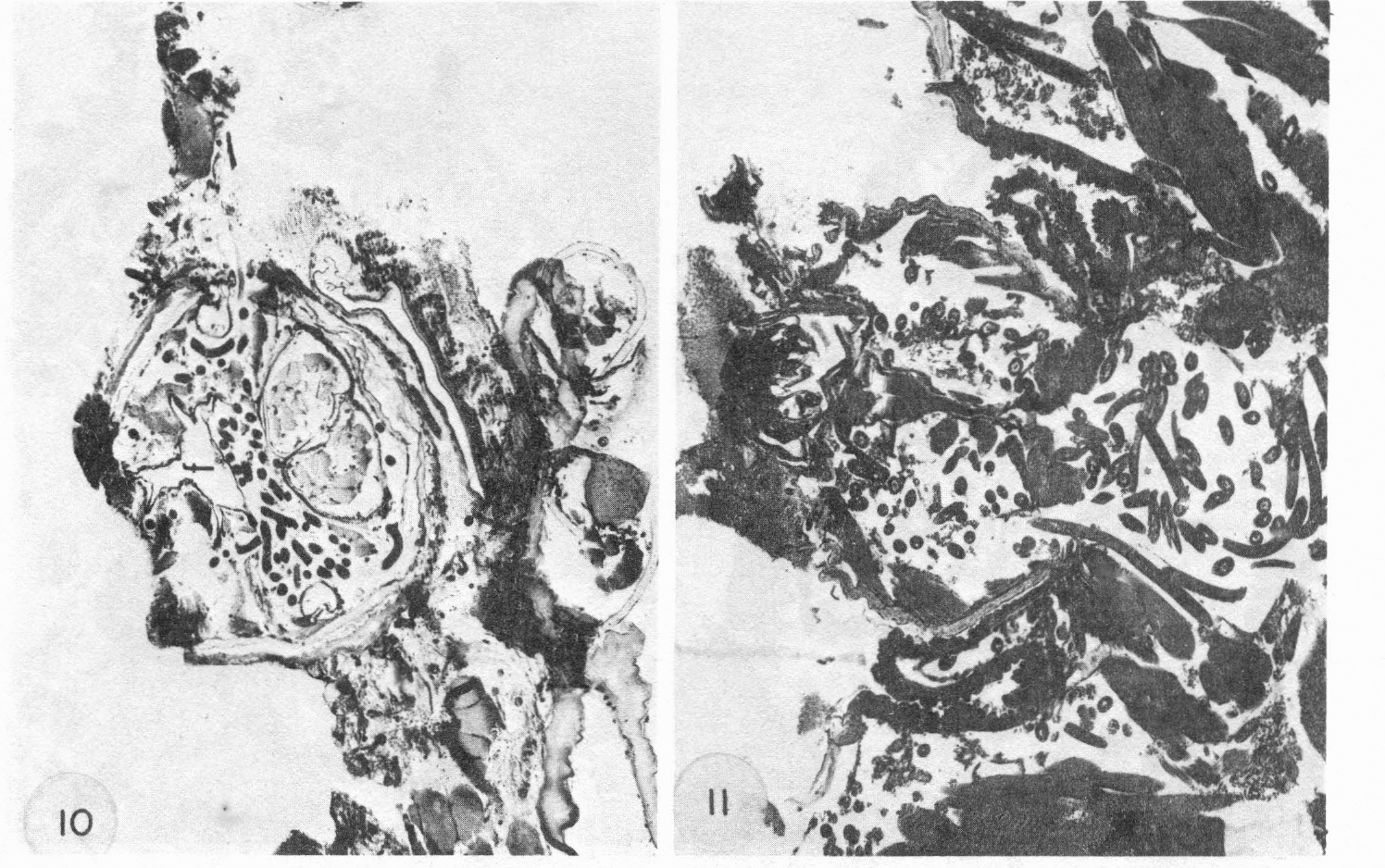
Secciones de garrapatas infectadas, sacrificadas y fijadas inmediatamente de removidas de los huéspedes.
Corte frontal del capítulo de una garrapata, después de 20 minutos de estar picando a un huésped; la foto muestra la terminación entre la faringe y la cavidad bucal. Las larvas (flechas) se encuentran agrupadas alrededor de la faringe y han comenzado a concentrarse alrededor de esta unión. Los músculos del capítulo han sido desorganizados y desplazados. 145X.
Corte transversal del capítulo cerca al esófago de una garrapata que estuvo picando a un huésped por 40 minutos. La faringe se observa rodeada por los músculos dilatadores y contractores (m), los cuales presentan una estructura y disposición normal. 97X.
Corte del capítulo a un nivel más anterior que en la Figura 9, cerca de la cavidad bucal. La faringe (f) presenta una perfecta configuración, aunque muchas larvas se encuentran en sus alrededores, especialmente entre la pared más delgada y los queliceros. 97Χ.
Sección frontal del capítulo de una garrapata infectada sacrificada 45 minutos después de estar picando a un huésped. La foto muestra la conexión entre la faringe y la cavidad bucal con una abundante concentración de larvas en este sitio. Una larva está cruzando por esta unión (flecha). Note que los músculos contractores de la faringe han sido desplazados por las larvas. Otro grupo de larvas se ve en el espacio hemocelómico detrás del capítulo. 97X.
Corte transversal de las partes bucales a nivel del hipostoma de una garrapata infectada y sacrificada a los 35 minutos de haber empezado a picar a un roedor. E! surco del hipostoma (sh) y la cavidad bucal son muy visibles, así como el salivarium (s) a cada lado de los queliceros. Una larva (flecha) se observa en el espacio hemocelómico comprendido entre la pared quitinosa externa y el techo del hipostoma.
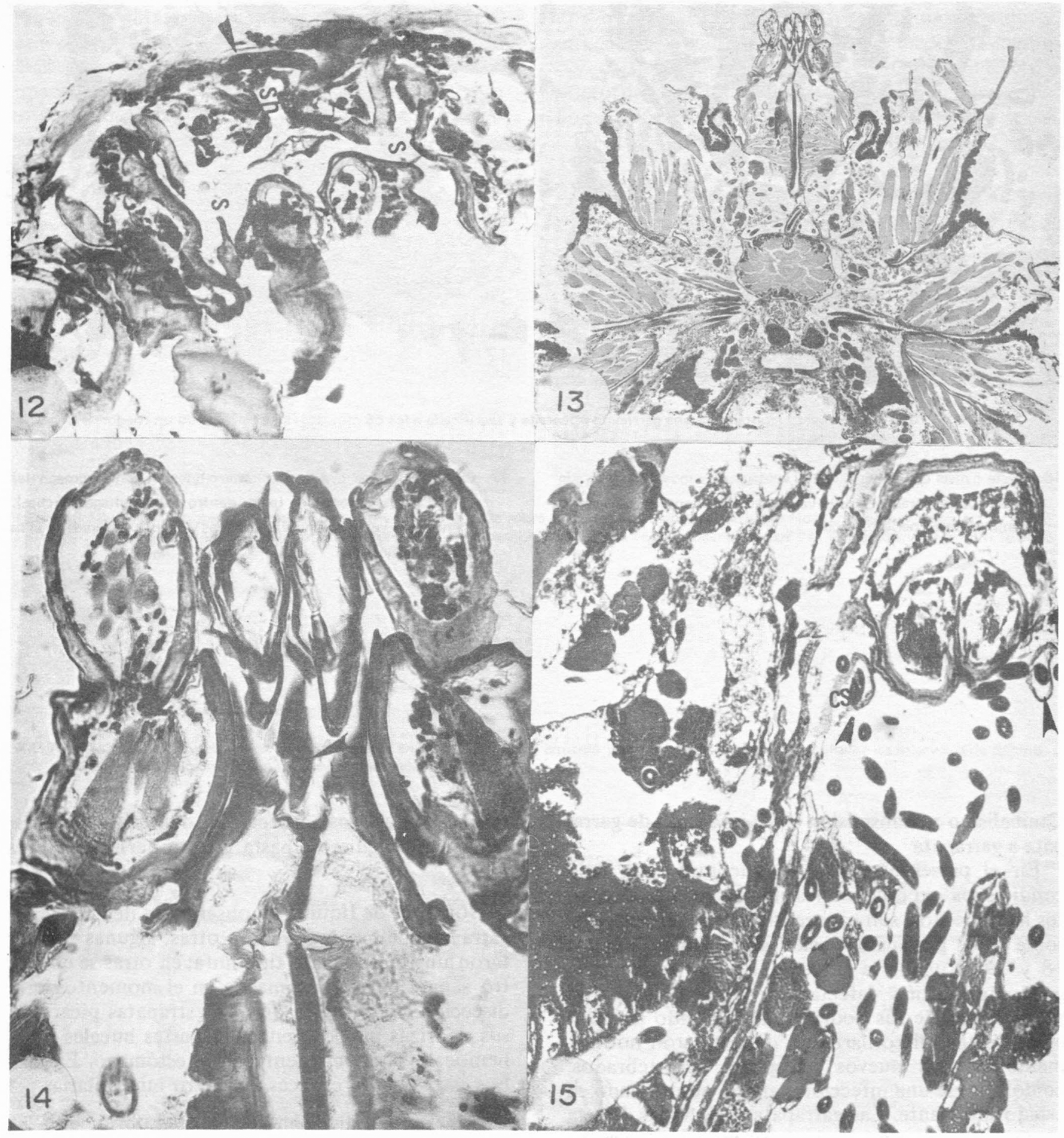
Sección frontal del capítulo de una garrapata infectada y sacrificada a los 45 minutos de estar picando a un huésped. Los cortes muestran la trayectoria exacta seguida por las larvas durante su transmisión.
Se ve una larva dentro del esófago, la faringe y la cavidad bucal (parte terminal). 97X.
La foto muestra las partes bucales a un mayor aumento; se hacen claros los cortes de las larvas (flecha). 240X.
Corte oblicuo -longitudinal de la porción anterior de una garrapata infectada después de picar a un roedor por espacio de 25 minutos. Se observan los conductos salivares (cs), cada uno con una larva en su interior (flechas). También se observan larvas concentradas en la superficie interna de las glándulas salivares.
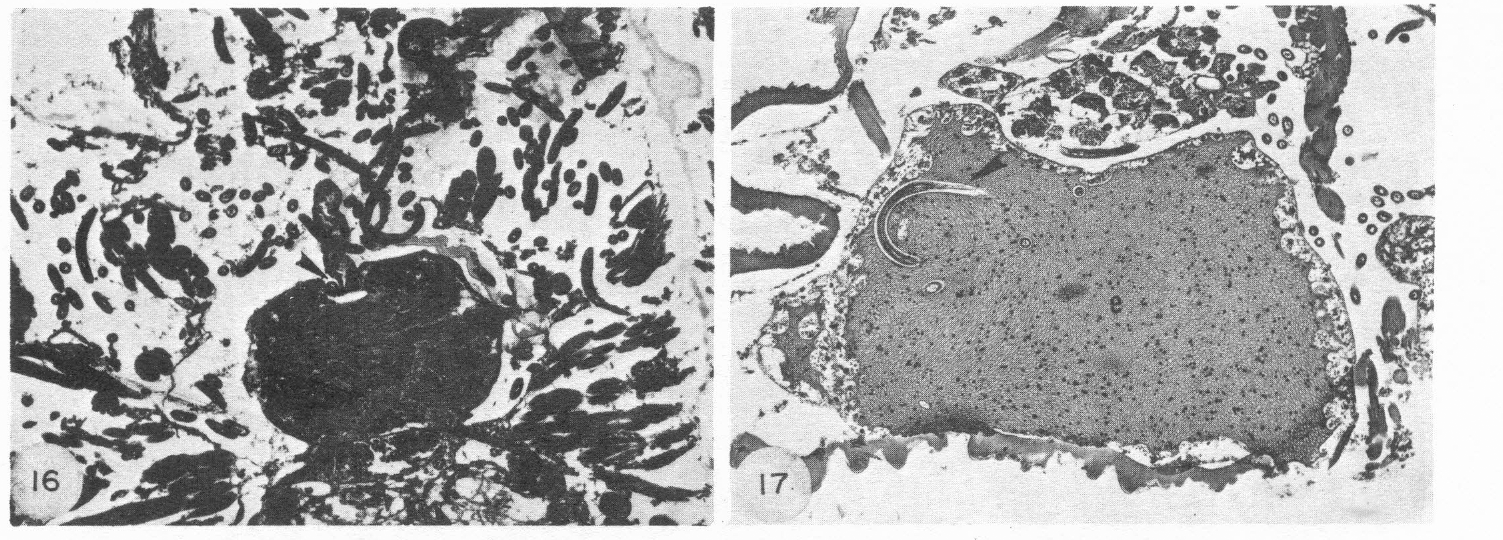
Secciones frontales de una garrapata infectada y sacrificada a los 55 minutos de estar picando un roedor. 97X.
Corte a nivel del cerebro (c) y el esófago, que muestra la entrada de éste por el cerebro. Dos larvas se ven claramente en el espacio hemocelómico periesofágico.
Corte a nivel de los lóbulos antero-laterales del estómago (e), el cual muestra cortes de larvas dentro del estómago (flechas). También se ven las glándulas salivares y grupos de larvas en el hemoceloma anterior.
Las larvas fueron también identificadas en cortes transversales y longitudinales dentro de todas las secciones del esófago, aún en la región de éste que penetra en el cerebro (Figura 13). También se encontraron dentro de las regiones proximal y media de los conductos salivares (Figura 15). Estando en el esófago las larvas pueden moverse o desplazarse tanto hacia adelante a buscar la faringe (Figura 13) y entrar a la cavidad bucal (Figura 14) o hacia atrás para entrar al estómago. Las larvas se vieron muy a menudo entrando al espacio hemocelómico periesofágico, que se encuentra, cuando el esófago entra por el cerebro (Figura 16); si las larvas penetran al esófago a este nivel, es fácil verlas entrando por el proventrículo del estómago a los lóbulos anteriores a éste (Figura 17).
Canibalismo y transmisión de la infección de garrapata a garrapata
En el presente estudio se encontró, que bajo condiciones experimentales ninfas jóvenes y adultos hambrientos, son capaces de picar y alimentarse sobre otras garrapatas recién alimentadas (Figuras 18 y 19). Cuando la alimentación se realizó sobre garrapatas recién infectadas, aquellas ingirieron microfilarias de sus nodrizas, adquiriendo la infección; dichas microfilarias se desarrollaron normalmente en sus nuevos huéspedes invertebrados, como si fuese una infección natural, adquiriendo su estado infectante. Las garrapatas infectadas de esta manera fueron capaces de transmitir las larvas 30 días después de la infección, cuando se les permitió picar a un huésped definitivo o inclusive a otras garrapatas normales.

Garrapatas pequeñas picando y alimentándose sobre otras recientemente engordadas. Note que las garrapatas nodrizas han ingerido sangre hasta repleción completa, aumentando hasta cinco veces su tamaño. Los dos ácaros eran del mismo tamaño antes de la alimentación.
Garrapatas con más de 30 días de infección, también transmitieron larvas infectantes, cuando éstas picaron a nodrizas normales, y de éstas se recobraron diferentes números de larvas infectantes así: trece larvas de una garrapata nodriza, once de dos, siete en una, seis en una, cinco en cinco y una larva en una garrapata. Las larvas infectantes se observaron activas e infectantes dentro de sus huéspedes intermediarios hasta por un período de tres meses.
Dos tipos de líquido se observaron dentro de las garrapatas alimentadas sobre otras; algunas presentaron un líquido claro tipo linfa; en otras se encontró sangre en sus estómagos en el momento de la disección. Esto indica que las garrapatas picaron a sus nodrizas introduciendo las partes bucales en el hemocelo o directamente en el estómago. En ambos casos fueron capaces de ingerir microfilarias.
En este estudio también se descubrió, que las garrapatas de la especie Ornithodoros tartakowskyi, eliminan microfilarias en el líquido coxal. Estos argásidos excretaron el líquido después de haberse alimentado, es decir, después de haber sido desprendidas del huésped. La emisión fue irregular, tanto en el tiempo, como en la cantidad emitida. Algunas garrapatas lo eliminaron en unos pocos minutos (12-20) después de haber sido desprendidas; otras, por el contrario tardaron un período más largo. Las garrapatas grandes eliminaron gotas grandes de líquido por una sola vez, las pequeñas, minúsculas gotas, las cuales se secaron rápidamente; a pesar de esto, se encontraron microfilarias en estas gotas pequeñas. Algunas garrapatas fueron capaces de emitir líquido en dos oportunidades en un período de pocas horas después de la alimentación completa.
Pocas microfilarias se encontraron en los líquidos emitidos a los pocos minutos después de la infección; el número aumentó considerablemente con el tiempo, observándose el mayor número de microfilarias a las tres horas (105 Mf) y a las cinco horas (96-185 Mf). Después de la quinta y sexta hora el número eliminado fue disminuyendo (Tabla 1).
Número de microfilarias (Mf) eliminadas en el líquido coxal emitido por garrapatas individuales a diferentes intervalos de tiempo, después de alimentarse en un roedor con microfilarias.
Garrapatas que emitieron líquido coxal en dos tiempos diferentes.
ND. No determinado.
Discusion
El análisis de los cortes histológicos de las garrapatas infectadas, tanto de aquellas que se pusieron a picar a un huésped, como de aquellas que no se les permitió picar después de la infección inicial, confirmaron las observaciones realizadas, de las garrapatas bajo el microscopio compuesto. Después de que las larvas se desarrollan y salen de las fibras musculares de sus vectores, permanecen migrando en grupos por el hemocelo, pero exhibiendo una mayor concentración en la mitad anterior de los ácaros. Esta distribución fue drásticamente alterada en el momento de la alimentación, tiempo durante el cual la mayoría de las larvas migraron hacia el extremo anterior, invadiendo toda la región del capítulo. Esta observación es similar a la reportada por Lavoipierre y Ho (1966). Estos autores estudiaron la transmisión de la filaria Brugia pahangi por el mosquito Aedes togol y encontraron que las larvas se concentran especialmente en las estructuras anteriores de los mosquitos. En las garrapatas la migración de las larvas hacia la estación anterior, permite que éstas escapen del hemocelo a la cavidad bucal, para ser transmitidas por cuatro posibles sitios: 1) La membrana laminar, localizada en la unión de la faringe con la cavidad bucal; 2) Los conductos salivares, especialmente las porciones medial y proximal; 3) El esófago y la unión de éste y el proventrículo; y 4) El techo del hipostoma.
Discutiendo el mismo aspecto de transmisión de la misma especie de filaria Bain (1967), sugirió, que el salivarium y la faringe eran las dos rutas de escape de las larvas. Sus evidencias histológicas no fueron sin embargo, muy convincentes. En su reporte, ella incluye solamente dos fotografías con relación a este problema. Una foto del capítulo con la faringe, mostrando un orificio de la pared y algunas larvas tratando de penetrar por él, y otra foto al mismo nivel con algunas larvas dentro de la luz de la faringe. En el presente estudio se observó sin embargo, que debido a la composición quitinosa de este órgano, la ruptura durante los cortes es demasiado frecuente, factor que puede inducir a conclusiones e interpretaciones falsas. De otra parte, la presencia de larvas en la faringe, no necesariamente indica que ellas han penetrado por la pared de este órgano. La evidencia histológica obtenida en este estudio, sugiere claramente, que las larvas penetran el esófago y los conductos salivares. Existe la posibilidad de que las larvas que penetran al esófago o cavidad bucal, migren hacia atrás y lleguen hasta el estómago, donde permanecen atrapadas. La retención de larvas en el estómago es comprobada por la observación de larvas muertas y en degeneración dentro del lúmen del estómago.
Se desconocen los factores, que inducen la migración de las larvas hacia las partes bucales. Sin embargo, se encontró que la temperatura juega un papel importante, ya que todas las observaciones realizadas en el estudio indican que la temperatura de la piel del nuésped y el acto de picar, aumentan la concentración y la actividad de las larvas en la región anterior de los ácaros. La posición adoptada por las garrapatas durante la picadura (formando un ángulo de 45 grados con la piel) y la actividad de las partes bucales con movimientos rítmicos hacia atrás y hacia adelante, podrían jugar un papel muy importante en la aglomeración y reunión de las larvas. Estos dos factores, podrían a su vez alterar la presión del líquido hemocelómico hacia la región anterior, en efecto, el hipostoma se vuelve más turgente, debido a la acumulación de hemolinfa. Otra observación fue el incremento de la actividad de los lóbulos del estómago, cuando las garrapatas se pusieron en contacto con la piel de los roedores.
Por los resultados obtenidos es obvio, que las microfilarias invaden las glándulas coxales de las garrapatas y que son eliminadas por este órgano. La baja eliminación de microfilarias pocos minutos después de la alimentación, probablemente se deba a que en este corto tiempo, pocas larvas han tenido la oportunidad de penetrar la pared del estómago y pasar al hemocelo; a medida que el tiempo transcurre, un mayor número de microfilarias migran al hemocelo y la concentración en las glándulas aumenta.
Que las microfilarias son capaces de penetrar rápidamente los tejidos de estos artrópodos, se demuestra en el presente trabajo por su eliminación en el líquido coxal, en un período de 15 a 60 minutos después de la infección. La presencia de microfilarias en el líquido coxal, indica que ellas deben penetrar los tejidos, ya que las glándulas coxales no tienen conexión con el tracto digestivo y terminan ciegas en la cavidad corporal (Lees, 1946). Además de esto, Kliks (1967) y Works et al. (1961), demostraron que las microfilarias de esta especie invaden las fibras musculares en unas pocas horas después de entrar en las garrapatas.
El mecanismo de eliminación de microfilarias en estos artrópodos es diferente al observado en los mosquitos, ya que éstos no poseen glándulas coxales, pero eliminan el líquido a través del ano. Raid (1953), trabajando con Anopheles stephensis, observó la eliminación de gotas de sangre que contenían microfilarias. Eliminación de microfilarias en las deyecciones de los mosquitos al poco tiempo de una infección, también ha sido encontrado en Mansonia annulifera y M. dieres (Wharton, 1957).
La eliminación de microfilarias en el líquido coxal por esta especie de argásido, podría ser considerada como un mecanismo de defensa, que tiende a evitar hiperinfecciones mortales de los huéspedes vectores.
La alimentación de unos individuos sobre otros; parece ser un fenómeno común entre ciertas especies de artrópodos hematófagos. Este hábito, en O. tartakowskyi, podría ser de una gran importancia en la transmisión de organismos patógenos, y podría servir a la vez como un mecanismo de propagación y conservación de esta especie de filaria en la naturaleza, tal como lo sugieren los resultados obtenidos en este estudio.
