Abstract
The mass rearing of Bracan kirkpatricki Wilkinson on larvae of Galleria mellanella (L.) was carried out in the Entomology Laboratory of the Universidad del Valle, at Cali, 970 masl with 2YOCand 65% of relative humidity. The object of the work was to evaluate an efficient method which would guarantee the mass rearing of the parasitoid B. kirkpatrickion G. mellanella larvae, with a commercial projection. Metal containers became a very functional mechanism for the rearing of G. mellanella. In regard to the occupation of space, 0,100 m3 was achieved against 0,232 m3 with its equivalent in glass flasks, .although as lar as the number of larvae produced is concerned, there were no marked differences between the systems. The most functional parasitation chamber was the large one (62 x 32 x 9 cm) with potential to generate between 3200 and 4560 parasitoids daily, with a sex relation 01 1♀:1♁, and 68% parasitism, obtaining 5.0 parasitoids/larvae.
Introducción
Las plagas del algodón que cobran importancia en nuestro medio por los daños causados a nivel de las estructuras reproductivas son: el picudo del algodonero Anthonomus grandis Boheman (Coleoptera: Curculionidae), el gusano rosado de la India, Pectinophora gossypiella (Saunders) (Lepidoptera: Gelechiidae) y el gusano rosado colombiano, Sacadodes pyralis Dyar (Lepidoptera: Noctuidae) (Andrews y Quezada 1989).
El primer intento para el control biológico de estas plagas se inició con Ectatoma tuberculatum (Olivier) (Hymenoptera: Formicidae), hormiga depredadora que al ser atraída por los nectarios del algodón, ataca y mata muchos insectos incluyendo adultos de A. grandis (Clausen 1978).
La búsqueda de insectos parasitoides se inició en el Perú durante 1941 a 1945, donde se encontraron larvas del picudo peruano del algodonero, A. vestitus Boheman, altamente parasitadas por un Chalcididae y dos especies de Braconidae (Hymenoptera) (Clausen 1978). Un parasitoide externo gregario y promisorio es Bracon kirkpatricki Wilkinson (Hymenoptera: Braconidae), el cual fue probado, con buenos resultados, tanto contra A. grandis como contra P. gossypiella (Cross et al. 1969).
Cross et al. (1969) presentaron técnicas para la cría masiva de B. kirkpatricki fundamentadas en el uso de cajas de parasitación, para lo cual usaron cajas de petri plásticas con nylon donde se colocaban las avispas, y bandejas con larvas de Spodoptera exigua (Hubner) (Lepidoptera: Noctuidae), como huésped, las cuales se cubrían con pañuelos faciales. La misma técnica fue empleada por León (1988), pero usando cajas mantequilleras y como huésped larvas de Galleria mellonella (L.) (Lepidoptera: Pyralidae).
El valor de B. kirkpatricki como parasitoide funcional de A. grandis, P. gossypiella, S. pyralis y Spodoptera frugiperda (J.E. Smith) (Lepidoptera: Noctuidae) motivó el presente trabajo, el cual consistió en evaluar una metodología para la cría masiva de B. kirkpatricki con proyección comercial, sobre larvas de G. mellonella.
Materiales Y Métodos
El trabajo se realizó en la laboratorio de la Sección de Entomología, Departamento de Biología, Universidad del Valle en Cali, a una altura de 970 msnm y con temperatura de 27°C y 65% de humedad relativa.
Comparación de la cría masiva de G. mellonella en dos tipos de estructuras de cría
A partir de una colonia básica de G. mellonella, mantenida en laboratorio, se obtuvieron las posturas necesarias para efectuar los ensayos de cría de las larvas, bien en porrones de vidrio o en recipientes metálicos.

Porrón de vidrio con dieta artificial e infestado con huevos de G. mellonella sobre tiras de papel toalla.
Recipiente metálico con dieta infestada con huevos de G. mellonella provistos en tiras de papel.
Para la evaluación comparada de las dos estructuras de cría se usaron dos tratamientos con tres repeticiones cada uno. Los tratamientos se montaron simultáneamente y las repeticiones se hicieron al tiempo para facilitar la toma de datos de las variables en estudio, las cuales fueron principalmente: producción total de larvas de G. mellonella y espacio ocupado por cada sistema.
Comparación de tres cámaras de parasitación para la cría masiva de B. kirkpatricki
Para la multiplicación del parasitoide, la metodología se basó en las desarrolladas por Cross et al. (1969) y Bryan et al. (1971). En los ensayos para establecer la mejor técnica de cría de B. kirkpatricki bajo condiciones de laboratorio, se emplearon tres tamaños de cámaras de cría: una pequeña de 12 x 18 x 9 cm, una mediana de 31 x 16 x 9 cm y una grande de 62 x 32 x 9 cm (Fig.3).

Tipo de cámaras de parasitación usadas para la cría masiva de B. kirkpatricki. a. pequeña b. mediana c. grande
La cepa del parasitoide se obtuvo del Laboratorio de Entomología del ICA, en Palmira; y como huésped se utilizaron larvas de G. mellonella de V instar, colocadas en paquetes de parasitación, consistentes en láminas de cartulina de 8 x 12 cm y forradas con pañuelos faciales. Con este material como base, se llevó a parasitar en cada una de las cámaras que según su dimensión proveen un número determinado de avispas. La relación parasitoide - huésped fue de cinco avispas de B. kirkpatricki por cada larva de G. mellonella, la relación de macho a hembra para el parasitoide fue de 1:1 (Tabla 1).
Distribución del material biológico por cámara de parasitación
El ensayo se efectuó durante 15 días, realizando dos parasitaciones diarias, de 4 horas cada una, y dejando entre cada exposición 1 hora de separación.
Los medios de parasitación se almacenaron y luego se trasladaron a cámaras de emergencia, donde las avispas se contaron y se separaron por sexos.
Los datos obtenidos se analizaron con base en un diseño completamente aleatorizado, con tres tratamientos y tres repeticiones cada uno. Además se realizó la prueba de Tukey para establecer diferencias entre los porcentajes de parasitismo. En este ensayo, las variables consideradas fueron: Número de machos y hembras producidos, relación de sexos y porcentaje de parasitismo.
Resultados Y Discusión
Comparación de la cría masiva de G. mellonella en dos tipos de estructura de cría
Al comparar los resultados de la cría masiva de G. mellonella en dos estructuras de cría diferentes, no se encontraron diferencias significativas.
Los porrones de vidrio tuvieron como producción promedia 11.509,33 ± 2.251,46 larvas, en tanto los recipientes metálicos tan solo produjeron, en promedio, 10.025,00 ± 247,49 larvas, debido al excesivo escape de estas. Muy probablemente, la caída accidental de rayos de luz sobre el recipiente causó el escape de las larvas, las cuales se caracterizan por ser fotosensibles.
Otras variables que se tuvieron en cuenta fueron: la eclosión de los huevos, que fue del 98% para ambos tratamientos; sin embargo, la producción final se vio afectada por el escape de las larvas pequeñas a través de la tela que cubrían los porrones o de las tapas de tela colocados sobre los recipientes metálicos.
Respecto a la producción de larvas por gramo de dieta, los porrones de vidrio produjeron, en promedio, 0,82 larvas, en tanto que en los recipientes metálicos se obtuvieron 0,71 larvas/g. Se aprecia que a mayor capacidad del recipiente, las larvas se pueden distribuir de tal manera que consumen lo suficiente para desarrollarse en forma adecuada y sin competencia por espacio.
En cuanto al tiempo de manipulación, se observaron diferencias entre las dos estructuras, siendo mayor para los porrones de vidrio, pues se requiere sacar la dieta de cada uno de ellos, resquebrajarla y obtener las larvas. En los recipientes metálicos, las larvas de quinto instar temprano e intermedio se aprovechan totalmente, pues se encuentran sobre las bandejas con dieta o desplazándose sobre las paredes del recipiente. Lógicamente, si se espera a que las larvas tejan el cocoon para empupar, el proceso se demorará más, sea cual fuese la estructura.
Tomando como base que la cantidad de dieta para 70 porrones es la misma que para un recipiente metálico (14 kilos), y aunque la relación larva por gramo de dieta varia de 0,82 larvas para porrones a 0,71 para recipientes metálicos, no existe diferencia en el costo por gramo de dieta producida. Por tanto, no se puede considerar, desde este punto de vista, como una desventaja para uno y otro sistema. El costo del gramo de dieta para los recipientes metálicos fue de $1,44.
Los recipientes metálicos se constituyeron en un mecanismo muy funcional para la cría de G. mellonella, puesto que el espacio ocupado por cada uno, 0,108 m³, fue menor comparado contra 0,232 m³ de su equivalente en porrones de vidrio.
El manejo de 70 porrones es más dispendioso y requiere de estantes metálicos para acondicionarlos, mientras que un recipiente metálico que ocupa el mismo espacio equivalente a su capacidad, puede acomodarse para efectos de manejo en una unidad modular de tres pisos, cada piso con dos recipientes, de tal forma que un total de seis ocupen un área de 0,832 mβ.
En consecuencia, resaltan las diferencias que favorecen los recipientes metálicos, por la manera como facilitan una mayor producción de larvas por unidad de espacio. En síntesis, condiciones ambientales como temperatura entre 27 a 30°C, humedad relativa del 65%, oscuridad total para los primeros instares de desarrollo (para evitar el escape de las larvas), comodidad para el establecimiento de las larvas en la dieta, mejor producción de larvas por gramo de dieta, menor tiempo de manipulación y menor espacio ocupado, favorecen el desarrollo de G. mellonella en estas estructuras.
Colateralmente, dentro de las observaciones generales efectuadas sobre G. mellonella, se encontró que algunas larvas, tanto en los porrones como en los recipientes metálicos, fueron afectadas, en pequeña proporción, por un patógeno. Los síntomas manifestados en coloración negra y cierta flacidez, hicieron presumir la infección por bacterias, lo cual concuerda con lo expuesto por Waage (1990).
Para determinar si efectivamente se trataba de algún tipo de bacteria, se realizó un aislamiento sobre agar nutritivo, lo cual corroboró su existencia, pues básicamente presentaba buen crecimiento sobre el medio, formaba esporas, a parte de haber sido extraído del fluído hemocélico. Esta sintomatología manifiesta similitud con infecciones ocasionadas por bacterias del género Bacillus. Por lo tanto, y según Waage (1990), se deben realizar pruebas de morfología descriptiva, técnicas de coloración y ensayos bioquímicos para identificar con mayor exactitud la especie.
Para determinar el posible factor de contaminación, se hizo un análisis. Se descartaron los porrones de vidrio o recipientes metálicos porque estos fueron previamente desinfectados. Probablemente en el proceso de preparación de la dieta aparezca el patógeno, aunque si bien es tratada con formaldehido al 10%, este preservativo no parece ser suficiente para impedir la contaminación de la bacteria, por lo cual se recomienda probar una dieta con antibióticos.
Comparación de tres cámaras de parasitación para la cría masiva de B. kirkpatricki.
En relación con los machos y hembras producidos, al evaluar las tres cámaras de parasitación se detectaron diferencias determinantes al momento de escoger el módulo propicio para la cría masiva.
En la cámara pequeña se obtuvieron en promedio 4.563,67 ± 662,20 avispas, alrededor de 304,24 parasitoides por día. El número promedio de machos fue de 3.009,00 ± 296,70 y el de hembras de 1.554,30±366,20 (Fig.4), lo que da una relación de sexos de 1♀:1,95♂. Los datos revelan la disparidad existente entre el número de machos y hembras, lo cual da un desbalance en la relación de sexos.
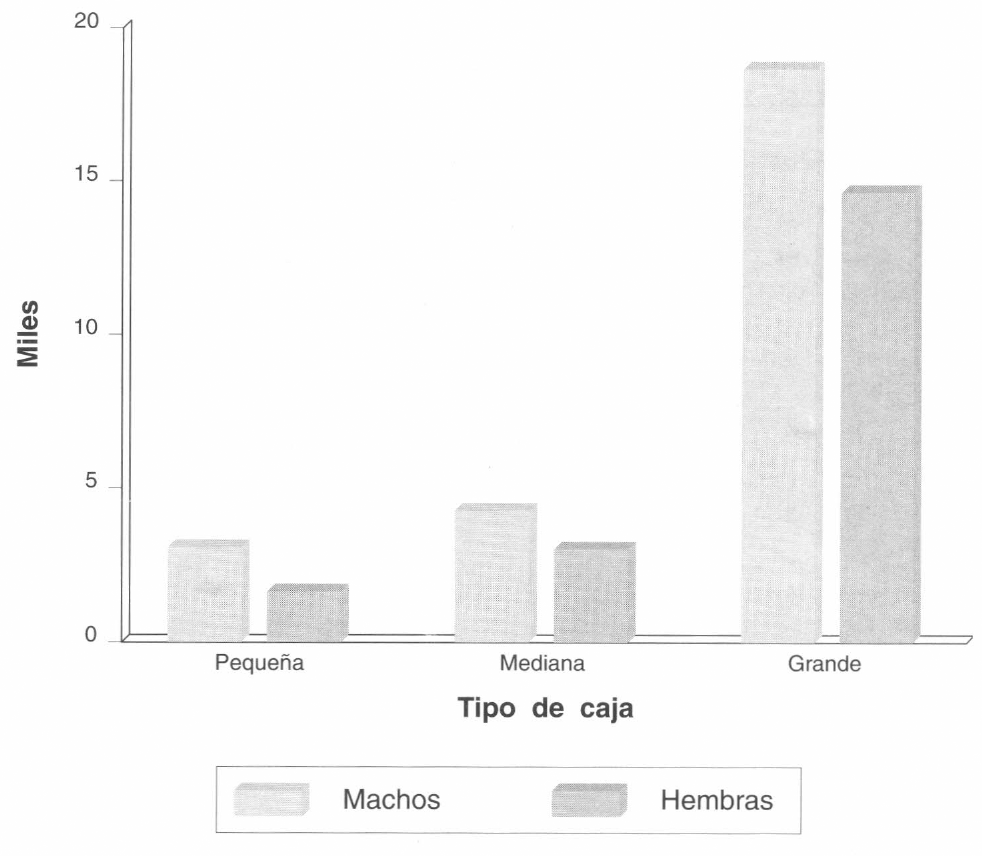
Producción de machos y hembras de B. kirkpatricki según la cámara de parasitación.
La cámara mediana aportó, en promedio, 7.195,30 ± 686,90 avispas, o sea 479,69 por día, lo cual representa 1,6 veces más que la pequeña, sin embargo, no es un valor alto, ya que se esperaba que la producción en esta cámara fuera dos veces superior a de la pequeña, debido al mayor número de larvas y al mayor volumen, lo cual favorece la interacción parasitoide-huésped, minimizando el hacinamiento que es causa de la reducción de los parasitoides y alteración de la relación de sexos. El número de machos estuvo alrededor de 4.228,30±353,40, y el de las hembras fue de 2.967,00 ± 385,70 (Fig. 4), con un relación de sexos de 1♀:1,42♂.
En el caso de la cámara grande se obtuvieron, en promedio, 33.338,00 ± 4.989,04 avispas, es decir 2.222,53 parasitoides por día, con un promedio de 18.705 ± 2.753,95 machos y 14.633,00 ± 2.235,65 hembras (Fig. 4), para una relación de sexos de 1♀:1,28♂. Esta cámara es 9 veces más grande que la pequeña y 4 veces más con respecto a la mediana, lo cual muestra que el volumen y por ende la cámara, se constituyen en variables determinantes en la producción de avispas y más aun, en una condición vital que reduce el hacinamiento y por tanto la relación de sexos.
Según los datos de producción de parasitoides por cámara, el número de avispas de B. kirkpatricki por la larva fue de 4,5 para la cámara pequeña, 5,9 para la mediana y de 5,01 para la grande. Lo cual indica que se pueden obtener alrededor de 5,1 parasitoides a partir de una larva de G. mellonella.
Para conocer qué tan diferentes eran las cámaras según el número de machos y hembras producidos, se estudiaron inicialmente los machos, bajo el efecto de los tres tratamientos o cámaras de parasitación, con una probabilidad P > 0,0001 se hallaron diferencias significativas entre los tres tratamientos.
Análisis posteriores determinaron que la variable "larvas parasitadas", con una probabilidad P > 0,0001, determinaba las diferencias significativas entre las tres cámaras, puesto que marcaba a qué nivel una cámara reportaba el mayor porcentaje de parasitismo y como consecuencia el mayor número de machos producidos.
Los valores de producción diaria para machos con datos ajustados, en términos de cuadrados medios y errores estándar, determinaron que la mínima diferencia para producción de machos por parte de las tres cámaras, lo presentaban la mediana y la grande con una P > 0,0343, lo cual reflejaba que las dos no se veían afectadas ni por el alimento, entendiéndose como la cantidad de larvas de G. mellonella expuestas para el parasitismo, ni tampoco por el volumen de las cámaras.
Por el contrario, se presentaron mayores diferencias entre la pequeña-mediana y pequeña-grande, puesto que el número de avispas macho para la mediana y grande superaba notablemente el valor de la pequeña, la cual se veía afectada por el fuerte hacinamiento al que estaban sometidas las avispas madre.
Para el caso de las hembras producidas, y bajo los tres tratamientos, con una P > 0,0001 se observaron diferencias significativas entre las tres cámaras de parasitismo. De la misma forma se encontró como en el caso de los machos, que las larvas parasitadas influían en esas diferencias significativas (P > 0,0001).
Los valores de producción diaria para hembras con datos ajustados, en términos de cuadrados medios y errores estándar, determinaron que la mínima diferencia entre los tratamientos, para la cría de hembras de B. kirkpatricki, se presentó entre las cámaras pequeña y mediana con una P > 0,0136, esto implica que bajo una u otra la producción es muy semejante. Sin embargo, cabe recalcar que para la pequeña, la producción no sólo será inferior sino por debajo del número de machos producidos, no favoreciendo la cría masiva que para efectos de producción en laboratorio y eficiencia en control biológico, debe guardar la proporcionalidad entre machos y hembras.
La cámara mediana produjo un poco más que la pequeña, pero no lo suficiente como para afirmar que a mayor número de larvas expuestas y mayor volumen de la cámara, la producción sería mejor.
Sin embargo, al comparar las cámaras se encuentra que la producción difiere totalmente entre la cámara pequeña y grande con una P > 0,7782, lo cual es reflejo del fuerte hacinamiento al que se ven sometidos 108 parasitoides en la pequeña, favoreciendo la competencia intraespecífica, la mayor producción de machos y la baja proporción de hembras, esto es producto del volumen de la cámara; por el contrario esto se corrige en la grande, al producir no sólo mayor número de avispas, sino también una relación de sexos más estable.
Los resultados de producción de machos y hembras de B. kirkpatricki han sido analizados, teniendo en cuenta la relación de sexos como variable de trascendental importancia en la cría masiva de esta especie.
Para la cámara pequeña se presentó un desequilibrio en la relación macho a hembra, lográndose un promedio de 2 machos respecto a 1 hembra. Esta situación es consecuencia del hacinamiento en las crías de parasitoides, lo cual causa superparasitismo, que en especies gregarias como B. kirkpatricki y en general para Hymenoptera, ocasionan alteraciones en la proporción de los sexos, por tanto hay mayor producción de avispas machos, y las hembras pueden seguir colocando huevos de machos en los huéspedes parasitados, lo cual tendrá una reacción marcada bajo condiciones de hacinamiento (Waage 1990).
Para el caso de la cámara mediana, la razón fue de 1,5 machos respecto a 1 hembra. Este tratamiento mejoró la relación de sexos, lo que indica que el volumen constituye una característica de importancia en la interacción parasitoide-larva, la cual se refleja en la descendencia.
Finalmente, en la cámara grande presentó una razón de sexos bastante ajustada a una relación de 1 macho a 1 hembra, lo cual indica que un ambiente propicio favorece tanto una buena producción como una razón sexual estable. En la que no existen presiones de hacinamiento, las cuales traen como consecuencia el superparasitismo y de allí la competencia intraespecífica.
Al estudiar el número de machos y hembras producidos como variables, que explican la existencia de diferencias entre las cámaras de parasitación, se encontró que las larvas parasitadas constituían otra variable que determinaba precisamente las diferencias significativas entre las tres cámaras. Las larvas parasitadas en relación al número de larvas expuestas para parasitación-día, constituyen el denominado Porcentaje de Parasitismo; para la cámara pequeña se presentó un promedio del 94%, para la mediana del 41% y para la grande del 68% de parasitismo.
Se encontró que el porcentaje de parasitismo con una P > 0.0001, marcaba diferencias entre los tres tratamientos, juega papel importante cada día de parasitación, pues es a lo largo de estos que el parasitismo incrementa o disminuye, favoreciendo o alterando la eficiencia de las cámaras.
La prueba de Tukey, con un nivel de significancia de 0,05, confirmó la existencia de esas diferencias, lo cual permite distinguir cada cámara y al mismo tiempo determinar por el grado de parasitismo, la más eficiente teniendo en cuenta la relación de sexos.
La cámara pequeña, al presentar un 94% de parasitismo, debería representar la mejor opción de cría en laboratorio, sin embargo, la desproporción en la producción de machos con respecto a las hembras (2:1), no la favorece para efectos de crías masivas.
En cuanto a la mediana, el 41% de parasitismo haría pensar en la poca eficiencia de la cámara; sin embargo, es a través de esta que se observó la estabilización de la relación de sexos, dándole paso a la grande donde el 68% de parasitismo no sólo refleja una muy buena producción sino, además, una relación de sexos ajustada a la proporción de sexos 1 macho: 1 hembra.
La producción en laboratorio de B. kirkpatricki sobre larvas de G. mellonella ha sido posible por los diferentes estudios básicos que han permitido conocer la biología y desarrollo del parasitoide sobre este huésped. Esto ha garantizado que se presenten bajo condiciones de cautiverio, cópula, fecundidad, fertilidad, en otras palabras el parasitismo, lo cual permite que la especie se reproduzca de generación en generación. Sin embargo, todos los resultados observados en el laboratorio están sujetos a modificaciones al momento de llegar al campo, ya que las condiciones ambientales controladas y más o menos estables no serían siempre las mismas, el huésped cambia de un alterno en laboratorio a otras especies en condiciones naturales, y el espacio de acción es otro. De allí que se puedan obtener porcentajes de parasitismo diferentes a los observados en los ensayos. A parte de las razones mencionadas debe incluirse el hecho que el huésped que no es el específico, está siendo criado con dieta artificial.
Cross et al. (1969) reportan que B. kirkpatricki es muy agresivo en el laboratorio sobre A. grandis, pero que los porcentajes de parasitismo en campo varían considerablemente por varias razones, entre ellas el hecho que A. grandis no sea el huésped natural.
De otra parte, los sustitutos del huésped verdadero, llamados ficticios, originan parasitoides que enfrentados con los producidos bajos los huéspedes naturales y en el campo, podrían ser de menor vigor, más pequeños y de menor fecundidad (Waage 1990).
Para elaborar un programa de producción de G. mellonella y B. kirkpatricki, se preparó un cronograma modelo, basado en los recipientes metálicos y en la cámara grande de parasitación (Figura 5).
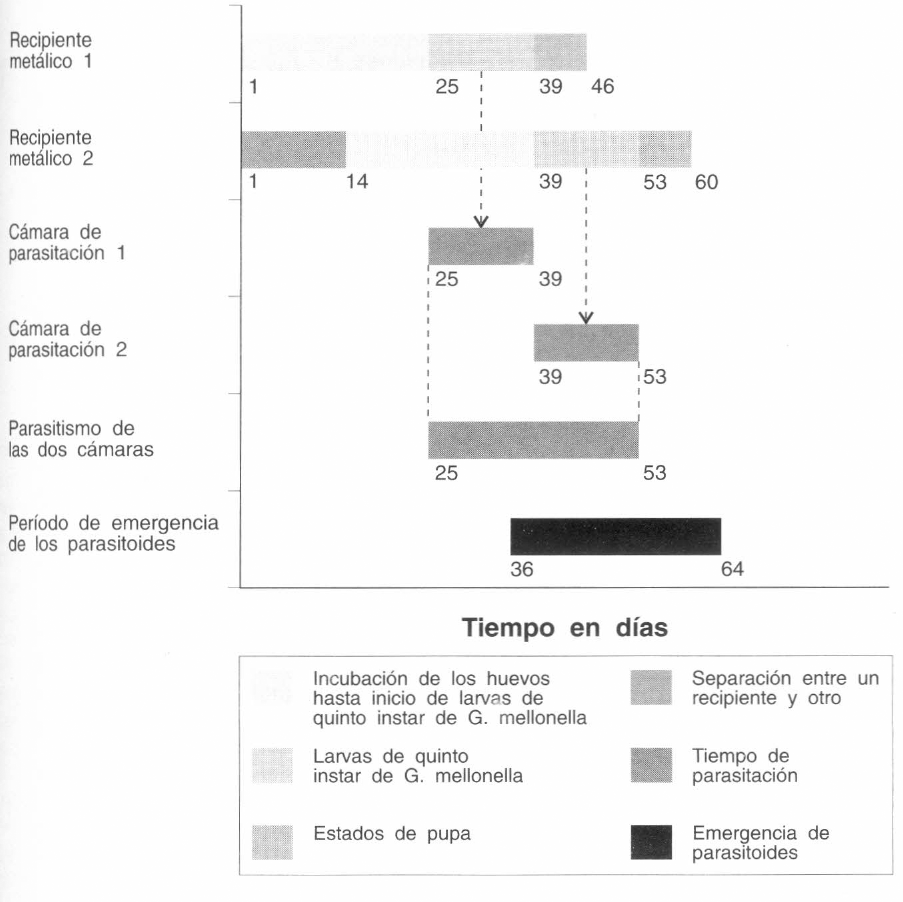
Diagrama de un modelo para la cría continua de G. mellonella y B. kirkpatricky.
Para este fin se montó inicialmente un recipiente metálico con aproximadamente 14.000 g de dieta, e infestados con cerca de 3,67 g de huevos de G. mellonella, equivalentes a 14.000 huevos.
Los huevos se obtuvieron de una pequeña colonia montada en porrones de vidrio, de la cual se tomaron 50 parejas de polillas que podían colocar el número de huevos requeridos para el recipiente.
Cada recipiente metálico debería ser montado con una diferencia de 13 días para garantizar la permanencia constante de larvas de quinto instar. A partir de los 25 días de montado se empiezan a obtener larvas aptas para ser parasitadas, este período dura alrededor de 14 días o sea 2 semanas, bajo las cuales se estaría parasitando.
Para la cámara se emplearían en total 700 larvas por día, es decir 350 larvas por cámara de parasitación con 1.750 avispas madres, en relación 1 a 1. Por tanto para los 14 días de parasitación se requieren 9.800 larvas, las cuales producirían cerca de 49.000 avispas.
Conclusiones
Para la producción masiva de G. mellonella, los recipientes metálicos representaron la mejor alternativa de cría, debido al menor espacio ocupado en comparación con los porrones de vidrio, la mejor producción de larvas por gramo de dieta y el menor tiempo de manipulación.
En cuanto a la cría masiva de B. kirkpatricki, para mantener dos cámaras de parasitación continua en un mes se necesitarían dos recipientes metálicos en producción de larvas de G. mellonella, cada uno de los cuales debería estar montado con 14 días de intervalo. Para un total de 700 larvas por día en las condiciones del trabajo se producirían diariamente 3.500 avispas con proyección a 24.500 semanales.
Un factor que puede diezmar notablemente la producción de larvas de G. mellonella es la contaminación con patógenos, entre ellos bacterias muy seguramente del género Bacillus.
Se presentaron diferencias significativas en la producción de B. kirkpatricki bajo el efecto de las tres cámaras de parasitación, siendo mejor la cámara grande (62x32 x 9 cm) con un promedio de 33.338 avispas en 15 días de parasitación.
La mejor eficiencia de producción está influenciada, entre otros factores, por la temperatura, la cual debe ser constante alrededor de los 27°C; por el tiempo de exposición de las larvas al parasitoide, el cual no debe exceder de 4 horas. Igualmente se observó que a mayor tamaño en la cámara de parasitación la tendencia a la estabilización en la relación de sexos hacia 1:1 era mayor.
Para las condiciones del experimento por cada larva parasitada se obtienen 5 avispas de B. kirkpatricki.
La cámara pequeña (12 x 18 x 9 cm), aunque aportó el mayor porcentaje de larvas parasitadas, presentó una relación de sexos desfavorable (1,95♂ : 1♀).
