Abstract
Durante la búsqueda de enemigos naturales de larvas de mosquitos de Colombia se encontraron cinco nuevas cepas del hongo patógeno Lagenidium giganteum. En 1989 se encontraron dos de ellas en ambientes naturales de la localidad de Urabá: CIB 79-MED en larvas de Aedes sp. y CIB 79-TDT, en larvas centinela, y una en el municipio de Quibdó CIB 164-PDCH, también en larvas centinela. En 1991, otras dos cepas se aislaron de la costa pacífica del Chocó (CIB 183-ARU en larvas de Orthopodomyia sp. y CIB 183-NUQ de larvas centinela). Las bacterias contaminantes provenientes de los criaderos de donde se aislaron los hongos se evaluaron con diferentes antibióticos. El crecimiento del micelio de diferentes aislamientos de Colombia, Australia y Norte América se evaluó cuando estos antibióticos se incorporaron a los medios de aislamiento. El crecimiento del micelio fue afectado fundamentalmente por los tratamientos con cloranfenicol. Todos los aislamientos crecieron más rápido en los medios con penicilina, estreptomicina y trimetoprim, y en los medios con las mezclas de penicilina-estreptomicina y penicilina-trimetoprim. El poco crecimiento de los contaminantes bacterianos con las mezclas de antibióticos mencionados anteriormente y el rápido crecimiento micelial permite recomendar estos medios para el aislamiento de este hongo patógeno en Colombia y tal vez en otras partes del mundo. La patogenicidad de estos hongos para larvas de Culex quinquefasciatus, en orden decreciente, fue: CIB 183-NUQ, CIB 79-MED, CIB 79-TDT, CIB 164-PDCH, y CIB 183-ARU.
Introducción
Lagenidium giganteum Couch (Oomycetos: Lagenidiales) es un hongo acuático, parásito facultativo de larvas de mosquito, cuyo potencial para programas de control biológico ha sido demostrado por Axtell (1983), Federici (1981) y la WHO (1984), y recientemente su estatus ha cambiado y su uso esta permitido por la Agencia de Protección Ambiental (EPA) de los Estados Unidos en programas operativos de control (Kerwin et al. 1990).
Este hongo patógeno ha sido aislado fundamentalmente en Norteamérica; sin embargo, reportes en la literatura indican que también se han realizado aislamientos en otros lugares del mundo (Couch y Romney 1973; Willoughby 1969; Goettel et al. 1983), aunque sus cultivos no fueron guardados para posterior evaluación y comparación. En 1988, Kerwin y Washino aislaron una nueva cepa de L. giganteum de California (Butte Sink), y Frances et al. (1989) aislaron otra cepa de este hongo patógeno en Australia.
En una búsqueda preliminar de antibióticos para incorporar al medio de aislamiento de L. giganteum se encontró que la mayoría de los contaminantes bacterianos obtenidos de criaderos de larvas de mosquito en la parte noroccidental de Colombia fueron susceptibles a cefotaxime, cloranfenicol, azlocilina, tobramicina, trimetoprim y cefoperazone.
En este estudio se informa sobre el aislamiento de cinco nuevas cepas de L. giganteum, así como sobre su patogenicidad en larvas de mosquitos, y el establecimiento de una nueva metodología para su aislamiento.
Materiales Y Métodos
Técnicas de aislamiento
Entre 1988 y 1990, el L. giganteum se encontró en tres criaderos de larvas de mosquito (Diptera: Culicidae) en Colombia: Dos en la zona de Urabá, de donde se aislaron las cepas CIB 79-MED infectando larvas de Aedes sp. y CIB 79-TDT en larvas centinela de Culex quinquefasciatus Say obtenidas en el laboratorio y expuestas en criaderos naturales. El tercer aislamiento se realizó en Quibdó (CIB 164-PDCH), usando la misma metodología de larvas centinela. Durante el primer semestre de 1991 se han aislado dos cepas más de este hongo patógeno en la costa Pacífica, uno de ellos (CIB183-ARU) infectando larvas de Orthopodomyia sp. colectadas de un criadero terrestre natural y el otro (CIB 183-NUQ) de larvas de laboratorio de Aedes aegypti (L.) expuestas a agua colectada de plantas de bromelia de la localidad de Nuquí (Chocó). En todos los casos, el hongo que se encontró infectando las larvas de mosquito es morfológicamente indistinguible de L. giganteum.
Las larvas infectadas fueron colocadas en recipientes plásticos desechables con 100 ml de agua declorinada, a los que se agregaron 15 larvas sanas, de 3 días de edad, de C. quinquefasciatus. Después de la muerte y antes de la formación de zoosporas, los cadáveres fueron lavados en agua estéril y sumergidos en una solución de gentamicina (4 mg/ml) por un minuto, después de lo cual fueron transferidos individualmente a cajas de petri con PYG (contenido por litro 1,3 g de peptona, 1,3 g de extracto de levadura, 3 g de glucosa y 2% de agar) como medio basal y uno de los siguientes antibióticos: penicilina V (PYGC) 10.000 unidades, estreptomicina (PYGS) 10 mg/ml, cloranfenicol (PYGC) 6 mg/ml y trimetoprin (PYGC) 3 mg/ml, para una concentración final de 0,5% de cada uno de los antibióticos. Las mezclas de estos antibióticos fueron: penicilina-estreptomicina (PYGC), penicilina-cloranfenicol (PYGC), penicilina-trimetoprim (PYGPT) y penicilina-estreptomicina-cloranfenicol (PYGPSC), para una concentración final de 0,5% de cada uno de ellos.
Origen y mantenimiento de los cultivos de L. giganteum
Las cepas de California (CA), Luisiana (LA) y Carolina del Norte (NC) fueron enviadas por J. Kerwin, Universidad de California, Davis. La cepa ARSEF fue suministrada por A.W. Sweeney, Army Malaria Research Unit, New South Wales, Australia. Todas las cepas de L. giganteum usadas en estos experimentos fueron mantenidas en agar-extracto de semilla de girasol (SFE), según las técnicas descritas por Jaronski y Axtell (1984) y Guzmán y Axtell (1986), y reaisladas de larvas de mosquito cada dos semanas a partir de larvas infectadas de C. quinquefasciatus.
Microscopía electrónica
Larvas de C. quinquefasciatus infectas con L. giganteum CIB 164-TDT y esporangios de esta cepa, cultivados en SFE por 48 horas, fueron fijadas con buffer de fosfatos pH 7,2 y 2,5% de glutaraldehido durante 2 horas. Luego se lavaron con el buffer de fosfatos y se oxidaron con vapores de tetróxido de osmio y, posteriormente, se deshidrataron con series de etanol (30-100%), seguido de un secado. Las muestras fueron cubiertas con una capa de 15 nm de una mezcla de oro-paladio y se examinaron en un microscopio electrónico de barrido Hitachi S-510.
Efecto de antibióticos en el crecimiento del micelio
Tres días después de que el hongo fue aislado de los cadáveres de larvas de mosquito, cuatro discos de micelio de 4 mm de diámetro fueron transferidos a los medios que contenían los siguientes tratamientos de antibióticos: penicilina, estreptomicina, cloranfenicol, trimetoprim, penicilina-cloranfenicol, penicilina-estreptomicina, penicilina-trimetoprim, penicilina-estreptomicina-cloranfenicol. Para cada cepa se estableció un control en PYG. El crecimiento radial del micelio se midió después de 48 horas, y 3 días después, cuatro discos del micelio (4 mm de diámetro) fueron transferidos a PYG sin antibióticos y el crecimiento radial del micelio se midió nuevamente a las 48 horas. Los resultados se analizaron utilizando un análisis de varianza y los promedios se compararon con la prueba de Tukey.
Tiempos de espoluración
Un disco de 20 mmβ de micelio se colocó por duplicado en una caja de petri con 15 ml de agua estéril, y cada tres horas se midió la cantidad de vesículas formadas.
Patogenicidad
El grado de patogenicidad de las diferentes cepas de L. giganteum se evaluó utilizando larvas de tercer instar de C. quinquefasciatus criadas en el laboratorio sobre una dieta de extracto de levadura y alfalfa seca (3:1); 1.500 larvas/2 litros de agua. En vasos plásticos desechables con 100 ml de agua declorinada se colocaron 20 larvas y se agregaron entre 1 y 5 discos de 20 mmβ con micelio. La mortalidad de las larvas de mosquito se registró 48 horas después de iniciada la prueba.
Resultados
De los criaderos de larvas de mosquito se colectaron 17 especies de bacterias, correspondientes a 7 géneros. Todas las especies probadas fueron resistentes a penicilina, Acinetobacter anitratus y Pseudomonas cepacea sp. 2 fueron resistentes a cloranfenicol; Aeromona hydrophila, Enterobacter aerogenes, Bacillus thuringiensis y B. maoquariensis resistentes a estreptomicina, B. pumilus y B. polymixar resistentes a trimetoprim.
En los medios de aislamiento que contenían penicilina y estreptomocina, el crecimiento bacteriano se observó en varios puntos de la superficie; en el medio con una mezcla de penicilina-cloranfenicol, el crecimiento bacteriano fue reducido; y en los que contenían mezclas de penicilina-estreptomicina-cloranfenicol y penicilina-trimetoprim, el crecimiento bacteriano fue reducido o nulo.
Microscopía electrónica
En las muestras evaluadas por microscopía electrónica de barrido se observó que el micelio y los esporangios que crecieron en el medio de cultivo SFE (Fig. 1) no presentaron ninguna diferencia morfólogica con las cepas de L. giganteum de otras partes del mundo. Igualmente se observó la formación de vesículas y zoosporas en los cadáveres de las larvas de mosquito (Fig. 2).
Efecto de antibióticos en el crecimiento del micelio
Los antibióticos penicilina y estreptomicina, a las concentraciones probadas, no tuvieron efecto adverso sobre ninguno de los nueve aislamientos probados, y el crecimiento radial varió de 11,7 mm en el aislamiento CIB 164- PDCH a 0,5 mm en el aislamiento CIB 79-MED. La combinación penicilina y estreptomicina, a una concentración de 0,5% de cada uno de los antibióticos, no afectó el crecimiento de micelio en la mayoría de las cepas; sin embargo, las cepas CIB 183-ARU y CIB183-NUQ mostraron un reducido crecimiento del micelio. Cuando se ensayó la mezcla penicilina-trimetoprim, ninguna de las cepas, exepto la CIB 183-NUQ, fue afectada en su crecimiento de micelio. En todas las pruebas que contenían cloranfenicol, las cepas de L. giganteum mostraron un crecimiento significativamente reducido comparado con los otros tratamientos de antibióticos y con los controles. El crecimiento del micelio del aislamiento CIB 79-MED fue muy pequeño y por lo tanto la evaluación del efecto de los antibióticos sobre el crecimiento de su micelio resulta muy complicada. La cepa CIB 183-NUQ fue la más afectada por los antibióticos empleados (Tabla 1).
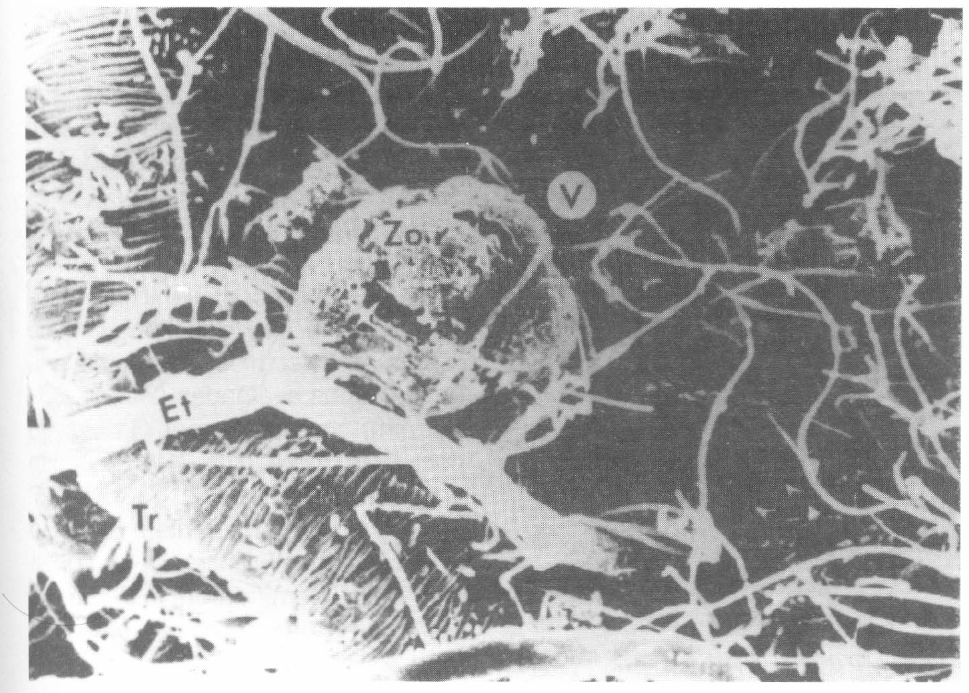
Zoosporas de Lagenidium giganteum dentro de una vesícula formadas en el exterior de una larva de Culex quinquefasciatus. Se observan los contaminantes bacterianos. Et, tubo de salida; Tr, Tráquea; V, Vesícula; Zo, zoosporas (barra 50μm)
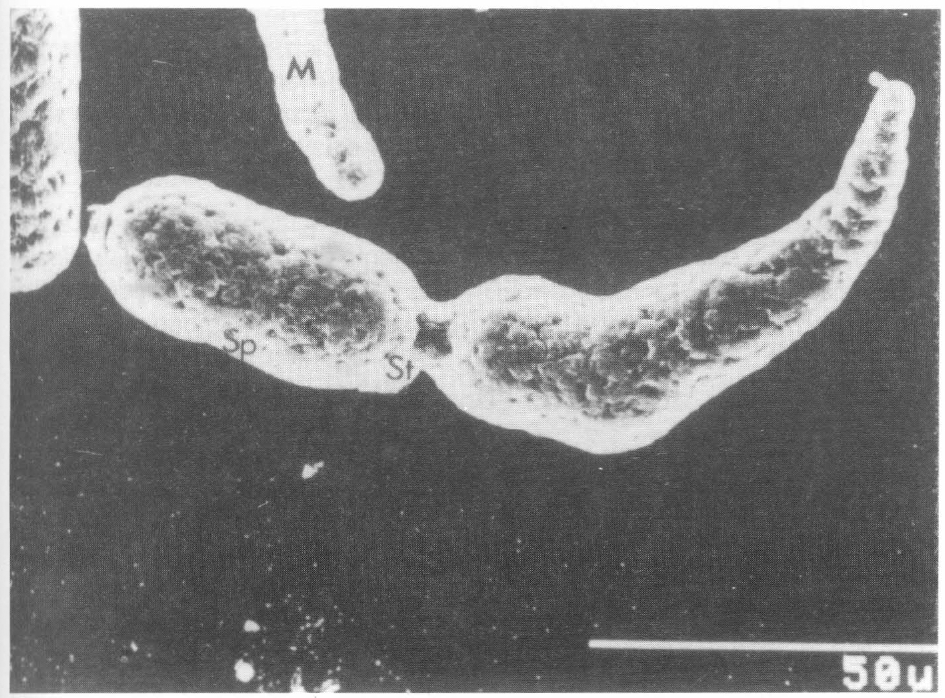
Esporangios de Lagenidium giganteum CIB 163-PDCH en medio de cultivo de extracto de semilla de girasol. Sp, esporangio, ST, septum (barra 50 µm).
Cuando los discos de agar fueron transferidos de los tratamientos de antibióticos a cajas con agar PYG, el crecimiento de los aislamientos CA, ARSEF, CIB 79-MED y CIB 183-ARU no mostró ninguna diferencia con sus respectivos controles (Tabla 2). Los aislamientos CIB 164-PDCH, CIB 79- TDT, LA y NC que venían de los tratamientos con cloranfenicol, mostraron un crecimiento más reducido que sus controles. Ninguno de los aislamientos que venían del tratamiento de penicilina mostraron diferencia con sus controles. En el tratamiento con estreptomicina, todos los aislamientos, a excepción de CIB 164-PDCH y CIB 183-NUQ, el crecimiento del micelio fue similar al de sus controles. A excepción de la cepa CIB 183-NUQ, las demás cepas provenientes de la mezcla de antibióticos penicilina-estreptomicina y penicilina-trimetoprim, no mostraron ninguna diferencia significativa con sus respectivos controles.
El tiempo de formación de vesículas con zoosporas diferenciadas varió en cada cepa (Fig. 3). La cepa ARSEF de Australia fue la que más cantidad de vesículas produjo y en el menor tiempo (3 a 6 horas), seguida en ese orden por las cepas NC y CIB 79-TDT. Las restantes cepas mostraron un pico de formación de vesículas 9 horas después de su inmersión en agua. Aunque la cepa CIB 183-ARU mostró un pico de producción de vesículas a las 3 horas, su número fue el menor de todos. Las cepas CIB 79-MED, CIB 164-PDCHH, CIB 183-NUQ Y CA mostraron un patrón similar en cuanto al tiempo de esporulación y al número de vesículas formadas.
La patogenicidad, para las larvas de mosquito, de las diferentes cepas de L. giganteum evaluadas también mostró un patrón particular para cada una. Las cepas CA, CIB 183-NUQ, CIB 79- MED y NC fueron las más patogénicas y las que casi en su totalidad, produjeron el 100% de mortalidad en los tratamientos con 1 y 2 discos de micelio. La cepa CIB 79-TDT mostró una moderada patogenicidad alcanzando sólo el 100% en la concentración más alta. Por el contrario, las cepas CIB 163-PDCH, CIB 183-ARU y ARSEF no produjeron mortalidad significativa, aún en las concentraciones más altas (Fig. 4).
Efecto de cuatro antibióticos y sus combinaciones sobre el crecimiento del micelio de cepas de Lagenidium giganteum de Australia, Norte y Sur América.
Medidas en mm. Los valores de los promedios son el resultado de dos experimentos, cada uno con cuatro replicaciones por tratamiento. Los promedios seguidos de la misma letra, en cada columna, no son significativamente diferentes. Prueba de Tukey (Alpha=0,05).
PYG: Peptona, extracto de levadura, glucosa; C: Cloranfenicol; P: Penicilina; S: Estreptomicina; T: Trimetoprim.
Crecimiento del micelio de cepas de Lagenidium giganteum de Australia, Norte y Sur América después del tratamiento con antibióticos.
Medidas en mm. Los valores de los promedios son el resultado de dos experimentos, cada uno con cuatro replicaciones por tratamiento. Los promedios seguidos de la misma letra, en cada columna, no son significativamente diferentes. Prueba de Tukey (Alpha=0,05).
PYG: Peptona, extracto de levadura, glucosa; C: Cloranfenicol; P: Penicilina; S: Estreptomicina; T: Trimetoprim
Discusión
Las observaciones de microscopía de luz y electrónica de barrido de las 5 cepas de L. giganteum reportadas en este estudio, no mostraron ninguna diferencia morfológica de importancia con las cepas de los Estados Unidos y de Australia, por lo tanto, esto indica que las cepas corresponden a la especie L. giganteum.
El reducido o nulo crecimiento bacteriano en los medios de aislamiento a los que se incorporaron las mezclas penicilina-estreptomicina y penicilina-trimetoprim, permitió el aislamiento del micelio del hongo sin ningún inconveniente. Este procedimiento de aislamiento fue facilitado debido al rápido crecimiento del micelio en la mayoría de las cepas avaluadas (Rango: 3,1- 1,7 mm) comparado por el obtenido por Brey y Remaudiere (1985) cuando emplearon la cepa CA (10 mm en 7 días), y también bastante mayor que el descrito por Frances et al. (1989) cuando suplementaron el PYG con estreptomicina y neomicina (diámetro 25 a 30 mm en 11 días). Las diferencias encontradas con el estudio de Brey y Remaudiere (1985) pudieron ser debidas al reducido espacio disponible en los tubos de ensayo que ellos usaron para aislar el hongo, contrario a las cajas de petri usadas en esta investigación, y al hecho de que este estudio fue realizado con varias cepas de L. giganteum que podrían tener diferencias fisiológicas con la cepa CA.
Las diferencias encontradas en el crecimiento del micelio entre los diferentes tratamientos de antibióticos pudieron ser debidas al modo de acción de estos agentes antimicrobianos (Neu 1985; Lietman 1985; Standiford 1985; Zinner y Meyer 1985). El menor crecimiento del micelio durante las primeras 36 horas, en el tratamiento que contenía penicilina, comparado con el del tratamiento después de transferir el micelio al medio sin antibióticos, pudo ser debido al efecto de la penicilina como fue demostrado por Gottstein et al. (1971), quienes encontraron que ciertos compuestos del tipo Beta-lactam poseen actividad antifúngica. Esta actividad ha sido también observada en antibióticos que bloquean la síntesis de las proteínas (Roberts 1980; Schwartz et al. 1972) y por la inhibición de la síntesis de ácido fólico (López y Armond 1968).
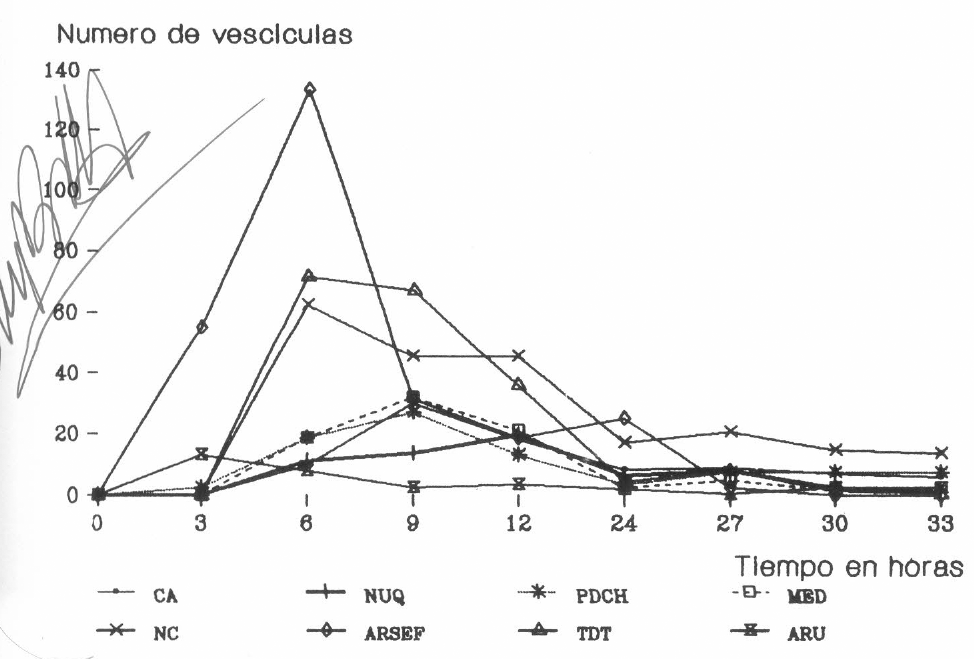
Tiempos de esporulación de ocho cepas de Lagenidium giganteum de varias partes del mundo.
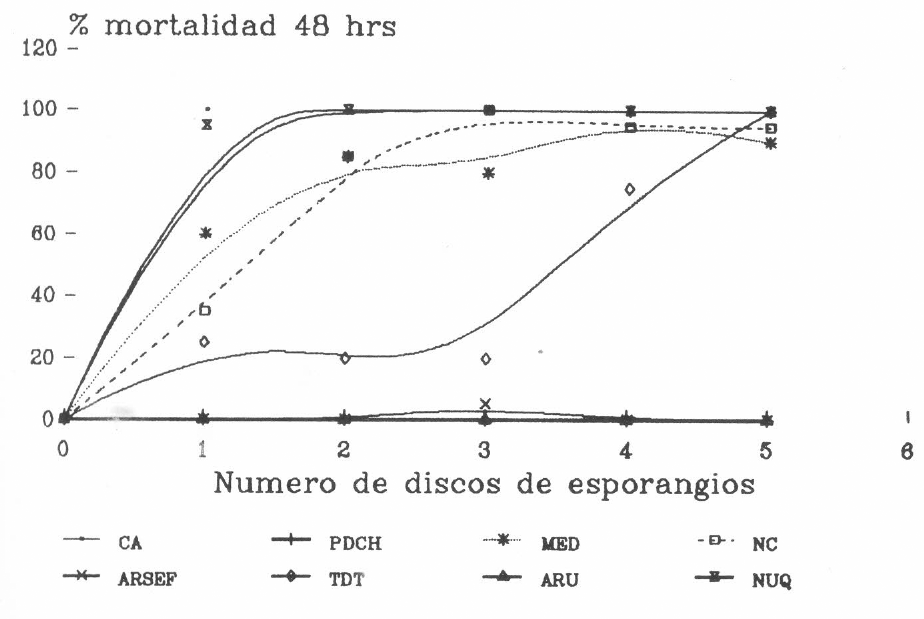
Mortalidad de larvas de Culex quinquefasciatus después de 48 horas de exposición a discos con esporangios de ocho cepas de Lagenidium giganteum de varias partes del mundo.
La ausencia de contaminantes y la alta tasa de crecimiento observada en todos los aislamientos de L. giganteum en los tratamientos con los antibióticos penicilina-trimetoprim y penicilina-estreptomicina permiten recomendar-los como buenos medios de aislamiento para ser empleados durante los trabajos de búsqueda de nuevas cepas de este hongo patógeno en la zona tropical colombiana y tal vez en otras partes del mundo.
Las diferencias en la capacidad para invadir y matar las larvas de mosquito delas cepas aquí estudiadas, así como el tiempo diferencial en la producción de zoosporas y la respuesta de crecimiento en medios con diferentes antibióticos permiten asegurar que las cepas colombianas son aislamientos adaptados a las condiciones tropicales del medio, y la patogenicidad demostrada por las cepas CIB 79-MED y CIB 183-NUQ permiten recomendarlas para posterior evaluación y estudio como integrantes adicionales de las estrategias de control de larvas de mosquito.
Footnotes
Agradecimientos
Este trabajo fue financiado por la Organización Mundial de la Salud (OMS) y COLCIENCIAS. Los autores desean expresar su agradecimiento a Gladys Cardona, Departamento de Biología, Universidad de Antioquia por su ayuda durante el trabajo de microscopía electrónica y a Lillyam Isaza por su colaboración en el trabajo mecanográfico.
