Abstract
In the cassava crop (
Introduccion
La yuca (
El control del ácaro verde de la yuca es un desafío importante hoy en día. De hecho, con el propósito de implementar su control biológico, el IITA (International Institute of Tropical Agriculture) organizó un proyecto colaborativo y multi-institucional. EICIAT (Centro Internacional de Agricultural Tropical) y EMBRAPA (Empresa Brasileira de Pesquisa Agropecuaria) se comprometieron en la búsqueda de ácaros depredadores de la familia Phytoseiidae, considerados como los más importantes enemigos naturales del
Cuarenta y cinco especies de ácaros fitoseiidos fueron identificadas asociadas con la yuca en el Neotrópico. En Colombia se obtuvo la mayor diversidad de especies de fitoseíidos, con 40 especies identificadas.
Desde 1984 se han enviado a Africa 10 especies de enemigos naturales del ácaro verde de la yuca. Con el propósito de mantener e incrementar una cantidad suficiente de los ácaros fitoseíidos para dichos envíos, se desarrollaron métodos de cría para su multiplicación. Para esto se mantuvieron permanentemente, en el CIAT, colonias del ácaro confinadas dentro de casas de malla, y fue allí donde se comenzó a detectar la presencia masiva de cadáveres del ácaro en el envés de las hojas de yuca. En 1985, el agente causal de dichas mortalidades fue identificado provisionalmente como una especie de
HUMBER, R.H. 1989. Boyce Thompson Institute. Cornell University, Ithaca, N.Y. U.S.A.
Demostrar la relación existente entre la presencia bajo condiciones de campo de ácaros enfermos de la especie
Identificar los hongos asociados con los ácaros enfermos y seleccionar el que ofrezca mayor grado de patogenidad, estudiar su biología y probar su efectividad bajo condiciones de laboratorio adecuadas y controladas.
Revision De Literatura
Una de las primeras observaciones de un hongo infectando ácaros de la familia Tetranychidae fue hecha por Fisher (1951) en la Florida, donde una especie de
En un trabajo realizado bajo invernadero en la U.R.S.S. se produjo infección sobre una población de
Es muy reducido el conocimiento a cerca del complejo de enemigos naturales del
Estudios y registros anteriores demuestran que los hongos acaropatógenos juegan un papel importante en la regulación natural de las poblaciones de estos artrópodos. El interés creciente se debe a que su aplicación no es puramente de naturaleza académica, sino también aplicada. El control biológico natural de hongos sobre poblaciones de ácaros puede causar mortalidades superiores a un 80% (Weiser y Numa 1966; Saba 1971; Smith y Furr 1975; Tsintsade et al. 1976; Carner 1976; Gardner et al. 1982; Smitley et al. 1986; Carrera et al. 1987).
Van der Geest et al. (1990) afirman que los hongos acaropatógenos tienen probablemente un gran potencial para aplicación en el trópico, donde la humedad relativa y la temperatura son altas, cuando las poblaciones de plaga están en su máximo nivel.
En cuanto a la identificación de los hongos patógenos de ácaros, los taxónomos que han trabajado con éllos no han dilucidado hasta el momento claves claras que permitan diferenciar las especies. Hasta la fecha hace falta mucho trabajo sistemático como guía para la determinación de hongos patógenos de ácaros y también son casi inexistentes los esquemas y ayudas visuales que ilustren su morfología, estructura y la sintomatología correspondiente a la infección que causan sobre los huéspedes (Alvarez 1990).
Materiales Y Metodos
Ubicación y Recolección de Muestras
El trabajo se realizó durante los años 1989 y 1990 en las instalaciones del CIAT (Palmira, Valle, Colombia), situado a 965 msnm, con una humedad relativa promedia de 70%, una precipitación promedio de 938 mm/ año, una temperatura máxima promedia de 29,21°C, mínima promedia de 19,1°C y media promedia de 24,2°C.
El proceso de investigación se inició con la recolección de ácaros en el campo y en las casas de malla destinadas a la cría masiva de acaros fitófagos, sitios donde se encontraron especímenes de
La muestra se dividió en tres grupos: El primer grupo se destinó para comprobar la presencia del patógeno; el segundo para realizar las pruebas de patogenicidad o reinfección efectuando los estudios de sintomatología, y el último grupo para la identificación del patógeno.
Comprobación de Infección
Para comprobar la presencia del hongo en las muestras, los ácaros del primer y tercer grupo se aclararon con una solución de lactofenol y se tiñeron con azul de algodón, en una caja plástica de las utilizadas para las pruebas de ELISA, con el fin de llevar un registro individual.
Pruebas de Patogenicidad
Los especímenes del segundo grupo se dividieron en dos, así: una parte de ellos se colocó individualmente sobre círculos de hoja de yuca de 2 cm de diámetro, en cajas petri con espuma saturada de agua para proporcionar condiciones similares a las de campo (T = 30°C en el día y 20°C en la noche y una H.R. = 60%, con un rango entre 40 y 80%). Allí se observaron los cambios que ocurrían en los ácaros momificados que se presumía habían muerto por la infección. La otra parte de los especímenes se destinó para efectuar las pruebas de reinoculación del patógeno. Una vez se determinaron los cambios que ocurrían en los ácaros momificados, se buscó dilucidar si la temperatura y la humedad relativa eran factores determinantes para que un ácaro momificado tomara una u otra apariencia, para la cual se formaron cuatro grupos de 32 ácaros. Cada grupo se mantuvo a una de cuatro temperaturas (20, 24, 28 y 32°C) y dos humedades relativas (<65% y >65%), llegando algunas veces a la saturación de humedad en el ambiente.
Para realizar los estudios de inoculación del patógeno se emplearon ácaros adultos obtenidos de colonias mantenidas en el laboratorio, las cuales se manejaron desde el estado de huevo, con el propósito de tener certeza acerca de su sanidad. Los individuos se sometieron a varias pruebas: 20 ácaros infectados muertos, previamente envueltos en tela de gaza, se lavaron por 30 segundos en hipoclorito de sodio al 0,05%, y posteriormente se maceraron en un homogenizador de cristal, mezclados con agua bidestilada estéril, y esta solución se asperjó sobre individuos sanos adultos de la misma edad colocados individualmente sobre círculos de follaje de yuca de 2 cm de diámetro, por medio de un microaspersor de Vilbis conectado a una bomba de vacío, a una presión de 20 PSI, para así conseguir una gota muy fina. Igualmente, la solución se asperjó sobre discos limpios de yuca que sirvieron de sustrato alimenticio a otros ácaros sanos. Como testigos se emplearon ácaros sanos y discos de yuca asperjados con agua bidestilada estéril. En total se trabajó con 50 individuos sanos en contagio y 20 testigos. También se empleó el macerado en seco, asperjado sobre hojas de yuca que sirvieron como sustrato alimenticio a los ácaros sanos. El inóculo inicial se cambió a las 48 horas por hojas limpias. Siempre se empleó yuca de la variedad CMC 40, escogida por ser una variedad susceptible al ataque de ácaros.
Se probó otro método de inoculación, el cual consistió en colocar durante 24 horas, en cámaras de humedad (cajas de petrí cubiertas), un ácaro sano en contacto directo con cuatro (4) ácaros momificados; después de este tiempo, las cajas se descubrieron y a las 48 horas se retiraron los ácaros momificados y se cambiaron los discos de yuca.
Para las pruebas descritas anteriormente se emplearon cajas de petri de 14,5 cm de diámetro provistas de espuma saturada con agua. Dentro de cada una se colocaron ocho (8) discos de hoja de yuca CMC 40 de 2 cm de diámetro, numerados y ubicados en círculo. Igualmente se emplearon frascos plásticos de confinamiento, de 2 cm de diámetro, los cuales se cubrieron con plástico adhesivo. Las observaciones se hicieron a partir de las 24 horas y se realizaron diariamente hasta la muerte de los ácaros. Con el propósito de determinar la sintomagología de la infección sobre los huéspedes se evaluó la mortalidad, la movilidad y los cambios en apariencia, tales como color y volúmen.
Inicialmente se trabajó bajo una temperatura de 28°C y con humedad relativa promedio del 65%, las cuales corresponden a las condiciones promedias de los sitios de recolección de las muestras en el campo, el fotoperíodo fue de 12 horas luz: 12 horas oscuridad.
En estos trabajos se redujo el intervalo de observación de 24 a 12 horas y en algunos casos a 6 horas, con el fin de determinar con la mayor aproximación la sintomatología de la enfermedad. Una vez se determinó el proceso de infección, cada síntoma externo se asoció con un estado de desarrollo del patógeno, para lo cual se hicieron montajes de individuos infectados en placas de microsopía, empleando el mismo sistema de aclarado, tinción y montaje de los individuos del primer y tercer grupos. De esta forma se determinó la biología del patógeno.
Permanencia de la Epizootia
Una vez se consigió reinfectar individuos sanos, se efectuó otro bioensayo con el propósito de comprobar si una epizootia o infección puede mantenerse o perdurar en una población de ácaros. Para ello se pusieron en contacto cinco (5) ácaros adultos sanos con dos (2) ácaros momificados y se replicó 20 veces, para un total de 100 individuos sanos y 40 momificados. Se trabajó con una temperatura promedio de 28°C y una H.R. promedia de 65%; se hizo una observación diaria para registrar los cambios en apariencia de los individuos vivos (color, volúmen, movimiento, mortalidad y momificación). El inóculo inicial (40 individuos momificados) se retiró al octavo día, también se retiraron todos los individuos que morían por causas naturales o mecánicas. Con el fin de hacer observaciones sobre una población que se incrementa normalmente, no se retiraron los huevos y se permitió que estos eclosionaran.
Velocidad de Infección y Estado más infeccioso
Conocida la sintomatología y el proceso de infección, se buscó mantener permanentemente individuos infectados, para lo cual fue necesario conocer cúal estado posterior a la momificación era más infectivo, cúal infectaba más rápido y cúal provocaba mayor número de individuos enfermos; para esto se montó un ensayo, colocando grupos de cinco (5) individuos sanos en contacto con un ácaro momificado, uno cristalizado, uno negro y uno con conidiogénesis. Este ensayo se replicó 5 veces, para un total de 25 ácaros sanos por cada estado de inóculo. Para la prueba con individuos momificados se mantuvo la humedad relativa por debajo del 20%, ya que se había comprobado que una humedad relativa alta provoca la conidiogénesis. Sólo se observó si se presentaba o no contagio en los primeros 8 días de contacto. Se consideró como éxito, obtener individuos momificados. La temperatura fue de 28°C.
Relación entre Temperatura e Infección
Después de detectar el estado infectivo, se buscó determinar cúal temperatura favorecía más el contagio. Para esto se montó un ensayo bajo cuatro regímenes de temperatura (20, 24, 28 y 32°C), colocando, sobre un disco de hoja de yuca, cinco (5) ácaros sanos en contacto con un ácaro esporulado. Por cada temperatura, el ensayo se repitió 16 veces, para un total de 320 ácaros sanos. La humedad relativa fue superior al 70%. Se hicieron observaciones cada 24 horas y se registró la presencia de síntomas y la mortalidad causada por la infección.
Prueba de Transmisión Transovárica
Se montó un ensayo para observar las generaciones descendientes de hembras infectadas, con el fin de conocer si la infección se transmite transováricamente; para esto se aislaron y observaron los huevos depositados por hembras con sintomatología de infección. Se evaluaron aproximadamente 80 huevos, sobre los cuales se observó la eclosión y se llevaron hasta el estado de adulto.
Pruebas de Patogenicidad sobre Acaros Phytoseiidae
Con el propósito de conocer si el patógeno de los ácaros fitófagos infecta también ácaros depredadores de la familia Phytoseiidae, a dos ácaros depredadores de la especie
Identificación del Patógeno
Resultados
Ubicación y recolección de muestras de ácaros
Las condiciones promedio de temperatura y humedad relativa durante los muestreos en los sitios de recolección en el campo fueron: T =30°C; H.R. = 51%; mientras que en las casas de mallas fueron T = 34°C; H.R. = 76 - 100%.
Durante las recolecciones de ácaros se encontraron individuos de
Comprobación de infección
En los ácaros momificados colectados que luego se aclararon, se detectó la presencia de cuerpos hifales y conidias adhesivas, estructuras típicas de los hongos de la familia Entomophtoraceae.
Por lo general, los ácaros momificados pasan por un proceso que consiste en la inducción de esporulación; algunos pueden tomar una coloración totalmente blanca; en los momificados se observa una pérdida de volúmen, generalmente asociada con la pérdida de las conidias sobre los individuos. Una vez estos ácaros han perdido sus conidias y disminuido su volúmen, comienzan a tomar una apariencia cristalizada un poco brillante y aquellos que en este momento no se han cristalizado son susceptibles de ser atacados por hongos saprófitos que los invaden, observándose un crecimiento miceliar sobre ellos.
Relacion entre Temperatura y Apariencia de Acaros Momificados
Una vez se conocieron los cambios que ocurren a partir de los ácaros momificados, se comprobó que la temperatura es un factor determinante de altos cambios. En los ácaros momificadas los colores oscuros se asociaron con temperaturas bajas y el color blanco con temperatura alta (32°C). Por el contrario, la conidiogénesis o esporulación es independiente de la temperatura, lo cual fue corroborado en las pruebas con las dos humedades relativas; con la H.R. inferior a 65% y en las cuatro temperaturas, probadas, los ácaros permanecieron momificados, y con la H.R. superior a 65%, en las cuatro temperaturas ocurrió la conidiogénesis. Este parámetro es muy útil en las pruebas de patogenicidad.
Los estudios sobre la sintomatología de los ácaros enfermos se realizaron mediante los métodos de inoculación del patógeno en ácaros sanos. En las pruebas que se utilizó la aspersión del macerado de ácaros momificados, no fueron satisfactorias; ningún individuo presentó momificación. En las pruebas donde se empleó el macerado en seco, únicamente un ácaro, de los 50 del ensayo, presentó momificación. El método de inoculación donde se empleó una cámara de humedad con cuatro ácaros momificados y uno sano dio buenos resultados. Al octavo día, de los 50 individuos con los que se inició el ensayo, 23 se observaron momificados, lo cuál corresponde a un 46%; 21 murieron por causas naturales o mecánicas y 6 permanecieron vivos.
Sintomatología
La muerte de ácaros por causas diferentes de la infección generalmente ocurrió por ahogamiento o mecánicamente cuando eran traspasados a un disco nuevo de hoja de yuca. Durante el proceso de infección, los ácaros van perdiendo progresivamente la movilidad, aumentan su volúmen y aclaran bastante su color. Posteriormente mueren y comienzan a oscurecerse, pierden el brillo y toman una apariencia opaca. El color pasa del amarillo al habano o café; en este punto ya están momificados y han ganado mucho volúmen, las patas delanteras generalmente quedan estiradas, las manchas ocelares rojas se tornan difusas y la momificación típica es bastante seca. El proceso entre la aparición de síntomas y la momificación dura entre 36 y 48 horas, a una temperatura promedia de 28°C. El conocimiento de los síntomas permitió reinfectar ácaros sanos y estudiar los cambios internos, al igual que determinar la biología del patógeno.
Cuando en el ácaro se observan los inicios de la sintomatología, internamente ha comenzado a ser invadido por unos pequeños cuerpos hifales que al principio son de forma redondeada (Fig. 1a), luego crecen un poco y algunos se dividen por fisión originando dos cuerpos hifales nuevos; posteriormente empiezan a alargarse y toman formas irregulares al comenzar a retorcerse. Luego, los cuerpos hifales se alargan, se agrupan, toman formas más regulares y llenan el hemocelo del ácaro; esta invasión interna es la causa real de la muerte del ácaro. Cuando el ácaro muere, comienza a momificarse (Fig. 1b) e internamente, los cuerpos hifales que ya han invadido todo el cuerpo del ácaro y se han agrupado, se elongan hasta alcanzar la superficie o cutícula del ácaro; cada cuerpo hifal tiene una forma ancha en su extremo que es la que llega a la pared del exoesqueleto, como buscando una salida (Fig. 1c).
La aparición de esporulación sobre el ácaro es el signo externo de la conidiogénesis (Fig. 1d). La emergencia de las conidias ocurre de la siguiente forma: cada cuerpo hifal se constituye en un conidióforo y pequeñas protuberancias van emergiendo; cada punta del cuerpo hifal presiona hasta romper el exoesqueleto por el medio de dos estrías (Fig. 1c). Los cuerpos hifales emergen por todas partes, menos por las patas, quelíceras y el escudo ventral. Cuando cada conidióforo maduro (Fig. 1e) alcanza el tamaño máximo, la punta se torna esférica y en el conidiófono se observa la línea por donde va a ocurrir el desprendimiento de la conidia, entonces se rompe originando una conidia primaria, que es redonda y deja la cicatriz de ruptura. La coloración externa blanca corresponde a una conodiogénesis abundante (Fig. 1d).
Cuando los ácaros toman una apariencia algodonosa y oscura, internamente se observa que han sido invadidos por otros hongos ajenos al causante de la muerte. Algunos de estos invasores fueron identificados como
Permanencia de la Epizootia
Se comprobó que bajo condiciones similares a las de campo, una epizootia se mantiene en una población. Sobre una colonia de 100 ácaros adultos sanos cogidos al azar se observaron primero dos ácaros momificados a los 10 días, la población siguió creciendo normalmente y aunque la infección jamás puso en peligro a la colonia, se observaron ácaros con síntomas, lo cual indica que estos van a servir de inóculo de infección a otros ácaros y la enfermedad puede continuar causando mortalidad en la población.
Relación entre Estado e Infección
El único estado capaz de provocar reinfección sobre individuos sanos fue el estado en el cual se presenta conidiogénesis. Ninguno de los otros estados provocó infección.
Relación entre Temperatura e Infección
Se determinó que de las temperaturas probadas las de 24 y 28°C fueron las que mayor número de individuos momificados provocaron, con un total del 81,3% de la población momificada, en ambos regímenes (Fig. 2). La temperatura de 20°C provocó la infección más rápida, con un 47,5% de la población momificada al quinto día. Al contabilizar los individuos vivos en el bioensayo, al décimo día se observó que a menor temperatura mayor número de individuos vivos, y que a mayor temperatura mayor mortalidad. Por lo tanto se cree que una temperatura adecuada para la infección permanente de los ácaros estaría entre 24 y 28C. Realmente no se puede determinar a cúal temperatura el patógeno es más eficaz, porque si bien a 32°C unicamente hay infección sobre el 21,3% de la población, esto no indica que el patógeno no sea eficaz a esta temperatura, pues ya en el día décimo ha ocurrido una mortalidad natural del 73,7%. Por lo tanto, es posible que el ciclo de vida de los ácaros se acorte hasta el punto de no dar oportunidad de infección al patógeno. Es decir, con una temperatura entre 24 y 28°C, el proceso de infección no es tan acelerado, pero se infecta un mayor porcentaje de la población; además, es posible que estos nuevos individuos momificados sean capaces de reproducir la infección en los individuos que aún se encuentran vivos.
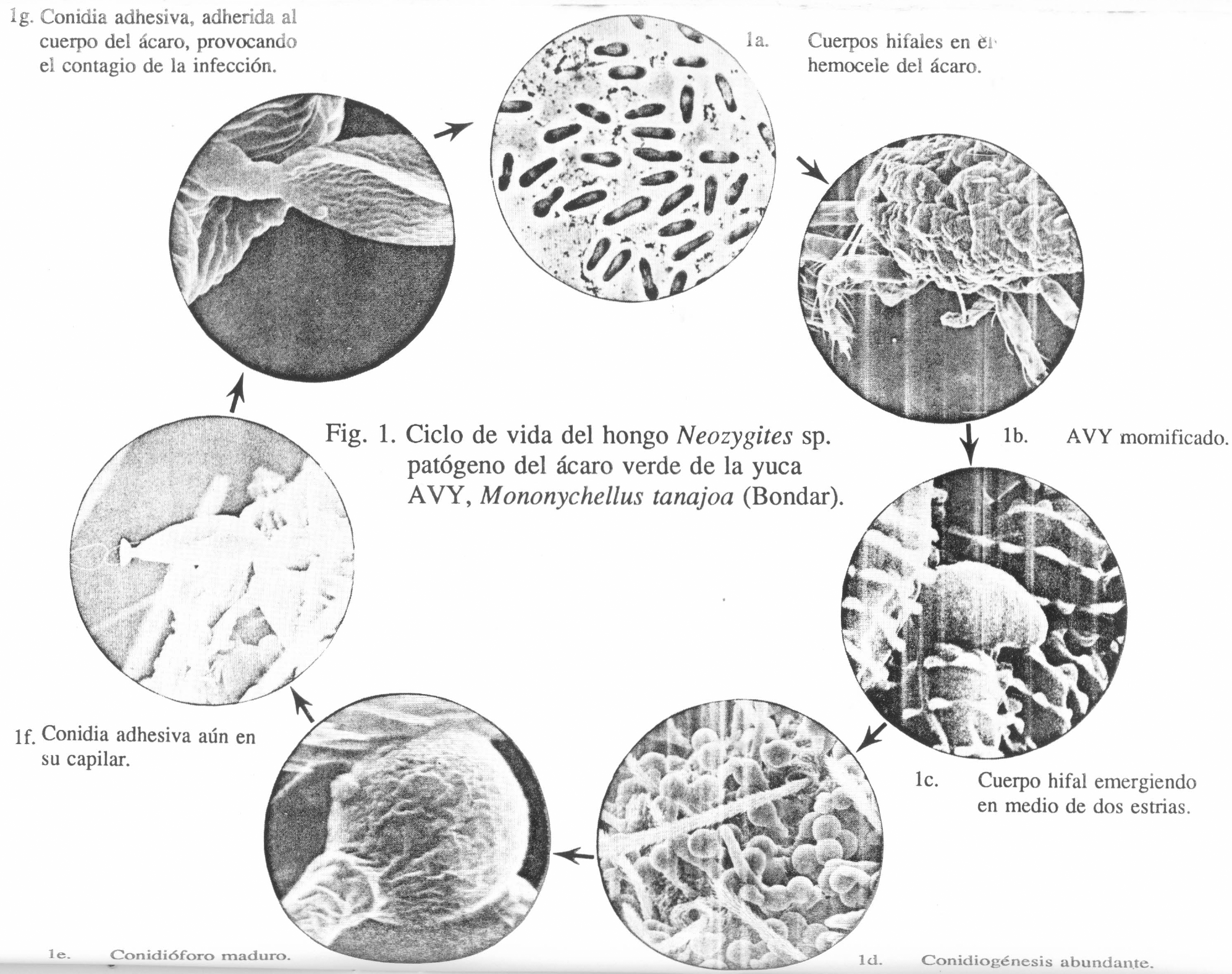
Ciclo de vida del hongo
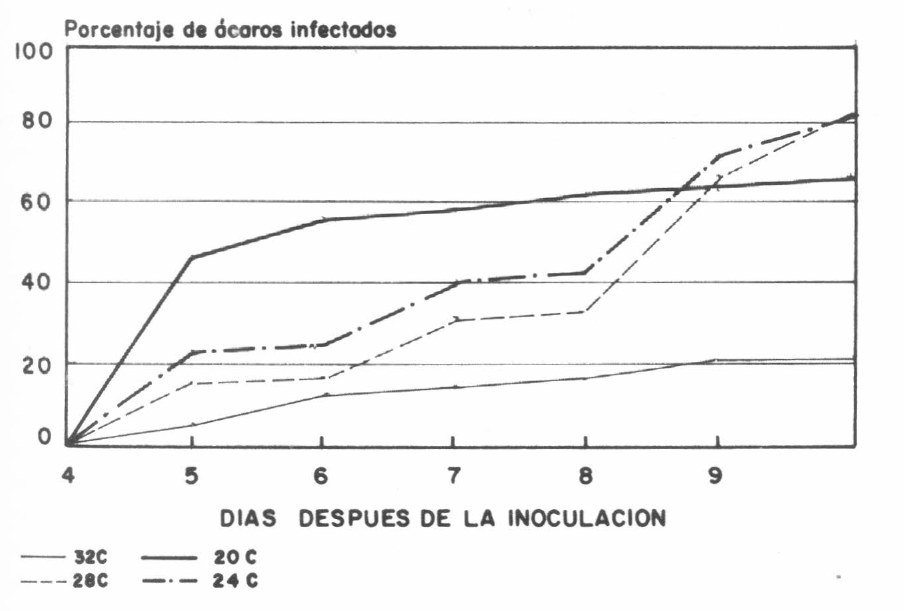
Relación entre infección y temperatura
Pruebas de Transmisión Transovárica
En las observaciones de la descendencia de hembras infectadas, ningún individuo mostró síntomas de infección. Los huevos que no eclosionaron se montaron en placas y bajo el microscopio no mostraron señas del patógeno.
Pruebas de Patogenicidad sobre Phytoseiidae
Nunca se observó infección sobre los ácaros Phytoseiidae. Sobre 12 ácaros depredadores observados nunca se determinó invasión de los cuerpos hifales. En dos hembras de T. limonicus se observaron capiloconidias sobre el dorso, pero sin presentar síntoma alguno de infección.
Identificación del Patógeno
Los individuos de
Sobre los individuos colocados en la campana de vacío se observó conidiogénesis en el primer registro a las 24 horas y en estas condiciones se obtuvo presencia de conidias primarias. Estas conidias generalmente fueron claras, sin núcleo y con cicatriz de ruptura. La emergencia de las conidicias ocurrió por todas las partes del cuerpo del ácaro, menos por el escudo ventral, las patas y las quelíceras. Las conidias fueron disparadas del conidióforo (Fig. 1e), formándo un halo en el huésped; la máxima distancia a la cual se disparó una conidia fue en promedio de 6 mm, lo cual daba un halo de aproximadamente de 13 mm de diámetro, incluido el milímetro del huésped. A las 48 horas se observó la presencia de conidias secundarias y algunas terciarias, las cuales eran oscuras. Las conidias primarias algunas veces se convierten en nuevos conidóforos, los cuales se elongan y dan origen a conidias secundarias. Igual ocurre con los secundarias que originan terciarias. Las conidias que no originan ninguna conidia continúan su desarrollo. En esta observación aparecieron las conidias adhesivas o capiloconídias.
A las 72 horas se observó una gran cantidad de conidias adhesivas o capiloconídias (Fig. 1f), originadas en su mayoría a partir de conidias primarias y algunas por las secundarias. Algunas capiloconídias dan origen capilares, sobre los cuales nacen capiloconídias secundarias y en ocasiones sobre estas últimas nacen capiloconídias terciarias. La germinación y crecimiento de estas conidias se realizó verticalmente sobre las placas de microscopía, y estas se observan soportando un bosque de conidias, donde cada fila vertical de capilares representa un árbol. Al efectuar los montajes, los capilares caen sobre la placa.
En resumen, las conidias mantenidas al 100% de humedad relativa producen muchos cambios; algunas se constituyen en nuevos conidióforos o cuerpos hifales que dan lugar a conidias secundarias y algunas veces estas originan las terciarias, las cuales sólo difieren en unas pocas micras de menos en tamaño; otras conidias en lugar de conidióforos, originan unos tubos delgados o capilares que crecen verticalmente y en la punta van formando un ángulo, sobre el cual crecen unas conidias, inicialmente redondeadas y posteriormente de forma ovalada que una vez maduran, presentan una estructura en forma de cono pequeño en el extremo distal (Fig. 1f).
El capilar que las sostiene se parte fácilmente y estas conidias una vez liberadas caen al sustrato donde se encuentren. Es frecuente observar estas conidias adheridas a las patas de los ácaros, y en ocasiones, adheridas a otras partes del cuerpo, lo cual hace presumir que el minúsculo cono tiene poder adhesivo y que posiblemente estas sean las estructuras de propagación de la infección sobre nuevos ácaros sanos (Fig. 1g), puesto que generalmente los ácaros con conidias adhesivas se encuentran vivos y con síntomas de infección o momificados. Además, algunas conidias adhesivas se observan abiertas longitudinalmente, como si ya hubieran cumplido la misión de pasar su contenido protoplasmático al ácaro (Fig. 1g). Por todo lo anterior, se pudo determinar que se trata de un hongo Entomophthoraceae, perteneciente al género
Discusion
En el campo, la recolección de ácaros tetranychidos infectados por "entomophthorosis" es fácil, y estos se reconocen por presentar una momificación típica. Para observar todas las estructuras del patógeno bajo el microscopio de contraste de fase es necesario aclarar los individuos y posteriormente teñirlos.
Bajo condiciones de laboratorio se consiguió provocar la reinfección de individuos sanos de
Como cada uno de los síntomas y signos se asoció con un estado del patógeno, fue posible, mediante el montaje de los individuos para observación al microscopio, determinar la biología y el género del hongo
Los cambios externos ocurridos sobre los ácaros momificados se deben a la conidiogénesis del patógeno. Para que sobre un individuo infectado por "entomophthorosis" ocurra la formación y desprendimiento de conidias primarias (Conidiogénesis) se requiere de una humedad relativa superior al 65%; de lo contrario, con una humedad relativa baja, el individuo permanece momificado. Esto indica la forma como se podrían preservar durante largo tiempo individuos de epizootias de campo. Individuos momificados, de 5 y 6 semanas, produjeron conidiogénesis en ambientes de humedad relativa alta y provocaron la reinfección de individuos sanos. La temperatura fue el factor determinante para que existieran diferentes coloraciones en la conidiogénesis. Mientras que la formación de conidias se favorece con una alta humedad relativa, esta impide la formación de conidias adhesivas.
Dentro de las campanas de humedad, a las 48 horas se condensó el agua en el ambiente, por tanto la humedad relativa bajó y fue por esta razón por la cual hasta ese momento comenzó a observarse la formación de conidias adhesivas.
Los ácaros con sintomatología de infección siempre presentan capiloconídias adheridas a las patas o al cuerpo; algunas de ellas abiertas y libres de su contenido protoplasmático, por lo cual se presume que las estructuras encargadas de propagar la infección son las capiloconidias o conidias adhesivas. Se comprobó que mientras un ácaro se encuentre momificado no tiene poder infectivo. Los individuos sobre los cuales se observaron síntomas de infección, murieron y posteriormente se momificaron, lo cual indica que la infección por causa del patógeno es irreversible y en cualquier caso conduce a la muerte del huésped.
Por medio del montaje de ácaros colectados de las epizootias en el campo, se constató que todos los estados del ácaro son susceptibles a la infección; los huevos fueron los únicos sobre los cuales nunca se observó signo de infección. No se observó transmisión transovarica del patógeno; los individuos obtenidos a partir de hembras infectadas se mantuvieron sanos y no presentaron signo alguno del patógeno.
Por medio de un ensayo durante el cual se proporcionaron condiciones similares a las de campo y se emplearon unos individuos momificados como inóculo incial, se observó que una epizootia puede mantenerse por sí misma. El contagio se obtiene a través de tres generaciones. A medida que se reinfectan nuevos individuos, estos pueden propagar la enfermedad a la siguiente generación, dependiendo de las condiciones ambientales. Es importante anotar que en un ensayo de laboratorio con características iguales, en Brasil, la patogenicidad se perdió después de la segunda generación.
La velocidad de infección fue mayor a la menor temperatura probada (20°C) y a 24 y 28°C hubo mayor número de individuos infectados. A 32°C el porcentaje de población infectada fue menor, pero esto no prueba que el patógeno sea menos infeccioso a determinada temperatura. A 32°C el ciclo biológico de los tetranychidos se acelera y muchas veces ocurre la muerte natural de estos antes de haberse expuesto al patógeno, mientras que a menores temperaturas el ciclo de los ácaros es más largo y da mayor oportunidad de infección.
Las condiciones ambientales pueden favorecer la invasión de los cadáveres de los tetranychidos por parte de patógenos secundarios. Los ácaros en estado de conidiogénesis son más susceptibles a la invasión de patógenos secundarios, que aquellos en estado de cristalización.
Las claves taxonómicas de los Entomophthoraceae se basan en la forma, tamaño, color y número de núcleos de las conidias primarias (King y Humber 1981); y a pesar de no tener una nomenclatura validada, es el carácter más aceptable. Luego se consideran las conidias adhesivas, la longitud de los capilares, la presencia o ausencia de rizoides, cystidias y esporas de resistencia.
Mediante el método de conidiogénesis diseñado en el laboratorio se determinó que si las conidias primarias presentan un incremento y un posterior decrecimiento en el tamaño, es muy riesgoso emitir un juicio en cuanto a la identificación taxonómica del patógeno, si no se conoce la edad de la conidia, o por lo menos se tiene un promedio del tamaño de conidias de diferentes edades. Es por esto que no se concluye en la ubicación taxonómica del patógeno de los tetranychidos, pues en una tabla de identificación de especies de
Aunque las conidias secundarias y terciarias son más oscuras que las primarias, es necesario observar el proceso para poder determinar si la medición se hace sobre una conidia primaria, secundaria o terciaria, pues estas últimas son más pequeñas que las primarias. Igualmente ocurre con los cuerpos hifales, pues cuando maduros, presentan formas irregulares y su desarrollo es igualmente proporcional al tamaño del cuerpo del ácaro, es decir que ácaros inmaduros presentan cuerpos hifales más pequeños que ácaros adultos momificados; y cuerpos hifales de machos momificados presentan menor longitud que los de hembras momificadas, por lo tanto la única medida de los cuerpos hifales que sirve como caracter taxonómico para la identificación de la especie, es la de aquellos que aún no se han dividido por fisión.
Las conidias primarias observadas al microscopio electrónico presentan una apariencia muy lisa en su estado joven en el conidióforo, posteriormente se tornan arrugadas y oscuras en el momento que van a ser liberadas (Fig. 1e). Estas conidias son disparadas alrededor del huésped y forman un halo hasta de 13 mm de diámetro. Este parámetro fue muy útil en los trabajos de inoculación de infección, pues los frascos de 2 cm de diámetro, con los cuales se trabajó, fácilmente se cubrieron de conidias, al colocar, en triángulo, tres individuos momificados y provocar la conidiogénesis; de esta manera se garantizó la presencia de inóculo de infección sobre toda el área por donde iban a caminar individuos sanos.
Las capiloconídias nacen redondas y sin disco adhesivo, en el extremo de los capilares de las conidias primarias, secundarias o terciarias; posteriormente se tornan ovaladas y desarrollan en su extremo distal el disco adhesivo. El capilar es más frágil en el extremo donde nace la conidia adhesiva, pues siempre se quiebra por este lado desprendiendo la capiloconídia.
El patógeno del ácaro verde de la yuca no presenta rizoides, cystidias, ni esporas de resistencia.
Conclusiones
El hongo
Conocida la expresión completa de síntomas de la infección causada por el hongo
La identificación de una especie de
La infección de los tetranychidos es transmitida por las capiloconídias del patógeno, estructuras que se originan a partir de las conidias primarias, secundarias o terciarias, mantenidas a una humedad relativa inferior al 65%; sin embargo, para que ocurra la conidiogénesis es necesario contar con una humedad relativa superior al 65% en el ambiente.
No se observó que el patógeno
