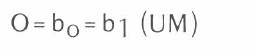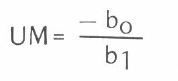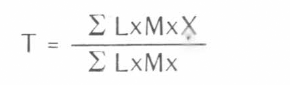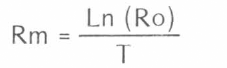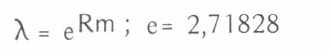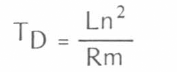Abstract
Staphylinidid beetles are predators of tetranychiid mites. On cassava,
Introduccion
La yuca
Los ácaros tetraníquidos de las especies
Estos ácaros muestran características como: ciclos de vida cortos, capacidad de incremento y de daño elevada, facilidad de dispersión y una alta capacidad para adquirir resistencia a los plaguicidas, razones por las cuales se les presta tanta atención y exigen que se analicen tácticas para su control.
En el Centro Internacional de Agricultura Tropical CIAT, una de las tácticas consideradas por el "Proyecto de Control Biológico de Acaros Fitófagos de Yuca", es la búsqueda de enemigos naturales de dichas plagas.
En el grupo de los insectos se ha reportado la presencia de los coleópteros
Con base en lo anterior, se planeó el presente trabajo con el objetivo de conocer algunos aspectos del ciclo de vida de la especie
Determinar una metodología de cría y colonización para
Establecer el efecto de la temperatura sobre el tiempo y la velocidad de desarrollo del predador.
Calcular el umbral mínimo de temperatura y la constante térmica en grados-día, requeridos para el desarrollo de dicha especie.
Establecer el efecto de dos presas, los tetraníquidos
Elaborar la tabla de vida de esta especie, a cuatro tempraturas, en función de tasa intrínseca de incremento natural (Rm) y tasa finita de incremento (λ).
Revision De Literatura
Borror et al (4) afirman que la familia Staphylinidae, cuyos representantes son conocidos como "escarabajos errantes", son delgados y alargados y pueden ser reconocidos generalmente por sus élitros muy cortos.
Los estudios efectuados sobre los estafilínidos hallados en cultivos de yuca, alimentándose de ácaros, indican la presencia de un complejo formado por dos especies del género
La relación entre temperatura y el tiempo de desarrollo arroja como resultado una curva en forma de "J" invertida; la misma relación, pero de una manera diferente, la temperatura versus tasa de desarrollo (inverso del tiempo de desarrollo), resulta en una curva sigmoidea en forma de "S" (11).
Los mismos autores consideran que para cada especie se presenta un límite inferior (umbral mínimo), uebajo del cual el desarrollo cesa. En la práctica una estimación de este umbral se obtiene por la proyección del segmento recto de la curva (tasa de desarrollo vs. temperatura) hasta interceptar el eje de la temperatura. Este método de "aproximación lineal", normalmente exagera el umbral mínimo de desarrollo, pero ésto es de poco interés en la práctica, ya que ocurre muy poco desarrollo en los puntos cercanos al umbral. Zalom et al. (12), expresan que al incrementarse la temperatura, el tiempo invertido en el desarrollo decrece, pero la acumulación de calor requerida para completar éste permanece aproximadamente igual. Esta unidad de medida de calor acumulado es conocida como "tiempo fisiológico". El tiempo fisiológico proporciona una referencia común para el desarrollo de los organismos.
Tanigoshi (10) enfatiza en la necesidad de cuantificar la capacidad de multiplicación de una especie con base en la estimación de su tasa intrínseca de incremento (Rm) a partir de las tablas de vida de Birch (3).
Según Deevy (6) las tablas de vida son la reunión de ciertos parámetros vitales de una población, comenzando con una cohorte real o imaginaria con todos sus miembros vivos, registrando para cada intervalo de edad el número de muertes, sobrevivientes y la esperanza de vida.
De acuerdo con Rabinovich (9) las tablas de vida representan la manera sinóptica y sintética de plasmar en forma cuantitativa y numérica, las principales características de la mortalidad específica por edades. Así como también, es un punto de partida para elaborar parámetros poblacionales, y de esta manera evaluar importantes características concernientes a la población en estudio.
Materiales Y Metodos
Establecimiento de Colonias de T. urticae y M. progresivus
Para establecer las colonias de las especies de Tetranychidae, se utilizó la variedad de yuca CMC-40, porque produce abundante follaje, hojas de tamaño grande y es susceptible al ataque de ácaros fitófagos.
En casas de malla, a 30 ± 10°C y 70 ± 10% de HR, se colocaron plantas de yuca de 1 a 2 meses de edad y se infestaron con hojas atacadas por las especies fitófagas; al cabo de dos semanas, las plantas presentaban poblaciones altas de los tetraníquidos. Cabe anotar que cada especie se colonizó en forma separada.
Establecimiento de Colonias de Oligota centralis
Con el propósito de establecer la cría masiva de este predador, se probaron los dos métodos que se describen a continuación:
Sistema de cría en jaula
Para este método se usó una jaula de madera de 90 cm de ancho, 110 cm de alto y 120 cm de largo, (forrada en tul), dentro de la cual se colocaron 15 plantas de yuca (Figura 1) provenientes de las casas de malla infestadas con las dos especies de tetraníquidos. En la base de la jaula se colocó tierra colectada en lotes experimentales del CIAT, la cual se mezcló con arena, en una proporción de cuatro partes de arena por una de tierra y cada dos días, se le agregó agua.
Semanalmente se colocaron plantas nuevas y sobre éstas se depositó el follaje de las plantas anteriores, que contenían estados inmaduros de
Este experimento se efectuó bajo tres condiciones ambientales:
En condiciones de la casa de malla, es decir, 30 ± 10°C y 70 ± 10% de H. R.
En condiciones de laboratorio en una cabina a 25°C y 70 ± 5% de H.R.
En un área bajo techo, a 25 ± 10°C y 60 ± 5% de H.R.

Jaula de madera forrada en tul para la cría masiva de O.Centralis.
Sistema de cría en bandeja
Simultáneamente se estableció la segunda metodología, que consistió en colocar hojas de yuca infectadas con los ácaros fitófagos, en un recipiente (bandeja) plástico transparente de 30 x 25 x 20 centímetros, con tapa hermética acondicionada con un orificio de 10 centímetros de diámetro, cubierto con tul para facilitar la aireación de las hojas (Figura 2). Acopladas a distintos niveles se dispusieron dentro de la bandeja dos parrillas, la primera, ubicada aproximadamente, a cinco centímetros de la base de la bandeja y consistía en una malla de hierro. La segunda, se colocó a cinco centímetros de distancia de la primera. Esta se construyó con un marco de aluminio atravesado por hilos de nylon.
En el fondo de la bandeja se colocó una toalla de papel para evitar el exceso de humedad.
Inicialmente se utilizaron 15 hojas de yuca infestadas con los ácaros fitófagos, cada una de ellas con el pecíolo dentro de un frasco con agua, la boca de cada vial se aseguró con parafilm, para evitar la salida del agua.
El follaje preparado en esta forma se colocó en la bandeja junto con los adultos de

Sistema de cría en bandeja para la cría de O. centralis.
Con este intercambio sucesivo de una bandeja a otra y de renovación del follaje, se estableció el presente método. Esta unidad de cría se dispuso en una cabina a 25°C y 70 ± 5% de H.R.
En los dos sistemas se colocó una población inicial de 100 adultos colectados en lotes experimentales del CIAT, con ayuda de un aspirador bucal. A los 30 y 60 días después del confinamiento de los primeros adultos en los dos sistemas, se procedió a contar los nuevos adultos.
Efecto de la temperatura sobre el tiempo de desarrollo de O. centralis
Para este experimento se adoptó la metodología utilizada en ciclos de vida de los Phytoseiidae, en el mismo Proyecto Acaros. Consistió en colocar en el interior de un frasco plástico transparente, de un centímetro de alto por tres centímetros de diámetro, discos superpuestos de papel filtro humedecido con agua y discos de hoja de yuca del mismo diámetro.
Para evitar el escape tanto de los ácaros ofrecidos como presa, así como de los predadores, los frascos se taparon con plástico adhesivo transparente, lo cual permitió realizar fácilmente las observaciones.
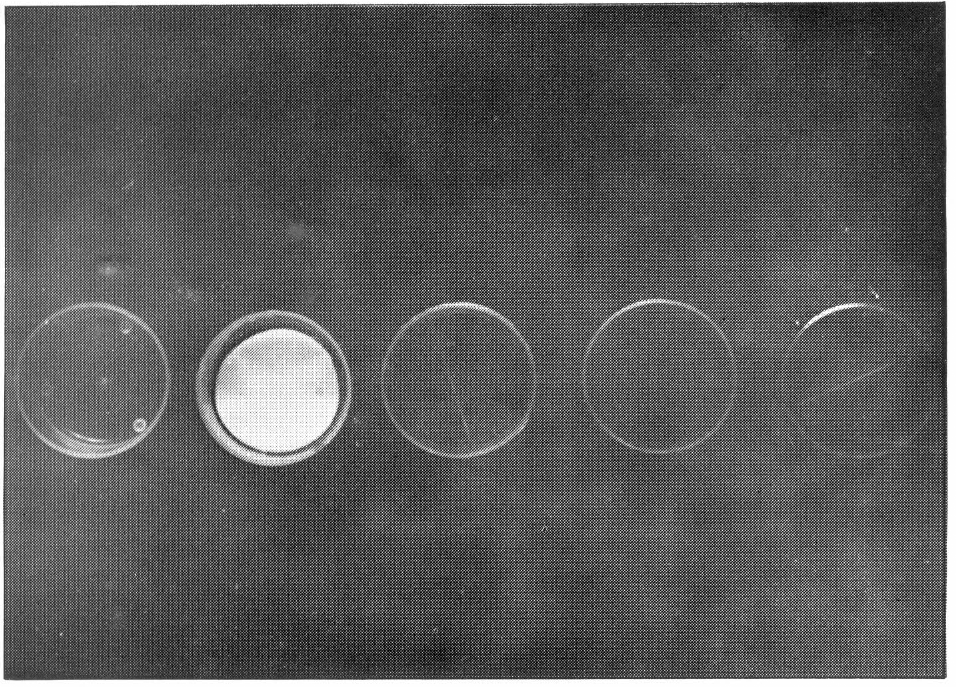
Frascos utilizados para las biologías de O. Centralis.
Los experimentos se realizaron a 15, 20, 25 y 30°C y 70 ± 5% de H.R. constantes. Para la obtención de los huevos del predador e iniciación de los experimentos, se colocaron 100 adultos de
Los ciclos de vida realizados a diferentes temperaturas tuvieron como presa a
Cálculo de la velocidad de desarrollo, umbral mínimo de temperatura y tiempo fisiológico o constante térmica
El cálculo de estos parámetros vitales se hizo de acuerdo con lo indicado por Zalon et al. (12); para cada estado biológico se calculó la velocidad de desarrollo (VD) a cada temperatura (T), multiplicando por 100 el inverso del tiempo de desarrollo (y) con la ecuación que ajusta la recta. (
es decir,
A partir del conocimiento del umbral mínimo es posible estimar el valor de la constante térmica (K) con la fórmula propuesta:
Donde:
y = Tiempo de desarrollo a la temperatura T.
T = Temperatura
UM = Umbral mínimo
Tablas de vida
Las tablas de vida fueron construidas de acuerdo con los principios establecidos por Andrewartha y Birch (1).
Los cálculos se hicieron a partir de los datos de sobrevivencia y fecundidad para cada edad específica. La información se organizó en forma de tabla de vida con las siguientes columnas:
Lx = Probabilidad de sobrevivencia específica por edad.
Mx = Tasa de natalidad o fecundidad específica por edad.
La sumatoria del producto (1xMx) sobre todos los grupos proporciona el valor de (Ro) o tasa reproductiva neta, conocida como tasa de reemplazo y refleja el número promedio de progenie hembra que es capaz de producir cada hembra de la población durante toda la vida, es decir, la capacidad de multiplicación, en el lapso de una generación.
El tiempo promedio de generación (T) es el tiempo que transcurre entre el nacimiento de los padres y el nacimiento de hijos y se calculó así:
La tasa intrínseca de incremento natural (Rm) que indica la capacidad reproductiva máxima de un organismo o sea su poder de aumentar numéricamente fue calculada con la ecuación:
Otros parámetros básicos que se estimaron fueron: la tasa finita de incremento (λ), es decir, el número de hembras adicionadas a la población, por hembra por día, con la ecuación:
El tiempo de duplicación, es decir, el tiempo necesario para que la población de cada especie estudiada se duplique, se calculó con la fórmula:
Resultados
Establecimiento de la Colonia de O. centralis
Como lo muestra la Tabla 1, se pudo establecer que el método más eficiente fue el de la bandeja, ya que 30 días después de colocar los adultos iniciales, se obtuvo una población de 136 adultos, mientras que en la jaula sólo se contabilizaron 15 adultos.
Resultados comparativos entre dos métodos de colonización para O. Centralis.
En la segunda evaluación, a los 60 días, se encontraron 12 adultos nuevos en la bandeja, mientras que en la jaula sólo se encontró un adulto.
El método de la bandeja, conocido en el proyecto como método de cría Mesa y Bellotti para la cría de Phytoseiidae, resultó ser el más exitoso en cuanto al número de individuos obtenidos; además, se pudo establecer un mejor manejo de todos los estados del insecto y así mantener condiciones climáticas más apropiadas.
Descripción de los estados de desarrollo de O. centralis
Huevo
Es de forma ovalada (Figura 4); recién colocados son lisos y de color amarillo claro; un día después aparece una fina reticulación en su superficie. Las hembras ovipositan aisladamente y a veces en grupos de tres a cuatro y hasta cinco huevos, a lo largo de la nervadura central de la hoja; inmediatamente después los cubren con exuvias y cadáveres de ácaros, para protegerlos. Los huevos tienen 0,32 mm. de diámetro polar y 0,22 mm de diámetro ecuatorial.
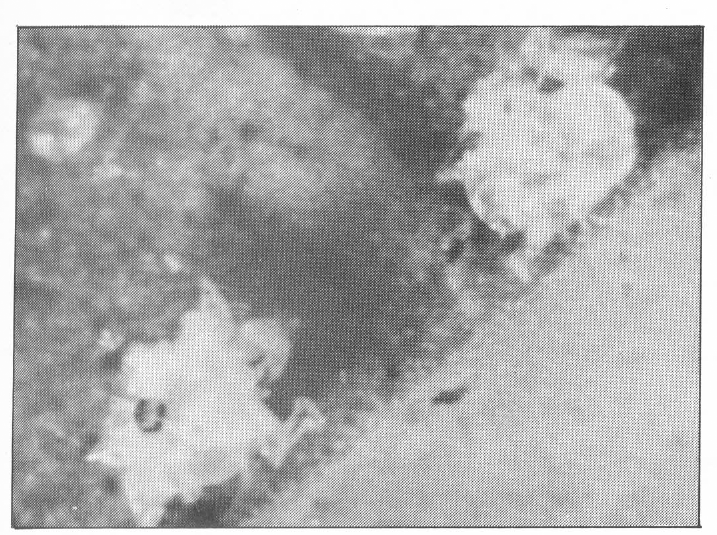
Aspecto del huevo de O, Centralis
El período de incubación varió en función de la temperatura; el huevo tardó 9,9 días a 15°C y sólo 3,5 cuando se sometió a 30°C (Tabla 2). En cuanto al porcentaje de eclosión (Tabla 3) se constató que el mayor valor se presenta a 25°C con un 86% de huevos eclosionados y el menor valor fue 79% a 15°C, lo cual está indicando un efecto marcado de tal factor ambiental en el desarrollo del huevo.
Duración (días) de los estados de desarrollo de
Duncan P = 0,05
Efecto de la temperatura sobre el porcentaje de eclosión de
Larva
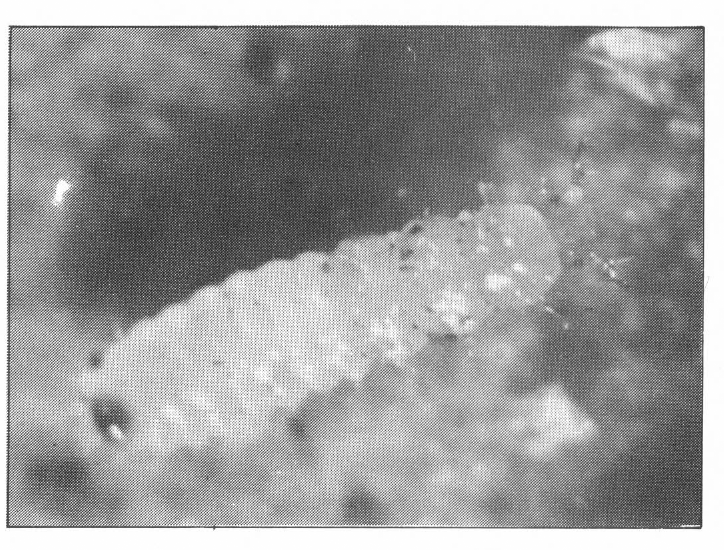
Aspecto de una larva de tercer instar de O, centralis
En el segundo instar la larva adquiere mayor tamaño, con una longitud promedia de 1,3 mm y se torna más activa. Antes de cada muda las larvas entran en un estado de quiescencia de corta duración; se puede observar que ocurre un rompimiento a lo largo de la línea media dorsal del tórax, emergiendo, en primer lugar, la cabeza y luego el resto del cuerpo. El tercer instar, de coloración amarillo intenso, es de mayor tamaño, su longitud promedia es de 1,8 mm; es el período de mayor actividad y consumo de presa.
Prepupa
La larva completamente desarrollada, inicia la búsqueda de un sitio para empupar; se observó que si no encuentra un lugar adecuado, en el término de dos días, ésta muere.
La larva empupa en el suelo a un apro-fundidad de 0,5 a 1 cm, y penetra en dicho sustrato en posición de "S", dejando el abdomen afuera; allí empieza a tejer un capullo de seda, secretada por glándulas situadas al final del abdomen, y para ello se dispone con la cabeza inclinada hacia abajo y el abdomen curvado hacia el dorso.
Todas estas observaciones coinciden con lo expresado por Badgley y Fleschner, citados por Quiñones (8).
Pupa
La pupa es de tipo exarata (Figura 6), tiene la cabeza deflejada y el abdomen curvado hacia arriba. Mide 1,12 mm de longitud, en promedio, su color es amarillo intenso al inicio de este período y se va tornando más oscuro a medida que avanza su desarrollo, hasta alcanzar el negro característico del adulto y una consistencia más quitinizada. La exuvia de la larva permanece dentro del capullo, pero no adherida a la pupa. La duración de este estado varía de 9 a 33,4 días dependiendo de la temperatura.
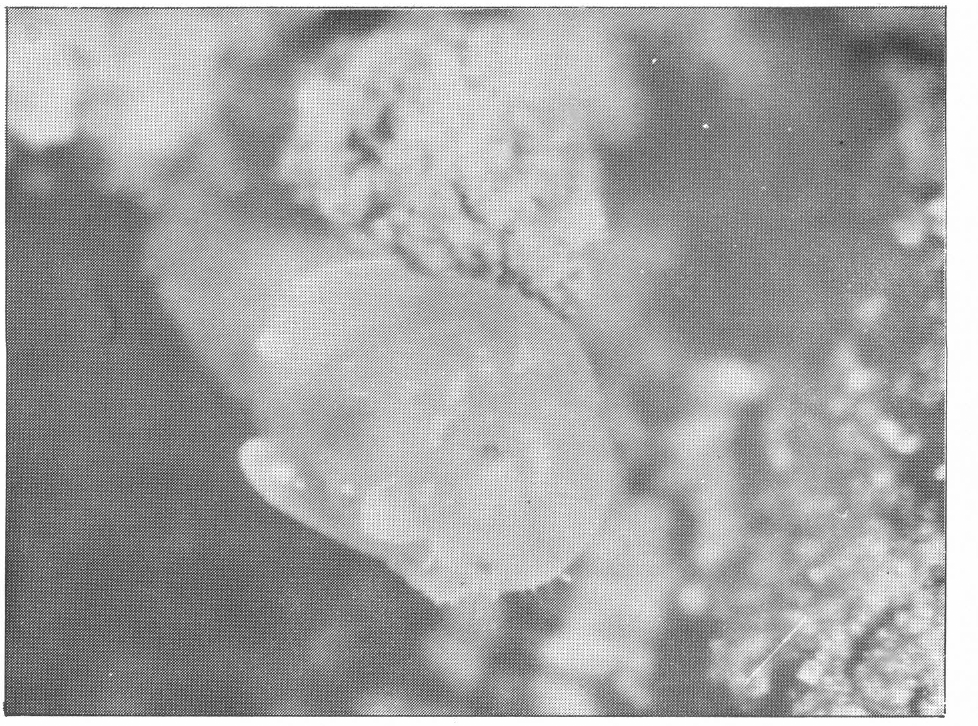
Aspecto de la pupa de O, centralis
Adulto
Es un pequeño escarabajo, típico estafilínido de color negro brillante, de élitros cortos, que no alcanzan a cubrir totalmente el abdomen, con el hábito característico de levantar los últimos segmentos abdominales hacia el dorso (Figura 7). El macho mide 1,2 mm y la hembra 1,4 mm de longitud, una vez se forma el adulto, éste inicia la búsqueda de su alimento en las colonias de ácaros más próximas a su lugar habitual sobre el follaje de la yuca.
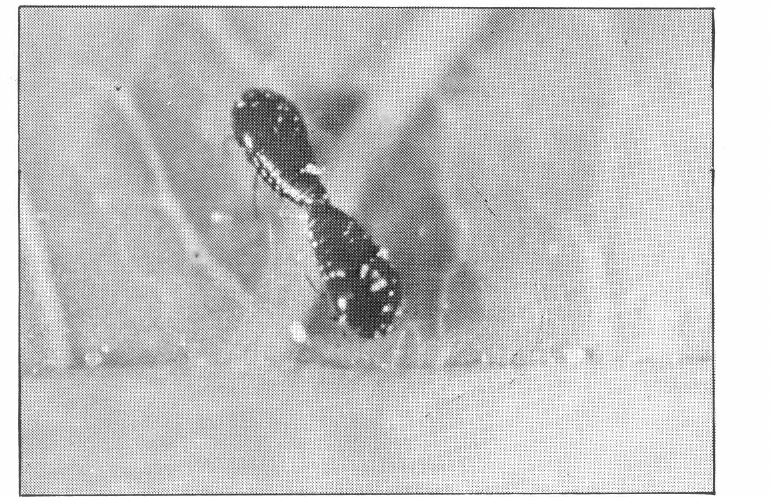
Aspecto de la posición de los adultos de O. centralis en la cópula.
En la Figura 8 se resume la duración del ciclo biológico de
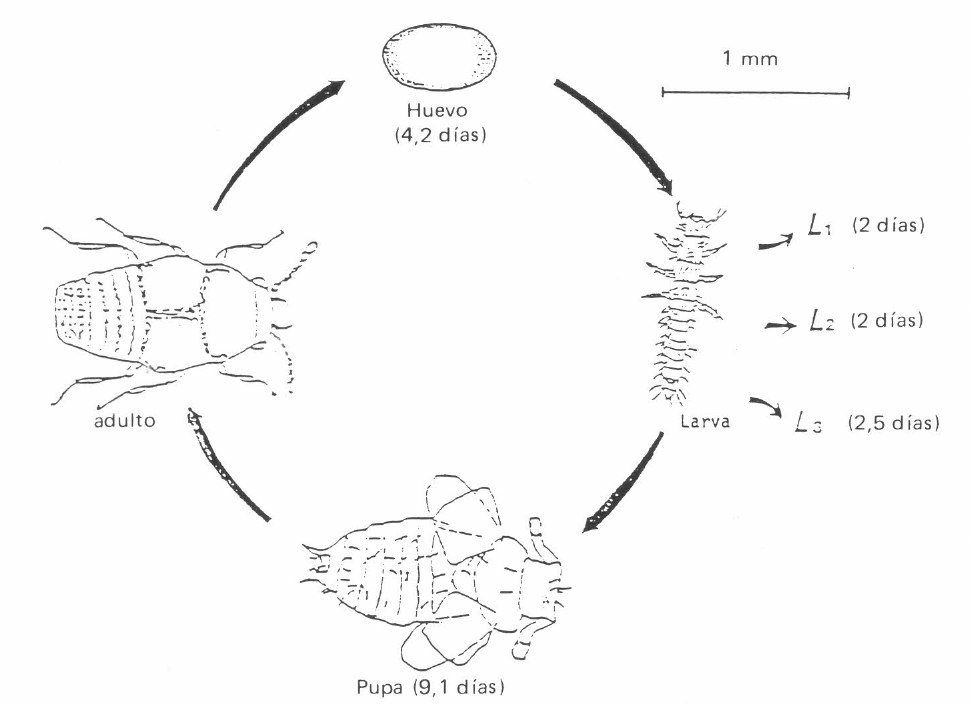
Esquematización del ciclo de vida de
Efecto de la temperatura sobre el tiempo de desarrollo
La Tabla 2 muestra la duración en días, para cada estado de desarrollo del ciclo de vida a diferentes temperaturas. Se puede apreciar que el desarrollo, desde huevo hasta adulto, se alcanzó en 59, 32, 19 y 16,5 días a 15, 20, 25 y 30°C, respectivamente. La menor duración en días ocurrió a la temperatura más elevada, es decir 30°C, lo que indica una relación inversamente proporcional entre dichas variables, pues a medida que se incrementa la temperatura, decrece el tiempo de desarrollo total; es así como el tiempo requerido a la más baja temperatura (15°C), equivale casi al triple del tiempo que se necesita a 30°C.
Quiñones (8) indica que
Vale la pena mencionar que aunque se trata de dos especies diferentes de
En general, se puede afirmar que el tiempo de desarrollo de los diferentes estados de
Como se observa, el estado de desarrollo que requiere más tiempo, con todas las temperaturas, es la pupa, con un rango de 9,0 a 33,4 días a 30° y 15°C, respectivamente.
Velocidad de desarrollo
En la Tabla 4 se presentan los resultados de velocidad de desarrollo de
Dichos datos indican que a 15°C se presentan los menores porcentajes de desarrollo para todos los estados; mientras que a 30°C, la velocidad de desarrollo adquiere sus valores máximos, es decir, 28,9%, 100%, 88,5%, 51,3% y 11,2%, para huevo, instares larvales (I, II, III) y pupa, respecitvamente.
Efecto de la temperatura sobre el desarrollo de Oligota centralis Sharp.
De acuerdo con los resultados obtenidos, se puede afirmar que la velocidad de desarrollo se afecta en forma directamente proporcional con la temperatura, ya que aumenta su valor al incrementarse este factor abiótico.
En la Figura 9 se describe gráficamente esta relación, colocando la temperatura en el eje X y la velocidad de desarrollo en el eje Y; se detallan allí los resultados encontrados respecto a estas variables para cada uno de los distintos estados de desarrollo de la especie, es decir, para huevo, instares larvales, pupa y duración total desde huevo hasta adulto.
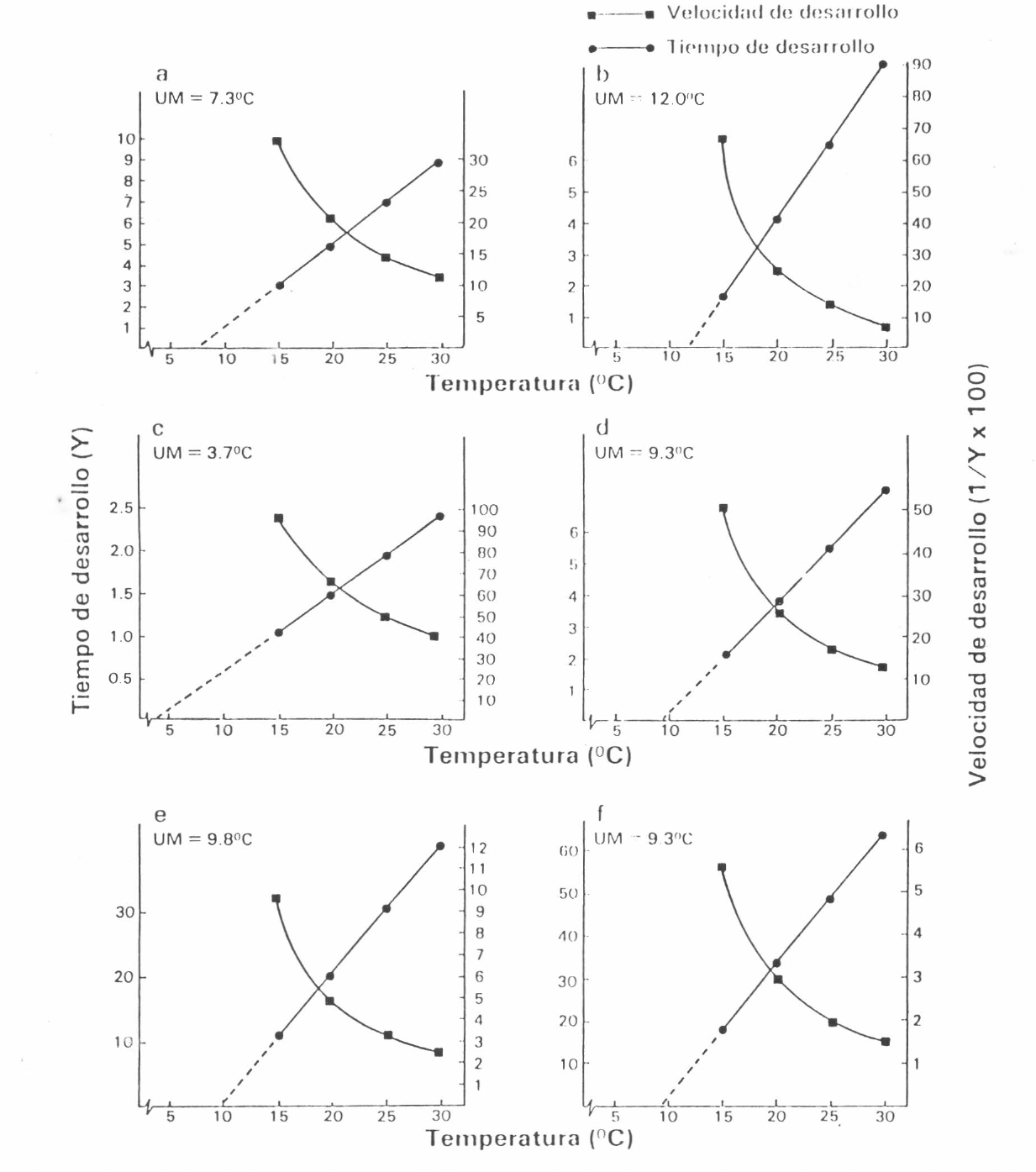
Efecto de la temperatura sobre el tiempo y velocidad de desarrollo de los estados inmaduros y el desarrollo total de
La curva describe una tendencia sigmoidea, indicando que a las más altas temperaturas se obtienen las más altas velocidades de desarrollo.
Según estos resultados, se puede concluir que los estados larvales presentan las más altas velocidades de desarrollo y las duraciones de desarrollo más cortas, todo lo cual está en función de la temperatura.
Umbral mínimo de desarrollo
Este concepto expresa en grados centígrados, el límite térmico por debajo del cual un organismo suspende su desarrollo; los resultados correspondientes se presentan en la Tabla 4 para cada estado biológico. Se señala allí que el huevo, los instares larvales primero, segundo y tercero, y la pupa, requieren de un umbral mínimo de 7,3; 12; 3,6; 9,2 y 9,8°C respectivamente para iniciar su desarrollo, o lo que es lo mismo, por debajo de dichos valores cesa todo desarrollo.
Quiñones (8) en estudios efectuados en México sobre otra especie de estafilínido, indica que
Tiempo fisiológico o contante térmica
En la Tabla 4 se presenta los valores del tiempo fisiológico (grados-día) requeridos para el desarrollo de cada estado biológico de
Tablas de vida
Los parámetros estimados de las tablas de vida de
La tasa intrínseca de incremento natural (Rm), o sea la capacidad de multiplicación de una población en el lapso de una generación, se vio afectada por la temperatura, aumentando desde 0,036 hasta 0,108 a 15 y 30°C, respectivamente.
En cuanto a la tasa finita de incremento lamda (λ), es decir, el número de hembras adicionadas a la población por día, se presentó entre 1,037 y 1,114 a 15 y 30°C.
En lo referente a la tasa reproductiva neta (ro), o sea el número promedio de progenie hembra que es capaz de producir cada hembra de la población durante toda su vida, se observó que este parámetro sufre un incremento desde 15 hasta 20°C punto en el cual muestra su valor máximo 67,9, para luego decrecer a 25 y 30°C, esto nos indicaría que la condición óptima para Ro se sitúa en los 20°C.
En cuanto al tiempo generacional (T), o sea el tiempo promedio entre dos generaciones sucesivas, desde huevo hasta huevo, se observó que la mayor duración se presentó a las temperaturas más bajas con valores que oscilaron entre 94,6 y 29,7 para 15 y 30°C respectivamente.
Con referencia a los parámetros restantes estimados en la tabla de vida (Tabla 5), conviene comentar lo siguiente: En el tiempo de desarrollo (huevo-huevo) se corroboró la tendencia general de que a menor temperatura, la especie emplea más tiempo para su desarrollo mientras que a temperaturas más altas, el tiempo para su desarrollo es menos, por ejemplo, a 15°C se necesitan 102 días, frente a 31,5 días que es lo que dura el tiempo de desarrollo con la temperatura a 30°C.
Tabla de vida del predador
El período de oviposición presenta el mayor valor a 20°C con 50,9 días. La fecundidad total muestra el mínimo valor de 36,9 a 15°C y el máximo, 115,3 huevos a 20°C. El número de huevos por hembra por día alcanza el valor superior de 4,4 a 25°C.
En la población aparecen con ventaja numérica las hembras con relación a los machos. Condición ésta que desde el punto de vista reproductivo parece ventajosa, poblacionalmente hablando.
En cuanto al tiempo de mortalidad del 50% de la población, se observa que el mayor porcentaje es a los 129 días y a 15°C de temperatura, decreciendo a 44 días a 30°C.
La Figura 10 representa la tasa de fecundidad a diferentes edades de la hembra de
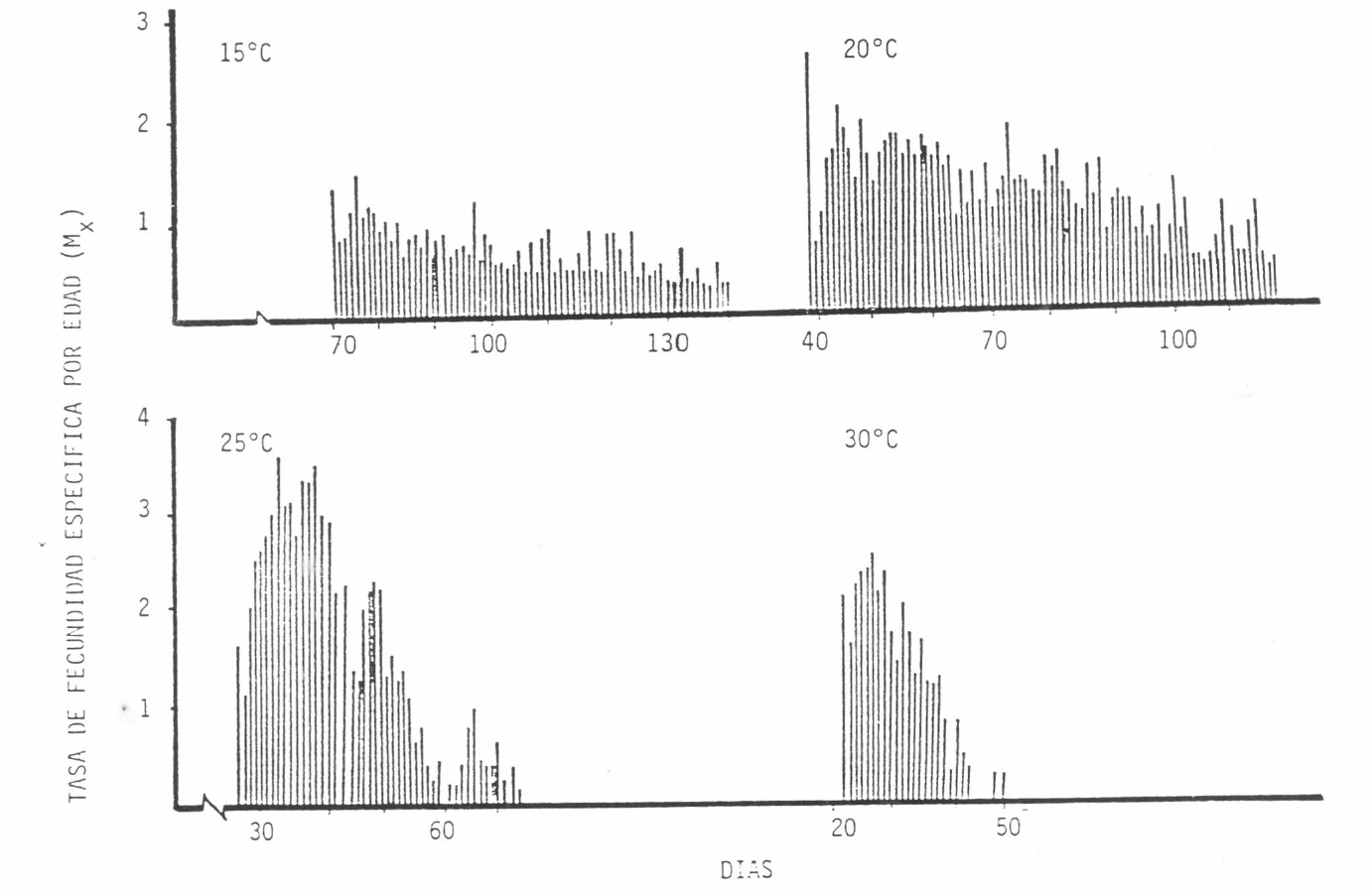
Efecto de la temperatura sobre la tasa de fecundidad específica por edad (Mx) de
La tasa de sobrevivencia de
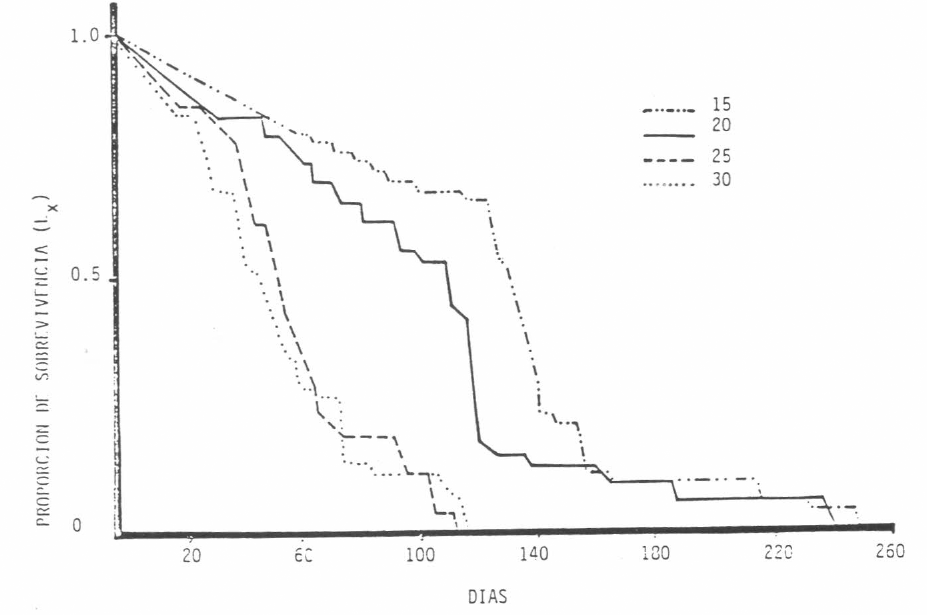
Tasa de sobrevivencia de los estados de desarrollo de
Conclusiones
La temperatura afecta la duración del ciclo de vida de
A 30°C se presenta la menor duración del ciclo de vida (16,5 días) y la más alta velocidad de desarrollo (6,1%); mientras que a 15°C se presenta la mayor duración del ciclo de vida (59,1 días) y la más baja velocidad de desarrollo (1,7%) por día.
El huevo, los instares larvales I, II, III y la pupa requieren para su desarrollo de 76,9; 19,6; 27,3; 38,6 y 166,32 grados-día, respectivamente.
El umbral mínimo de temperatura requerido para el desarrollo de huevo a adulto es de 12°C y la constante térmica equivale a 328,7 grados-día.
El desarrollo total de huevo a adulto registró un mayor promedio cuando el predador consumió
Entre los dos métodos probados para la colonización de
La tasa reproductiva neta (Ro) es mayor a 20°C con un valor de 67,9; la tasa de incremento natural (Rm) y la tasa finita de incremento (λ) presenta mayor valor cuando las temperaturas son más elevadas.
El tiempo de generación (T) y el tiempo de duplicación es menor a 25 y 30°C.