Abstract
Larva of
Introduccion
La polilla de la papa
El insecto se ha registrado atacando cultivos de papa de diferentes zonas del país, tanto bajo condiciones de campo como en almacenamiento. Actualmente, el manejo de esta plaga se basa en diferentes medidas de control. Lo más frecuente es el uso de insecticidas químicos, que aunque efectivos en parte, originan problemas de residuos tóxicos, riesgos para la salud humana y desequilibrios ecológicos en el medio ambiente. También se implementan labores culturales que van desde la correcta preparación del suelo hasta la destrucción de material atacado por la polilla. A estos programas se hace necesario incluir métodos de control biológico que armonicen con estas medidas como es el caso de enfermedades virosas.
El objetivo de esta investigación fue evaluar el virus granuloso
Para este estudio fue necesario obtener la información básica sobre la biología y cría masiva de la polilla bajo las condiciones ambientales de la Estación Experimental "Tulio Ospina". La evaluación del virus incluyó la determinación de porcentajes de mortalidad de larvas de diferentes concentraciones del virus, concentración letal media (CL50) y tiempo letal medio (TL50).
Por último, se evaluó la susceptibilidad al virus de dos poblaciones de la polilla procedentes de Antioquia y Cundinamarca.
Revision De Literatura
En los tubérculos se comporta como barrenador y puede presentarse en el campo sobre papas expuestas y bajo condiciones de almacenamiento (Saldarriaga, 29). Por la forma como la larva agrupa sus excrementos en la parte superior de la mina puede diferenciarse claramente del daño causado por otros insectos (Raman, 25; Valencia, 30). López y Perry (18), registran infestaciones altas en cultivos de menos de 90 días y anotan que relacionándolos con el ciclo vegetativo de la planta pueden distinguirse tres ataques así: el primero dirigido a hojas iniciales y puntos de crecimientos del tubérculo-semilla, si éste no ha sido bien cubierto; el segundo ocurre entre el aporque y la floración, el cual no afecta el rendimiento, y el tercer ataque, próximo a la cosecha en tubérculos destapados, los cuales llevarán la infestación al lugar de almacenamiento. Aunque no se ha establecido el nivel económico de daño para nuestras condiciones, se han calculado algunos registros de evaluación de daño en almacenamiento. Según el CIP (11), 60 larvas en 20 kg de papa dañan 100 tubérculos en 110 días a partir de la infestación.
En cuanto a su incidencia en el clima cálido, cuando no se hace un control adecuado, las pérdidas alcanzan un 50% de daño en campo y un 90% en almacenamiento (CIP, 13). En Túnez, Argelia y Turquía se evaluó el daño y se encontró que la polilla puede causar hasta el 86% de daño en tubérculos almacenados durante tres meses, a pesar de usar insecticidas como el malathion en polvo para su protección (CIP, 12).
En Colombia se han llevado a cabo varias evaluaciones de su incidencia y tamaño. Benavides (3), halló que de 16 municipios de Boyacá y tres de Cundinamarca, el 10% del área sembrada estaba infestad y los rendimientos significativamente afectados para cultivos menores de 90 días. En Toca, Boyacá dos años más tarde, se registraron ataques del 100% en tubérculos almacenados donde las pérdidas sobrepasaron los 100 millones de pesos (Vergara, 31). En la zona papera del Oriente Antioqueño se presentaron ataques de importancia económica en 7 de 13 municipios muestreados, encontrándose mayor incidencia de la plaga en Sonsón, La Unión y Carmen de Viboral. Su presencia se atribuyó a la entrada de semilla de otros departamentos donde se había presentado inicialmente (Piedrahita y Muñoz, 21).
Según evaluaciones realizadas en la misma zona en 1985, el municipio de Sonsón presentaba un daño en campo de 11% en promedio y en papa almacenada de 4,8%. En los demás municipios el daño fue bajo, pero en general la zona mostraba porcentajes de infestación más altos en toyas y en papa almacenada que en tubérculos en el momento de la siembra (Bustillo y Muñoz, 10).
La polilla de la papa es afectada por numerosos enemigos naturales y por microorganismos. Actualmente se le está dando énfasis al desarrollo del
De acuerdo con Amonkar et al. (1) el virus granuloso de P. operculella tiene las siguientes dimensiones: virión 355,3 mm x 65,3 mm y 470,3 mm x 270,5 mm para el cuerpo de inclusión.
En pruebas de campo el patógeno ha mostrado ser tan efectivo como los insecticidas químicos (Dieldrín, DDT, Methildemeton) para prevenir daños, y bajo condiciones favorables el virus ha persistido de un cultivo al siguiente. En pruebas de campo y de laboratorio Amomkar et al. (1), verificaron su acción y encontraron que el virus mantiene su efecto hasta por 60 días. Bajo condiciones de laboratorio Red y Springett (28) obtuvieron mortalidades entre 90 y 100%.
Durante pruebas realizadas en campo Reed (27) comparó la producción del virus usando larvas alimentadas con tubérculos y con follaje y halló una mayor producción del virus en follaje, cuando empleó una concentración de 6 × 106 partículas del virus por mililitro de agua.
Para propagar el virus a gran escala Matthiesen et al. (20), hicieron aplicaciones de una suspensión acuosa de larvas pulverizadas y filtradas previamente almacenadas a -20°C con una dosis equivalente a 6250 larvas enfermas. Este material se asperjó en cultivos experimentales de 500 hectáreas; cuando el 50% de larvas mostraron síntomas de la enfermedad, se efectuaron recolecciones masivas de insectos afectados para macerar, filtrar y conservarlo en una solución buffer (ph = 7,5) centrifugada y almacenada a 4°C hasta por cuatro semanas. El virus fue purificado con un gradiente de densidad de 5-60% de sucrosa; el volumen de cada gradiente fue de 25 ml y 0,5 ml de la solución del virus, centrifugado a 5.000 r.p.m. durante veinte minutos.
La extracción se hizo mediante diálisis en la noche y luego se lavó con agua destilada y se logró la peletización a 13.000 r.p.m. Después de evaluar su efecto se calculó que en 35 g de polvo seco hay 1,35 × 1015 partículas del virus. El equivalente por larva es de 3 × 105 partículas granulosas. El peso de una partícula es 2,54 × 1014 g.
Reed (27) encontró que el período de inoculación del virus varía con la dosis, la temperatura y la edad de la larva. Con dosis altas las larvas recién emergidas mueren a las 48 horas intoxicadas por el virus, pero no por el desarrollo de la enfermedad. La muerte por enfermedad ocurre al cabo de tres semanas. Factores tales como riego, pájaros acumulación de partículas de virus en el suelo y cadáveres de larvas infectadas, favorecen la dispersión del virus entre plantas y entre cultivos de papa. Los virus que se depositan en la superficie se ven afectados por efectos ambientales que los hacen poco accesibles para la polilla; esto se puede obviar utilizando altas concentraciones para que penetren por los estomas al interior de las hojas (Reed, 27).
Briese y Mende (7) hallaron variabilidad significativa en la respuesta al virus de la granulosis entre 16 poblaciones de la polilla colectadas en el campo en Australia; al compararlas con la población de laboratorio, ésta presentó una CL50 30 veces mayor que algunas de las poblaciones de campo, debido probablemente a que esta población fue sometida al virus durante mucho tiempo y se seleccionó hacia individuos más resistentes. Briese (6) sostiene, que existe un factor genético de resistencia al virus de la granulosis, que es hereditario, se manifiesta por la selección natural y es controlado por factores clásicos mendelianos. Briese y Mende (8) advierten que el uso indiscriminado del virus en el campo puede desestabilizar la frecuencia de genes resistentes-susceptibles y promover o mantener el desarrollo de resistencia al virus en la polilla.
Materiales Y Metodos
La presente investigación se realizó en la Estación Experimental "Tulio Ospina" del ICA, ubicada en el municipio de Bello, Antioquia. Se evaluaron dos poblaciones de polillas, una obtenida a partir de recolecciones de adultos y larvas en cultivos de papa en los municipios de la Unión y la Ceja. La otra población procedente de Cundinamarca fue suministrada por el Dr. Luis Valencia de la Sección de Entomología del CIP en Bogotá.
El virus fue suministrado por el Dr. R.J. Wilner de la División de Entomología del CSIRO, Camberra, Australia y se mantuvo en un refrigerador por espacio de dos años hasta la realización de esta investigación. Los tubérculos utilizados, como sustrato alimenticio para las diferentes pruebas se consiguieron sin tener en cuenta la variedad.
Biología del Insecto
Para obtener la información básica sobre la biología y comportamiento de la polilla se realizaron los siguientes ensayos: se usaron vasos plásticos de 10 cm de largo por 7,5 cm de diámetro y orificio lateral de 0,7 cm donde se colocó una mota de algodón impregnada con una solución de miel de abejas; en cada uno de ellos se confinaron una hembra y un macho de la polilla de 24 horas de emergidos. Este recipiente se cubrió con tapa hermética provista de tela negra (Fig. 1b). En un diseño completamente al azar con 10 repeticiones por cada tratamiento se evaluó el efecto de adicionar: 1) solución de miel al 5% más una rodaja de papa sobre la tapa del recipiente. 2) solución de miel al 5%. 3) un testigo al cual no se le suministró nada. Tanto la solución de miel como la rodaja de papa se cambiaron diariamente y se tomaron los registros del número de huevos depositados, número de huevos eclosionados y longevidad de los adultos.
La información sobre el número, duración de instares y ancho de la cápsula cefálica se obtuvo utilizando vasitos plásticos de 3,8 cm de largo por 4,0 cm de diámetro tapados herméticamente; en cada uno de ellos se colocó una rodaja de papa fresca con una larva de menos de 24 horas de emergida por rodaja; en total se utilizaron 50 larvas. La duración de la prepupa y pupa se obtuvo de grupos de 20 a 25 larvas del cuarto instar colocados en vasos plásticos sobre una fina capa de arena esterilizada, anotando la fecha de iniciación y emergencia de adultos.
Cría Masiva
La cría masiva de la polilla se desarrolló basándose en estudios previos (Platner y Oatman, 22; Finney et al, 15; Briese 4), utilizando tres unidades diferentes para la cría.
Cámara de Alimentación Larval y Empupamiento
Consiste en una bandeja plástica de 25 x 25 x 7,5 cm con cubierta aireada; en su interior se colocó una capa fina de arena esterilizada sobre la cual se depositaron larvas del primer instar. Una vez llegan al estado de pupa se separan a través de tamices, y si hay necesidad de sexarlas se extraen manualmente de sus capullos.
Unidad de Emergencia de Adultos y Oviposición
En el experimento se usaron vasos plásticos transparentes de 10 cm de largo por 7,5 cm de diámetro y orificio lateral de 0,7 cm de diámetro donde se colocó una mota de algodón impregnada con una solución de miel de abeja; en cada uno de ellos se depositaron pupas macho y hembra. Este recipiente se cubrió con una tapa hermética, provista de tela negra (Figura la y 1b). De esta unidad se retiraron las tapas con los huevos adheridos y se pasaron a un dispositivo para emergencia de larvas; éste consiste en un vaso plástico similar al anterior, sin orificio. Las larvas al emerger se transfieren a los tubérculos mediante un pincel fino, humedecido con agua para facilitar la manipulación de las mismas (Figura 1c).

Unidades para la cría masiva de la polilla a) emergencia de adultos; b) copula y oviposición y c) detalle de la tapa de la unidad de eclosión de larvas.
Las larvas al emerger se transfieren a los tubérculos mediante un pincel fino, humedecido con agua para facilitar la manipulación de las mismas.
Patogenicidad del Virus
Las pruebas de patogenicidad del virus se llevaron a cabo con larvas del tercer instar para facilitar su manipulación. Haciendo variaciones al método de Briese y Mende (7), se utilizaron vasitos plásticos de 3,8 cm de largo por 4,0 cm de diámetro, en cada uno de ellos se colocó una rodaja de tubérculo de papa de 1,5 cm de diámetro por 0,2 cm de espesor a las cuales se les aplicó 0,1 ml de concentración del virus; sobre los tubérculos se depositaron las larvas. Transcurridas las 48 horas de inoculación se cambió la porción de papa por otra de igual tamaño, libre de virus, la cual fue renovada constantemente para mantener alimento fresco a las larvas.
Las concentraciones evaluadas se prepararon mediante diluciones en agua esterilizada, utilizando el equivalente larval de 3,86 × 1010 partículas del virus por mg del polvo seco del virus calculado por Matthiessen et al. (20). Las concentraciones evaluadas fueron 9,8 × 109; 4,8 × 109; 1,54 × 109; 7,72 × 108; 4,89 × 104 y 4,89 × 102 cápsulas del virus por ml de agua; los datos se compararon con un testigo al que se aplicó 0,1 ml de agua destilada y con otro al cual no se aplicó nada. Estas diluciones del virus se mantuvieron a una temperatura de 3°C. Antes de ser utilizadas se realizaron observaciones cada dos días, hasta la muerte de la larva o emergencia de los adultos; se registró la fecha de aparición de síntomas, fecha de muerte y número de larvas muertas por día, en cada uno de los tratamientos. Los datos se analizaron bajo un diseño completamente al azar tomando como unidad experimental 25 larvas y usando cuatro repeticiones. Los porcentajes de mortalidad se ajustaron en relación con el testigo empleando la fórmula de Henderson y Tilton.
Para cada concentración se calculó tanto el porcentaje de mortalidad diario como el tiempo letal medio (TL50), éste último se estimó graficando los porcentajes de mortalidad acumulados diariamente contra el número de días. La tendencia de los datos sobre mortalidad y tiempo letal medio se determinó mediante un análisis de regresión lineal. La concentración letal media (CL50) se obtuvo gráficamente por el método de Probit (Hubert, 17).
Para hacer comparaciones entre las poblaciones de polillas de Cundinamarca y Antioquia se aplicaron dos concentraciones del virus, 1,54 × 109 y 7,72 × 108 cápsulas del virus/ml a larvas de la población de Cundinamarca. Se mantuvo un testigo para hacer los ajustes de mortalidad por otras causas. La forma de aplicación y los datos registrados fueron similares a los anteriormente descritos. El análisis de los datos se hizo usando un diseño experimental completamente al azar, comparando los datos de la población de Cundinamarca con los previamente obtenidos para la población de la polilla de Antioquia.
Resultados
Biología del Insecto
En cuanto a la longevidad y oviposición los adultos de
Efecto de tres tratamientos alimenticios en la oviposición, eclosión de huevos y longevidad de adultos de
Prueba de Duncan (P = 0,01)
El hecho de adicionar una rodaja de papa, además de la solución de miel no incrementó la oviposición, tampoco se encontraron diferencias entre los tratamientos con respecto al porcentaje de eclosión de huevos, y la longevidad fue mayor en machos que en las hembras, lo cual contrasta con lo registrado por Zenner (32). De lo anterior se concluye que se justifica alimentar los adultos de
El número promedio de huevos depositados por una hembra fue de 204,5 (± 69,6) con un intervalo de 76-390 huevos. Los huevos tomaron 5-6 días para eclosionar y las larvas pasaron por cuatro instares, el estado larval duró 17,7 días en promedio, la prepupa 1,28 y la pupa 10,20 días. Los datos sobre ancho de la cápsula cefálica permiten establecer el instar del insecto para programar las crías masivas (Tabla 2).
Duración promedia (
N = Número de observaciones
DE = Desviación standar
Cría Masiva de la Polilla
En general el sistema de cría masiva fue de manejo fácil, económico y eficiente, adaptable a diferentes tipos de recipientes. Sin embargo, el procedimiento de sexar pupas se justifica al iniciar la cría para manejar más eficientemente el material recolectado, pero al manipular grandes cantidades de individuos requiere mucho tiempo para su realización y se puede omitir ya que la relación de sexos encontrada (1:1,16) favoreció ligeramente a los machos, lo cual asegura un número casi igual de individuos de ambos sexos.
Patogenicidad del Virus
El virus de la granulosis demostró ser patogénico en larvas de
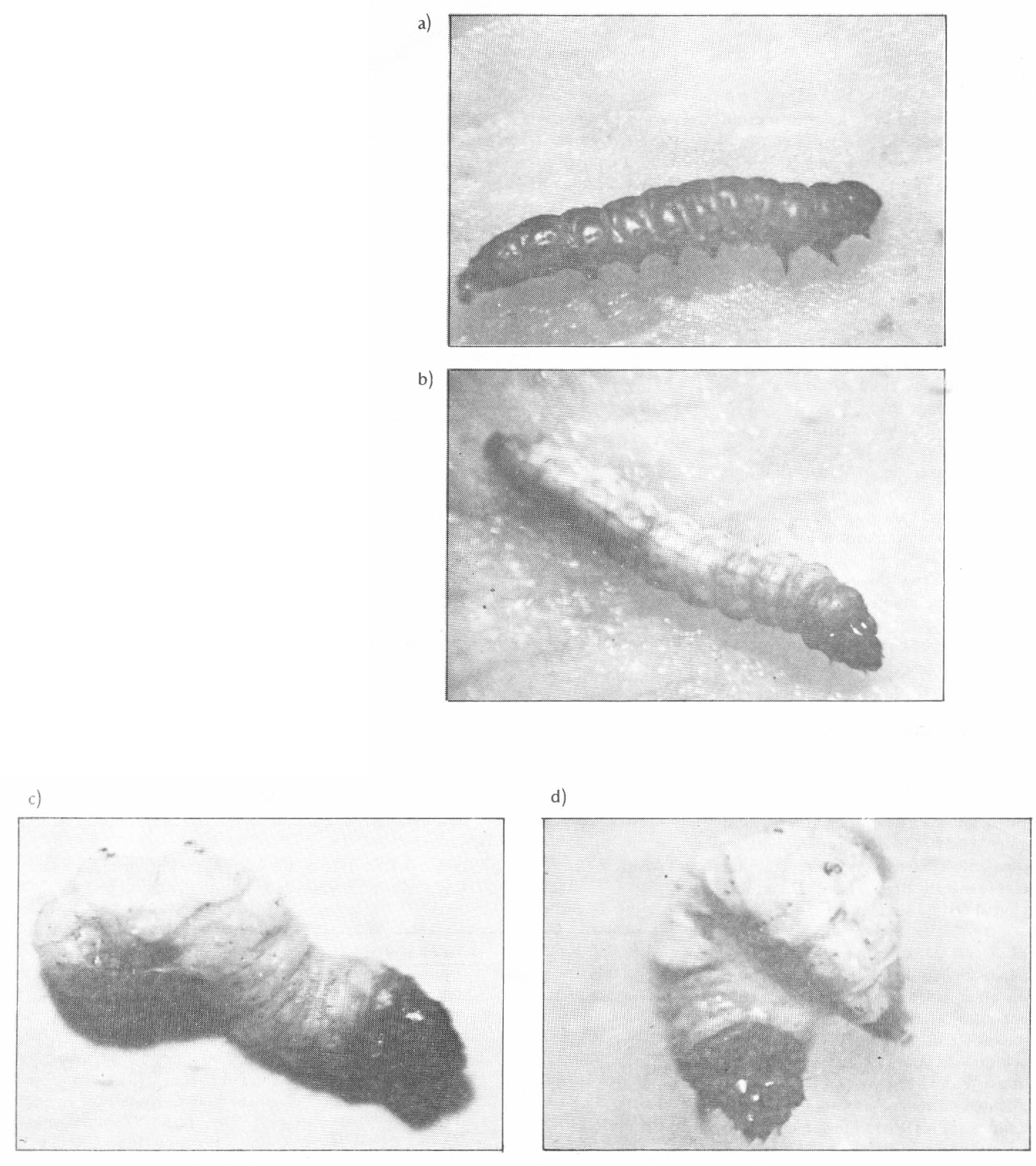
Síntomas de la enfermedad originada por el virus a) larva sana; b) larva opaca ligeramente blanca; c) síntoma de desintegración del contenido interno y d) estado flácido y lechoso.
Para las concentraciones de 6,72 × 108; 4,89 × 106; 4,89 × 104 y 4,89 × 102 cápsulas del virus/ml, la duración del estado larval se incrementó en 23,5; 37,6; 23,5 y 16,4%, respectivamente en relación con el testigo, el cual tuvo una duración de 16 a 17 días en este estado. El tamaño de las larvas enfermas fue siempre menor que el de las larvas testigo.
Con relación a los días que tomó la enfermedad para mostrar los primeros síntomas, se presentaron diferencias altamente significativas entre los tratamientos (Tabla 3). Las larvas tratadas a concentraciones altas (109 cápsulas/ml) presentaron síntomas al cabo de cinco días; y en las contaminadas a las otras concentraciones los síntomas se observaron después de 7 y 8 días. El tiempo que tardan en morir las larvas resultó altamente significativo. Las concentraciones inferiores a 10 cápsulas del virus/ml tomaron entre 9-15 días para morir (Tabla 3). Los porcentajes de mortalidad fueron significativamente diferentes entre los tratamientos.
Aparición de síntomas y mortalidad de
Prueba de Duncan (P=0,01)
De acuerdo con la fórmula de Henderson y Tilton
La mortalidad de las larvas varió entre 50 y 100% para la menor y mayor concentración. Debido a que el testigo presentó una mortalidad del 16%, los datos se ajustaron para determinar la concentración letal media (CL50) (Tabla 3). La concentración letal media se estimó de acuerdo con la prueba probit (Tabla 4), se encontró una dosis de 5,85 × 103 cápsulas del virus/ml; similar a las encontradas por Briese y Mende (7) en poblaciones de campo y de laboratorio de la polilla en Australia. En condiciones de campo y de laboratorio, se confirmó que la mortalidad es directamente proporcional a la concentración, siendo más alta a mayor dosis (Tabla 5); el TL varió de 5,2 a 16,2 días. De los tratamientos evaluados, sólo las concentraciones bajas permitieron al insecto alcanzar el estado adulto. Un 3% para las concentraciones de 4,89 × 106; 32,69 y 38% para las concentraciones de 4,89 × 104 y 4,89 × 102, respectivamente.
Cálculo de la CL50 en larvas de tercer instar de
C= % de mortalidad en el testigo
CL50= 5,6 × 103 cap. del virus/ml
Tiempo letal medio (TL50) para diferentes concentraciones del virus de la granulosis en larvas de tercer instar de
La población de
Comparación de la susceptibilidad del virus granuloso de dos poblaciones de
% ajustado por fórmula de Henderson y Tilton.
Conclusiones
En general las pruebas de patogenicidad del virus de la granulosis larval de
La mortalidad larvasl de
