Abstract
The use of resistance varieties is one of the most economical ways of insect control. Before starting the process of breeding, it is necessary to know the insect variability in natural and artificial conditions. The conditions of electrophoretic separation on total proteins and esterases were established for the most important insect of the potato crop in Colombia, Premnotrypes vorax (Hustache). Insect stages were analysed, also gel conditions, electrode buffer and extraction media, in order to establish the genetic variability of the andean weevil populations.
The abdomen of the male without the chitin cover was found to be the part of the insect most adecuate to work with. For the separation of esterases 20% sucrose should be used and 10% gel with alpha esterase and 15% with beta esterase; the buffer of the gel is 0.074M Tris - 0.009M Citric acid, ph = 8.4; the buffer of the electrodes is a stock solution of 0.036M LiOH and 0.194M Boric acid, pH = 8.25 diluited 1:3 for the cathode and 1:4 for the anode.
1. Introduccion
Una de las plagas que afecta gravemente al cultivo de la papa en el país es el gusano blanco,
Anualmente, los cultivadores gastan más de 25 millones de dólares en su control, constituyéndose así en uno de los problemas más graves para el cultivo de la papa. Se requiere investigar sobre aspectos que disminuyan o eliminen la aplicación de insecticidas, de tal manera que la producción del tubérculo económicamente sea más competitiva a nivel nacional e internacional.
Una de las formas más económicas de controlar el insecto es mediante el uso de variedades resistentes. El Instituto Colombiano Agropecuario (ICA) ha venido trabajando en la evaluación de materiales en campo y en invernadero. En un programa de mejoramiento se hace necesario evaluar gran cantidad de individuos, para tener la probabilidad de encontrar uno o algunos más resistentes y para ello se requiere de metodologías que permitan identificar con cierta seguridad y rapidez los genotipos resistentes.
En todo plan de mejoramiento para resistencia a hongos o a insectos, el paso inicial, para justificar la búsqueda de dicha resistencia, es conocer la variabilidad del patógeno o del insecto. Si la variabilidad es muy grande, sería preferible utilizar otras medidas de control diferentes a las genéticas.
La caracterización bioquímica ha sido utilizada en otros cultivos para establecer la variabilidad genética del insecto o patógeno (1,7,9,11,13,14,15) y para la identificación de genotipos resistentes (2,5,6,8,16,17). Como etapa inicial en la producción de variedades de papa resistentes a gusano blanco, se identificaron parámetros bioquímicos del insecto que puedan ser utilizados para la determinación de su variabilidad.
2. Revision De Literatura
2.1. Aspectos del Insecto
En la región andina se reconocen varias especies de Curculiónidos como plagas de papa y sus nombres comunes son "Gusano de papa", "Gorgojo de la papa" o simplemente "Gusano blanco".
De la familia Curculionidae, para el cultivo de la papa, el género más importante es
El gusano blanco de la papa,
El ciclo de vida de este insecto varía considerablemente, de acuerdo con la temperatura ambiental, la humedad del suelo y la disponibilidad de alimento. Para el caso del CNI Tibaitatá, situado a 2620 msnm y con una temperatura promedio de 14°C, Zenner de Polania (1986) observó el siguiente ciclo:
2.2 Fundamentos de la electroforesis
La electroforesis es una técnica cromatográfica ampliamente utilizada para separar mezclas de compuestos iónicos, como, por ejemplo, proteínas, con base en el tamaño y la carga de las moléculas.
Las proteínas son los productos primarios de los genes estructurales y, por ello, son de principal interés en estudios genéticos. Si ocurren cambios en la secuencia básica que codifica las proteínas, sucederán cambios en la estructura primaria de las proteínas y, al realizar la electroforesis, la sustitución de un solo aminoácido tendrá efectos marcados en la migración (12). Si se desea hacer visible (colorear por formación de complejos) el gran número de proteínas que contiene el extracto crudo de un tejido animal o vegetal, se presentará una serie compleja de bandas que hace casi imposible distinguir proteínas (alélicas) homólogas y no homólogas. Esto se obvia trabajando con proteínas funcionales, conocidas como enzimas y, más específicamente, con isoenzimas que participan sólo en reacciones específicas, lo cual permite visualizar únicamente la isoenzima de interés. La palabra isoenzima es un término operacional, usado para describir varias moléculas distinguibles que se encuentran en el mismo organismo y que catalizan la misma reacción. La variación en los patrones de bandas permite clasificar genéticamente los individuos de manera similar a cualquier otro fenotipo (12).
La existencia de estas isoenzimas tiene varias causas, que se dividen en dos categorías (10):
a) Causas primarias o genéticas, debidas a genes múltiples, cada uno de los cuales codifica un diferente tipo de subunidad enzimática.
b) Causas secundarias o postranslaciones, en que las unidades de las enzimas homogéneas son modificadas diferencialmente, para producir un rango de subunidades a partir de un gen único.
Por esta la razón, existen muchas asociaciones oligoméricas de subunidades polipeptidicas, de las cuales las comunes son las estructuras cuaternarias dimérica y tetramérica.
La existencia de más de un tipo de subunidad enzimática en la célula y de diferentes subunidades que se pueden unir en diferentes combinaciones, forman un conjunto de isoenzimas.
En cada conjunto hay una o más isoenzimas que contienen los mismos tipos de subunidades. Estos conjuntos se denominan isoenzimas híbridas, que poseen propiedades químicas y físicas intermedias y presentan velocidad de migración, también, intermedia, lo cual depende, de las subunidades que las componen.
En la molécula compleja, asumiendo que las subunidades se asocian al azar, el número total de las diferentes formas o isoenzimas que se pueda presentar, se expresa por:
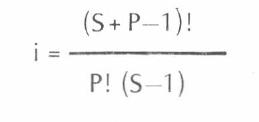
i = Número de isoenzimas.
P = Tipo de polímero
S = Número de subunidades diferentes
P=3: dímero
P=3: trímero
P=4: tetrámero
Sin embargo, la complejidad del conjunto de isoenzimas está restringida, debido a que, en la naturaleza no se encuentran todos los posibles híbridos, ni todos los locus genéticos se expresan al mismo tiempo en la misma célula (12).
2.3. Importancia de las isoenzimas como marcadores genéticos
La utilidad de las isoenzimas como marcadores genéticos en la evaluación de la variabilidad ha sido bien demostrada y esta técnica puede usarse, entre otros, en la caracterización de insectos, identificación de genotipos, discriminación de mezclas genéticas y correlación de genotipos con su origen geográfico. (1,7,9,11,15).
Desde el punto de vista técnico, es importante el hecho de que el análisis de isoenzimas por medio de electroforesis puede realizarse convenientemente, en forma simultánea, sobre un número grande de muestras, utilizando cantidades extremadamente pequeñas (10-50 ug).
Desde el punto de vista de la interpretación de los electroforegramas, se puede destacar que las isoenzimas alélicas se expresan codominantemente, o sea, que un alelo no se enmascara por la presencia de otro y, por lo tanto, en un heterocigoto, estarán presentes ambas subunidades de isoenzimas codificadas, mientras que, en el homocigoto, sólo se encuentra una subunidad. Así, el genotipo de un individuo se manifiesta a partir de su fenotipo enzimático (12).
Debido a la complejidad metabólica, las características morfológicas son el resultado de la interacción de muchos locus genéticos diferentes y, por ésto, para seguir la actividad genética a nivel de producto polipeptídico, es necesario llevar a cabo un análisis genético preciso de los locus individuales y, así, abolir el problema de interferencia de otros locus.
Por este motivo, la separación electroforética de isoenzimas se convierte en una herramienta de gran utilidad para genetistas, bioquímicos, fitomejoradores y demás investigadores interesados en conocer aspectos genotípicos que, posteriormente, serán de utilidad para resolver problemas concretos de mejoramiento.
3. Materiales Y Metodos
El trabajo se realizó en el Centro Nacional de Investigaciones Agropecuarias Tibaitatá del ICA, localizado en el Municipio de Mosquera, Cundinamarca.
Se utilizó una unidad para electroforesis Protean II, diseñada para trabajar placas de poliacrilamida (PAA) de 1.5 mm de espesor y una fuente de poder Beckman. Durante el corrimiento, la unidad permaneció dentro de una nevera para facilitar el control de la temperatura.
Para el análisis, las muestras se colocaron en los orificios de una placa plástica, semejante a la utilizada para realizar pruebas de ELISA. Se adicionó el medio de extracción y se maceró con una pequeña varilla de vidrio.
Para el análisis de esterasas, la extracción se hizo sobre baño de hielo. Durante la tinción, los geles se mantuvieron en cubetas sobre un agitador orbital.
Para determinar el mejor medio de extracción, se observó su comportamiento utilizando medios de diferente composición, pH y polaridad. En el corrimiento, fue necesario determinar el valor óptimo de potencial y el tiempo durante el cual se debe aplicar.
Para buscar el marcador apropiado, se observaron patrones obtenidos para proteínas totales, cuando se coloreaba con Coomassie Blue y cuando se empleaban iones plata. Dentro del grupo de isoenzimas, se trabajó con alfa y beta esterasas.
La estandarización de la metodología se hizo con el fin de establecer las condiciones apropiadas para obtener patrones que permitan caracterizar las poblaciones, analizando los diferentes estados del insecto: huevo, pupa y adulto. No se trabajó con larva debido a que, en este estado, el insecto se alimenta constantemente y, por lo tanto, las proteínas que se separen corresponderán no sólo al insecto sino, también, al alimento que permanece en el aparato digestivo.
3.1. Huevos
Se utilizaron huevos recién ovopositados y se probaron diversos medios de extracción (Tabla 1). Se abarcó rango de pH 6.38.8 y se varió la polaridad de los medios y se observaron los patrones obtenidos, al emplear detergentes y sustancias que desnaturalizan la proteína.
Medios de extracción para las diferentes muestras de huevos, pupas y adultos de Gusano Blanco.
Para preparar el extracto, se maceró cada huevo con 7 ul del medio, se adicionó 7 ul de indicador (azul de bromofenol) y 7 ul de sucrosa al 20%, con el objeto de aumentar la densidad del extracto y facilitar el manejo posterior de la muestra al colocarla en el orificio del gel. De esta muestra, se tomaron 10 ul y se colocaron sobre el gel. Se ensayó coloración de proteínas totales con Coomassie Blue y con iones plata.
3.2. Pupas
Se trabajó con pupas próximas a emerger como adultos y con adultos recién emergidos. Se probaron diversos me-dios de extracción (Tabla 1). Cada ejemplar fue macerado con 200 ul del medio y se centrifugó a 10.000 r.p.m. durante 10 minutos. El material sobrenadante se retiró y se le adicionó 20 ul de sucrosa al 20% y 20 ul de indicador (azul de bromofenol). De la muestra así preparada, se colocaron 20 ul sobre el gel. La coloración se hizo en Coomassie Blue.
3.3. Adultos
En adultos, se experimentó con isoenzimas y, específicamente, con esterasas, por ser uno de los sistemas más ampliamente utilizados y que ha dado excelentes resultados en el caso de otros insectos (1,9,11,15).
Al igual que en los casos anteriores, el primer paso consistió en encontrar el medio de extracción apropiado.
Los ejemplares, en este caso machos adultos con cuarenta y ocho horas de ayuno, fueron colocados en una caja petri sobre baño de hielo y se les quitó el caparazón de quitina y se tomó solamente el abdomen (Figura 1). Este abdomen se meceró con 50 ul de solución extractora (Tabla 1), 40 ul de sucrosa al 20% y 10 ul de indicador (Azul de Bromofenol). De este extracto, se aplicaron 20 ul en cada orificio del gel.
ADULTO DE PREMNOTRYPES ABDOMEN DEL MISMO, LI[BRE DEL] CAPARAZON DE QUITINA.
En la tabla 2 se encuentran consignados los diferentes sistemas analizados, tanto para el gel como para las soluciones de los electrodos.
Sistemas de buffer para el gel y electrodos, ensayados con aduitos de gusano blanco en la electroforesis de esterasas.
El corrimiento se llevó a cabo a 20 mA en forma constante por 4 horas. El revelado de alfa y beta esterasas se hizo siguiendo la metodología de Belalcázar (3).
4. Resultados Y Discusion
4.1 Huevos
El método de coloración con Coomassie Blue fue insensible a la cantidad de proteína presente en un huevo. Con iones plata (método mucho más sensible), cuando se emplearon los siguientes medios de extracción, enunciados en su orden de eficiencia: etanol al 70%, ácido acético 0,1M, mercaptoetanol al 1% en Tris-HCI de 0,5 M. Tris-HCI 5% PH 6,8, etanol, agua, urea 8M, 5D5 al 5% y Tris-HCI 0,05M pH 8,3, se obtuvieron patrones de bandas intensas y bien definidas.
De los diversos medios estudiados, cuando se empleó como buffer del gel, un sistema Tris-HC1 0.5M, ph = 6.8 el cual contenía una concentración de SDS del 0.7%, se encontraron los mejores resultados. Para el buffer del electrodo, cuando se empleó un sistema Tris 0.025M glicina 0.192M, ph = 8.3 y una concentración de SDS de 0.1%, se obutvieron buenos resultados.
Experimentalmente, se encontró que, para obtener patrones de proteínas totales bien definidos, tanto en huevos como en pupas se requiere colocar inicialmente la fuente a 22 mA y 50V por espacio de 150 minutos. Posteriormente, se eleva el potencial a 100 V, manteniendo la corriente constante a 22mA por espacio de 60 minutos y, finalmente, se lleva a 120 V y 32 mA por dos horas.
En la Figura 2 se observa la separación de proteínas totales de huevos recién ovipositados, cuando se realiza la electroforesis en las condiciones antes mencionadas. Se puede apreciar que, aunque las bandas están muy bien definidas, se tiene un espectro continuo lo cual no es deseable desde el punto de vista de interpretación y de análisis del electroforegrama.
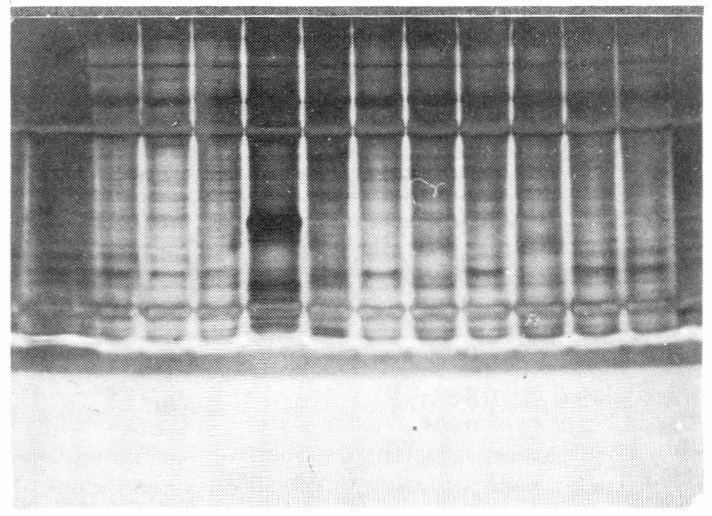
Electroforegrama de proteínas totales de huevos de Gusano Blanco de la papa, recién ovipositados. La coloración se hizo con iones plata. Cada columna corresponde a un huevo.
4.2. Pupas
De los diversos medios de extracción examinados, al emplear agua, úrea 8M, ácido acético 0.1M, Tris-HC1 0.5M con pH= 6.8, y mercaptoetanol al 1% en ácido acético 0.1M, se encontraron los mejores resultados, mencionados en forma decreciente de eficiencia. Esto se puede observar en la Figura 3 en las bandas correspondientes a las muestras Nos. 10; 2; 8; 1 y 5, respectivamente.
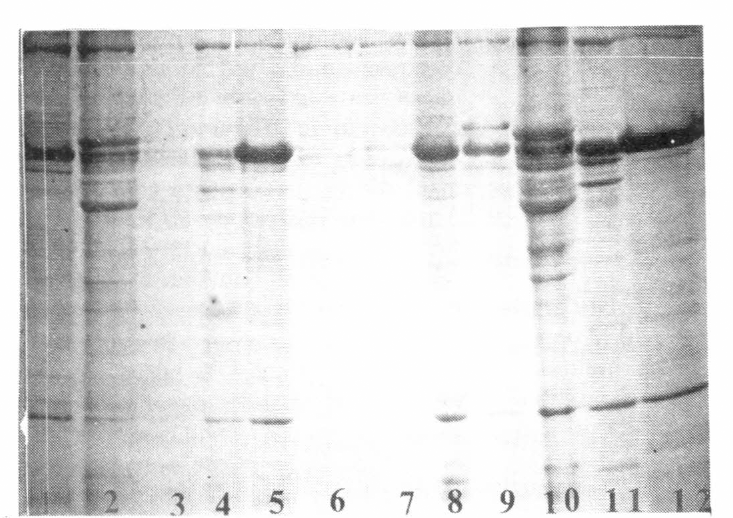
Electroforegrama de Proteínas totales de doce pupas empleando en la extracción de cada una diferente medio (Tabla 1).
En este caso, el método de coloración con Coomassie Blue es sensible a la cantidad de proteína presente y se obtuvieron bandas bien definidas. Como en el caso de las observaciones en huevos, se presenta un espectro continuo que dificulta el análisis del resultado, lo cual se puede observar en la Figura 3. En esta figura se compara el efecto de diferentes medios de extracción (Tabla No. 1).
En pupas es difícil determinar con exactitud la edad del individuo que se utiliza como muestra y, por esto se obtiene un numero alto de patrones diferentes y cada patrón corresponde a un estado de desarrollo.
4.3. Adultos
De los diversos medios de extracción probados (Tabla No. 1), se obtuvieron los mejores resultados con úrea 8M (Figura 4, muestras Nos. 7 y 11) у con sucrosa al 20% (Figura 4, muestras 6 y 8) y se observan patrones de bandas intensas y muy bien definidas. Se presentaron seis tipos de patrones diferentes, debido a que los individuos que utilizamos eran adultos pero no todos tenían la misma edad.
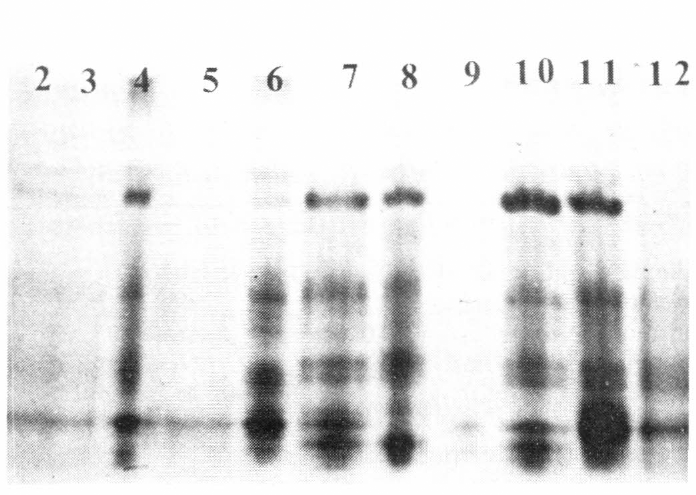
Electroforegrama de Alfa esterasas de doce adultos, Para la extracción de cada uno se empleó un medio diferentes (Tabla 1).
Después de analizar un número alto de patrones de hembras y de machos, se estableció que, al utilizar hembras, aumentaba considerablemente el número de patrones diferentes, debido posiblemente a que, el patrón de los huevos fecundados que se encuentran en la hembra se superpone al patrón de ésta. Por lo tanto, es aconsejable trabajar con hembras vírgenes o con machos.
Se encontró que, para trabajar con esterasas en adultos de gusano blanco, el sistema más indicado es el siguiente: Buffer del gel: 0.074M Tris y 0.009M en ácido cítrico con pH= 8.4.
Buffer del electrodo: Preparar un stock 0.036M en LiOH y 0.194M en ácido bórico con pH = 8.25. Esta solución se diluye 1:3 para el cátodo y 1:4 para el ánodo.
En la Figura No. 5b se observa un gel al 10% en poliacrilamida. Cada columna, cuando se revela para alfa y beta esterasas, corresponde al patrón obtenido de un individuo tratado con diferente medio de extracción.
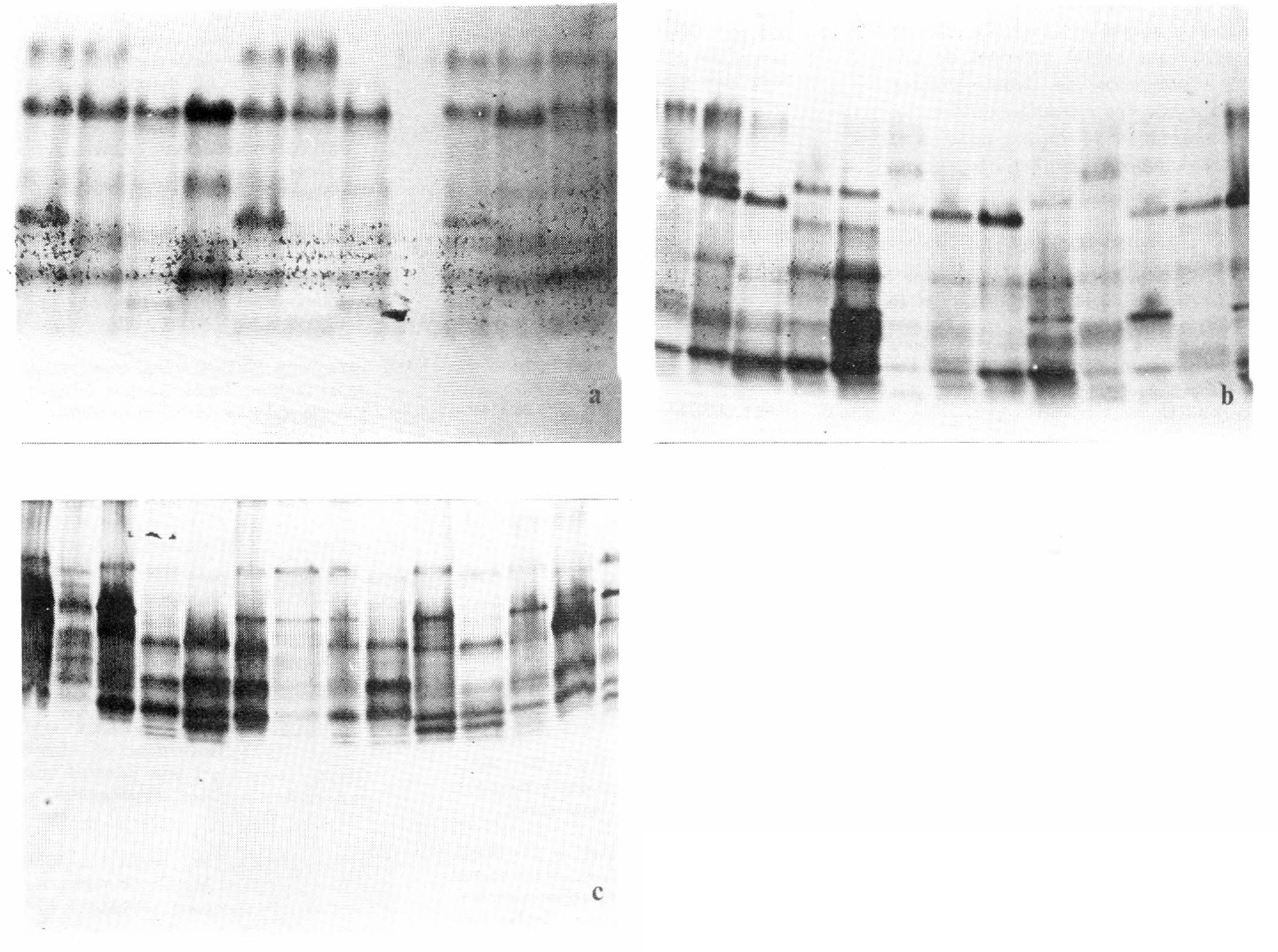
Electroforegrama de Alfa y Beta esterasas de machos adultos de Gusano Blanco, obtenidos cuando se extrae con Sucrosa al 20% y se utiliza geles de PAA al 80% (a), al 10% (b) y al 15% (c).
Desde el punto de vista técnico, resultó ideal el hecho de que la sucrosa se comportara muy bien como medio de extracción, ya que éste se puede manejar con facilidad en el momento de colocar el extracto en el gel, lo cual permitió decidir utilizar sucrosa al 20% y observar los patrones obtenidos al variar la concentración de PAA y se trabajó con geles al 8%, 10% у 15%.
En geles al 8%, se obtiene buena separación, pero las bandas no son bien definidas y se aprecian difusas (Figura No. 5a). En geles al 10%, se obtiene buena resolución especialmente de alfa esterasas. Se observaron tres zonas que, probablemente, permitirán caracterizar las poblaciones de gusano blanco (Figura No. 5b).
Con geles al 15%, se obtiene mejor resolución de las beta esterasas y bandas más definidas, pero se pierde separación de las alfa esterasas (Figura No. 5c).
5. Conclusiones Y Recomendaciones
Si se desea analizar, por medio de separación electroforética, el comportamiento de las esterasas en gusano blanco, con la perspectiva de utilizarse como marcador genético para evaluar la variabilidad de este insecto, se recomienda lo siguiente:
Utilizar machos adultos (debe determinarse la euad) libres de caparazón de quitina.
Extraer esterasas a 4 grados centígrados con sucrosa al 20%.
Utilizar geles de poliacrilamida al 10%, para análisis de alfa esterasas y al 15%, para beta esterasas.
En el gel, deberá emplearse un buffer 0.074M en Tris y 0.009M en ácido cítrico, ajustando el pH a 8.4.
Para los electrodos, deberá prepararse una solución stock 0.036M en hidróxido de litio y 0.194M en ácido bórico y ajustar el pH a 8.25, diluyendo posteriormente 1:3 para el cátodo y 1:4 para el ánodo.
El corrimiento se debe realizar a 20mA durante 4 horas.
