Abstract
El presente estudio se realizó para contribuír al conocimiento del ciclo de vida y hátibos de Aphidius colemani Viereck, parasitoide muy frecuente y activo sobre poblaciones de Myzus persicae (Sulzer) en la Sabana de Bogotá. Este trabajo se llevó a cabo bajo condiciones controladas de laboratorio (T = 21°C; H. R. = 65%), en la Facultad de Agronomía de la Universidad Nacional de Colombia en Bogotá. A. colemani es un endoparásito solitario. El período de desarrollo de huevo a adulto fue de 20 días; la longevidad de los adultos fue de 9.05 días bajo el régimen de Agua y miel y de 2.76 de las con sólo agua. El período de Precópula fue de máximo una hora; el macho puede copular con más de una hembra, mientras que la hembra rechaza cualquier nuevo apareamiento. Normalmente se reproduce en forma sexual, pero además presenta partenogénesis del tipo arrenotoquia. El período de pre-oviposición. fue de menos de 30 minutos y la relación de sexós fue de 2:1
Introduccion
Colombia es el primer exportador de flores a los EE. UU.y el segundo después de Holanda en el mercado Europeo. Los crisantemos ocuparon el segundo renglón de las exportaciones de flores colombianas en el año 1984, constituyendo los ingresos por su exportación 32.5 millones de dólares (Asocolflores, 1985).
El pulgón verde de la papa, Myzus persicae (Sulzer), por su abundancia y ataque directo, es una plaga de importancia en el cultivo de crisantemos, ya que un ataque severo ocasiona poco desarrollo de las plantas jóvenes, encrespamiento de las hojas y deformación de la flor, mermando la calidad y la cantidad del producto final.
M. persieae se ha constituído en una de las plagas de mayor importancia mundial, por su alta capacidad de reproducción y su distribución sobre un amplio número de plantas de importancia económica, a las cuales no sólo causa daño directo, sino que es capaz de trasmitir cerca de 100 enfermedades virales. además, este insecto desarrolla rápidamente resistencia a los insecticidas clorados y organofosforados, los cuales son comunes en el manejo de la plaga en la Sabana de Bogotá.
Como una nueva alternativa en el manejo de las poblaciones de este áfido, el presente contribuye al conocimiento del ciclo de vida y hábitos de Aphidius colemani Viereck para el control biológico de M. persicae en la sabana de Bogotá.
El escaso conocimiento de los parasitoides de áfidos que entrarían a formar parte de un programa de control integrado y la aparición de A. colemani, un parasitoide de alta inicdencia y permanencia sobre poblaciones de M. persicae en cultivos de cirsantemo de la Sabana de Bogotá, hacen de A. colemani un buen candidato de estudio.
Revision De Literatura
M. persicae es una plaga muy generalizada e importante en plantas ornamentales bajo invernadero; ataca principalmente crisantemos durante todo el año (Durán, 1982; Nielson, 1981; Scopes, 1970).
En una revisión que hacen van Emden et al. (1969), sobre la ecología de N. persicae, registran como enemigos naturales a parasitoides, depredadores y patógenos. Dentro de los parasitoides, incluyen a la familia Aphidiidae (Hymenoptera) con 9 génerosm entre los que sobresalen: Aphidius con 11 especies, Binodoxys con 4, Ephedrus con 5, Lysiphlebus con 3 y Praon con 10; y la familia Aphelindiae (Hymenoptera) con 5 especies del género Aphelinus.
Stary (1974) presenta una lista de los Aphidiidae enemigos de M. persicae a nivel mundial, en la cual incluye su distribución, huéspedes, datos bioecológicos y sinonimia, y registra a Aphidius ervi (Haliday, A. Gifuensis Ashmead, A. matricariae Haliday, A. picipes(Nees y A. Platensis Prethes.
Entre los enemigos naturales registrados por M. persicae en Colombia, Posada y García (1976) sólo traen Lysiphlebus testaceipes Cresson para la Sabana de Bogotá.
A. colemani fue descrito para Suramérica como A. platensis por Brethes en 1913; sin embargo, Stary (1975) esatablece que esta especie es originaria de la India y fue descrita anteriormente por Viereck en el año 1912; otras sinónimas de A. colemani son:
Aphidius colemani Viereck, 1912. Proc, U. S. Nat. Mus. 42:141.
Aphidius platensis Brèthes, 1913. Ann. Mus. Nac. Hist. Nat. B. Aires. 24:41.
Aphidius hübrichi Brèthes 1913. Ann. Mus. Nac. Hist. Nat. B. Aires 24:42.
Aphidius porteri Brethes, 1915. Ann. Zool. Apt. 2:13.
Aphidius aphidiphilus Benoit, 1955. Ann. Mus. Conge Tervuren Ser. 8, Zool. 36:349.
Aphidius lerovi Benoit, 1955. Ann. Mus. Congo Tervuren Ser. 8, Zool. 36:350.
Aphidius transcaspicus Telega, 1958. Vzbek. Biol. Zurn. 2:55-56.
A. colemani se encuentra distribuído en Asia y Africa Pantropical, Europa Mediterránea y Amércia Neotropical; además, esta especie ha sido introducida a las islas Británicas, Noruega y Checoeslovaquiea para el control biológico de M. persicae (Stary, 1975). ΕΙ parasitoide presenta un buen número de huéspedes, todos pertenecientes a la familia Aphididae; el número de especies hospedantes varía según la región, siendo más amplio en los trópicos (Stary, 1974).
Todas las especies del género Aphidius son endoparásitos solitarios. La especificidad de estos parasitoides es usualmente estrecha si su huésped es monoico, pero si los áficos son dioicos, como lo es M. persicae, pueden tener más de una especie de Aphidius como parasitoides (Stary, 1974).
La aceptación del huésped para algunos Aphidius requiere que el áfido se mueva; todos los estados del áfido son parasitados, pero los instares ninfales intermedios son usualmente los preferidos por A. matricariae (Shalaby y Rabasse, 1979).
El primer día de la emergencia, la hembra del parasitoide es capaz de ovipositar. El período de preoviposición puede ser corto, cerca de 20 minutos, pero la oriposición usualmente se inicia a las 2 horas de la emergencia del adulto y los intervalos de oviposición son aproximadamente de un minuto (Hagen y van den Bosch, 1968).
El número de huevos depositado por las hembras del género Aphidius fluctúa entre 50 y 1.500 (Millan, 1956: Hofsvang y Hagvar, 1975b, Shalaby y Rabasse, 1979).
El ciclo de vida de estos parasitoides está determinado por diversos factores ambientales, principalmente por la temperatura y además por el tamaño y el instar de su huésped (Mackauer, 1973 y Cambell y Mackauer, 1975, citados por Chorey y Mackauer, 1979).
El período de desarrollo desde la oviposición hasta la emergencia del adulto varía con la temperatura; para A. ervi a 15°C es de 27.3 días y a 21°C es de 19.9 días; para A. platensis a 15°C es de 19.9 días, a 21°C es de 14.2 días y a 24°C es de 12.4 días (Hofsvang y Hagvar, 1975); para A. matricariae a 20°C es de 13.3 días (Shalaby y Rabasse, 1979).
Los estados de desarrollo que presentan son: El huevo es translúcido y alargado; ha sido descrito para A. platensis por Millan (1956): para A. nigripes por Pare et al. (1979) y para A. matricariae por Shalaby y Rabasse (1979).
El número de instares larvales reportados en la literatura para las diferentes especies de Aphidius varía de 3 a 5, siendo el primero de tipo caudata y los siguientes de tipo himenopteriforme (Hagen y van den Bosh, 1968; Hosfvang y Hagvar, 1978; Chorey y Mackayer, 1979; Pare et al., 1979; Shalaby y Rabasse, 1979).
La pupa del género Aphidius ha sido muy poco estudiada, y ha sido descrita como del tipo extra para A. platensis por Milian (1956) y para A. matricariae por Shalaby y Rabasse (1979).
La longevidad de los adultos depende del ambiente físico y de la cantidad y calidad de alimento. A una temperatura de 20 a 25°C la longevidad promedio de I mayoría de las especies de Aphidius es de 6 a 25 días, cuando se les suministra el alimento adecuado (Hogsvang y Hagvar, 1975; Shalaby y Rabasse, 1979; Shu-Sheng y Carver, 1985). En el laboratorio, el uso de miel de abejas mas agua ha sido registrado como el alimento más satisfactorio para la mayoría de las especies de Aphidius; varios azúcares con o sin levaduras han sido citados como almento para A. ervi (Stary, 1964).
La secreción azucarada producida por los áfidos es probablemente el alimento de los Aphidius en el campo (Hofsvang y Hagvar, 1975).
Los parasitoides del género Aphidius son partenogenéticos, en donde las hembras vírgenes normalmente producen únicamente progenie de machos (arrenotoquia); sólo se conoce la excepción de A. ambiguos, el cual presenta partenogénesis telitoquica (Rasen, 1967; citado por Hagen y van den Bsch, 1968). La hembra de los Aphidius sólo se aparea una sola vez mientras que los machos lo hacen varias veces (Hagen y van den Bosch, 1968).
En el laboratorio la proporción de sexos es de 1: 1 (Shalaby y Rabasse, 1979), aunque Stary (1964), citado por Hagen y Van den Bosh (1968), reporta una proporción de 2: 1 para A. megourae.
Materiales Y Metodos
El presente trabajo se realizó en la Facultad 'de Agronomía, de la Universidad Nacional en Bogotá, bajo condiciones controladas de laboratorio (T = 21°C; H. R. = 65%).
La población inicial del parasitoide se obtuvo de recolecciones de áfidos parasitados sobre Chrysanthemun morifo/ium de La finca “F lores del Bosque” del municipio de Madrid (Cund.).
Para la identifjicación del parasitoide se emplearon las claves diagnósticas del género Aphidius de Eady (1969) Y se confirmó con el envío de especfmenes del enemigo natural al doctor P. Starv, del Instituto de Entomologra de la Academia de Ciencias de Checoeslovaquia.
La cría masiva del insecto hospedante, Myzus persicae, se hizo sobre plantas de rábano (Raphanus sativus) cultivadas en materos y colocadas en una cámara de cría.
La cría del rparasitoide, se realizó sobre su huésped natural, M. persicee, empleando para ello plantas de crisantemo cultivadas en materos y colocados dentro de una cámara de cr Ia,
Para observar el desarrollo del ciclo de vida del parasitoide, diaremente se hicieron disecciones de muestras de áfldos parasitados hasta que ocurrió la emergencia del adulto. Las disecciones se hicieron en especímenes en lactofenol y aclarados con la solución de Hoyer para observar al miroscopio sus diferentes estados de desarrollo y sus estructuras. Al mismo tiempo, se hicieron observaciones sobfe la biolgía y comportamiento del parasitoide.
Resultados Y Discusion
Identificación del Parasitoide.
Con base en las claves diagnósticas de Eady (1969) inicialmente se identificó el parasitoide como Aphidius p/atenesis Bréthes. Posteriormente, con el envío de especímenes al doctor Starv, se confirmó que el enemigo natural de M. persicae encontrado en la Sabana de Bogotá es A. colemani Viereck, el cual es muy conocido bajo su nombre sinónimo A. p/atensis.
Este parasitoide fue recolectado en el municipio de Madrid (Cund.). y no había sido registrado antes en el pa ís, por lo tanto es el primer reporte que se hace de esta especie para Colombia.
Descripción y Ciclo de Vida de A. colemani
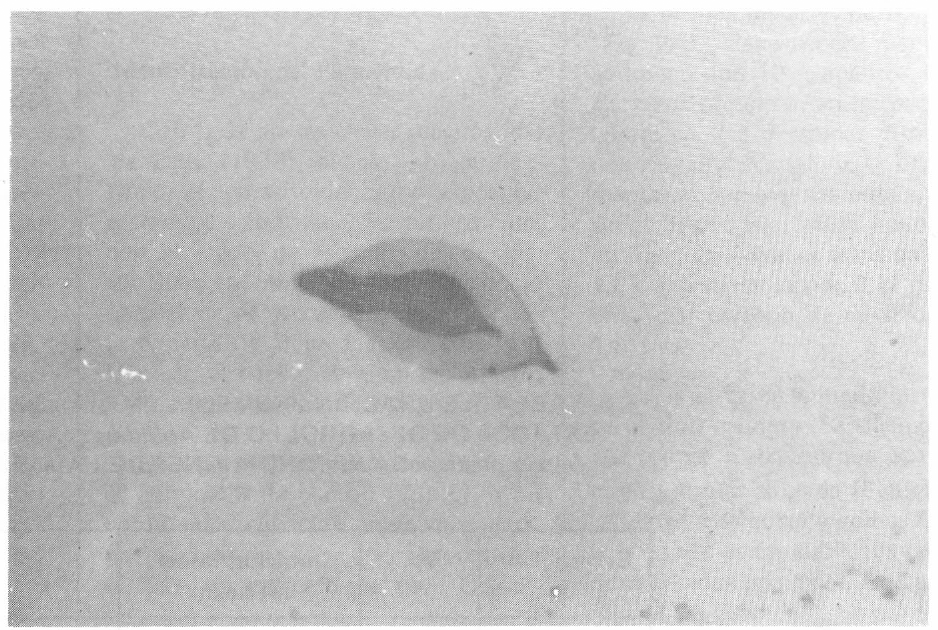
Huevo de Aphidius colemani recién ovipositado. 51,2 Χ.
Millan (1956) lo describe en igual forma, pero anota que su tamaño aumenta a medida que se desarrolla porque absorbe los humores de su huésped, aunque conserva en general su forma inicial.
DURACION PROMEDIA EN DIAS DE LOS DIFERENTES ESTADOS DE DESARROLLO DE Aphidius colemani PARASITOIDE DE Myzus persicae BAJO CONDICIONES DE LABORATORIO (T = 21°C.; H.R. = 65 %
El número de instares larva les registrados en la literatura para las diferentes especies de Aphidius varía de 3 a 5 (Hagen y van den Bosch, 1968); esta variabilidad parece ser una consecuencia de diferencias en la interpretación de las estructuras diagnósticas de los instares y no diferencias de las estructuras mismas (Chorey y Mackauer, 1979).
Las observaciones en este esudio están de acuerdo con las registradas para A. colemani (Hofsvang y Hagvar, 1978), A.1mithi Sharma & Subba Rao (Chorey y Mackauer, 1979), A. nigripes Ashmead (Pare et al., 1979) y A. Matricariae (Shalaby y Rabasse, 1979).
El primer instar es de tipo caudate (Fig. 2A). Tiene cabeza mandibulada; abdomen don 1O seqrnentos, los nueve primeros presentan en la parte dorsolateral de 2 a 8 espinas dispuestas en una fila transversal, y el último segmento abdominal presenta una cauda simple bien desarrollada y cubierta con espinas. La larva es translúcida, mide 1.03 mm de largo por 0.17 mm de ancho y su período de desarrollo es de 1.6 días.
En la larva de segundo instar persiste el tipo caudata. Se distingue de la del primer instar porque es más voluminosa y más curvada (Figura 2B). La cauda es más corta y roma. El cuerpo y la cauda están cubiertos con numerosas espinas pequeñas. Es translúcida, mide 1.98 mm. de largo por 0.25 mm. de ancho y su período de desarrollo es de1.2días
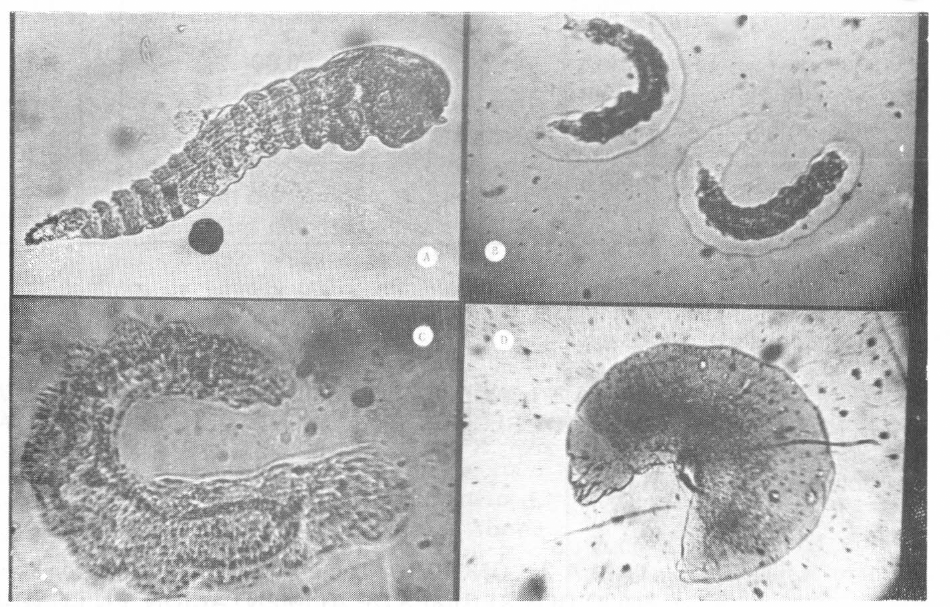
Estados larvales de A. colemani A. Primer instar 160 X. B. Segundo instar 51,2 X. C. Tercer instar 160 X. D. Cuarto instar 51,2 X.
La larva de tercer instar es de tipo himenopteriforme-amandibulada (Figura 2C). El cuerpo tiene forma de C. La cabeza es aplanada anteriormente y el último segmento caudal redondeado y bilobulado. El integumento es brillante, cubierto con numerosas espinas conspicuas. Es blanquecina, mide 2.64 mm de largo por 0.37 mm de ancho y su período de desarrollo es de 1.55 días.
La larva de cuarto instar es también himenopteriforme (Figura 2Dl. pero con mandíbulas de color café y fuertemente quitinizadas. La cutícula está cubiera densamente con tubérculos. El sistema traqueal y los espiráculos se observan ya desarrollados. EI extremo caudal del abdomen es redondeado y abultado. Es de color amarillo limón, nide 3.35 mm de largo por 0.47 mm. de ancho y su período de desarro 110 es de 3.35 días.
Pupa. Es de tipo exarata; se encuentra dentro de un cocón de seda con la cabeza orientada hacia la región caudal del huésped; se observa muy encorvada con el abdomen doblado casi en contacto con la parte ventral del tórax. Al principio es de color amarillo con los ojos y ocelos dde color rojo y cerca de su abdomen se observa acumulación de excrementos en forma de bol itas de color café.
En este estado ocurre la unión del protodeo con el intestino medio, los cuales se encontraban separados; esto permite la excreción del material fecal acumulado en el intestino medio durante el período larval.
A medida que se desarrolla, el cuerpo se torna de color oscuro hasta adquirir las características del futuro adulto. Mide 3.04 mm. de largo y su período de desarrollo es de 8.6 días.
Bajo las condiciones del estudio, la duración promedia desde la oviposición hasta la emergencia del adulto fue de 20 días (Tabla 1). Hofsvang y Hagvar (1975), trabajando con A. platensis en M. persieae sobre pimentón, a 210 C y 70% de H. R., reportaron una duración de 14.2 días¡ para el mismo período.
La tasa de desarrollo está determinada por diversos factores, entre los que se incluyen las condiciones ambientales, el tamaño y el instar rlel huésped al momento de la parasitación (Mackauer, 1973; Campbell y Mackauer, 1975, citados por Chorey y Mackauer, 1979).
Adulto. Los adultos tienen las características típicas del género Aphidlus. Las antenas son de tipo filiforme; alas anteriores con un estigma bien diferenciado, primera celda discal y primera cubital fusionadas y cerradas en todas sus márgenes (Powell, 1982) (Figura 3A y B).
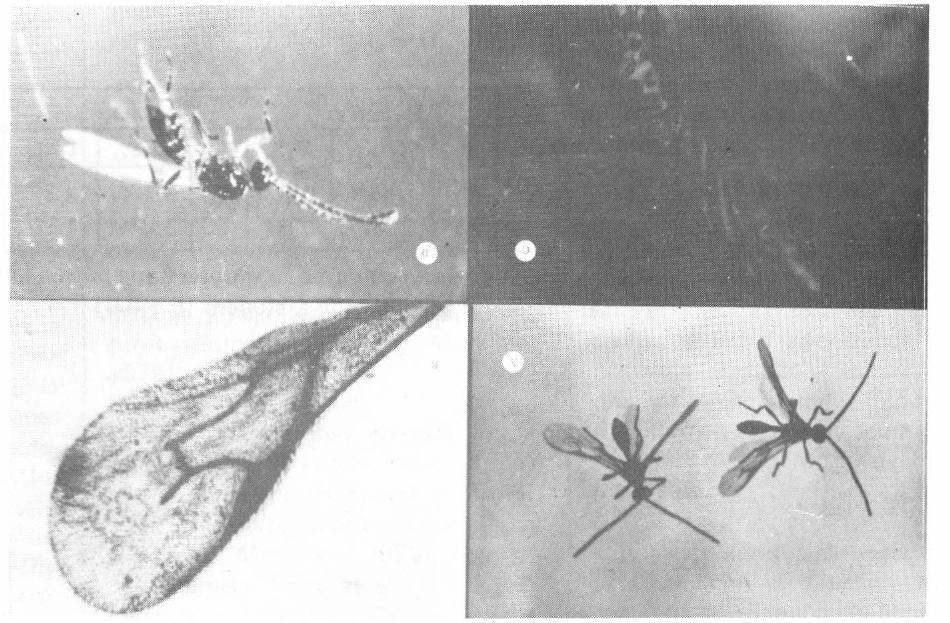
A. Macho y hembra B. Ala anterior. C. Primer segmento abdominal 300X. D. Hembra de A. colemani.
Además, como características específicas presenta el primer segmento abdominal peciolado, con una serie de 4 a 6 crestas lineales en su parte anterolateral (F igura 3C) y la antena de la hembra con 14 a 16 segmentos.
En la hembra, la cabeza es de color negro, más larga que ancha y tan ancha como el tórax; los ocelos ubicados en el centro del vértice y dispuestos en un triángulo acutángulo; mandíbulas encorvadas y aguzadas en el ápice; palpos maxilares de cuatro artejos; palpos labiales de dos segmentos; antenas de tipo filiforme e insertadas a la altura de la línea media transversal de los ojos, con 14 a 16 segmentos (Figura 3D).
Tórax de color negro con pronoto estrecho y oculto por la qibosidad 'del escudo del mesonoto; escudete con la superficie algo rugosa; metanoto bastante ancho con un par de impresiones sub laterales; propodeo liso con una carina mediana longitudinal que se bifurca antes de alcanzar la gruesa carina transversa.
El abdomen es fusiforme y puntiagudo en su extremo caudal, más largo que la cabeza y el tórax juntos; del segundo al quinto segmento abdominal de clor café oscuro y el pecíolo y el último segento caudal de color café claro. La longitud del cuerpo en promedio es de 2.78 mm.
El macho se diferencia de la hembra por tener antenas formadas por 17 - 19 segmentos; el tamaño de los especímenes es menor, con una longitud del cuerpo promedio de 2.5 mm y la intensidad de la coloración del cuerpo es más oscura.
La longevidad de los adultos fue estimada en el laboratorio bajo dos regímenes de nutrición: col') miel de abejas yagua y con sólo agua destilada. La importancia de la miel se ilustra en la Tabla 2. La longevidad fue mayor bajo el régimen de agua y miel, con un promedio de 9.05 días, contra los alimentados con sólo agua 2.76 días. Diversos autores han demostrado la importancia de la miel en la longevidad de los parasitoides de áfidos (Hofsvang y Hagvar, 1975; Shalaby y Rabasse, 1979).
LONGEVIDAD DEL ADULTO DE A. colemani PARASITOIDE DE M. persicae BAJO DOS REGIMES DE ALIMENTACION, EN CONDICIONES DE LABORATORIO (T = 21°C. H. R. = 65%)
Promedio en la misma columna seguidos de una misma letra no presenta diferencias significativas, según la prueba de t, student (P = 0,01 +)
Aunque de acuerdo con la Tabla 2, bajo el régimen de miel yagua las hembras viven más que los mahcos y bajo el régimen de sólo agua destilada los machos vien más que las hembras, no hay diferencias significativas entre la longevidad de machos con relación a la de hembras. Las diferencias de longevidad entre los sexos es también pequeña en otras especies de Aphidius. Hofsvang y Hagvar (1975) reportan de igual manera la longevidad de hembras y machos para A. ervi y A. platensis; en cambio Shalaby y Habasse (1979) reportan que los machos de A. matricariae viven más que las hembras bajo el régimen de agua y miel.
Hábitos. El lugar preferido de la planta para la búsqueda del áfido por parte del parasitoide son las hojas del tercio superior y los botones florales de la parte apical. En la búsqueda del huésped, las hembras recorren las hojas por el haz y el envés y al ascender o descender por el tallo cambian de una hoja a otra. En su recorrido, la hembra del prasitoide vibra las antenas en forma alterna hacia arriba y hacia abajo, pero una vez es detectado el huésped mediante el contacto antenal, el parasitoide se detiene.
Al localizar el huésped, la hembra se coloca en posición de ataque, con las antenas flexionadas hacia el dorso y con el abdomen arqueado por debajo de las patas en dirección del áfido, y con un rápido movimiento agita las alas y oviposita, (Figura 4A).

A. Posición de ataque. B. Copula de A. colemani. C. Afido de 2 días de parasitación. D. Afido de 11 días de parasitación.
El período de preoviposición es menor de 30 minutos. El sitio preferido de oviposición es usualmente en los segmentos abdominales, en la región cerca de los cornículos, pero muchas veces se observó que la hembra del parasitoide ovipositó en los segmentos toráxico; la oviposición en las patas del huésped fue también observada.
Millan 1956 para A. platensis y Shalaby y Rabasse (1979) para A. metrieariae reportan de igual manera la forma de oriposición.
El número de intentos de oviposición realizados por el parasitoide depende de la capacidad de fuga o de rechazo del huésped M. persieae; si el afido escapa, la hembra lo persigue en posición de ataque; si lo hace rápidamente, la hembra lo persigue en posición de búsqueda y lo ataca de frente o de lado hasta lograr ovipositar exitosamente.
Cuando el áfido no huye, sir.o que rechaza al parasitoide mediante movimientos bruscos con las patas o el abdomen, sin sacar el estilete de la hoja donde se está alimentando, la hembra del parasitoide cambia el ángulo de posición de ataque hasta lograr ovipositar.
Las mismas formas de rechazo fueron registradas para Hyperomyzus lectucae contra A. soncbi por Shu-Sheng y Carver (1985) Y para M. persieae contra A. matricariae por Shalaby y Rabasse (1979).
La ejergencia del adulto de A. colemani ocurre a cualquier hora del día y su emergencia la realiza de la misma forma como la describen Shalaby y Rabasse (1979) para A. matricariae. Para emerger, mastica el integumento del huésped hasta realizar una abertura en forma redonda, dorsalmente en el extremo final de abdomen; luego, con presión de la cabeza y de las patas anteriores levanta el opérculo del orificio y sale al exterior.
Recién emergidos, tanto la hembra como el macho, se acicalan las mandíbulas y las antenas con las patas anteriores y mueven las alas para extenderlas; luego la hembra se presiona el abdomen hacia atrás con las patas posteriores, permaneciendo quieta; el período de precópula es menor a 30 minutos.
Cuando el macho está en capacidad de aparear a la hembra, se hace más activo, agitando fuertemente las alas y las antenas; enseguida se sube al abdomen de la hembra y agitando constantemente las antenas, dobla el abdomen para entrar en contacto con el ovipositor de la hembra (Figura 4B).
El promedio de duración de la cópula es de 2 minutos.
El macho es capaz de aparearse con una nueva hembra después de aproximadamente 20 minutos de haber ocurrido la cópula anterior; mientras que una hembra copulada rechaza aparearse de nuevo.
A. colemani se reproduce normalmente en forma sexual, pero además se reproduce por partenogénesis de tipo arrenotóquico. Estas formas de reproducción son iguales a las registradas en otras especies de Aphidius (Hagen y van de Bosch, 1968).
Las hembras copuladas de A. colemani dieron origen a una progenie constituída por hembras y machos en una proporción de 2:1, aunque la proporción de sexos más común registrada en el laboratorio es 1:1 (Shalaby y Rabasse 1979).
A. colemani parasita todos los estados de desarrollo del áfido, pero las formas aladas son poco atacadas. La hembra del parasitoide pone un solo huevo a través del integumento del huésped; a los áfidos parasitados no se les nota ningún cambio aparente durante los primeros días (Figura 4C); cuando la larva del parasitoide llega al tercer instar, ocho días después de haber sido parasitado el áfido, éste aparece más hinchado en relación a otros áfidos sin parasitar; además, sus movimientos se van haciendo cada vez más lentos.
Diez días después de la parasitación, el afido se torna de color café (Figura 4D y se observan los movimientos de la larva de cuarto instar del parasitoide; doce horas después, los áfidos son fijados a la hoja por su parte ventral. A este estado del áfido parasitado en la literatura se denomina como “momia”. La larva del parasitoide realiza la fijación del áfido parasitado mediante la perforación de toda su parte ventral; luego por medio de hilos de seda que segrega en forma de puntos cubre la abertura, confromando la base de fijación.
Aunque bajo condiciones de laboratorio se ha observado superparasitismo, cuando la larva del parasitoide se encuentra en primer instar larval, sólo emerge un parasitoide por áfido para sitado; esto es debido posiblemente a que hay una competencia de tipo interespecífico por canibalismo, ya que se han observado restos de mandíbulas de otras larvas en el tracto digestivo de las larvas de cuarto instar del parasitoide. Millan (1956) opina, y cita a otros autores, en el sentido de que la eliminación de las larvas competidoras se efectúa por una enzima llamada citocilina que inhibe el desarrollo de aquellas, permitiendo que prospere la larva más adelantada. Aunque el superparasitismo ocurre en el laboratorio, éste no es común en el campo (Hagen y van den Bosch, 1968).
Conclusiones
El enemigo natural encontrado en Myzus persicae (Sulzer) se identificó como Aphidjus colemani Viereck; siendo la primera referencia que se hace de este insecto benéfico en Colombia.
El desarrollo de A. colemani de huevo hasta la emergencia del adulto dura 20 días; la longevidad del adulto fue de 6.29 días bajo el régimen de miel y agua.
La cría masiva de A. colemani se puede realizar fácilmente sobre M. persicae como huésped.
Por estar adaptado a las condiciones ambientales bajo invernadero, A. colemani es un buen candidato para el control de M. persicae en el cultivo de flores bajo esas condiciones.
