Abstract
The main objetive of this research was to determine the pathogenicity of Nomuraea rileyi (Farlow) Samson (Hyphomycetes) on third instar larvae of Spodoptera frugiperda (J. E. Smith) (Lepidoptera: Noctuidae), host on which the fungus usually causes epizootics in corn fields. Three concentrations of conidia (0.3, 3.1 and 30.6 conidia/mmβ of foliar area) were tested against third instar larvae in a completely randomized design with four replications. Each experimental unit consisted of 25-40 larvae. Larvae were allowed to feed during 48 hours on treated leaves and them on untreated leaves until death. The development of N. rileyi in S. frugiperda was divided in two phases, one from inoculation to death and other from death to conidiogenesis. During the first phase the initial symptoms of infection are brown necrotic spots on the insect integument, which indicate the fungus penetration, later the larva turns pale in color, inappetent, slugish, and swollen toward the last abdominal segments. Larvae died during this phase in 9.03 to 12.09 days, time increased as conidia concentrations decreased. Second phase is characterized by pathogen signs and lasted about four days at all concentrations tested. This phase can be described as follows: 36-48 hours after death, larvae are completely covered by white mycellium, and 24-36 hours later occurs the conidiogenesis characterized by the green appearence of the larva. The dislodgement of conidia occurs 12 hours after iniciation of conidiogenesis. Total life cycle of N. rileyi varied from 12.81 days for the highest concentration (30.6 conidia/mmβ) to 15.74 days to the lowest concentration (0.3 conidia/mmβ). Average percent mortality in larvae of N. rileyi to concentrations of 0.3, 3.1 and 30.6 were 40.90, 83.75 and 93.0, respectively. No significant differences were found between the concentrations 3.1 and 30.6 conidia/mmβ. The median lethal time (LT50) was 7.86 and 7.82 days for concentrations of 3.1 and 30.6 conidia, respectively. The median lethal concentration (LC50) was 0.87 conidia/mmβ. Results of this research indicate that this isolate (NRB1) of N. rileyi from Bello, Antioquia, is highly virulent against S. frugiperda.
Introduccion
El gusano cogollero del maíz, Spodoptera frugiperda (J. E. Smith) (Lepidoptera: Noctuidae), es un insecto plaga que anualmente ocasiona considerables reducciones en la producción de maíz si no se controla oportunamente. Este insecto, además de maíz, ataca por lo menos otros 36 cultivos en Colombia (ICA, 1972-85; Posada et al., 1976). Las prácticas actuales de manejo para el control del cogollero se basan en la aplicación de insecticidas; sin embargo, existe conciencia para reducir la dependencia de agroquímicos e implementar medios de control armónicos dentro de un programa de manejo integrado de plagas.
El S. Frugiperda es atacado por una diversidad de enemigos naturales (parásitos, predatores y patógenos), entre los cuales se destaca el hongo Nomuraea rileyi (Farlow) Samson (Hyphomycetes). Este Entomopatógeno se encuentra distribuido en diversos agroecosistemas y zonas geográficas, en donde juega un papel importante en la regulación de las poblaciones no sólo del gusano cogollero sino de otras 12 especies de importancia económica, entre las cuales merecen citarse Anticarsia gemmatalis (Hübner), Pseudoplusia includens (Walker), Trichoplusia ni Hübner) y Heliothis virescens (F.).
En Colombia, a pesar de que N. rileyi se registra con frecuencia (ICA, 1972-1985), existe un desconocimiento sobre su biología, modo de acción, patogenicidad y factores que favorecen sus epizootias. Actualmente hay interés en desarrollar entomopatógenos como insecticidas microbiales y se considera que N. rileyi puede ser una buena alternativa por su virulencia, rango de huéspedes y distribución geográfica.
En este trabajo se registran los resultados sobre biología y patogenicidad del hongo en larvas de S. frugiperda alimentadas con maíz.
Revision De Literatura
Sobre el hongo N. rileyi existe un gran volumen de información en la literatura extranjera. A pesar de que este hongo fue descubierto hace más de 100 años (1883), solamente hasta 1955 se hicieron los primeros intentos experimentales para usarlo en un programa de control biológico (Chambarlin y Dutky, 1958). En Colombia, fuera de los registros de su presencia (Tabla 1) no existe ningún estudio de N. rileyi. Recientemente en labores de reconocimiento de enemigos naturales de S. Frugiperda en el Valle de Aburrá se ha encontrado que N. rileyi juega un papel importante en la dinámica de poblaciones de esta plaga (Torres y Uribe, 1985; Bustillo, datos no publicados).
INSECTOS HUESPEDES SUSCEPTIBLES A Nomuraea rileyi OBSERVADOS EN DIFERENTES CULTIVOS Y LOCALIDADES EN COLOMBIA
* 1 = ICA (1972-1985)
2 = Posada y García (1976)
L = Patogenicidad bajo condiciones de laboratorio.
Taxonomía e identificación.
Nomuraea rileyi (Farlow) Samson es un hongo imperfecto que pertenece a la subdivisión Deuteromcotina, clase Hyphomycetes, orden Moniliales, familia Moniliaceae. Su posición genérica es muy reciente, kish et al. (1974) lo reubicaron en Nomuraea después de estar durante mucho tiempo en el género Spicaria. Los sinónimos de N. rileyi son: Beauveria rileyi (Farlow) Gosswald, Botrytis prasina (Maublanc) Savada y S. rileyi (Farlow) Charles (Ignoffo, 1978; Samson, 1974).
Los estados sexuales de Nomuraea se desconocen; sin embargo, Evans (1982) señala que Cordyceps es uno de ellos. Patiño et al. (1977) encontraron en una plantación de caucho atacada por Erinnys ello (L.) un hongo sobre este insecto que identificaron como Spicaria sp. Senalan que el hongo difiere de N. rileyi en que “El crecimiento fungoso no se torna de color verde al esporular”. Además, identificaron la fase perfecta de este hongo como Cordyceps; ésta se obtuvo manteniendo al insecto afectado bajo una capa de aserrín húmeda.
Descripción del hongo en medios de cultivo.
Samson (1974), Kish et al. (1974) e Ignoffo (1978, 1981) han descrito el crecimiento y comportamiento de N. rileyi en varios medios de cultivo. En Agar-Maltosa a 25°C las colonias crecen muy lentamente y en un mes alcanzan un diámetro de 0,7-1,2 cm. El crecimiento inicial es similar a las levaduras por gemación del tubo germinal de una conidia. Después de unos pocos días estos cuerpos hifales en forma de levadura producen un crecimiento de color crema pegajoso, con olor a humedad. La esporulación es bastante localizada inicialmente y luego se dispersa a través de la colonia. El color de la colonia progresa de blanco a verde pálido hasta un verde intenso. Las hifas vegetativas miden de 2-3 um de diámetro; son septadas. hialinas a ligeramente pigmentadas. Los conifióforos que crecen de hifas sumergidas son erectos, septados, miden hasta 150 um en longitud y 2-5 um de diámetro. Las ramas que se forman cerca a cada septo se desarrollan en ramilletes cada uno dando origen entre 2 y 4 fiálidas. Las ramas miden 5-8 por 2-4 um son por lo general cilíndricas y ocasionalmente con una base hinchada. Las conicias en cadenas divergentes, son lisas, elipsoides, verdes palidas y con dimensiones de 3,4-4,5 por 2-3,1 um.
El crecimiento óptimo de N. rileyi se obtiene a 25°C en el medio Sabouraud-maltosa-agar fortificado con 1%de extracto de levadura (SMAE); temperaturas superiores o inferiores a ésta causan un crecimiento más lento. El hongo no crece a temperaturas superiores a 32 C. La esporulación a 25°C ocurre a los 9 días; ésta se inhibe a temperaturas superiores a 30°C. La luz no tiene ningún efecto en el crecimiento o esporulación (Ignoffo et al., 1976a).
Patogénesis
El estado infectivo de N. rileyi son las conidias, que después de germinar inician la penetración a través del integumento produciendo una escasa invasión micelial, con ensanchamiento, que externamente semejan apresorios. La invasión del hemocelo ocurre en las 24 horas siguientes a la exposición de las larvas a las conidias. El crecimiento inicial del hongo es por gemación, semejante al de la levadura para producir las plastosporas, las cuales se distribuyen por todo el hemocelo produciendo un tapete micelial después de 3 a 5 días. Los primeros síntomas de la infección aparecen después de 1 a 3 días de ser expuestas las larvas a las conidias. Inicialmente se manifiestan por pequeños puntos amarillos a marrón sobre el integumento. Despues las larvas pierden movimiento, cesan de alimentarse, el cuerpo se torna pálido y ocurre una ligera hinchazón de los segmentos abdominales posterioes. La muerte ocurre a los 5-8 días de expuestas a las conidias. Las larvas se modifican y se cubren de un micelio denso y blanco que 1-2 días más tarde produce gran cantidad de conidias verdes pálidas, que se desprenden y distribuyen fácilmente por el vinto (Ignoffo, 1978).
El ciclo biológico de N. rileyi comprende dos fases: una patogénica y otra saprofítica. La fase de patogénesis ocurre cuando el hongo entra en contacto con el tejido vivo del huésped. La muerte del insecto es ocasionada por la acción de toxinas producidas durante los estados iniciales del crecimiento micelial. La fase saprofítica se presenta cuando el hongo inicia su desarrollo en tejido muerto, sin actividad patógena sobre el huésped. El ciclo de desarrollo de N. rileyi en larvas de lepidoptera n-fectadas es de casi 10 días (Ignoffo, 1978). Bell (1975) determinó la patogenicidad de las conidias y blastosporas de N. rileyi obtenidas en medio de cultivo sólido y líquido aireado, aplicadas externamente sobre larvas de Heliothis zea (Boddie) de 6 días, encontrando que las conidiosporas producen el 98% de mortalidad después de 14 días y que las blastosporas no producen mortalidad después de 21 días. Kish et al. (1974) encontraron que el tiempo de la exposición al patógeno y la muerte de las larvas de A. gemmatalis promedió 6 días. Rao y Phadke (1977) lograron obtener un 100% de mortalidad en larvas de Spodoptera litura (F.) de 4-6 días de edad.
El ciclo biológico de N. rileyi varía de acuerdo con el huésped, la concentración de conidias; la virulencia y las condiciones ambientales. La duración del ciclo biológico en larvas de primer instar de T.ni tomó de 8-12 días al ser expuestas a una concentración de 1000 conidias/mmβ sobre la superficie de hojas (Ignoffo, 1981). En larvas de A. gemmatalis el tiempo entre la exposición al patógeno y la muerte, promedió 6 días y 3,5 días desde la formación de los conidióforos a la conidiogénesis (Kish y Allen, 1978)
Biotipos
Del hongo N. rileyi se han obtenido varios biotipos geográficos que muestran diferentes grados de patogenicidad. Ignoffo (1978), en pruebas de infectividad empleando cepas provenientes de cuatro regiones (Missouri, Mississipı, Brasil y Florida), encontró que la susceptibilidad de T. ni fue igual para las cepas de las tres primeras localidades y 7 a 17 veces menos susceptible a la cepa de Florida. Boucias et al. (1982) encontraron que la mortalidad de S. frugiperda variaba usando dos aislamientos diferentes de N. rileyi. En uno denominado FI-78 obtuvieron 33% de mortalidad, mientras que con FI-74 obtuvieron 82%.
Susceptibilidad
Dentro de una raza específica de N. rileyi la patogenicidad varía de acuerdo cor el huésped y con el estado de desarrollo. Boucias et al. (1982), al evaluar seis especies de noctuídos, encontraron una gran variación en la mortalidad de cada una dentro de una misma raza de N. rileyi. En cuanto a la susceptibilidad por instares se ha encontrado también variación. En T. ni los instares más susceptibles son el primero y el segundo, mientras que en H. zea el tercero y el quinto son los más susceptibles (Ignoffo, 1981).
Se ha encontrado que a medida que se incrementa la concentración del inóculo, la patogenicidad del hongo es mayor. Ignoffo et al. (1976c) encontraron que larvas de T. ni de segundo instar expuestas a cinco concentraciones tuvieron una mortalidad mayor y más rápida con las concentraciones más altas.
La temperatura y la humedad relativa juegan un papel importante en la invasión y desarrollo de la infección. Ignoffo (1981) registró que 25°C es la temperatura óptima para el desarrollo de N. rileyi en larvas de primer instar de T. ni. Por otra parte, Kish y Allen (1978) establecieron que el límite más bajo de humedad relativa para la infección de las larvas por N. rileyi está entre 50-70%. Los niveles bajos de humedad afectan la germinación de las conidias que son el único estado infectivo del hongo (Ignoffo, 1978).
Huéspedes y distribución.
El hongo N. rileyi es patogénico a un gran número de insectos no sólo bajo condiciones de campo, sino en el laboratorio. Pruebas de patogénicidad han mostrado que N. rileyi puede desarrollarse normalmente en cerca de 37 lepidópteros y dos coleópteros (Ignoffo, 1978; ICA, 1972-85, Posada y García, 1976). En Colombia, los registros de N. rileyi cubren una gran parte del territorio nacional y se ha encontrado sobre 13 lepidópteros en diferentes cultivos (Tabla 1). N. rileyi es un hongo cuya distribución mundial abarca los continentes de América, Africa y Asia, hasta el momento se ha registrado en 14 países diferentes (Ignoffo, 1981).
Inocuidad
N. rileyi no germina, ni crece ni esporula a temperaturas superiores a 35°C, lo cual indica que no afecta invertebrados homeotérmicos. Las conidias expuestas a jugos gástricos de humanos se inactivan rápidamente. Cuando se administró a ratas en dosis de 1,1X 07 conidias/litro de aire durante una hora no se observó anormalidades clínicas, patológicas o histopatológicas (Ignoffo, 1981).
El hongo también es inofensivo a ciertos parásitos y predatores. Tres predatores (Hippodamia convergens Guérin-Méneville Chrysopa carnea Stephens, Podisus maculiventris Say), tres parásitos (Voria ruralis Fall, Cotesia (=Apanteles) marginiventris (Cresson), Campoletis sonorensis) y un parásito de huevos (Telenomus proditor) no fueron susceptibles cuando se los expuso a dosis 25 veces más altas que las usadas en experimentos de campo para inducir epizootias (Ignoffo et al., 1976b; Phadke y Rao, 1978). En ciertas ocasiones se ha observado disminución en el parasitismo por insectos benéficos cuando el huésped es atacado simultáneamente por N. rileyi (Burleigh, 1975; King y Bell, 1980).
Materiales Y Metodos
Para el desarrollo de este estudio se mantuvo una colonia de S. frugiperda alimentada con follaje de maíz. El inóculo inicial de N. Rileyi se obtuvo de especímenes enfermos colectados durante el segundo semestre de 1984 en un campo de maíz de la Estación Experimental “Tulio Ospina” del ICA, en Bello (Ant.). Este aislamiento se denominó NRB1 y se mantuvo en dicha Estación. La zona corresponde a la formación ecológica bosque húmedo-premontano, con una precipitación promedia de 1400 mm, temperatura media de 23°C y 1440 m.s.n.m.
El inóculo se aumentó y mantuvo en el laboratorio sobre larvas del cogollero. Cuando el hongo fructificó a las conidias se desprendieron, se colectaron y almacenaron en frascos de vidrio tapados con algodón y cubiertos con papel aluminio. La edad promedia de las conicias utilizadas en el experimento fue de 20 días. Para estudiar la patogenicidad del hongo se preparó una solución madre de conidias en agua destilada, adicionándole 0,05% del agente humectante Tween 20, que permite la obtención de una solución de conidias homogéneas. La concentración de las conidias se determinó con un hemocitómetro.
El inóculo se preparó de una solución madre que contenía 5,4 x 106 conidias. Posteriormente a través de diluciones seriales se obtuvieron tres concentraciones para evaluar (5,4 x 105; 5,4 x 104; 5,4 x 10³ conidias/ml). De cada concentración se aplicó 0.1 ml a cada lado de una área promedia de 1.764 mmβ de follaje de maíz para obtener una densidad de 30,6; 3,1 y 0,3 conidias/mmβ respectivamente. El follaje se desinfectó previamente con una solución de 0.5% de hipoclorito de sodio durante cinco minutos; 10 larvas de tercer instar del cogollero se expusieron al follaje una vez que la aspersión se secó y se les permitió alimentarse de este material por espacio de 48 horas. Estas larvas se mantuvieron en platos Petri con papel filtro húmedo y dentro de un desecador a una humedad cercana a la saturación y temperatura promedia de 22,87°C ± 0,46° C.
Al cabo de 48 horas las larvas se colocaron en forma individual en platos de petri, proporcionándoles follaje aséptico sin tratamiento cada dos días y manteniéndolas en condiciones de laboratorio (T=21°C, HR =84%). El experimento se organizó en un diseño completamente al azar, con cuatro tratamientos (0; 0,3; 3,1; 30,6 conidias/mmβ) y cuatro repeticiones cada una con 25-40 larvas. Se hicieron observaciones sobre síntomas externos, comportamiento del insecto, porcentaje de mortalidad y cálculos del tiempo, letal medio y concentración letal media siguiendo la metodología de Ignoffo et al. (1976c).
Resultados Y Discusion
La cepa de N. rileyi de Bello (Ant.) (NRB1), presentó patogenicidad sobre larvas de tercer instar de S. frugiperda. El proceso de la enfermedad produce distintos síntomas externos, de acuerdo con la intensidad de la infección. Cuando la larva muere aparecen los signos del patógeno que junto con los síntomas permiten diagnosticar la enfermedad causada por N. rileyi.
Los síntomas iniciales de la infección son manchas o puntos de color marrón sobre el integumento que posteriormente se tornan necróticas (Figura 1). Al avanzar la infección la larva se vuelve pálida, pierde apetito, movimiento y puede ocasionalmente rnanifestar hinchazón en los últimos segmentos abdominales. El cuadro de síntomas observado es muy similar al descrito por Ignoffo et al. (1978) en larvas de T. ni y por Boucias et al. (1982) sobre seis especies de noctuidos. El síntoma más notorio y persistente en larvas atacadas por N. rileyi son las manchas marrones descritas arriba que aparecen sobre el integumento aproximadamente 1-2 días después de la exposición al inóculo. Estas manchas a los 3-4 días se tornan necróticas, evidenciando los sitios de penetración del hongo como respuesta a la acción lítica de sus enzimas liberadas durante la penetración (Mohamed et al., 1978). La necrosis del tejido se encuentra comúnmente en el lado ventral de la larva; sin embargo, también se puede presentar lateral o dorsalmente. Algunas larvas murieron sin presentar síntomas de penetración del hongo a través del integumento, lo que indica, que el hongo tiene otras vías de penetración al huésped. Esto concuerda con lo minifestado por Kish y Allen (1978), quienes comprobaron que N. rileyi penetra no sólo a través del integumento sino también por vía oral.
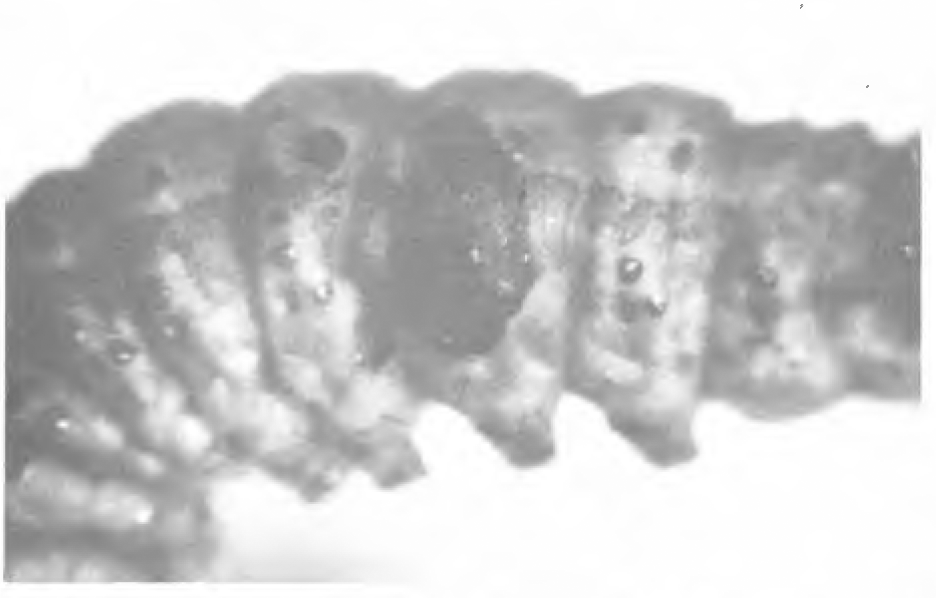
Mancha necrótica sobre el integumento de una larva de Spodoptera frugiperda causada por la penetración de Nomuraea rileyi
Un bajo porcentaje (4.0%) de larvas que recibieron 0,3 conidias/mmβ presentaron síntomas de infección y palidez, muriendo at empupar. En los cadáveres no se desarroló el hongo N. rileyi, ni otro ortanismo por lo que esta mortalidad se registró bajo otras causas. Este fenómeno no puede interpretarse como un caso de resistencia o tolerancia en las larvas que no permite el desarrollo de la enfermedad, posiblemente debido a la exposición a concentraciones bajas de conidias que sólo provocan una infección latente. La muerte de la larva al llegar a pupa pudo ser una causa fisiológica, probablemente por competencia de nutrientes que impide el desarrollo de ambos organismos.
Con la muerte por la acción de N. rileyi termina la fase de patogénesis y empieza la fase de saprogénesis, en la cual el hongo se desarrolla a partir del tejido muerto (Ignoffo et al., 1978). Con el desarrollo externo de los signos del patógeno comienza la reproducción de N. rileyi a través de una serie de etapas diferenciables por sus características y duración. Al morir la larva, el cuerpo se vuelve de color café pálido, es de consistencia blanda y se estira comp.etamente.
Transcurrido un tiempo de 12 a 24 horas, el cuerpo eimpieza a cubrirse de un micelio blanco poco denso; 36 a 48 horas después de la muerte se cubre de micelio blanco muy denso que le da al cadáver momificado la apariencia de tiza blanca. La conidiogénesis del hongo empieza 24 a 36 horas más tarde y se manifiesta por el cambio de color del micelio de blanco a verde (Figura 2). El desprendimiento de las conidias ocurre a las 13 horas de iniciada la conidiogénesis. Las conidias se desprun-den fácilmente de los conidióforos favoreciéndose la dispersión del hongo en el campo o su recolección en el laboratorio.
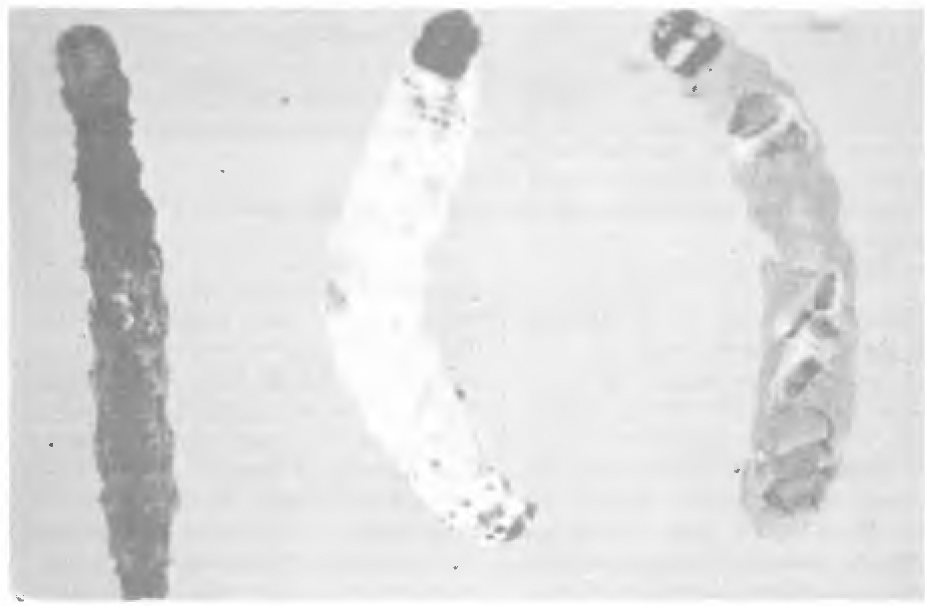
Diversas etapas de desarrollo del Nomuraea rileyi en larvas de Spodoptera frugiperda. De izquierda a derecha: Larva recien muerta con crecimiento micelar blanco; larva totalmente cubierta por el micelio color blanco generalizado; larva sobre la cual se inició la conidiogénesis color verde.
El desarrollo de N. rileyi en las larvas de S. frugiperda se dividió en dos etapas. Una desde el momento de la inoculación hasta la muerte de la larva y la otra a partir de la muerte hasta la conidiogénesis incluyendo el desprendimiento de las conidias. La duración de estas etapas aparece en la Tabla 2. Las concentraciones mayores mataron más rápidamente las larvas pero no se observaron direrencias apreciables en la segunda etapa. El ciclo de vida total de N. rileyi varió desde 12,81 días para la mayor concentración hasta 15,84 días para la menor concentración (Tabla 2). En la figura 3 se presenta el ciclo biológico y la sintomatología causada por el hongo en larvas de tercer instar inoculadas con 30,6 conidias/mmβ
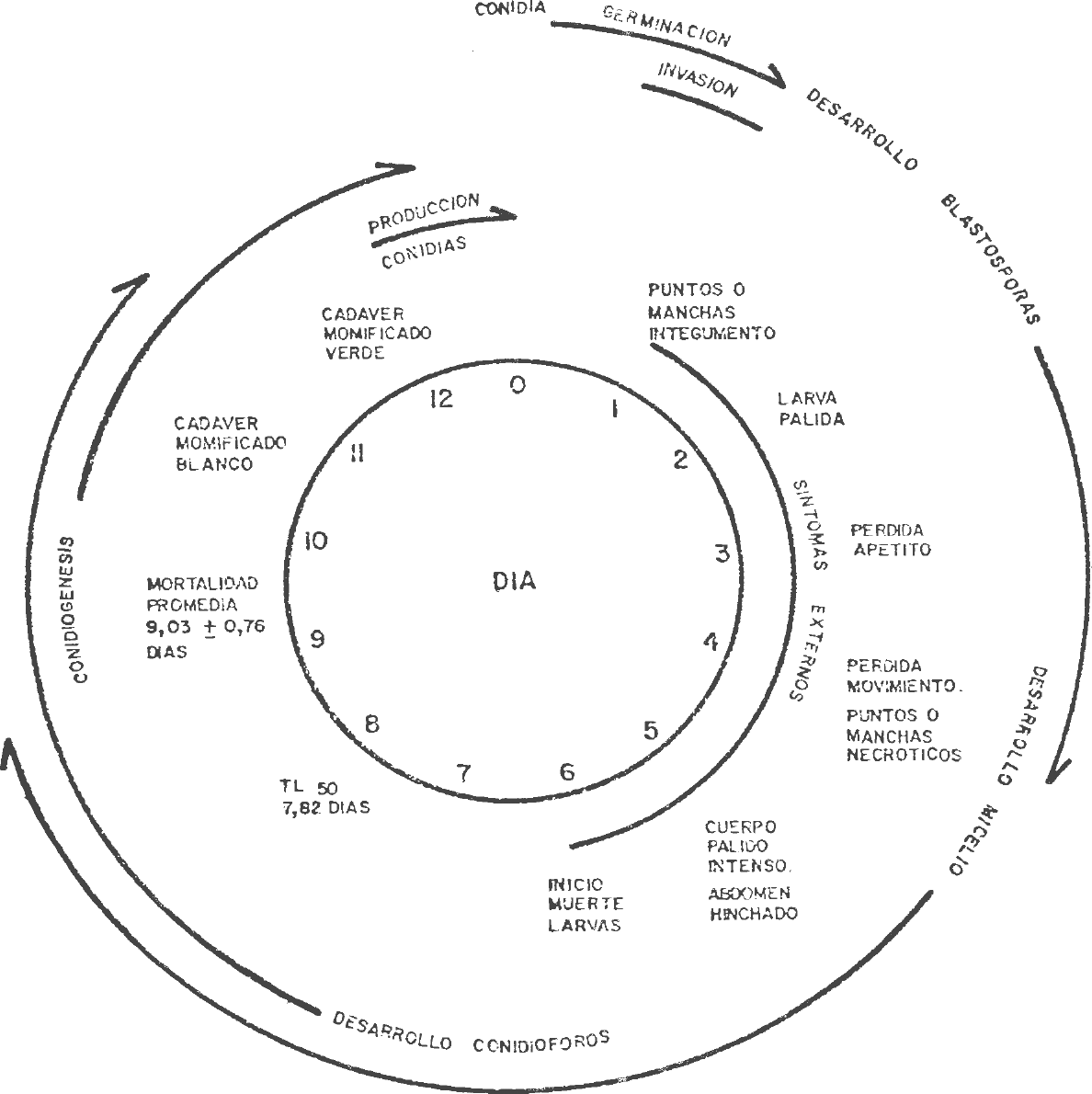
Ciclo biológico y sintomalogía del hongo Nomuraea rileyi en larvas de tercer instar de Spodoptera frugiperda.
DURACION DE LAS ETAPAS DE DESARROLLO DE N. rileyi SOBRE LARVAS DE TERCER INSTAR DE S. frugiperda INOCULADAS CON TRES CONCENTRACIONES DE CONIDIAS DURACION PROMEDIA EN DIAS
Número de individuos observados.
Intervalo de confianza:
La mortalidad causada por N. rileyi en los diversos tratamientos presentó una distribución diferente (Figura 4). Las larvas de S. frugiperda utilizadas al momento de la inoculación tenían 12 días de edad (tercer instar). Con la concentración de 3,1 conidias/mmβ la mortalidad se inició a partir del quinto día y se prolongó hasta el día 24.
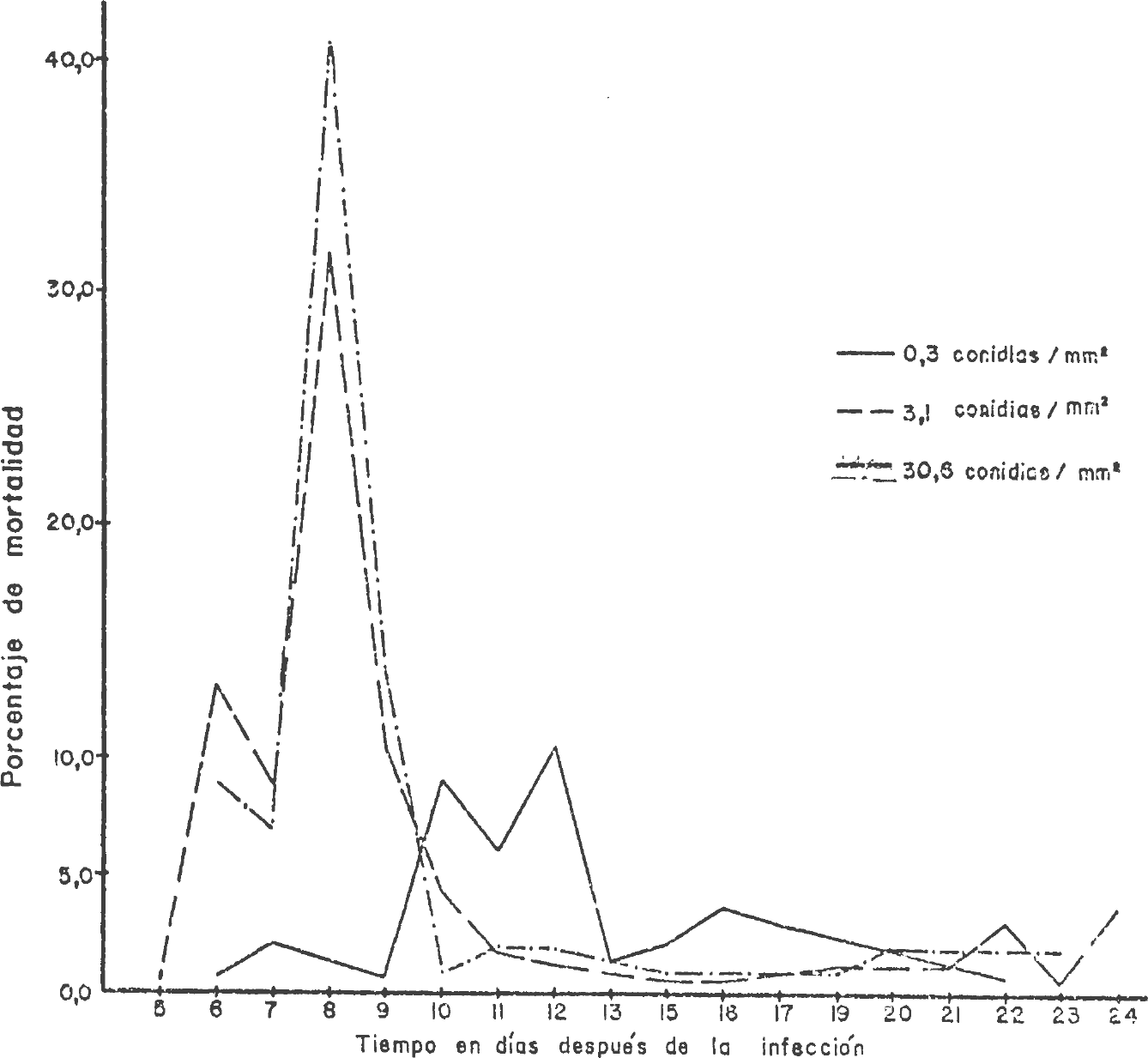
Mortalidad diaria en porcentaje de larvas de Spodoptera frugiperda de tercer instar expuestas a tres concentraciones de conidias de Nomuraraea rileyi.
Para las concentraciones de 0,3 y 30,6 conidias/mmβ empezó a partir del sexto y se extendió hasta los días 22 y 23, respectivamente. Comparando estos resultados con los 24 días en promedio que duró hasta el estado de larva en el testigo, se encontró que en los tratamientos de 0,3; 3,1 у 30,6 conidias/mmβ se presentó una prolongación en la duración del estado larval de 11,36%; 11,25% y 7,0% respectivamente. Esta prolongaciór probablemente se debe a la facultad que tienen las toxinas producidas po” N. rileyi en el proceso de infección, de retardar la metamorfosis cuando no causan la muerte rápida de las larvas (Ignoffo, 1981). La mortalidad diaria más alta se obtuvo en el octavo día con las concentraciones de 3,1 y 30,6 conidias/mmβ; mientras que con la concentración de 0,3 conidias/mmβ se obtuvo al día 12 después de la exposición de las larvas al inóculo (Figura 4).
La Tabla 3 presenta la mortalidad de S. frugiperda de tercer instar por N. rileyi. La mortalidad mayor se obtuvo con el tratamiento de 3,1 conidias/mmβ (83.75%) sequido por el de 30,6 conidias/mmβ (83,0%) y la menor con 0,3 conidias/mmβ (40.90%). Estos resultados demuestran que la patogenicidad de N.rileyi fue mayor a las concentraciones altas y que las larvas de S. frugiperda de tercer instar son muy susceptibles al hongo. Boucias et al. (1982) obtuvieron con una cepa virulenta 82.0% de mortalidad en larvas de S. frugiperda de segundo instar expuestas a una concentración alta (7.500 conidias/mmβ). Sin embargo, ellos expusieron las larvas al inóculo en dietas artificiales, lo cual implica que se requiera concentraciones más altas debido a las sustancias antimicrobiales que se adicionan a estas dietas (García e Ignoffo, 1978).
MORTALIDAD EN LARVAS DE Spodoptera frugiperda DE TERCER INSTAR EXPUESTAS A DIFERENTES CONCENTRACIONES DE N. rileyi
Los promedios seguidos por la misma letra no son significativamente diferentes de acuerdo a la nueva prueba de los rangos múltiples de Duncan (P <0,01).
El tiempo letal medio (TLso) y la concentración letal media (CL50) de los tratamientos se obtuvieron mediante extrapolación en las figuras 5 y 6. El tiempo letal medio (TL50), o sea el tiempo en el que murió la mitad de la población de las larvas de S. frugiperda para las concentraciones de 3,1 y 30,6 conidias/mmβ fue casi igual (7,86 y 7,82 días respectivamente). Para la concentración de 0,3 conidias/mmβ no se calculó debido a que la mortalidad fue inferior al 50,0%. La concentración letal media (CL50) para las larvas de S. frugiperda se estableció en 0,87 conidias/mmβ. Esta CL 50 se considera baja si se compara con resultados obtenidos por otros autores que han utilizado diferentes cepas, huéspedes y condiciones de cría (Ignoffo et al., 1976c; Puttler et al., 1978). Los resultados en general de este estudio indican que la cepa NRB1 de N. rileyi aislada en Bello es altamente virulenta y promisoria para el control microbiológico de S. frugiperda y probablemente de otras especies susceptibles.
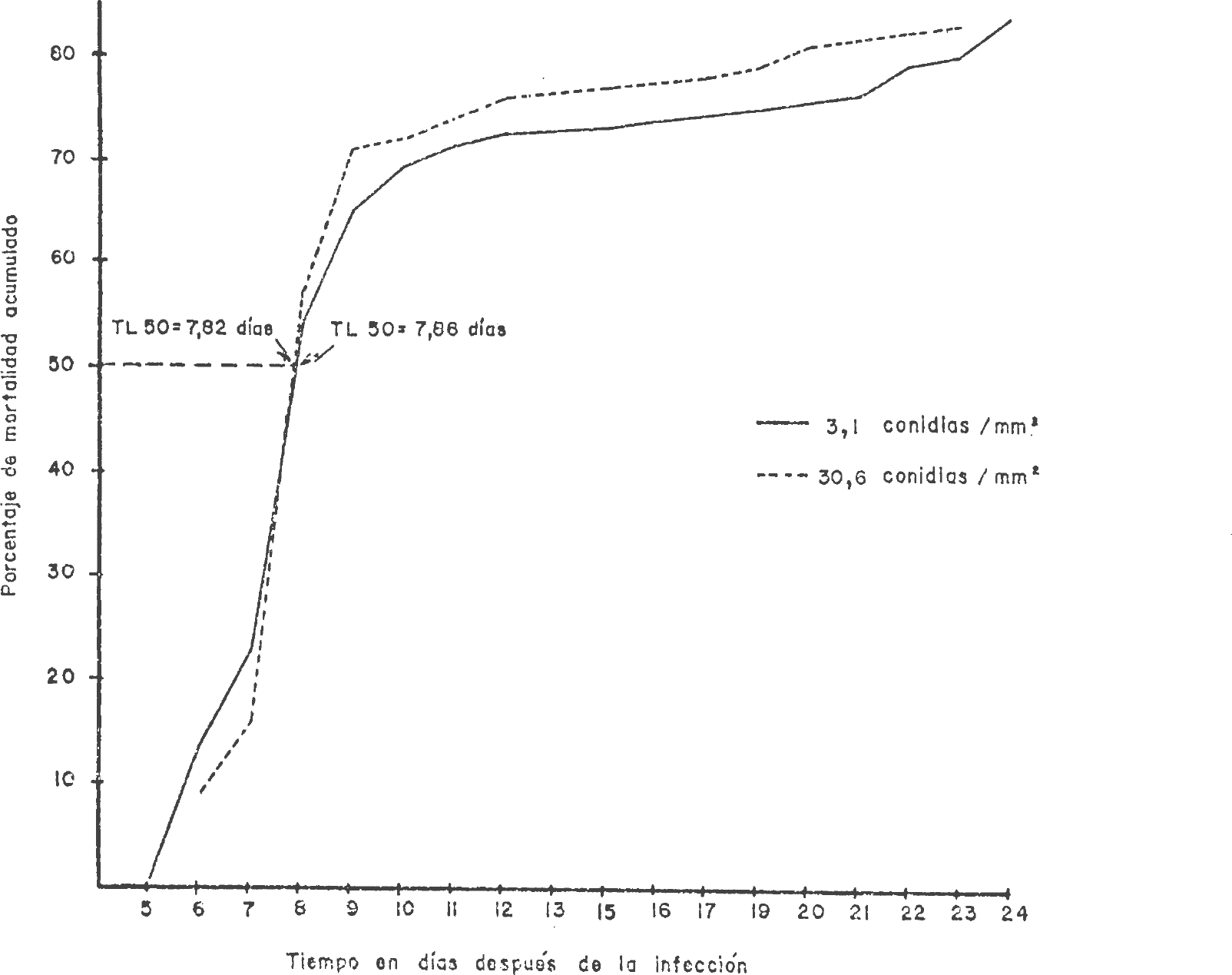
Tiempo letal medio (TL50) en larvas de tercer instar de Spodoptera frugiperda estimado para dos concentraciones de Nomuraraea rileyi.
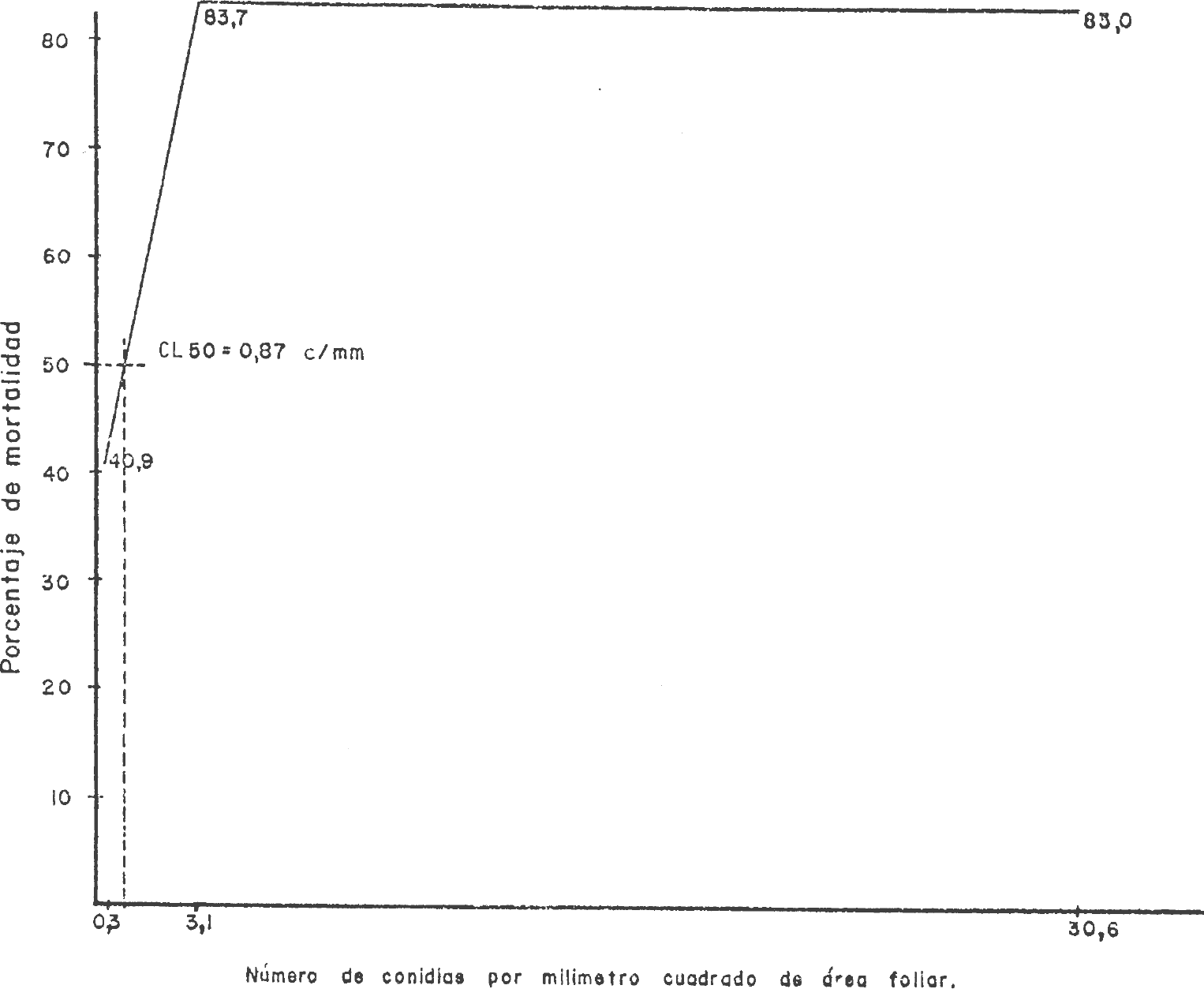
Determinación de la concentración letal media (CL50) de Nomuraea rileyi en larvas de tercer instar de Spodoptera frugiperda.
Footnotes
Agradecimientos
Los autores agradecen a la Señorita Amantina Osorio por el trabajo de mecanografía y al Señor Gabriel Franco por su ayuda en el mantenimiento de las colonias del insecto.
