Abstract
En cultivos de algodonero del Sinú, de 80 días de edad, se presentó durante la cosecha 83-84 una malformación de botones y "capullos" que al ocasionar la caída de las estructuras del tercio superior pudo reducir la producción hasta en 700 Kg./ha, según estimativos preliminares. En muchos casos, la malformación estuvo seguida por una pudrición bacterial producida por Pseudomonas sin tener aún claridad sobre la relación patógeno-insecto. La especie responsable de estos daños Contarinia gossypii (Diptera: Cecidomyíidae) tiene larvas rosáceas, de 2 mm. de longitud cuando maduras, las cuales se alimentan internamente de pétalos y androceo, pudiéndose encontrar hasta 185 de ellas por botón de 6 mm. de diámetro. Las larvas abandonan las estructuras atacadas mediante un salto característico para empupar en el suelo. Las pupas son obtectas, oscuras, de 1,2 mm de largo y protegidas por un cocon sedoso el cual se encuentra a poca profundidad de la superficie del suelo. Los adultos son típicos cecidomy íidos de antenas y patas muy largas, recubiertos de pilosidad oscura y densa que les da un aspecto de diminutas mosquitas grisáceas; miden aproximadamente de 1 a 2 mm. de longitud. Observaciones de laboratorio indican que la emergencia ocurre en las últimas horas de la tarde. Como enemigo natural se ha encontrado un parásito de larvas de la familia Platygasteridae, cuyos puparios también se encuentran en el suelo. Fuera del algodonero no se ha encontrado otra planta hospedante. Los registros de C. gossípii en Cereté, Montería, San Carlos, San Pelayo, Ciénaga de Oro y Lorica señalan su amplia distribución en el Departamento de Córdoba.
Introduction
A finales de Octubre de 1983 se reci- bió en Sanidad Vegetal de Turipaná una consulta sobre un nuevo y raro disturbio que estaba afectando la ma- yoría de los botones y "capullos" del tercio superior de las plantas de algo- dón llegando a ocasionar pérdidas en algunos lotes hasta de 700 Kg/ha. Los botones y "capullos" afectados pre- sentaban ciertas protuberancias o mal- formaciones, seguidas por necrosis y caída de las estructuras atacadas.
Las primeras hipótesis sobre las causas de este disturbio recayeron sobre patógenos o aspectos relacionados con la fisiología de la planta, semilla, suelo y humedad. A raíz de comparaciones de los lotes afectados, sin aplicaciones de insecticidas hasta los 80 días por ha- berse manejado con principios de Con- trol Integrado, con lotes vecinos libres de problema y con aplicaciones para el control de picudo desde los 60 días, se formuló la contrahipótesis de que en el problema debía estar involucrado un insecto. Esta última hipótesis se re- forzó al observar la persistencia de los síntomas en plantas localizadas al- rededor de los árboles y donde los in- secticidas no llegaban e igualmente en lotes sin aplicaciones y se confirmó a principios de Enero del 84 cuando se encontraron dentro de las estructuras recién afectadas larvas de un díptero de la familia Cecidomyíidae, identi- ficado en el Laboratorio de Entomolo- gía Sistemática del Departamento de Agricultura de los Estados Unidos como Contarinia gossypii Felt. Dado que ni esta especie ni sus daños habían sido registrados en Colombia, este tra- bajo presenta las observaciones preli- minares realizadas durante el período de soca, de Enero a Abril del 84, en el Laboratorio de Sanidad Vegetal en el ICA Turipaná (Cereté-Colombia) como un aporte a su manejo, con el fin de re- ducir la amenaza de la plaga en los planes de control integrado.
Revision de Literatura
En cuanto al daño, existe un olor ca- racterístico en los botones y "capu- llos" muy infestados. Las partes inter- nas de las estructuras florales se oscu- recen y pudren llegando a ser acuosas. En las cápsulas atacadas la fibra se de- colora, y las cápsulas en sí se ablandan y las semillas finalmente se arrugan (Barnes, 1949).
En la zona bajo estudio se han encon'- trado infestaciones del cecidomyíido en plantas que pasan los 80 días de edad.
Felt (citado por Barnes, 1949) descri- bió por primera vez ambos sexos de la especie como típicos
Según la cita de Barnes (1949) Ballow estableció que los estados de huevo y larva duraban 12 a 14 días, el estado pupal de 10 a 14 y los adultos vivían 2 a 3 días. Reinwater (citado por Barnes, 1949) registró hasta más de 100 larvas en cápsulas de algodones silvestres, en éstas, las hembras "pican" con el ovipositor la superficie para colocar en su interior los huevos. Esta forma de oviposición no es usual ya que
Ballou (Citado por Barnes, 1949) esta- bleció que un pteromálido del género
Las medidas de control, según Ballou, fueron: prácticas culturales como siembra temprana, lo cual permitía la formación de cápsulas antes de la ovi- posición del Cecidomyíido; mantener la superficie del suelo bien pulverizada, seca y libre de malezas; destrucción de algodón silvestre; recolección de es- tructuras afectadas y así como el uso de un fumigante. Finalmente, Callan (citado por Barnes, 1949) señala que el tiempo húmedo con suelos enchar- cables favorecen el empupamiento mientras que el tiempo seco con con- diciones de suelos secos lo impiden.
Materiales Y Metodos
Las observaciones de los diferentes es- tados de la plaga se hicieron en el La- boratorio de Diagnóstico de Sanidad Vegetal "Turipaná" en Cereté (Córdo- ba), durante los meses de Enero a Marzo de 1984 y bajo condiciones na- turales.
Por no encontrar el estado de pupa dentro de las estructuras afectadas, se ensayó como posibles medios de empu- pamiento arena seca, húmeda y satu- rada. Las larvas maduras, que se reco- nocían por el color y por la tenden- cia a saltar, se colocaban con la ayuda de un pincel (1-2 días después de emergidas) en platos de Petri que con- tenían el medio de empupamiento.
Otra metodología usada para la obten- ción de pupas consistió en colocar te- rrones pequeños y húmedos recogidos del mismo campo de donde provenían las larvas y dentro de las bolsas plásti- cas que contenían los botones afecta- dos.
También se ensayó suelo cernido, es- terilizado y húmedo, tapando el frasco de cría con papel filtro o toalla para impedir el escape de las larvas.
Para buscar las posturas se tomaron botones pequeños y medianos sin sín- tomas de malformación y en ellos se hizo una búsqueda cuidadosa al este- reoscopio entre los pétalos y alrededor de los estambres.
La descripción de las larvas, pupas y adultos, se hizo bajo un estereoscopio y para facilitar los dibujos, los diferentes estados se montaron en placas, siguien- do la técnica de montaje utilizada para microhymenópteros,
Resultados
Las larvas medianas aún pueden encon- trarse entre los pétalos, agrupadas en cantidades altas, de tal modo que las protuberancias externas de los pétalos en los botones y "capullos" jóvenes parecen corresponder al sitio de ali- mentación y es precisamente allí don- de se inicia el necrosamiento externo.
Las larvas de
Parece que lo normal es que dentro de una estructura floral todas las larvas son de edad uniforme, de ahí, que cuando maduran todas abandonan el sitio para empupar sin dejar huellas de su presencia. En el período de soca la presión de altas poblaciones del in- secto sobre un bajo número disponible de estructuras florales permiten encon- trar en botones con gran deterioro, larvas de varios tamaños, lo cual no es lo usual durante la cosecha cuando el número de botones es mayor.
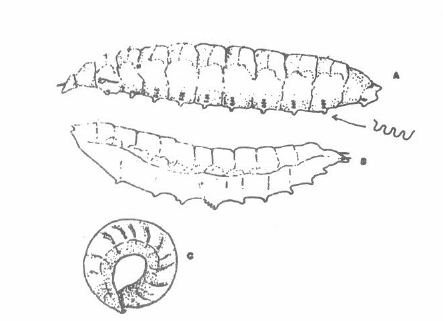
FIS. I LARVAS MADURAS DE
Las larvas expuestas a medios de em- pupamiento (arena, suelo cernido, te- rrones, etc.) muy saturados de hume- dad no empupan y gradualmente van perdiendo su tonalidad amarillenta, ad- quieren un aspecto transparente, con- servan su hábito gregario; también se encontraron agrupadas alrededor de las gotas de agua en las bolsas plásticas donde duraron vivas 15 días. Las larvas están asociadas con unos nemátodos hialinos que no parecen afectarlas. Cuando las larvas quedan en medio seco, sobreviven muy pocos días y mueren deshidratadas.
Aunque las larvas medianas también saltan, esta tendencia es extraordina- riamente marcada en las larvas madu- ras, las cuales presentan un geotropis- mo muy fuerte. Esto explica el hecho de que existiendo millones de larvas en un lote densamente infestado, no se encuentra una sola sobre el follaje.
Para saltar, las larvas arquean comple- tamente el cuerpo, apoyando el extre- mo caudal contra la parte ventral del protorax (Fig. 1C) e impulsándose co- mo un resorte, saltan de nuevo tạn pronto caen sobre una superficie dife- rente al suelo. Estos saltos, que pueden ser de 12-15 cms de longitud, les per- miten escapar desde el fondo de reci- pientes medianos o de las bolsas plás- ticas.
Cuando las larvas alcanzan su comple- to desarrollo, abandonan la estructura sin dejar huellas de su salida, saltando por encima del cáliz. Esta salida del botón se efectúa en las horas de la noche.
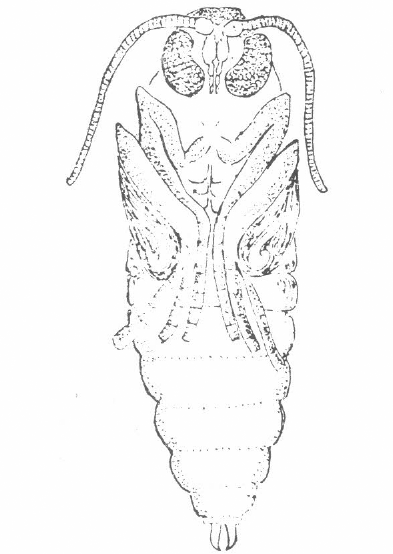
PUPA DE
De las pupas maduras extraídas del cocón no emergieron los adultos. La duración entre el momento de colocar las larvas maduras en el medio del em- pupamiento y la emergencia de adultos fue de 7 días bajo las condiciones na- turales del laboratorio
La longitud del cuerpo es de aproxima- damente 2 mm para las hembras y un poco más de 1 mm para los machos, con patas y antenas largas.
Los adultos a simple vista parecen di- minutas mosquitas grisáceas, tonalidad dada por la alta pilosidad oscura que recubre el cuerpo, el cual es incoloro; resaltan los ojos negros, compuestos, que ocupan más del 800/0 de la ca- beza.
Existe un dimorfismo sexual que per- mite reconocer los machos por la ma- yor longitud de sus antenas, las cuales poseen 24 segmentos en el flagelo y 2 basales, son moniliformes y presentan haces de setas largas que parecen tripli- car el grosor dándole la apariencia plu- mosa; los machos vivos tienden a en- roscar las antenas (Fig. 3A). Las hem- bras poseen antenas más cortas, filifor- mes, de 12 segmentos en el flagelo y los 2 basales (Fig. 3B).
Las alas típicas del género son basal- mente estrechas y llevan manchas en bandas de color gris, formadas por la pilosidad oscura en la cara superior. Entre el ángulo humeral y el borde api- cal del ala se observan flecos cortos, mientras que en el margen anal estos son bastante largos, recién emergidos los adultos.
El tórax tiene varias setas largas en la unión con la cabeza. El abdomen en los machos es de 9 segmentos y en las hembras es de 8 aparentemente y están cubiertos de abundante pilosidad oscu- ra en los bordes de cada uno de ellos, siendo mayor en el margen dorsoven- tral y especialmente a la salida del ovis- capto, el cual es cónico, y envuelve un ovipositor sumamente largo de aspecto capilar y que termina algo recurvado (Fig. 3B). Esta pilosidad se pierde en los especímenes conservados en alco- hol o en seco.
La relación de sexo fue de 1,3: 1 a favor de las hembras, para las observa- ciones hechas entre Marzo-Abril, mien- tras que en las últimas (Julio) los ma- chos eran más bien escasos.
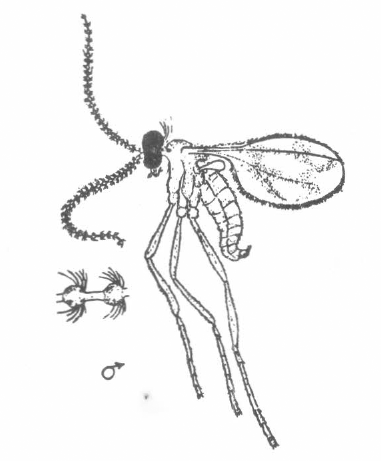
MACHO DE
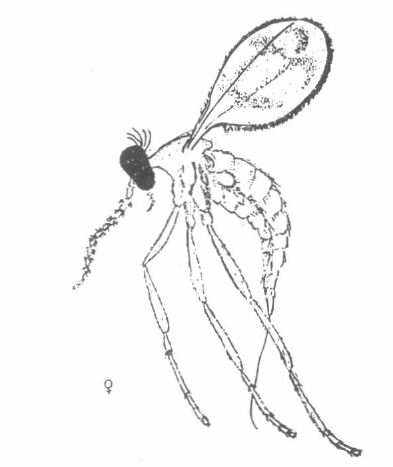
HEMBRA DE
Descripción de síntomas del daño:
Las observaciones sobre botones y "ca- pullos" sanos marcados en el campo permitieron un seguimiento del desa- rrollo gradual de la sintomatología externa.
Antes del 50. día los botones sanos marcados muestran la malformación (Fig. 4A-E), la cual comienza por un ligero cambio del perfil normal, pre- sentándose protuberancias en la base de los pétalos o en forma irregular (Fig. 4B). Los "capullos" más jóvenes (Fig. 4F-J) adquieren el aspecto de "capullos" florales de papaya (Fig. 4G). Luego los botones deformes, los cuales conservan las brácteas en posi- ción y el color normal, exhiben un ligero cambio de color y necrosamien- to de la base de los pétalos despegán- dose del cáliz, (Fig. 4D, 41, 4J), este paso puede durar 5 días y de 4 a 5 días más tarde los botones caen. La pudri- ción en estos botones puede ser a veces seca o húmeda. A veces el cáliz de los botones presenta en su base un anillo violáceo irregular. Los "capullos" afec- tados no abren como flor caracterizán- dose por un aspecto de tornillo o péta- los arrugados (Fig. 4L-M) y una colo- ración rojiza en el extremo apical, dando señales de polinización, lo cual se confirmó por el desarrollo de cápsu- las que conservaban restos de pétalos con las corrugaciones típicas (Fig. 4M). Sin embargo, los pocos "capu- llos" florales afectados y marcados en el campo no llegaron a abrir por ata- ques del gusano Rosado Colombiano (
Por la sintomatología externa, el as- pecto de un campo a los 100 días con ataques iniciales desde los 80 días, es el de una masa de follaje verde con au- sencia, o un mínimo, de flores abiertas amarillas o rojas; el tercio superior pre- senta una carga aparentemente normal de botones que al abrir sus brácteas revelan la malformación y pudrición de os pétalos; también se puede obser- var el desarrollo de cápsulas medianas y grandes con los restos de pétalos necrosados. Al final del ataque, alrede- dor de las plantas se encuentran boto- nes caidos indicando un alto derrame. Los campos más afectados pueden per- der completamente la carga media y superior.
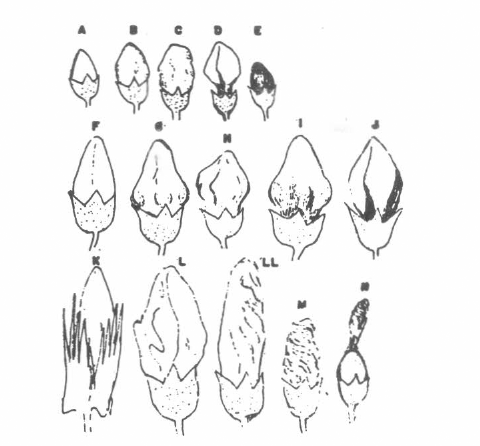
SECUENCIA DEL DESARROLLO DE LOS SINTOMAS EXTERNOS DEL DAÑO DE
Al inicio de las malformaciones y re- cién abandonado el botón por las lar- vas, se aprecia un ligero cambio de color de la masa de anteras pasando de crema a algo grisáceo y se observa pér- dida de turgencia; luego las anteras ba- sales toman un color pardo-amarillento y cuando el necrosamiento es evidente, la consistencia es gelatinosa; la masa de anteras se vuelve más oscura; el conec- tivo, tejido que une a los dos lóbulos de la antera, se vuelve negro y la necro- sis estilar es total; los pétalos en su cara interna también se necrosan, se vuelven acuosos y con un olor caracte- rístico de bacteria pero no muy repelente.
En el estereoscopio, desde el inicio de los sintomas se observan unas lesiones tenues no continuas que se localizan a lo largo del filamento de las anteras basales. Igualmente se aprecian lesio- nes como minaduras a lo largo del esti- lo, que van desde la cercanía del estig- ma hasta el tejido que bordea el ova- rio, donde las lesiones son hundidas, pero sin interesar este órgano en nin- guno de los casos observados. La cara interna de los pétalos presenta corruga- ciones y cambio de color a pardo, ini- ciándose la pudrición en la parte basal y continuando hacia arriba (Fig. 5).
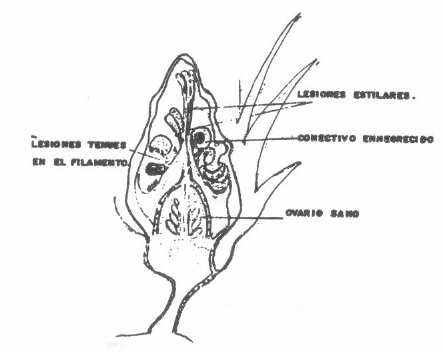
SINTOMAS INTERNOS EN BOTON FLORAL. CORTE LONGITUDINAL.
Por comunicación personal de Asis- tentes Técnicos se conoce que esta sintomatología se ha observado, sin importancia económica, en la Dorada (Caldas), Armero (Tolima) y en el De- partamento de Sucre.
Conclusiones
El registro de
Por sus hábitos y biología y por su aso- ciación con la bacteria
Es necesario establecer el ciclo de vida del insecto, determinar el umbral de daño económico, evaluar productos para su manejo, y definir un método para evaluar la eficiencia de aplicacio- nes de insecticidas.
La presencia de
Finalmente, por ser un insecto que persiste en la soca del algodon, único hospedante conocido, se refuerza la necesidad de destrucción de ésta.
