Abstract
The European Medicines Agency (EMA) has adopted assessment systems and drug registration procedures to respond to the needs for rapid patient access to therapies, such as Conditional Marketing Approval (CMA) and Under Exceptional Circumstances approval (UEC). The Italian Medicine Agency (AIFA) has introduced tools for governing prescriptive behaviour in order to promote appropriateness and correct use of drugs and to manage the uncertainty of financial impact, including Managed Entry Agreements (MEAs). The MEAs are conditional access agreements to the market for new drugs aimed at managing the uncertainty on the clinical and economic effects of the drugs themselves. The aim of this study is to analyse, through the use of the information systems of the AIFA and the institutional website of the EMA, how the drugs authorised by EMA with CMA or UEC have been managed on the access side to the Italian NHS. This in order to understand how the uncertainty deriving from the authorisation processes was subsequently reflected on the reimbursement processes to be borne by the NHS. From the analyses carried out, it emerges that 64% of the drugs approved with CMA were admitted to reimbursement and 68% of those approved with the UEC procedure. Furthermore, it can be noted that approval with CMA is predictive for the application of a financial-based or outcome-based MEA (61%), with the application of a monitoring register, unlike the drugs approved UEC for which no conditional reimbursement arrangements have been applied at the patient level. Furthermore, by carrying out a comparative analysis of the time of access to market following negotiation, from the positive opinion of the CHMP to the decision published in the Official Gazette of the Italian Republic, it emerged that the drugs approved by the UEC procedure take on average more time (897 days) to arrive at the price and reimbursement (P&R) compared to CMA drugs (636 days). Considering instead only the period from the request for P&R to the determination of P&R for the same group of drugs, the process seems to be on average faster for the drugs classified as UEC than for those with CMA (329 vs. 510 days).
Keywords
Introduzione
Il Regolamento CE n° 726/2004 (1), nell’ambito della revisione della normativa farmaceutica europea, relativamente all’accesso precoce da parte dei pazienti per esigenze di tutela della salute, afferma che “al fine di soddisfare … le legittime aspettative dei pazienti e per tener conto del progresso sempre più rapido della scienza e delle terapie, dovrebbero essere istituite procedure di valutazione accelerate, riservate ai medicinali di maggiore interesse terapeutico e procedure per ottenere autorizzazioni temporanee soggette a condizioni annualmente verificabili”.
In attuazione delle disposizioni del regolamento n° 726/2004, l’Agenzia Europea del Farmaco (European Medicine Agency - EMA) ha pertanto adottato nel tempo diversi strumenti per poter rispondere alle esigenze di accesso precoce alle terapie farmacologiche da parte dei pazienti, attraverso un più diffuso ricorso a procedure di autorizzazione, quali il
Il Conditional Marketing Approval (approvazione condizionata - CMA) è un’Autorizzazione all’Immissione in Commercio (AIC) subordinata alla presentazione di ulteriori dati a supporto e consolidamento delle evidenze di efficacia e sicurezza, derivanti sia da studi ancora in corso al momento dell’autorizzazione per acquisire i risultati finali su ulteriori endpoint, sia l’avvio di studi ex novo (specific obbligations - SOs). L’autorizzazione condizionata è valida per un anno, in seguito rinnovabile annualmente e, successivamente alla presentazione dei dati richiesti, può essere convertita in standard marketing authorisation inizialmente valida 5 anni poi rinnovabile con validità illimitata. I farmaci per uso umano, per poter avere un’approvazione condizionata dall’EMA devono essere: farmaci orfani, farmaci da utilizzare in situazioni di emergenza, oppure utilizzati allo scopo di trattare, prevenire o diagnosticare patologie seriamente debilitanti o che mettono in pericolo la vita.
La AIC Under Exceptional Circumstances (approvazione in circostanze eccezionali - UEC) viene concessa in assenza di dati completi a supporto del rapporto beneficio/rischio che, tuttavia, non è possibile ottenere nemmeno dopo l’autorizzazione a causa delle caratteristiche specifiche della malattia in cui sono indicati (e.g., la rarità della malattia). Tale AIC ha validità per 5 anni, eventualmente rinnovabile, ma il rapporto beneficio/rischio è rivalutato annualmente dal CHMP (Committee for Medical Products for Human Use) dell’EMA. Questo tipo di autorizzazione non viene generalmente convertita in un’autorizzazione standard.
Questo tipo di autorizzazioni vengono utilizzate allo scopo di promuovere un rapido accesso al farmaco da parte dei pazienti esclusivamente per quei prodotti per i quali il CHMP ha ritenuto che il beneficio conseguente alla disponibilità immediata sul mercato superi il rischio derivante dalla parziale mancanza di dati richiesti; e venendo incontro alle esigenze terapeutiche non soddisfatte l’approvazione in circostanze eccezionali può essere concessa solo per ragioni oggettive e verificabili e deve basarsi su un presupposto che il richiedente non sia in grado di fornire dati completi sull’efficacia e la sicurezza in normali condizioni di utilizzo (3).
Dopo l’autorizzazione con procedure accelerate a livello Europeo, seguono le procedure finalizzate all’accesso nei diversi stati. Con riferimento all’Italia, sono stati introdotti diversi strumenti normativi finalizzati ad accelerare l’accesso a carico del SSN da parte dei pazienti: rimborso per un uso off-label ai sensi della Legge n. 648/96 (4), dispensazione a singoli casi documentati con le risorse stanziate nell’ambito del fondo del 5% (Legge n. 326/2003) (5), che si aggiungono all’uso compassionevole (D.M. 8 maggio 2003) (6), recentemente aggiornato dal D.M. 7 settembre 2017 (7), già consentito dalla normativa comunitaria.
Indipendentemente se a carico del SSN o eventualmente dell’azienda farmaceutica (con l’uso compassionevole), l’accesso al farmaco è comunque possibile a fronte della sua commercializzazione prima della conclusione del percorso di negoziazione del prezzo e rimborso, sulla base della classificazione in C-NN (istituita dalla Legge n. 189/2012) (8): i farmaci già autorizzati e in attesa della valutazione ai fini della rimborsabilità da parte di AIFA, vengono inseriti in tale classe entro 60 giorni dalla data di pubblicazione della determina di autorizzazione all’immissione in commercio sulla Gazzetta Ufficiale dell’Unione Europea. Tale classificazione è possibile salvo il caso in cui l’azienda non faccia immediata domanda di prezzo e rimborso che a questo punto posticipa la commercializzazione del farmaco dopo la pubblicazione del relativo provvedimento in Gazzetta Ufficiale Italiana. In altri termini, la C-NN consentirebbe l’accessibilità al farmaco prima del percorso di definizione del prezzo e della rimborsabilità, di conseguenza il costo è a totale carico del cittadino (essendo di fascia C), oppure a carico dell’ospedale (ovvero a carico del SSN per esigenze specifiche di cura dei pazienti presi in carico e in assenza di alternative disponibili).
La legge n. 648 del 23 dicembre 1996 prevede la possibilità di dispensare farmaci a specifici gruppi di pazienti totalmente a carico del SSN, previo parere consultivo (vincolante) della Commissione Tecnico-Scientifica di AIFA (CTS), che deve accertare l’assenza di alternative terapeutiche valide, nel caso di: medicinali innovativi in commercio in altri Stati ma non sul territorio nazionale, medicinali non ancora autorizzati ma sottoposti a sperimentazione clinica, medicinali da impiegare per un’indicazione terapeutica diversa da quella autorizzata (off-label). Oppure, quando fosse disponibile un’ alternativa terapeutica valida, per medicinali da impiegare per un’indicazione terapeutica diversa da quella autorizzata purché tale indicazione sia nota e conforme a ricerche condotte nell’ambito della comunità medico-scientifica nazionale e internazionale, secondo parametri di economicità e appropriatezza (9).
Come ulteriore strumento di accesso precoce al mercato nazionale, in attesa della commercializzazione a seguito di negoziazione, la legge n. 326/2003 ha previsto un fondo alimentato dal 5% delle spese annualmente sostenute delle aziende farmaceutiche per le attività di promozione dirette ai medici (nel 2014 circa 15,6 milioni di euro, nel 2015 circa 17,8 milioni di euro e nel 2016 circa 17,5 milioni di euro). Tale fondo a norma di legge è ripartito per il 50% all’acquisto da parte delle strutture del SSN di farmaci orfani per malattie rare e farmaci non ancora autorizzati, ma che rappresentano una speranza di cura per patologie gravi e per il restante 50% al finanziamento di progetti di ricerca sull’uso dei farmaci. Nel primo caso, relativo all’accesso precoce ai farmaci, le istanze di acquisto con le risorse del fondo del 5% vengono inoltrate all’AIFA, tramite le Regioni, dai Centri di riferimento che hanno in cura i malati, o da strutture specialistiche individuate dalle Regioni, con la definizione della diagnosi e del piano terapeutico.
Con riferimento all’uso compassionevole, è stato disciplinato in Italia con D.M. 8 maggio 2003, successivamente aggiornato dal D.M. 7 settembre 2017, che consente l’uso terapeutico di medicinali non ancora autorizzati, sottoposti a sperimentazione clinica, medicinali provvisti di AIC per indicazione diversa rispetto a quella per cui si richiede l’utilizzo, medicinali autorizzati non ancora disponibili sul territorio nazionale, forniti a titolo gratuito da parte dell’azienda per il trattamento di malattie rare, di pazienti gravi, in pericolo di vita, oppure affetti da malattie per cui non esistano ulteriori valide opportunità terapeutiche.
La normativa italiana ha, inoltre, previsto un percorso accelerato di definizione del prezzo e della rimborsabilità ai sensi della legge n. 189/2012 che riguarda nello specifico i farmaci orfani, i farmaci di eccezionale rilevanza terapeutica e sociale (su valutazione da parte della CTS) e per i farmaci di uso esclusivo ospedaliero. Secondo tale normativa le istanze di rimborsabilità e prezzo (P&R) possono essere presentate anteriormente al rilascio dell’AIC valida in UE, ovvero subito dopo il rilascio del parere positivo del CHMP di EMA, e il termine di conclusione del procedimento è ridotto a 100 giorni.
L’Agenzia Italiana del Farmaco (AIFA) ha introdotto inoltre numerosi strumenti per la regolamentazione della rimborsabilità e dell’uso appropriato dei medicinali, finalizzati in alcuni casi a gestirne l’incertezza clinica ed economica conseguente all’accesso ad un medicinale (Managed Entry Agreements - MEAs) (10). In questo ambito è opportuno distinguere gli strumenti di regolamentazione dell’uso appropriato dei medicinali, da quelli di monitoraggio dell’uso. Nel primo caso, le cosiddette “note AIFA” rappresentano uno strumento regolatorio per indirizzare l’attività prescrittiva dei medici sulla base delle migliori prove di efficacia presenti in letteratura, escludendo le indicazioni d’uso non rimborsate dal SSN. Sempre nella prima categoria rientrano anche i Piani Terapeutici (PT), che hanno l’obiettivo di limitare l’uso rimborsato dal SSN a specifiche indicazioni e/o sottogruppi di pazienti compresi nell’ambito delle indicazioni registrate. Rientrano in questo ambito anche una tipologia di Registri di monitoraggio AIFA, sviluppata a partire dal 2005, che è finalizzata esclusivamente a certificare l’avvio al trattamento di specifiche categorie di pazienti/indicazioni, oltre a rilevare le modalità d’uso del medicinale e la durata del trattamento.
I registri di monitoraggio AIFA sono stati lo strumento attraverso cui sviluppare alcuni tipi di MEAs, finalizzati a gestire l’incertezza rispetto agli effetti clinici ed economici conseguenti all’uso in pratica clinica di medicinali di recente autorizzazione. Al riguardo, si differenziano in MEA di tipo finanziario (financial-based MEA, patient-level) quali sconti sul costo dei primi cicli di terapia per tutti i pazienti eleggibili al trattamento (modello di cost-sharing), oppure MEA dipendenti dall’esito clinico (outcome-based MEA). I modelli di accesso outcome-based possono assumere la forma del Payment-By-Result (il costo del trattamento che ha avuto esito in un fallimento terapeutico è interamente a carico dell’azienda farmaceutica titolare del medicinale in questione) e Risk Sharing (ovvero un Payment-By-Result in cui viene restituita una percentuale inferiore al 100% del valore del fallimento terapeutico). Esistono inoltre altri accordi di tipo finanziario che non poggiano sui registri di monitoraggio AIFA (population-level) come: la scontistica confidenziale per la vendita alle strutture del SSN, gli accordi prezzo-volume e i tetti massimi di spesa (11).
Obiettivo del presente studio è analizzare come i farmaci autorizzati da EMA con approvazione condizionata (CMA), a partire dal primo utilizzo di questo strumento nel luglio 2006, o in circostanze eccezionali (UEC) siano stati gestiti sul versante dell’accesso al SSN. Ciò al fine di comprendere come l’incertezza derivante dai processi di autorizzazione si sia riflessa successivamente sui processi di rimborsabilità a carico del SSN (i), attraverso uno specifico ricorso a MEA basati su registri di monitoraggio AIFA (ii) e, infine, come ha inciso sulla tempistica complessiva delle procedure di negoziazione del prezzo e della rimborsabilità a carico del SSN.
In particolare, si desidera verificare con quale frequenza e con quale modalità è stata raggiunta la rimborsabilità nei due gruppi di farmaci analizzati e verificare se ci può essere una tempistica di market access differente nei medicinali autorizzati tramite CMA, rispetto a quelli autorizzati tramite UEC (Figure 1 e 2).
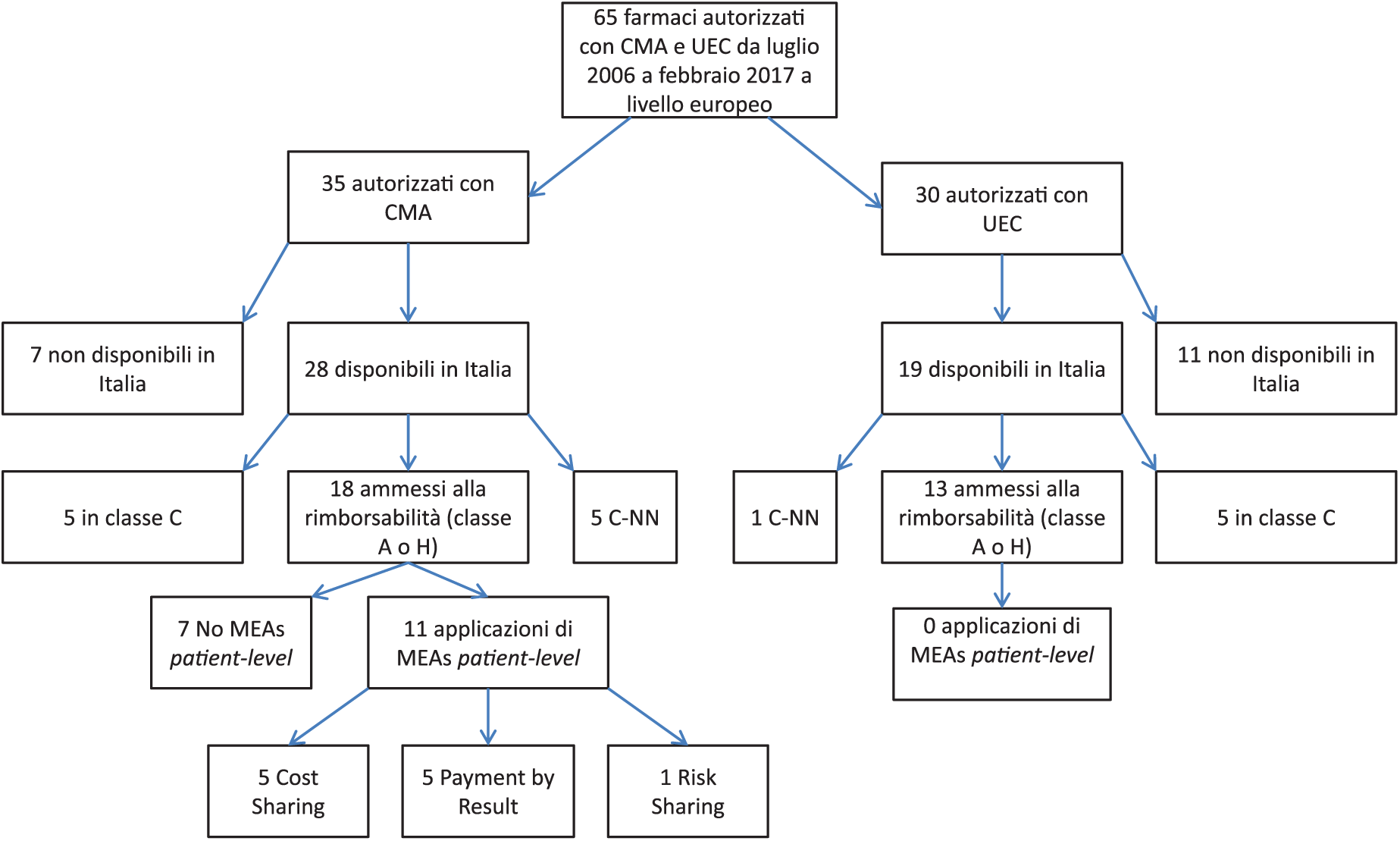
Diagramma di flusso del processo di market access dei medicinali autorizzati da EMA con Conditional Marketing Authorization (CMA) o Under Exceptional Circumstances (UEC), nel periodo compreso tra luglio 2006 e febbraio 2017.
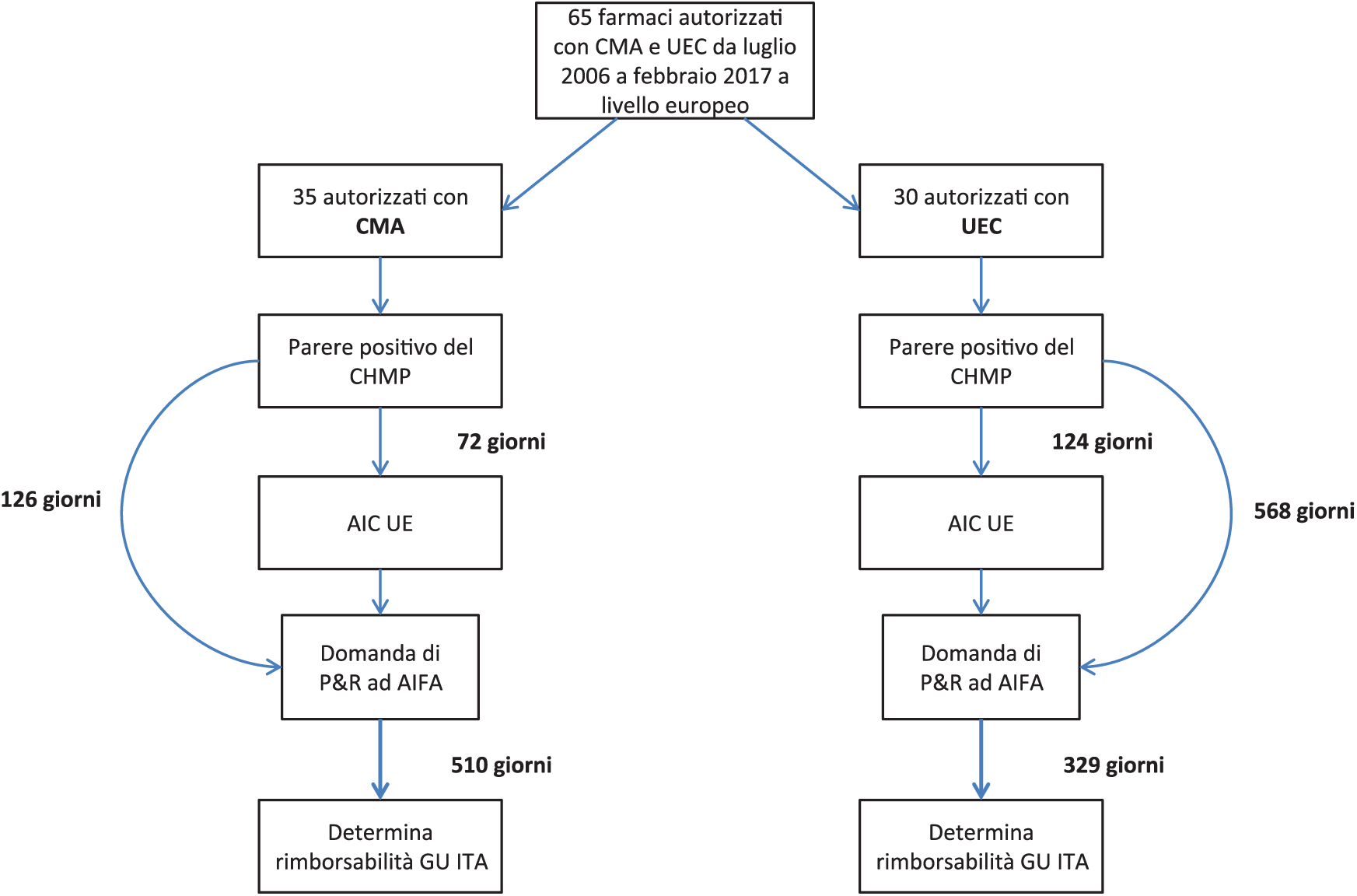
Diagramma di flusso rappresentante le tempistiche relative ai diversi step di market access per i medicinali autorizzati dall’EMA con Conditional Marketing Authorization (CMA) o Under Exceptional Circumstances (UEC), nel periodo compreso tra luglio 2006 e febbraio 2017.
Metodi
In primo luogo, sono state individuate attraverso il sito istituzionale dell’EMA (12) le procedure di autorizzazione di CMA e UEC effettuate da luglio 2006 a marzo 2017. In particolare sono stati considerati: gli elementi base per la concessione della CMA, eventuale conversione in standard marketing authorisation e relative tempistiche, area terapeutica di riferimento dei prodotti oggetto di ricerca. La GU (13) e la documentazione AIFA (14) sono invece alla base delle informazioni sulla commercializzazione dei prodotti nel nostro Paese e sulla loro classificazione e relativi eventuali accordi negoziali: classe di rimborsabilità del farmaco, regime di dispensazione, applicazione di eventuali MEAs.
È stato successivamente effettuato un test di confronto tra proporzioni per valutare se il numero di farmaci rimborsati tra quelli approvati con CMA è maggiore rispetto a quelli autorizzati UEC (Tabella 1).
Farmaci disponibili in Italia raggruppati per modalità di approvazione e rimborsabilità.

Con riferimento ai tempi del processo di definizione del prezzo e della rimborsabilità, è stata rilevata la data del Positive Opinion del CHMP (15) e di autorizzazione al commercio valida nell’UE (data di pubblicazione della determina in Gazzetta Europea), la data di sottomissione del dossier di prezzo e rimborso (P&R) da parte dell’azienda titolare dell’AIC all’AIFA, la data dell’eventuale determina di classificazione in C-NN pubblicata nella GU Italiana (disponibile solo per i farmaci approvati post decreto legge n. 158 del 13 settembre 2012), la data dell’eventuale inserimento nelle liste previste dalla legge n. 648/96 ed infine la data della determina di classificazione e prezzo pubblicata in GU Italiana.
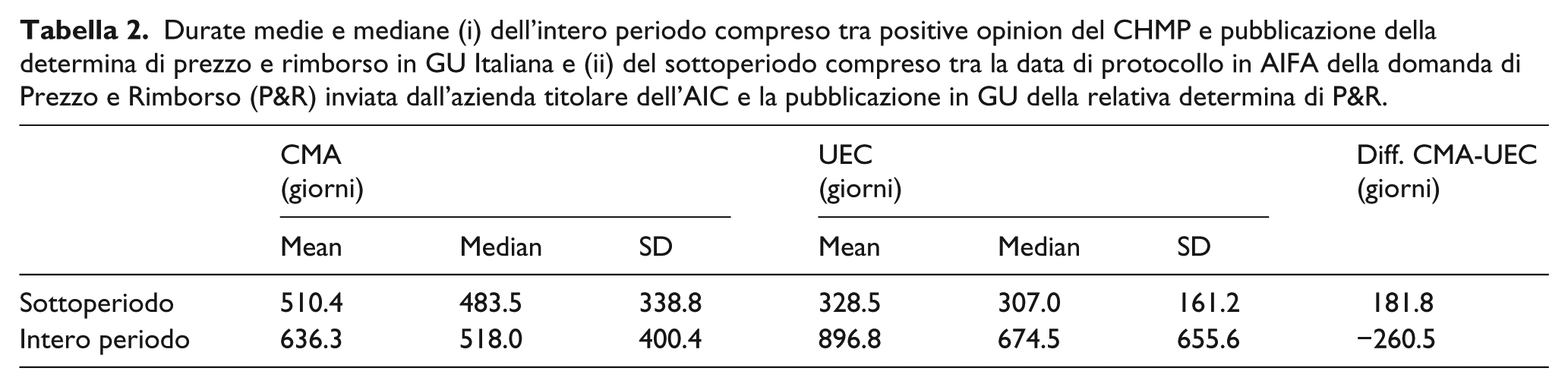
È stata quindi condotta un’analisi statistica per confrontare la durata di diverse fasi dell’intero processo che rende disponibile sul mercato nazionale un farmaco. In particolare, sono state testate eventuali differenze nei due gruppi di farmaci autorizzati con CMA e UEC, sia rispetto al periodo compreso tra la positive opinion del CHMP di EMA e la pubblicazione in GU della determina di prezzo e rimborso, sia rispetto al periodo relativo alla negoziazione nazionale compreso tra la data di sottomissione del dossier di prezzo e rimborso da parte dell’azienda all’AIFA (data di protocollo della domanda) e la data di pubblicazione della determina di prezzo e rimborso in GU Italiana (Tabella 2).
Durate medie e mediane (i) dell’intero periodo compreso tra positive opinion del CHMP e pubblicazione della determina di prezzo e rimborso in GU Italiana e (ii) del sottoperiodo compreso tra la data di protocollo in AIFA della domanda di Prezzo e Rimborso (P&R) inviata dall’azienda titolare dell’AIC e la pubblicazione in GU della relativa determina di P&R.
Risultati
La presente sezione analizza i risultati con una distinzione tra farmaci approvati con CMA e farmaci approvati UEC ed effettuando un confronto tra i due gruppi di farmaci considerati, relativamente alla loro eventuale rimborsabilità e alle tempistiche di accesso al mercato nazionale a seguito della negoziazione di prezzo e rimborso in AIFA (e pubblicazione di relativa determina in GU Italiana).
Farmaci approvati con Conditional Marketing Approval
Da luglio 2006 a marzo 2017, 35 specialità medicinali sono state approvate dall’EMA con CMA (17 sono farmaci orfani); per 12 (34%) di questi farmaci le autorizzazioni sono state convertite in standard marketing authorisation in un tempo medio di 4 anni. Gli elementi base per la concessione di un’approvazione condizionata sono stati in genere forniti da due studi principali di fase II/III che, per lo più delle volte, sono studi in aperto e randomizzati (dati che devono essere completati tramite evidenze generate da studi specifici -specific obligations- richiesti dal CHMP entro una data predefinita).
Dei 35 farmaci approvati a livello europeo in modo condizionato, 21 appartengono all’area terapeutica oncologica (60%) e 9 all’area malattie infettive (26%) (Figura 3).
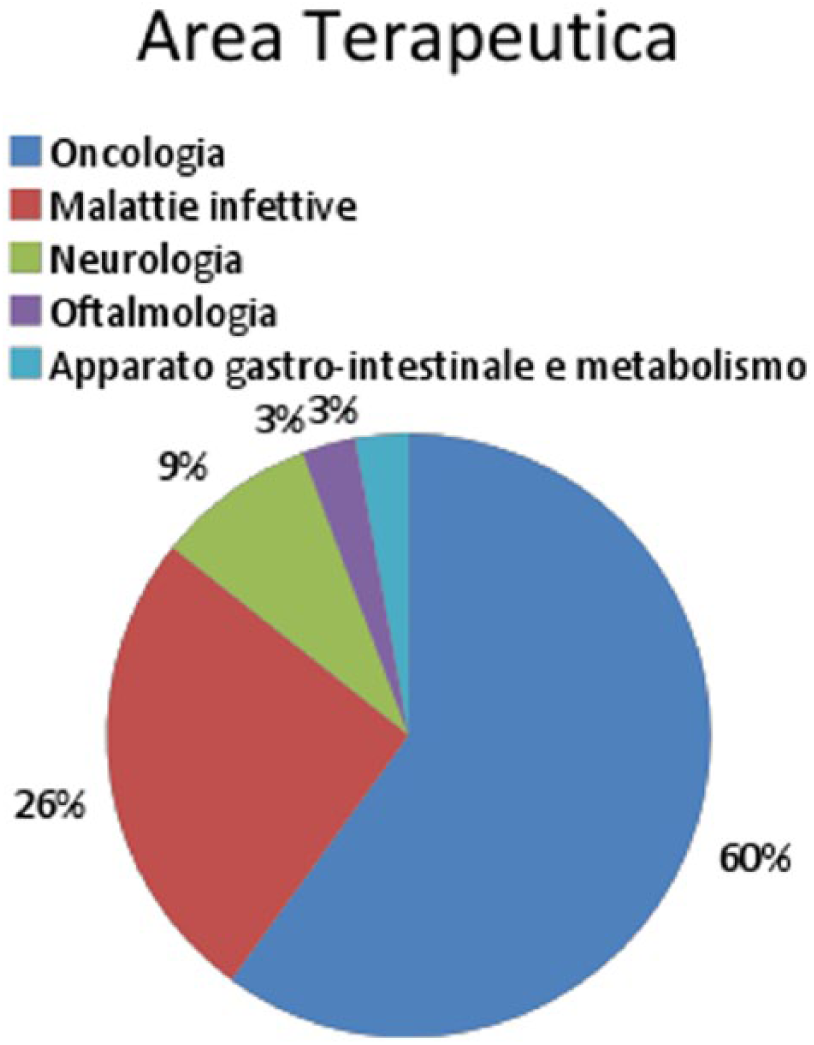
Area Terapeutica dei farmaci approvati con conditional approval (CMA) da luglio 2006 a marzo 2017.
Delle 35 specialità medicinali approvate da EMA con conditional approval sono 28 (80%) quelle commercializzate in Italia attualmente o in passato, di cui 18 sono state ammesse alla rimborsabilità (64%, 17 sono state inserite in classe H e 1 in classe A), 5 sono in classe C e 5 risultano, all’ultima data di valutazione, in classe C-NN.
Tre delle 18 specialità medicinali (brentuximab vedotin, ataluren, crizotinib) sono state inserite nelle liste della legge n. 648/96 prima di aver negoziato classe di rimborsabilità e prezzo. Dalla data di rilascio dell’AIC valida in UE al loro ingresso nelle liste della legge n. 648, sono trascorsi dai 113 giorni ai 264 giorni).
Delle 18 specialità medicinali rimborsate, per 11 (di cui 9 oncologici) è stato stipulato un MEA con applicazione di registro (patient-level) (61% sul totale: si tratta di 5 accordi di tipo finanziario e 6 con accordi outcome-based. Infine, a 13 farmaci (72%) è stato applicato un registro di monitoraggio e/o un Piano Terapeutico (PT).
Con riferimento ai tempi del processo approvativo e di rimborso (le statistiche non comprendono i vaccini), i dati evidenziano come: (i) dal parere positivo del CHMP di EMA alla data di rilascio dell’AIC valida in tutta l’Unione Europea siano trascorsi in media 72 giorni (35-158 giorni); (ii) dal parere positivo del CHMP alla data di ricezione in AIFA della domanda dell’Azienda di P&R, siano passati in media 126 giorni (minimo 7 giorni, massimo 494 giorni); (iii) dalla data di ricezione in AIFA della domanda dell’Azienda di prezzo e rimborso alla data di pubblicazione della determina AIFA nella GU Italiana, siano trascorsi in media 510 giorni, con un range che va dagli 88 giorni ai 1782.
Analizzando i dati specifici per sottoclassi di farmaci, per i pochi farmaci approvati con CMA e inseriti nella lista della legge n. 648/96 i tempi di accesso al mercato sono più rapidi, mentre quelli di rimborsabilità (dall’autorizzazione UE alla pubblicazione in GU Italiana della determina di P&R) sono più lunghi (805 giorni in media contro i 548 di tutti i farmaci non inseriti in lista 648), con un intervallo temporale particolarmente ampio tra autorizzazione europea e sottomissione del dossier di P&R in AIFA.
I farmaci la cui negoziazione di prezzo e rimborso si è conclusa con la stipulazione di un MEA con registro (patient-level) presentano tempi complessivi tra AIC europea e pubblicazione in GU della determina di P&R inferiori agli altri farmaci (538 giorni medi quando è stato applicato un accordo outcome-based, 468 quando invece è stato applicato un accordo financial-based, mentre 643 giorni per i farmaci a cui non è stato applicato un MEA patient-level).
Si osserva infine dei 12 farmaci che sono passati a standard marketing authorisation 7 non hanno subito variazioni nell’indicazione coperta dal SSN e 5 hanno avuto estensioni di indicazione successivamente alla data di trasformazione dell’autorizzazione a standard (dati aggiornati a marzo 2017).
Farmaci approvati in circostanze eccezionali
Da luglio 2006 a marzo 2017, 30 specialità medicinali sono state approvate da EMA come UEC (14 sono farmaci orfani) e 5 sono state attualmente ritirate dal commercio (celecoxib, 2 vaccini per influenza pandemica (H5N1), rilonacept, drotrecogin alfa). Dei 30 farmaci approvati da EMA in circostanze eccezionali, 7 appartengono all’area terapeutica oncologica (23%), 6 all’area malattie infettive (20%) (Figura 4).
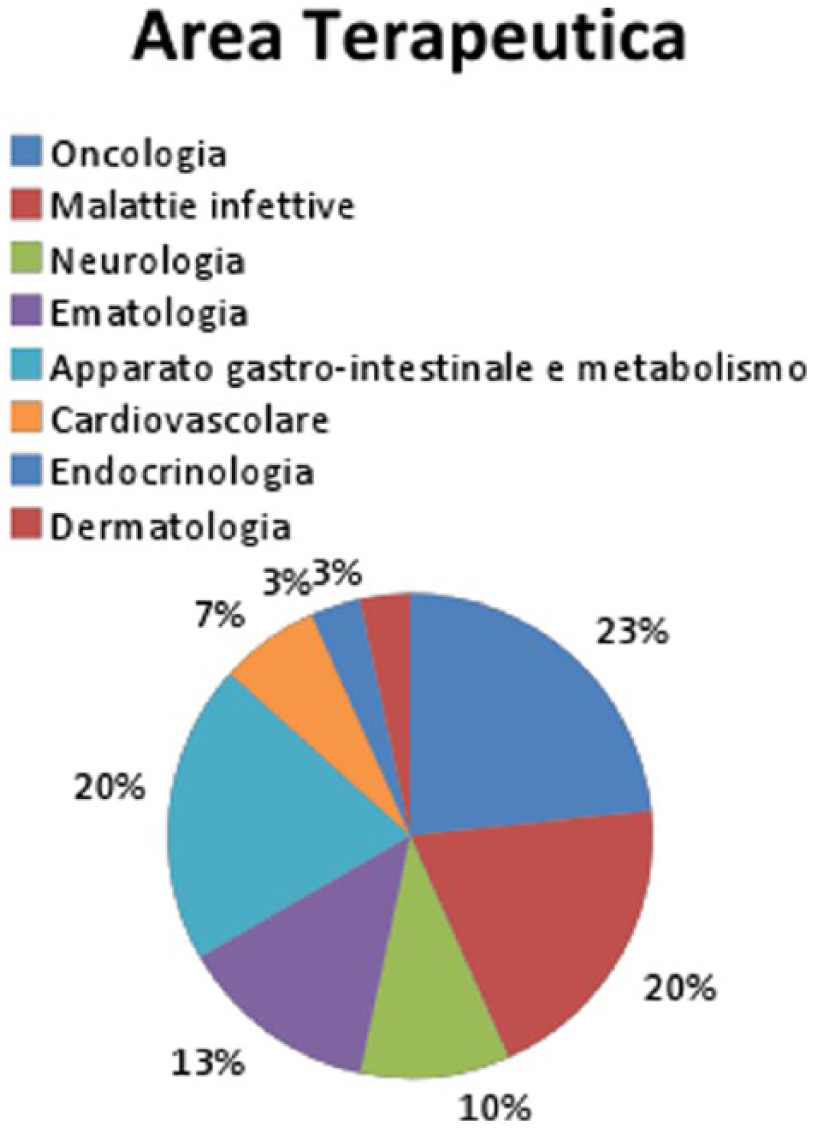
Area Terapeutica dei farmaci approvati in circostanze eccezionali (UEC) da luglio 2006 a marzo 2017.
Delle 30 specialità approvate UEC, 19 sono (o sono state) disponibili in Italia (63%): 13 sono stati ammessi alla rimborsabilità (68%), 12 in classe H e 1 in classe A, mentre 5 sono in classe C e 1 in C-NN. Nessuno dei farmaci approvati UEC rimborsato in Italia è stato negoziato tramite l’applicazione di un MEA patient-level di tipo financial-based o outcome- based, mentre per 4 farmaci, è stato applicato un registro di monitoraggio e/o un PT.
Sei delle 19 specialità medicinali sono state inserite nelle liste della legge n. 648/96.
Dalla data di rilascio dell’AIC valida in tutta l’Unione Europea al loro ingresso nelle liste della legge n. 648/96 sono trascorsi da 22 a 1065 giorni.
Facendo invece riferimento ai tempi del processo approvativo e di rimborso (le statistiche non comprendono i vaccini), i dati evidenziano come: (i) dal parere positivo del CHMP di EMA alla data di rilascio dell’AIC valida in tutta l’Unione Europea siano trascorsi in media 124 giorni, (27-1001 giorni); (ii) dal parere positivo del CHMP alla data di ricezione in AIFA della domanda dell’azienda di P&R, siano passati in media 568 giorni (minimo 43 giorni, massimo 2371 giorni); (iii) dalla data della ricezione in AIFA della domanda dell’azienda di richiesta di classificazione e prezzo alla data della pubblicazione della determina AIFA nella Gazzetta Ufficiale Italiana, siano trascorsi in media 329 giorni, con un range che va dai 138 giorni per ai 653.
Anche in questo caso, analizzando i dati specifici per sottoclassi di farmaci, per i pochi farmaci approvati UEC e inseriti nella lista della Legge n.648/96, i tempi di accesso al mercato sono più rapidi, mentre quelli di rimborsabilità dall’autorizzazione UE alla pubblicazione in GU della determina di P&R sono più lunghi (818 giorni in media contro i 713 di tutti i farmaci non inseriti in lista della legge n. 648/96) con un intervallo ampio tra autorizzazione europea e sottomissione del dossier di P&R in AIFA (dati aggiornati a marzo 2017).
Confronto tra farmaci autorizzati con CMA e UEC
Effettuando un confronto tra i due gruppi oggetto di ricerca, emerge che la proporzione di farmaci rimborsati è circa 64.3% per il gruppo CMA e circa 68.4% per il gruppo UEC, con una differenza di 4.1% punti percentuali. L’intervallo di confidenza stimato al 95% per la differenza tra le due proporzioni è pari a (-35.7% a 27.4%) e il risultato del test è che non si può concludere che la proporzione di rimborsati sia diversa tra i due gruppi.
Per quanto riguarda la durata dell’intero periodo (giorni trascorsi tra la positive opinion del CHMP e la pubblicazione della determina di P&R in GU Italiana) e il sottoperiodo compreso tra la data di protocollo in AIFA della domanda di P&R inviata dall’azienda titolare dell’AIC e la pubblicazione in GU della relativa determina di classificazione e prezzo, sono state testate eventuali differenze nei due gruppi CMA e UEC. Una prima sintesi dei tempi (media, mediana e standard deviation), nei due diversi periodi temporali e per i due gruppi CMA e UEC, è riportata nella Tabella 2.
La differenza nei tempi medi tra i due gruppi è simile in valore assoluto, tuttavia va in direzioni opposte se consideriamo il sottoperiodo o l’intero periodo (vedi Figura 5). Quindi, complessivamente, i farmaci approvati con procedura UEC impiegano mediamente più giorni (897 giorni) ad arrivare alla determina di P&R rispetto ai farmaci del gruppo CMA (636 giorni), ma se consideriamo solo il periodo dalla domanda di classificazione e prezzo, alla determina di P&R per lo stesso gruppo di farmaci, il processo sembra essere mediamente più veloce rispetto ai farmaci in CMA (329 vs 510 giorni). Ciò può significare che nel caso delle autorizzazioni UEC le aziende farmaceutiche effettuano valutazioni strategiche differenti rispetto alle CMA, richiedendo la rimborsabilità al SSN sia con una frequenza significativamente inferiore, sia con un ritardo nella sottomissione del dossier all’AIFA notevolmente maggiore. D’altronde, una volta richiesta la rimborsabilità per un medicinale UEC, in considerazione del fatto che vanno a rispondere a dei clinically unmet needs, il processo della rimborsabilità si sviluppa con una tempistica più rapida rispetto alle CMA, che riguarda medicinali che presentano evidenze, comunque, ancora preliminari.
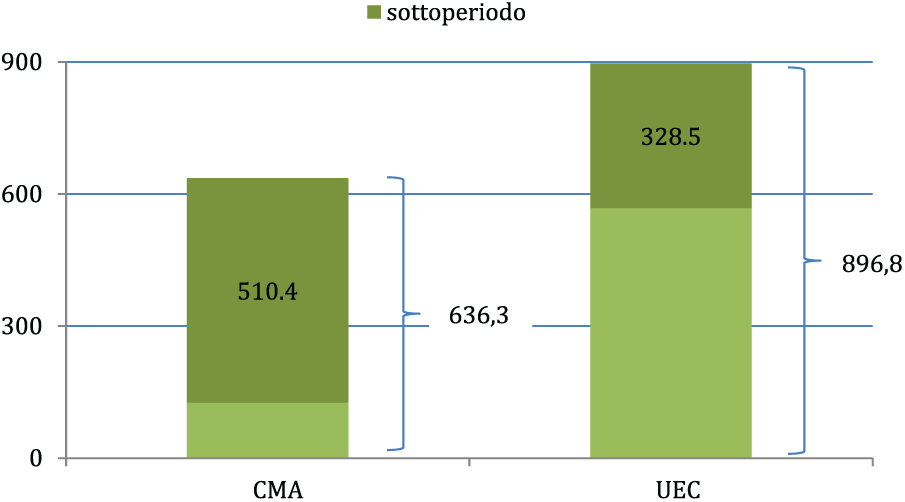
Durata del processo per i farmaci approvati con CMA o UEC.
La distribuzione dei tempi è rappresentata nei grafici in Figura 6 (il primo relativo all’intero periodo e il secondo relativo al sottoperiodo).
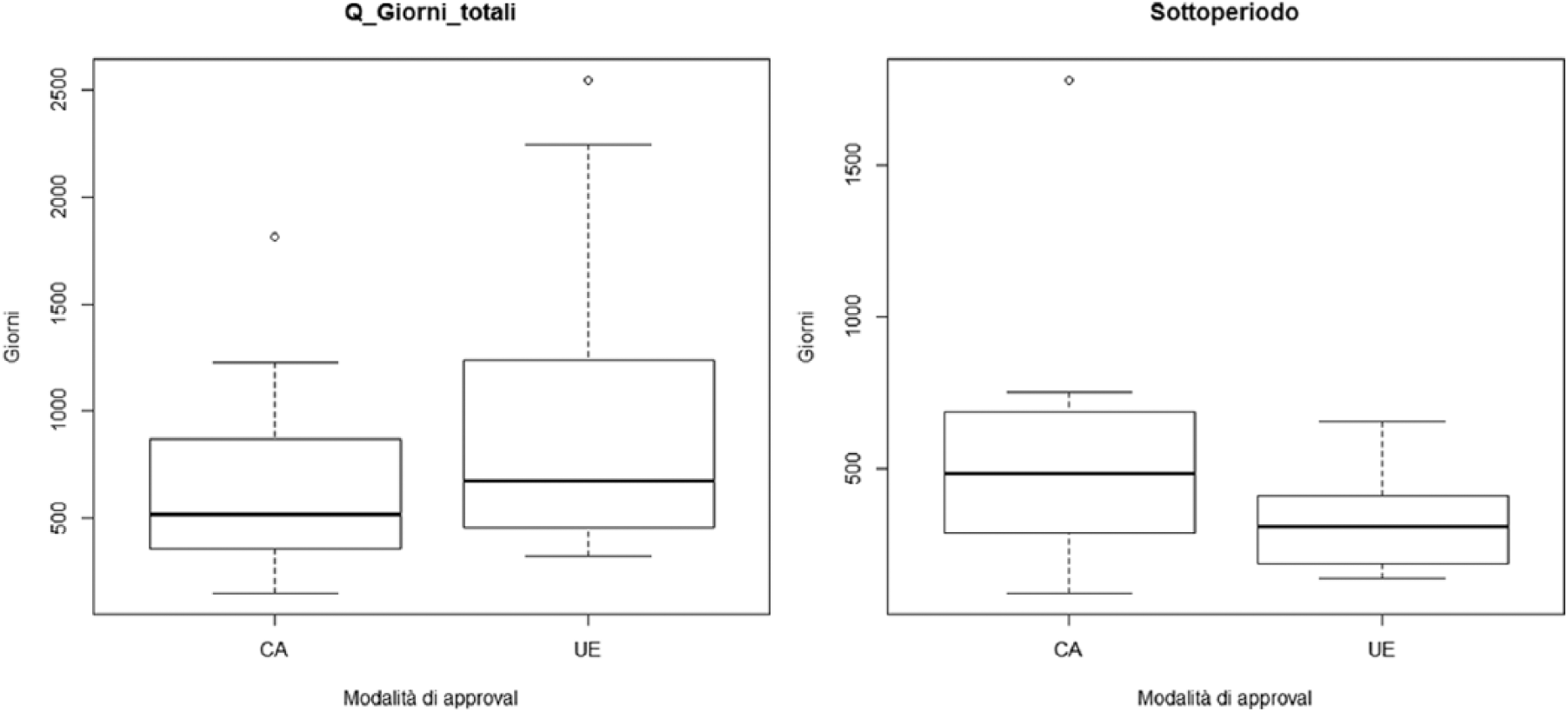
Boxplot della durata del processo relativa all’intero periodo o ad un sottoperiodo per i farmaci approvati con CMA o UEC.
È stato infine condotto un test di confronto tra i due gruppi CMA e UEC per verificare l’ipotesi che la distribuzione dei tempi (intero periodo e sottoperiodo) possa essere considerata uguale. È stato applicato il test non parametrico di Mann-Whitney-Wilcoxon (nel quale non viene usata l’assunzione di normalità dei dati). Relativamente all’intero periodo, il test ha concluso che non si può ritenere che i tempi siano statisticamente diversi ad un livello di significatività pari al 5%.
La stessa metodologia è stata impiegata per analizzare i tempi del sottoperiodo e in tal caso le durate risultano significativamente diverse tra i gruppi CMA e UEC.
Discussione e conclusioni
L’approvazione accelerata dei farmaci a livello europeo rappresenta da una parte un’occasione di accesso anticipato a terapie importanti, dall’altra un fattore di attenzione per la maggiore incertezza generata dalle evidenze esistenti al momento del lancio del prodotto sul mercato (16).
L’approvazione europea non rappresenta però il momento dell’accesso al mercato italiano: tale accesso avviene con la pubblicazione della Determina di P&R di AIFA, anche se poi in diverse regioni è necessario l’inserimento dei farmaci nel prontuario regionale, a meno che il rimborso anticipato non avvenga per effetto dell’inserimento nella lista della legge n. 648/96, con l’acquisto dalla classe C-NN, tramite l’accesso al fondo 5% o all’Uso Compassionevole (17).
Lo studio non ha effettuato un confronto nello stesso arco temporale tra farmaci approvati con procedure accelerate e farmaci autorizzati con procedura ordinaria. Esistono però in letteratura delle evidenze sui tempi di approvazione dei farmaci, anche se non del tutto comparabili alla presente analisi per dettaglio dei dati riportati. Secondo i dati IMS Health riferiti all’anno 2014 (18), il tempo medio trascorso dall’approvazione di una nuova molecola a livello europeo e la Determina di P&R sarebbe pari a 460 giorni e, quindi mediamente inferiore ai tempi di accesso dei farmaci con procedura accelerata. I tempi per la prima vendita del farmaco sarebbero pari a 435 giorni (considerando il tempo medio intercorso tra l’AIC e la prima vendita, per i farmaci con prima vendita nel 2014). Uno studio più recente sui farmaci oncologici ha evidenziato come la valutazione di un nuovo farmaco da parte di AIFA nel 2013-2015, considerando come range la data della prima valutazione della CTS e la decisione del CPR, sarebbe pari a 248 giorni (19).
Effettuando poi un confronto tra i tempi medi di accesso al mercato di farmaci transitati dall’elenco dei medicinali erogabili a totale carico del SSN, ai sensi della legge n. 648/96 e successivamente rimborsati a seguito di negoziazione, con quelli che non sono stati inseriti in tale elenco è possibile constatare che, se da un lato l’introduzione in tale elenco permette un accesso al mercato molto più rapido rispetto alla procedura di negoziazione standard (195 giorni contro i 548 per i farmaci autorizzati con CMA e 313 giorni contro i 713 per i farmaci autorizzati UEC), dall’altro ritarda la procedura di negoziazione prezzo e rimborso (805 giorni per i farmaci transitati dalla legge n. 648/96 contro i 548 per quelli negoziati con CMA e 818 giorni contro i 713 per i farmaci approvati UEC).
Il secondo elemento caratterizzante le approvazioni anticipate è la maggiore incertezza degli effetti dei farmaci, dato il mancato completamento del processo di sviluppo. Le analisi effettuate mostrano come l’approvazione con CMA sia predittiva per l’applicazione di un MEA (61%) di tipo finanziario o outcome-based con l’applicazione di un registro, a differenza dei farmaci approvati UEC. Con riferimento nello specifico ai 28 farmaci oncologici autorizzati con CMA e UEC, 9 risultano autorizzati con CMA. Di questi, 6 hanno ottenuto un accordo negoziale basato su outcome e 3 un accordo finanziario patient-level. La minore disponibilità di dati clinici sperimentali per questi farmaci sembra generare una presenza di accordi basati su outcome. Si sottolinea però che la dimensione numerica degli accordi di tipo finanziario è sottostimata, non avendo preso in considerazione la presenza di un eventuale sconto negoziato tra AIFA e impresa titolare dell’AIC (gli accordi finanziari tracciati sono soltanto MEAs a livello paziente).
L’analisi presenta essenzialmente quattro limiti. In primo luogo, come sopra specificato, non è stato possibile effettuare un confronto tra tempi e modalità di accesso dei farmaci ad approvazione accelerata e altri farmaci. Questo rende parziale l’analisi degli effetti di tale modalità di approvazione sui tempi e modalità di accesso dei farmaci.
Il secondo limite, collegato all’aspetto precedente, è che non è stato possibile effettuare una valutazione comparativa di quanto altri elementi (ad esempio, designazione di farmaco orfano, richiesta di prezzo rispetto ai concorrenti, impatto previsto sul budget complessivo) hanno pesato, rispetto all’iter approvativo europeo, sull’allungamento dei tempi negoziali e sulla stipulazione di contratti di accesso condizionato. Infine, il campione dei farmaci analizzati, nonostante l’arco temporale considerato piuttosto vasto, risulta essere abbastanza ridotto e questo può in parte rendere il dato dei tempi medi di accesso al mercato non estremamente significativo.
Il quarto limite rappresenta l’impossibilità di considerare i clock-stop del processo negoziale in AIFA ed eventuali altre interruzioni dell’iter amministrativo derivanti da errori nella trasmissione di materiale da parte dell’azienda, che condizionano significativamente le tempistiche oggetto di analisi.
Nonostante i limiti segnalati, tale analisi consente di evidenziare come, in un momento storico in cui la crescente scarsità di risorse per il SSN deve essere coniugata con la possibilità di accesso rapido ai farmaci a valore aggiunto per il SSN, risulta fondamentale agire da una parte su un’ottimizzazione dei tempi di accesso e dall’altra su un’attenta valutazione degli effetti previsti del farmaco. Nella presenza di elevate incertezze, è poi importante stipulare accordi che consentano al SSN di assicurarsi a priori su un effetto del farmaco diverso da quanto ci si sarebbe potuto aspettare dagli studi registrativi (20).
Footnotes
Authors’ Note
Le opinioni espresse in questa pubblicazione sono personali e non riflettono necessariamente il punto di vista di AIFA.
Declaration of Conflicting Interest
The authors declare that there is no conflict of interest.
Funding
This research received no specific grant from any funding agency in the public, commercial, or not-for-profit sectors.
