Abstract
Aim:
This article reports on a retrospective quarterly cost description (CD) performed on 401 patients with stable chronic obstructive pulmonary disease (COPD) at enrolment in the national, multicenter, noninterventional SATisfaction and adherence to COPD treatment (SAT) study.
Methods:
Examined from the perspective of the Italian National Health Service, health care resources were costed via published sources and expressed in euro (€) 2017 on a per patient basis. Incomplete data were addressed via multiple imputation (MI) with 20 completed datasets.
Results:
384 patients were evaluable (moderate COPD: 76.00%). Most patients (61.47%) reported no COPD exacerbations during the year before the enrolment. Under Available Case Analysis the mean quarterly cost was €328.59 (standard deviation – SD: €537.25); 187 patients (48.69%) reported missing completely at random (MCAR) or missing at random (MAR) data. Their mean quarterly cost (€191.30; SD: €356.86) was significantly lower (bootstrap p-value < 0.0001) than that of patients with complete data (€458.90; SD: €638.85). Under MI the mean quarterly cost reached €662.48 (SD: €1476.03). Oxygen therapy (265.73; SD: €807.19) and drugs (€179.27; SD: €103.49) added up to 67.17% of the total quarterly cost. The mean quarterly cost for ICS/LABA/LAMA drugs (€295.03; SD: €64.48) was 64.57% higher than the overall mean quarterly cost for drugs. The difference between mean quarterly cost for severe and moderate BPCO patients was +179.90%.
Conclusions:
Preliminary results of the SAT study highlight the need to further investigate appropriate and sustainable drug treatment for moderate and severe COPD. MI increases the reliability of CD estimates when MCAR and MAR data are taken into account.
Introduzione
Con 3 milioni di decessi totalizzati nel corso del 2012 (6% di tutti i decessi), la broncopneumopatia cronico-ostruttiva (BPCO) costituisce la quarta causa di mortalità nel mondo.1,2 In Italia, la prevalenza della BPCO, non stratificata per fasce di età, si attesta intorno al 4,5%. 3 La BPCO è caratterizzata da sintomi respiratori persistenti e limitazione al flusso aereo. 2 Tra i principali fattori di rischio della BPCO si annoverano il fumo di sigaretta e gli inquinanti ambientali, seguiti da fattori genetici, familiarità ed anamnesi di infezioni delle basse vie respiratorie contratte durante l’infanzia.2,4
La diagnosi di BPCO si avvale della spirometria: il riscontro di un rapporto
Adottando la prospettiva del Servizio Sanitario Nazionale (SSN) del nostro Paese, pregresse esperienze di ricerca hanno evidenziato che il costo annuo della BPCO, espresso a valori riferiti al periodo 2003-2004, oscilla tra €1.0406 a €6.700, 7 in funzione, principalmente, del numero e della gravità degli episodi di riacutizzazione, che possono aumentare sin del 54% il costo della fase di mantenimento della patologia. 8
Obiettivo
Il presente manoscritto riporta la descrizione dei costi
9
trimestrali totalizzati dai pazienti affetti da BPCO moderata o grave, calcolati retrospettivamente sulla base del consumo di risorse sanitarie riferito dal paziente in occasione della visita di arruolamento prevista dal protocollo dello studio osservazionale, nazionale, multicentrico
Materiali e metodi
Caratteristiche demografiche e cliniche dei pazienti
Sono state esaminate le variabili demografiche (sesso; razza; stato civile; situazione abitativa; livello di istruzione; stato occupazionale; ubicazione geografica) e cliniche (tabagismo; parametri respiratori; presenza e numero di patologie concomitanti; numero di riacutizzazioni di BPCO avvenute nel corso dell’ultimo anno, ad eccezione dei tre mesi precedenti l’arruolamento; gravità della patologia) relative a 384 pazienti valutabili su 401 arruolati (pari al 95,76% del totale), sottoposti, previo consenso informato e nel rispetto della dichiarazione di Helsinki, alla prima visita prevista dal protocollo dello studio SAT presso i 20 centri partecipanti all’indagine (Nord: 11; Centro: 3; Sud: 6; strutture ospedaliere pubbliche: 18; strutture ospedaliere private accreditate: 2), previa approvazione, da parte dei rispettivi comitati etici, della metodologia e delle finalità dell’esperienza di ricerca (Tabella MS1). Secondo il protocollo dello studio SAT, nei tre mesi precedenti l’arruolamento i pazienti dovevano essere in trattamento farmacologico stabile per la BPCO e non dovevano aver avuto riacutizzazioni di BPCO.
Una riacutizzazione è stata definita come un aumento o nuova insorgenza di almeno un sintomo (tosse, espettorato, respiro sibilante, dispnea o oppressione toracica) per una durata di almeno tre giorni e che porta a iniziare un trattamento con steroidi sistemici e/o antibiotici (esacerbazione moderata) o al ricovero in ospedale (grave esacerbazione).
Identificazione e quantificazione delle risorse
Sono state identificate e quantificate le risorse sanitarie il cui consumo, riferito dai pazienti, nel trimestre precedente alla visita di arruolamento nello studio SAT, fosse attribuibile esclusivamente a BPCO. Per la diagnosi di BPCO è stato considerato necessario un rapporto post-broncodilatatore di FEV1/FVC < 70% alla spirometria. La gravità dell’ostruzione al flusso aereo nella BPCO è classificata spirometricamente come lieve quando FEV1 > 80% predetto, di media gravità quando 50% < FEV1 < 80% del predetto, grave quando 30% < FEV1 < 50% del predetto, molto grave quando FEV1 < 30% del predetto.
Le terapie farmacologiche attive prescritte ai pazienti sono state suddivise in 10 schemi di trattamento farmacologico (Altro;
Al fine di contemplare la presenza di anno bisestile, la durata del trimestre è stata approssimata a (365,25/4) = 91,31 giorni. 11
Modello di valutazione economica dei programmi sanitari utilizzato
Adottando la prospettiva del SSN, è stata condotta una valutazione economica dei programmi sanitari del tipo descrizione dei costi. 9
Valorizzazione delle risorse
I costi delle risorse di carattere sanitario di pertinenza del SSN, stratificati per gravità della patologia, sono espressi in euro (€), a valori 2017, per paziente.
Terapie farmacologiche ed ossigenoterapia sono state monetizzate utilizzando fonti liberamente accessibili,12,13 considerando la configurazione di prezzo al pubblico (Tabelle MS2-MS5). Per il calcolo del costo delle terapie farmacologiche, si è moltiplicato il prezzo al pubblico per unità posologica per somministrazione per il numero di somministrazioni giornaliere e per la durata del ciclo terapeutico, espresso in giorni. Nel caso di somministrazioni di farmaci definite
Sono state inoltre monetizzate le risorse sanitarie necessarie all’effettuazione delle somministrazioni delle terapie farmacologiche per via endovenosa (Tabella MS6),
14
poiché le restanti somministrazioni per via inalatoria e
Il costo dell’ossigenoterapia è stato calcolato moltiplicando il prezzo unitario al litro dell’ossigeno per il volume di litri erogati al minuto, per le ore giornaliere di ossigenoterapia, per la durata dell’ossigenoterapia, espressa in giorni.
Per valorizzare ciascun episodio di ricovero ospedaliero si è fatto riferimento ai codici
Gli accessi in PS sono stati valorizzati tramite l’unico riferimento ufficiale disponibile (Tabella MS6). 18
Le visite effettuate presso l’ambulatorio del MMG sono state monetizzate facendo ricorso all’accordo nazionale di rimborso dell’attività di tale professionista, 19 mentre le visite specialistiche, gli accertamenti laboratoristici, strumentali e per immagini sono stati valorizzati utilizzando la versione più recente accessibile del revisore del nomenclatore tariffario nazionale delle prestazioni specialistiche ambulatoriali (Tabella MS7). 20
Analisi statistica
Statistiche descrittive
Per le variabili continue sono state calcolate media e deviazione standard (DS). 21 Per le variabili binarie sono state riportate le frequenze assolute e relative. Se non diversamente indicato, le statistiche descrittive si riferiscono ai pazienti.
Valori mancanti e troncati a sinistra
L’estratto del
Inoltre, per alcuni pazienti terapie farmacologiche ed ossigenoterapia attive terminavano prima del trimestre di osservazione, tipicamente perché all’assistito era stata prescritta la sospensione dell’ossigenoterapia o una sostituzione di principio attivo: tali dati sono stati considerati troncati a sinistra (
Poiché, ai fini della loro gestione, i dati
Come raccomandato dalla letteratura,23–25,29 per ciascuna delle variabili caratterizzate da dati incompleti ne è stato determinato il meccanismo e il modello caratterizzante.
Sulla base del meccanismo, i dati incompleti si definiscono:22-25,27,29
Mentre esistono test formali per indagare se il meccanismo causa del dato incompleto è MCAR o MAR CDM,24,27,29,31,32 non è possibile determinare analiticamente se quest’ultimo sia, invece, MNAR.
Inoltre, i dati incompleti possono essere classificati in due modelli principali:22,24,29
monotonici, che si verificano allorché, ordinando una serie di variabili in ordine decrescente per frequenza di dati mancanti, ciascuna variabile contiene valori mancanti se anche la precedente variabile contiene valori mancanti;
non monotonici, caratterizzati dall’impossibilità di sistematizzare i dati mancanti secondo un criterio preordinato.
Imputazione multipla
Mentre per la gestione dei dati MNAR sono raccomandati i modelli di selezione
33
e i
Al contrario, l’esclusione dei dati incompleti, attuata limitando le statistiche ai casi completi (
Mediante modelli di regressione di interpretazione frequentista o, bayesiana,27,41 l’IM permette la creazione di più copie complete (da 5 a 50; più frequentemente 20)42,43 del
L’IM si è articolata nelle seguenti fasi:24,25,27–29
determinazione, per ciascuna variabile avente dati incompleti, del meccanismo e del modello relativi alla
sviluppo di modelli di IM coerenti con quanto al punto precedente. Si sono privilegiati modelli di imputazione “a catena” (
Per la totalità dei modelli di IM si sono utilizzati, quali predittori, le seguenti variabili complete, di carattere demografico (sesso; razza; età all’arruolamento ed alla diagnosi di BPCO, espresse in anni) e clinico (durata BPCO dalla diagnosi, espressa in anni).
La variabile demografica definita ubicazione geografica dei pazienti, ancorché completa, non è stata impiegata quale predittore, a causa dell’evidente differenza del numero di pazienti arruolati nelle diverse macroregioni del nostro Paese.
La medesima ragione ha informato l’esclusione, dal novero dei predittori, dei centri pneumologici ai quali i pazienti afferivano.
Infine, la variabile clinica completa definita tabagismo, precedentemente inclusa tra i predittori, è stata poi abbandonata poiché predittore perfetto della totalità dei dati binari in una o più delle 20 imputazioni.
Ai suddetti predittori si sono aggiunti, quali variabili ausiliarie:28,29 flusso al minuto di ossigeno e durata espressa in ore giornaliere (per IM ossigenoterapia); classe terapeutica e nome principio attivo molecola (per IM terapie farmacologiche);
realizzazione, per ciascun modello di imputazione di 20
calcolo di media e DS per le variabili di interesse per ciascuno dei 20 M;
calcolo di media e DS
a) stima della media (

b) stima della varianza
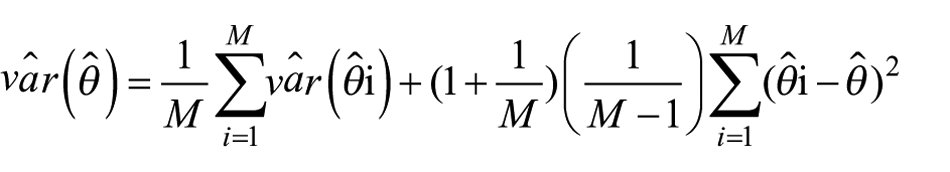
Il primo termine dell’equazione a destra del segno di uguale si riferisce alla varianza di ciascuno dei 20
Infine, il termine
Sebbene l’IM sia principalmente utilizzata a supporto di analisi inferenzial,
24
i principi metodologici che la informano permangono validi anche per le statistiche descrittive,
35
precisando che, in questo caso, non essendovi inferenza su alcun parametro, la varianza si riduce alla media delle varianze registrate in ciascuno dei
L’IM è stata preceduta da un
Le analisi statistiche sono state supportate dal software Statatm/SE versione 14.2 per Windows® 2010 (StataCorp LP, College Station, TX, USA).
Medie e DS
Risultati
Sono stati riportati i risultati relativi sia all’ACA, sia all’IM, al fine di facilitare il confronto tra i due approcci (
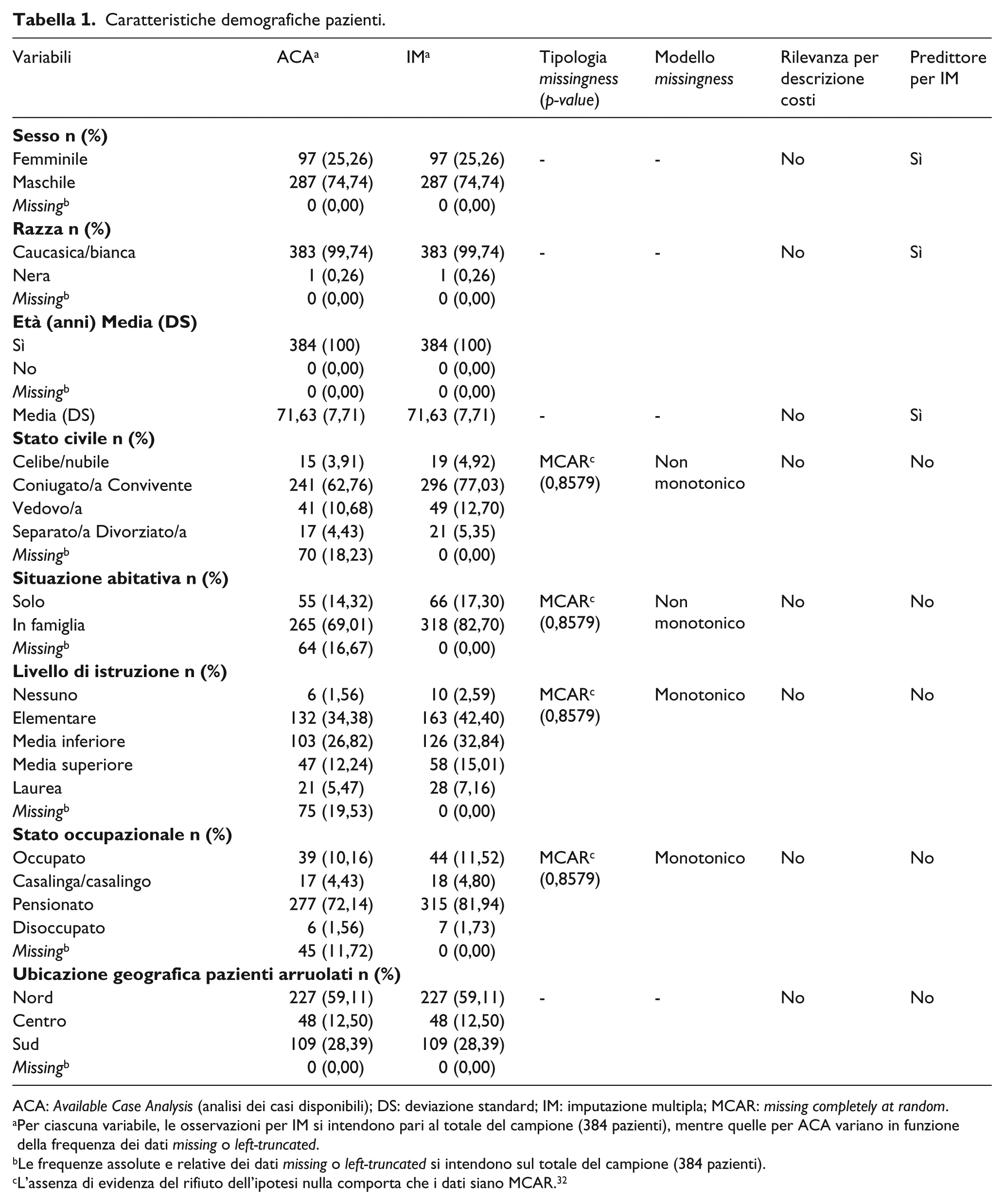
Caratteristiche demografiche pazienti.
ACA:
Per ciascuna variabile, le osservazioni per IM si intendono pari al totale del campione (384 pazienti), mentre quelle per ACA variano in funzione della frequenza dei dati
Le frequenze assolute e relative dei dati
L’assenza di evidenza del rifiuto dell’ipotesi nulla comporta che i dati siano MCAR. 32
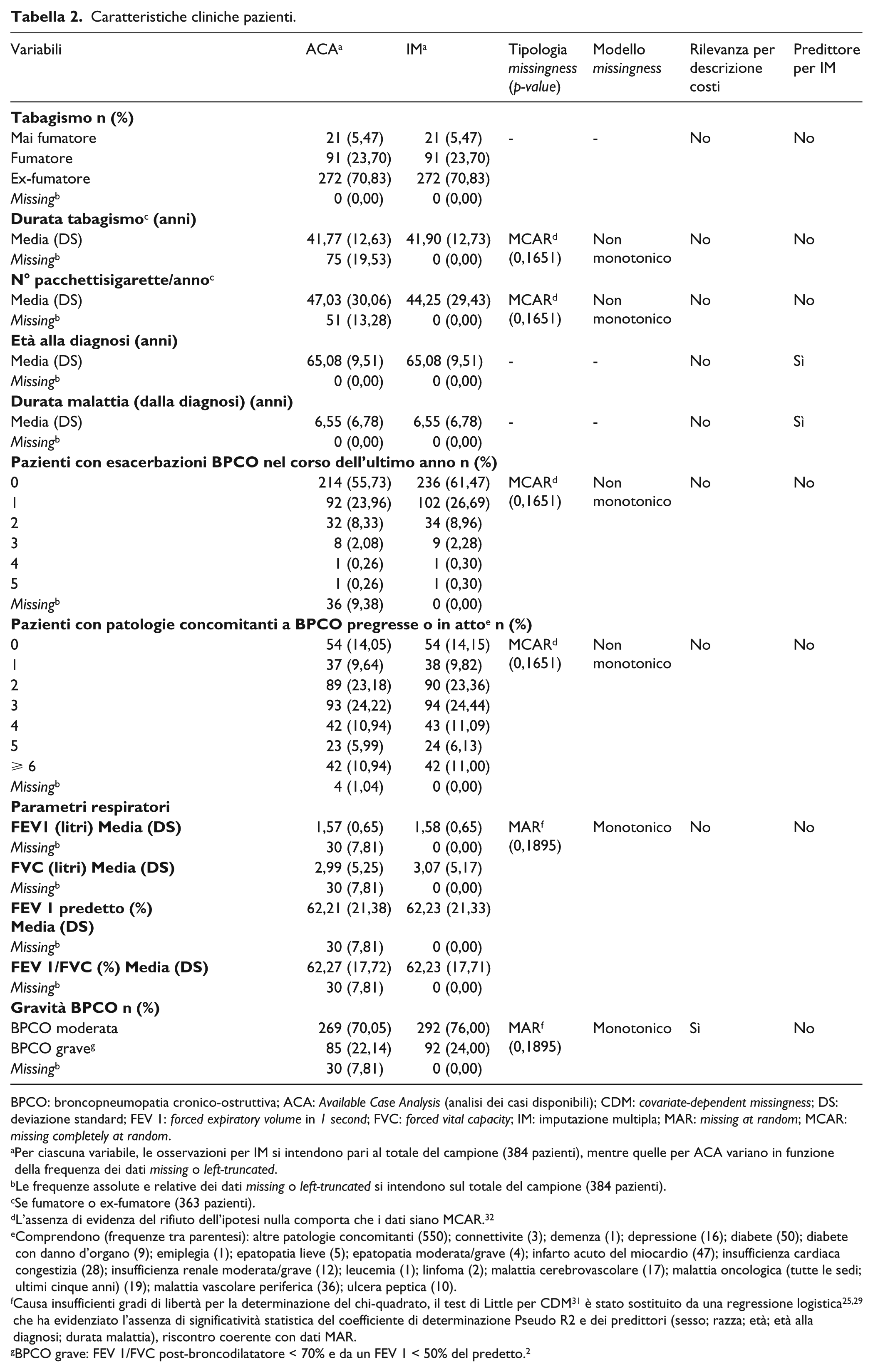
Caratteristiche cliniche pazienti.
BPCO: broncopneumopatia cronico-ostruttiva; ACA:
Per ciascuna variabile, le osservazioni per IM si intendono pari al totale del campione (384 pazienti), mentre quelle per ACA variano in funzione della frequenza dei dati
Le frequenze assolute e relative dei dati
Se fumatore o ex-fumatore (363 pazienti).
L’assenza di evidenza del rifiuto dell’ipotesi nulla comporta che i dati siano MCAR. 32
Comprendono (frequenze tra parentesi): altre patologie concomitanti (550); connettivite (3); demenza (1); depressione (16); diabete (50); diabete con danno d’organo (9); emiplegia (1); epatopatia lieve (5); epatopatia moderata/grave (4); infarto acuto del miocardio (47); insufficienza cardiaca congestizia (28); insufficienza renale moderata/grave (12); leucemia (1); linfoma (2); malattia cerebrovascolare (17); malattia oncologica (tutte le sedi; ultimi cinque anni) (19); malattia vascolare periferica (36); ulcera peptica (10).
Causa insufficienti gradi di libertà per la determinazione del chi-quadrato, il test di Little per CDM 31 è stato sostituito da una regressione logistica25,29 che ha evidenziato l’assenza di significatività statistica del coefficiente di determinazione Pseudo R2 e dei predittori (sesso; razza; età; età alla diagnosi; durata malattia), riscontro coerente con dati MAR.
BPCO grave: FEV 1/FVC post-broncodilatatore < 70% e da un FEV 1 < 50% del predetto. 2
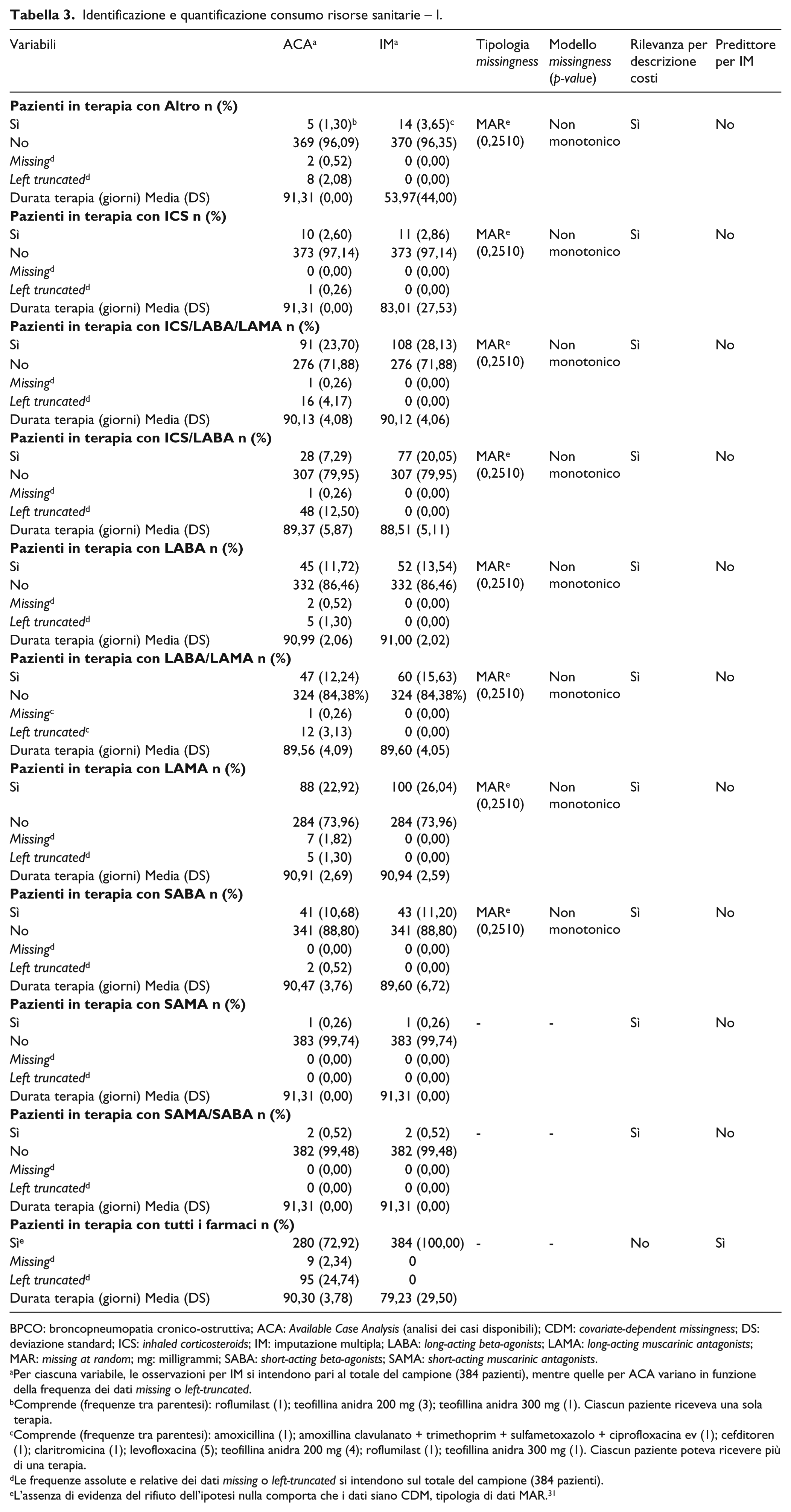
Identificazione e quantificazione consumo risorse sanitarie – I.
BPCO: broncopneumopatia cronico-ostruttiva; ACA:
Per ciascuna variabile, le osservazioni per IM si intendono pari al totale del campione (384 pazienti), mentre quelle per ACA variano in funzione della frequenza dei dati
Comprende (frequenze tra parentesi): roflumilast (1); teofillina anidra 200 mg (3); teofillina anidra 300 mg (1). Ciascun paziente riceveva una sola terapia.
Comprende (frequenze tra parentesi): amoxicillina (1); amoxillina clavulanato + trimethoprim + sulfametoxazolo + ciprofloxacina ev (1); cefditoren (1); claritromicina (1); levofloxacina (5); teofillina anidra 200 mg (4); roflumilast (1); teofillina anidra 300 mg (1). Ciascun paziente poteva ricevere più di una terapia.
Le frequenze assolute e relative dei dati
L’assenza di evidenza del rifiuto dell’ipotesi nulla comporta che i dati siano CDM, tipologia di dati MAR. 31
Identificazione e quantificazione consumo risorse sanitarie – II.
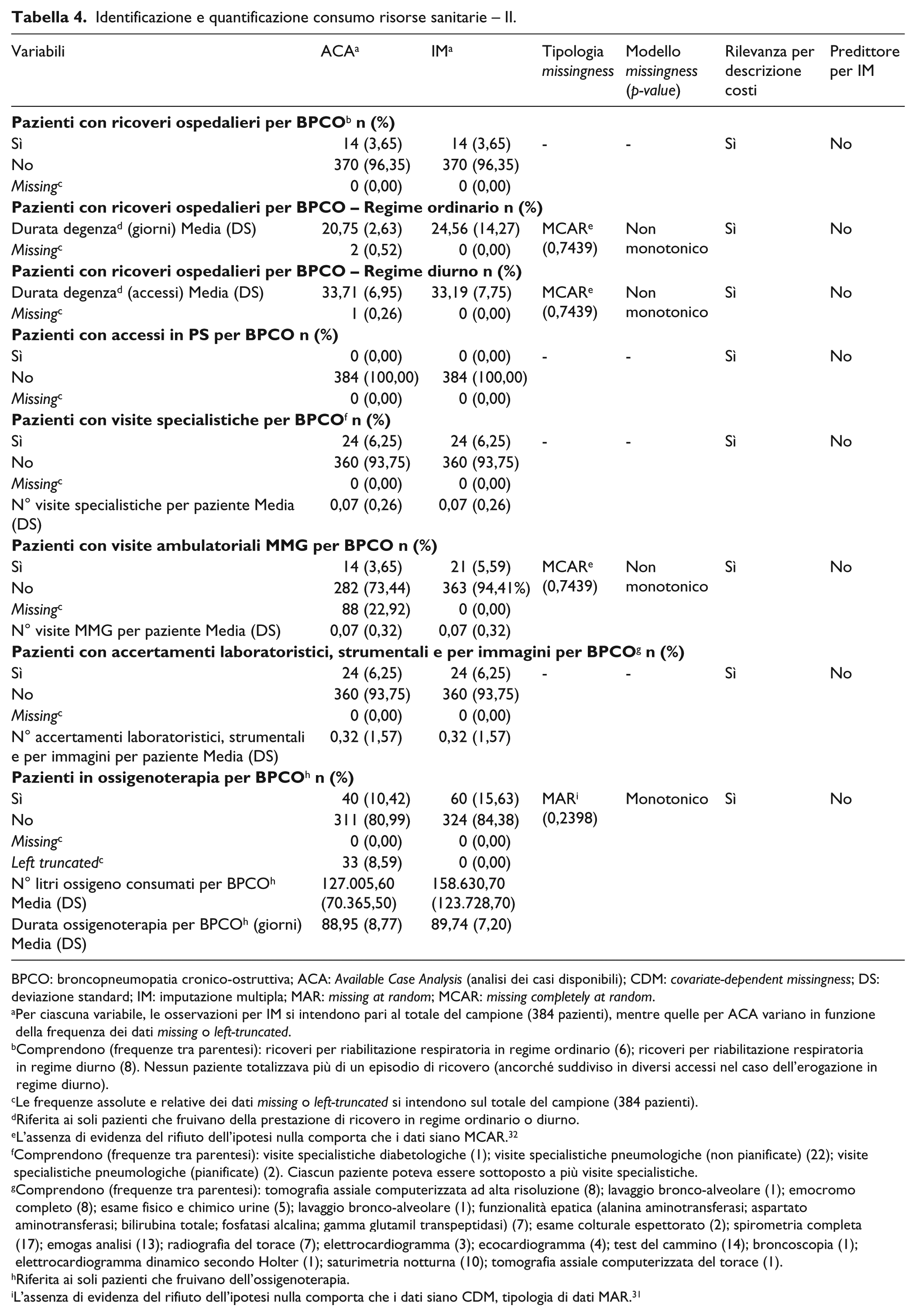
BPCO: broncopneumopatia cronico-ostruttiva; ACA:
Per ciascuna variabile, le osservazioni per IM si intendono pari al totale del campione (384 pazienti), mentre quelle per ACA variano in funzione della frequenza dei dati
Comprendono (frequenze tra parentesi): ricoveri per riabilitazione respiratoria in regime ordinario (6); ricoveri per riabilitazione respiratoria in regime diurno (8). Nessun paziente totalizzava più di un episodio di ricovero (ancorché suddiviso in diversi accessi nel caso dell’erogazione in regime diurno).
Le frequenze assolute e relative dei dati
Riferita ai soli pazienti che fruivano della prestazione di ricovero in regime ordinario o diurno.
L’assenza di evidenza del rifiuto dell’ipotesi nulla comporta che i dati siano MCAR. 32
Comprendono (frequenze tra parentesi): visite specialistiche diabetologiche (1); visite specialistiche pneumologiche (non pianificate) (22); visite specialistiche pneumologiche (pianificate) (2). Ciascun paziente poteva essere sottoposto a più visite specialistiche.
Comprendono (frequenze tra parentesi): tomografia assiale computerizzata ad alta risoluzione (8); lavaggio bronco-alveolare (1); emocromo completo (8); esame fisico e chimico urine (5); lavaggio bronco-alveolare (1); funzionalità epatica (alanina aminotransferasi; aspartato aminotransferasi; bilirubina totale; fosfatasi alcalina; gamma glutamil transpeptidasi) (7); esame colturale espettorato (2); spirometria completa (17); emogas analisi (13); radiografia del torace (7); elettrocardiogramma (3); ecocardiogramma (4); test del cammino (14); broncoscopia (1); elettrocardiogramma dinamico secondo Holter (1); saturimetria notturna (10); tomografia assiale computerizzata del torace (1).
Riferita ai soli pazienti che fruivano dell’ossigenoterapia.
L’assenza di evidenza del rifiuto dell’ipotesi nulla comporta che i dati siano CDM, tipologia di dati MAR. 31
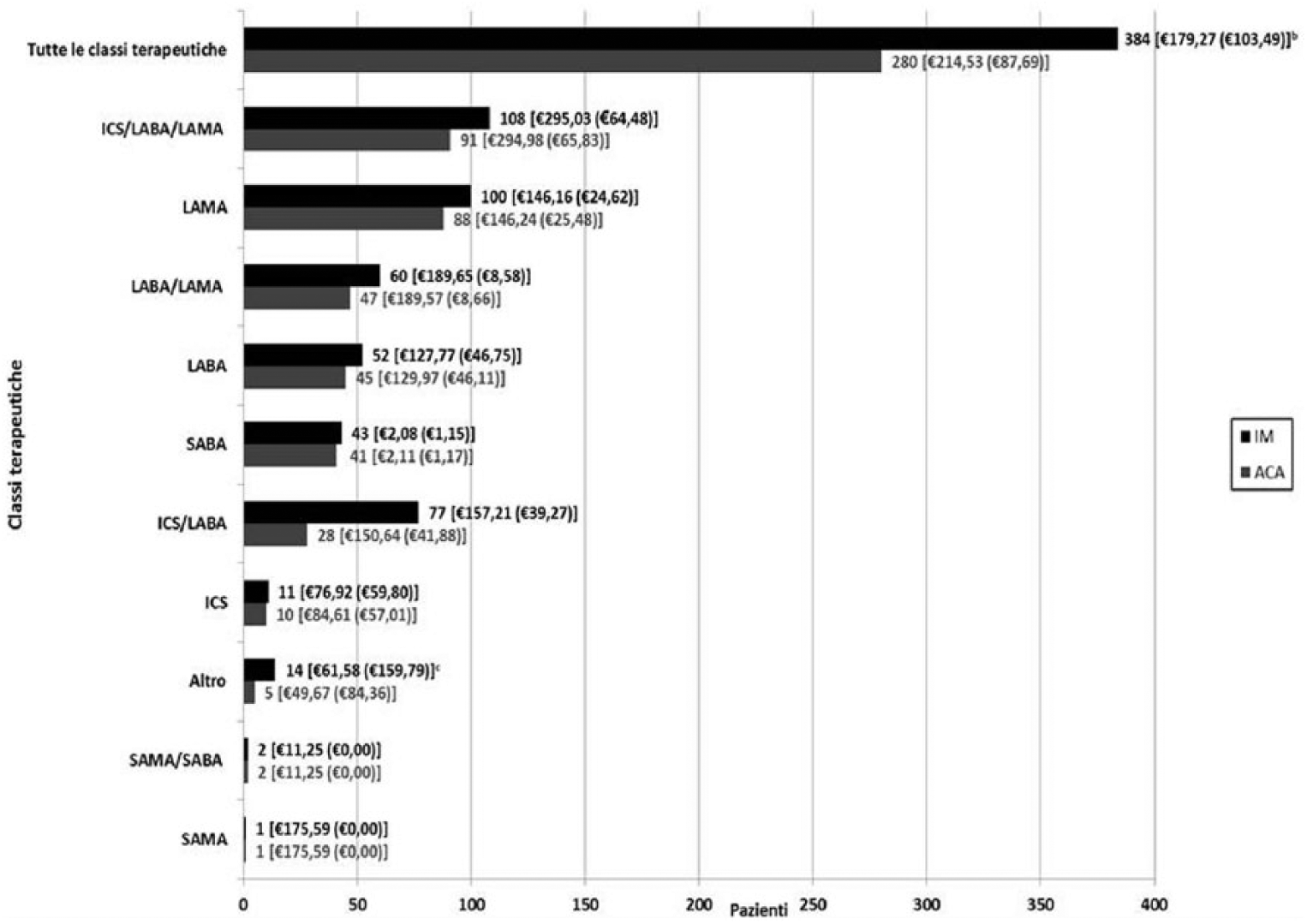
Frequenza pazienti e costo [media (DS)] per schema di trattamento farmacologico (€2017)a.
Caratteristiche demografiche e cliniche dei pazienti
Considerando le variabili demografiche complete, la maggioranza dei 384 pazienti valutabili è di sesso maschile (287 pazienti, pari al 74,74% del campione), razza caucasica/bianca (383 pazienti, pari al 99,74% del campione), riporta un’età media pari a 71,63 anni (DS: 7,71) e proviene dal Nord Italia (227 pazienti, pari al 59,11% del campione) (Tabella 1).
Le restanti variabili demografiche sono gravate da una proporzione di dati MCAR (
L’IM permette di stimare che la maggioranza dei 384 pazienti è coniugato/a o convivente (296 pazienti, pari al 77,03% del campione), vive in famiglia (318 pazienti, pari all’82,70% del campione), ha conseguito il diploma di scuola elementare (163 pazienti, pari al 42,40% del campione) ed è pensionato (315 pazienti, pari al 81,94% del campione).
Per quanto concerne le variabili cliniche con dati completi, la maggioranza dei pazienti è composta da ex-fumatori (272 pazienti, pari al 70,83% del campione), presenta un’età media alla diagnosi di BPCO pari a 65,08 anni (DS: 9,51) ed una durata media di malattia che raggiunge 6,55 anni (DS: 6,78) (Tabella 2).
Le altre variabili cliniche presentano una proporzione di dati MCAR (
L’IM ha consentito di stimare che la durata media del tabagismo, per fumatori ed ex-fumatori, eguaglia 41,90 anni (DS: 12,73), con un consumo medio di pacchetti di sigarette/anno pari a 44,25 (DS: 29,43) e che la maggioranza dei pazienti non ha subito riacutizzazioni di BPCO nel corso dell’anno precedente all’arruolamento nello studio SAT (236 pazienti, pari al 61,47% del campione), è affetta da 3 patologie concomitanti a BPCO, pregresse o in atto (94 pazienti, pari al 24,44% del campione), registra valori medi di FEV1 e FVC pari, rispettivamente a 1,58 litri (DS: 0,65) ed a 3,07 litri (DS: 5,17) e valori medi di FEV1 predetto e FEV 1/FVC che eguagliano, rispettivamente, il 62,23% (DS: 21,33%) ed il 62,23% (DS: 17,71%) ed è affetta da BPCO moderata (292 pazienti, pari al 76,00% del campione); il restante 24% dei pazienti è affetto da BPCO grave.
Identificazione e quantificazione delle risorse
Terapie farmacologiche ed ossigenoterapia
La maggioranza delle terapie farmacologiche è somministrata per finalità di mantenimento della BPCO (Tabella 3; Figura 1).
Nonostante il 76% del campione presenti BPCO moderata, per la quale la terapia di combinazione con tre molecole non era indicata né al momento dell’arruolamento, né secondo le linee-guida internazionali relative alla gestione del paziente affetto da BPCO (Global Initiative for Chronic Obstructive Lung Disease, 2017), l’IM permette di apprezzare che l’associazione estemporanea di ICS/LABA/LAMA rappresenta lo schema di trattamento farmacologico maggiormente prescritto (108 pazienti, pari al 28,13% del campione), con una durata media della terapia che raggiunge 90,12 giorni (DS: 4,06) (Tabella 3).
Gli schemi di trattamento farmacologico al bisogno sono caratterizzati da dati completi e comprendono SAMA (1 paziente, pari allo 0,26% del campione) e SAMA/SABA (2 pazienti, pari allo 0,52% del campione); per entrambe, la durata media della terapia è pari a 91,31 giorni (cioè ad un trimestre). I rimanenti schemi di trattamento farmacologico presentano dati MAR (
Infine, tra le variabili originariamente caratterizzate da dati incompleti, si riscontra il ricorso all’ossigenoterapia (60 pazienti, pari al 15,63 del campione), con consumo medio di 158.630,70 litri di ossigeno (DS: 123.728,70) e durata media di 89,74 giorni (DS: 7,20) (Tabella 4).
Risorse sanitarie diverse da terapie farmacologiche ed ossigenoterapia
Tra le variabili con dati completi, il maggiore consumo di risorse sanitarie (24 pazienti, pari al 6,25% del campione) si registra per visite specialistiche ambulatoriali (media per paziente: 0,07; DS: 0,26) ed accertamenti laboratoristici, strumentali e per immagini (media per paziente: 0,32; DS: 1,57), mentre gli accessi in PS non risultano utilizzati da alcun paziente (Tabella 4).
L’esigenza di ricovero, in regime ordinario (8 pazienti, pari al 2,08% del campione) o diurno (6 pazienti, pari all’1,57% del campione), unicamente per riabilitazione respiratoria, risulta contenuta (14 pazienti, pari al 3,65% del campione).
Le restanti variabili relative al consumo di risorse sanitarie presentano una proporzione di dati MCAR (
Valorizzazione delle risorse e descrizione dei costi
Con riferimento alla CCA, la differenza tra i costi medi trimestrali riportati dai pazienti aventi almeno un dato incompleto (187 pazienti, pari al 48,69% del campione; €191,30; DS: €356,86) rispetto a quanti avessero la totalità dei dati completi (197 pazienti, pari al 51,31% del campione; €458,90; DS: €638,85), raggiunge la significatività statistica (
Descrizione dei costi trimestrali BPCO (€2017).
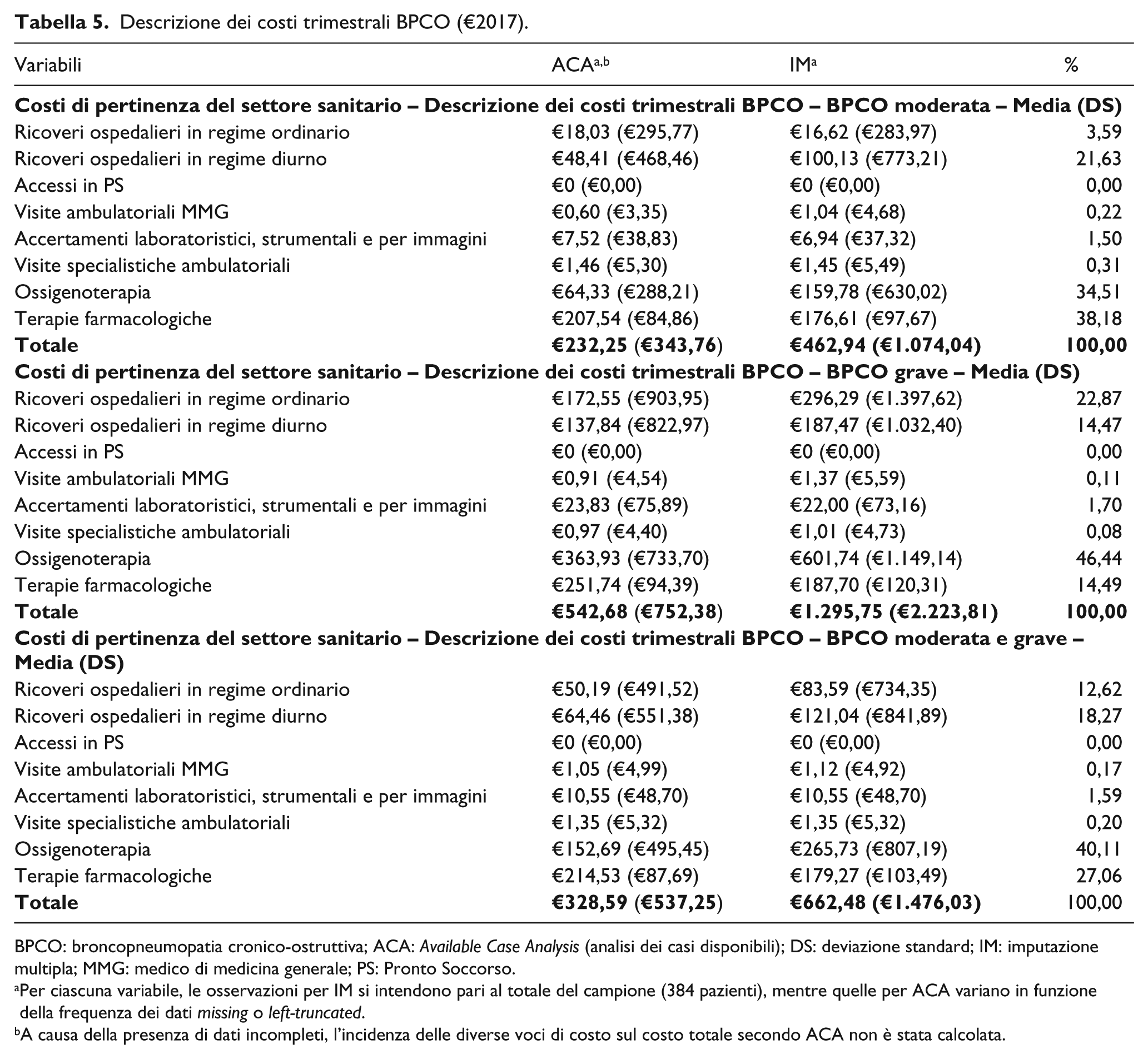
BPCO: broncopneumopatia cronico-ostruttiva; ACA:
Per ciascuna variabile, le osservazioni per IM si intendono pari al totale del campione (384 pazienti), mentre quelle per ACA variano in funzione della frequenza dei dati
A causa della presenza di dati incompleti, l’incidenza delle diverse voci di costo sul costo totale secondo ACA non è stata calcolata.
La differenza tra il costo medio trimestrale totalizzato da pazienti con BPCO grave o moderata è pari a +179,90% (€1.295,75 vs €462,94).
Terapie farmacologiche ed ossigenoterapia
L’IM consente di apprezzare che, nel corso del trimestre di osservazione, la terapia farmacologica con SABA registra il minor costo medio per paziente, pari ad €2,08 (DS: €1,15) (Figura 1).
I costi medi relativi alla somministrazione dei farmaci (€2,99; DS: €11,35) si verificano solo per la miscellanea di principi attivi raccolti nella categoria Altro, che, aggiunti al costo medio di tali farmaci (€58,59; DS: €149,14), generano un costo medio trimestrale per tale gruppo di molecole pari ad €61,58 (DS: €159,79).
Complessivamente, il costo medio dei principi attivi è pari ad €178,64 (DS: €102,94), mentre il costo medio per la somministrazione dei medesimi, alla determinazione del quale partecipano anche gli schemi di trattamento diversi dalla categoria Altro, i quali, non prevedendo somministrazione per via endovenosa, totalizzano un costo pari a zero, eguaglia €0,47 (DS: €6,25), per un totale pari, in media, ad €179,27 (DS: €103,49) al trimestre; tale importo è superato del 64,57% dal costo medio della sola terapia farmacologica con ICS/LABA/LAMA, pari ad €295,03; (DS: €64,48), la quale presenta i maggiori costi medi per paziente (Tabella 5; Figura 1). Nel campione studiato il costo totale stimato per le terapie farmacologiche è pari ad €68.597,76 al trimestre; si apprezza il differente contributo percentuale di ciascuna classe terapeutica (Figura 2).
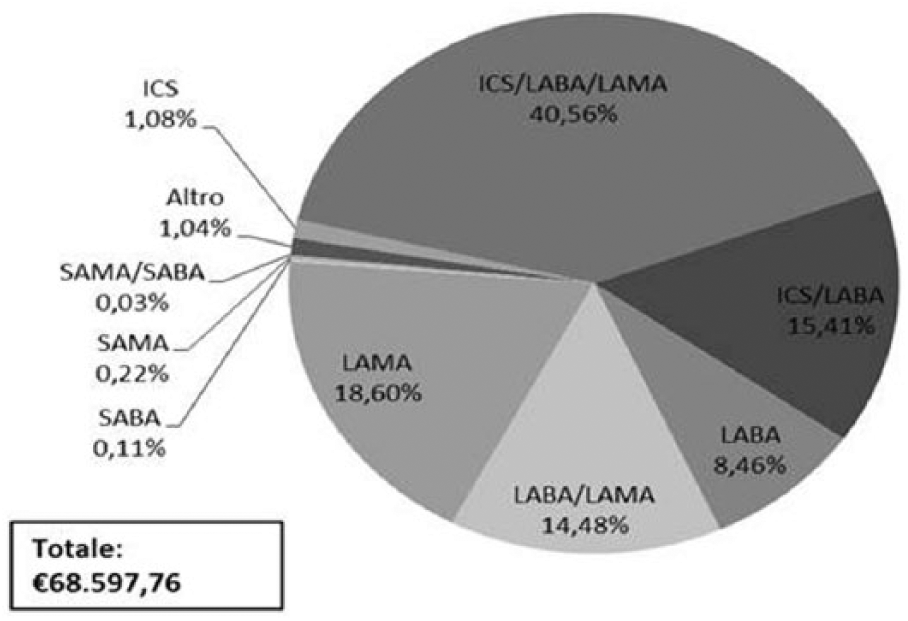
Contributo percentuale alla spesa totale trimestrale per terapie farmacologiche BPCO (€2017)a.
L’ossigenoterapia rappresenta il
Ossigenoterapia e terapie farmacologiche generano una quota pari al 67,17% del costo medio trimestrale della BPCO.
I contributi percentuali delle varie voci di costo di pertinenza del settore sanitario ai costi trimestrali per la BPCO moderata e grave sono riportati graficamente (Figura 3).
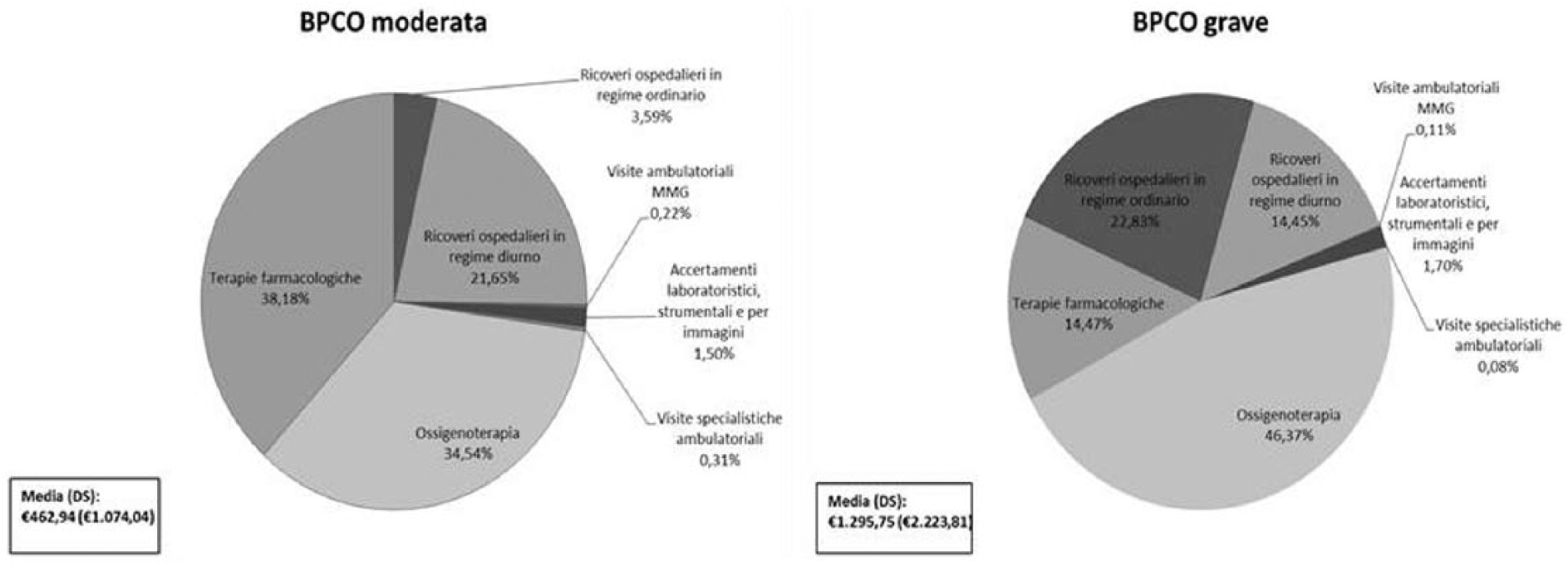
Composizione percentuale dei costi trimestrali BPCO (€2017)a.
Risorse sanitarie diverse da terapie farmacologiche ed ossigenoterapia
La risorsa sanitaria che presenta il costo medio trimestrale più elevato, che eguaglia €121,04 (DS: €841,89) si identifica con i ricoveri ospedalieri in regime diurno (18,27% dell’importo complessivo) (Tabella 5).
La risorsa sanitaria che genera il minore costo medio trimestrale, pari ad €1,12 (DS: €4,92), è rappresentata dalle visite presso l’ambulatorio del MMG (0,17% dell’importo complessivo).
Discussione e conclusioni
Il presente manoscritto ha per oggetto la descrizione retrospettiva dei costi delle risorse sanitarie totalizzati dai pazienti affetti da BPCO moderata o grave in fase stabile nel trimestre antecedente la visita di arruolamento dello studio SAT.
I principali risultati indicano che per la BPCO in fase stabile:
il costo totale trimestrale medio è di €662,48 (DS: €1.476,03) con una differenza tra i costi totalizzati dai pazienti affetti da BPCO grave rispetto ai pazienti con BPCO moderata di +179,90% (€1.295,75 vs €462,94);
il costo medio della terapia farmacologica è di €179,27 (DS: €103,49) al trimestre (27,06% dell’importo complessivo); ICS/LABA/LAMA rappresenta la categoria di farmaci più costosa, pari ad €295,03 (DS: €64,48) (+64,57% del costo medio);
con un valore pari ad €265,73 (DS: €807,19), l’ossigenoterapia (utilizzata dal 15,63% dei pazienti) rappresenta il
La descrizione dei costi presenta un limite.
Sulla scorta di precedenti esperienze di ricerca condotte su altre patologie 50,51, si è scelto di confinare la valutazione economica a un intervallo temporale contenuto, pari ad un trimestre, al fine di minimizzare il rischio di
Vi è tuttavia da osservare che, con riferimento alla descrizione dei costi della BPCO condotta secondo la prospettiva del SSN, un intervallo temporale minore dell’anno, pari ad un semestre, era già stato adottato nella letteratura nazionale. 53
Peraltro, in tale esperienza di ricerca 53 si riportava una differenza tra i costi (semestrali) totalizzati dai pazienti affetti da BPCO grave rispetto ai pazienti con BPCO moderata inferiore a quanto riscontrato nella fase retrospettiva (trimestrale) dello studio SAT (+98,67% vs +179,90%).
Poiché nei tre mesi precedenti l’arruolamento nello studio SAT i pazienti non dovevano avere avuto esacerbazioni di BPCO, la totalità degli episodi di ospedalizzazione registrati nello studio SAT è finalizzata alla riabilitazione respiratoria. Pertanto, il rilevo economico dell’ospedalizzazione in regime ordinario, pari a circa il 31% del costo medio trimestrale, risulta inferiore rispetto a quanto recentemente pubblicato da altri Autori che comprendevano anche i ricoveri per esacerbazione da BPCO, utilizzando la prospettiva del SSN. 7 Queste ultime, infatti, se gravi, impongono il ricovero del paziente in regime ordinario, con conseguente aumento dei costi per il terzo pagante.6–8
Fatto salvo il limite sopra indicato, i risultati elaborati consentono di formulare alcune riflessioni.
Una caratteristica qualificante della descrizione dei costi riportata nel presente manoscritto è l’utilizzo dell’IM per la gestione dei dati incompleti MCAR e MAR, ancorché per statistiche esclusivamente descrittive. Pare interessante notare che l’analisi
Il numero dei centri di arruolamento risulta dissimile nelle macro-aree geografiche relative al Nord (11) ed al Sud del Paese (6), mentre solo 3 sui 20 centri partecipanti allo studio SAT sono ubicati nell’Italia centrale.
Tuttavia, indipendentemente dalla macro-area geografica, la preponderanza del sottosistema ospedaliero pubblico (pari al 90% delle strutture pneumologiche in questione), integrato dalle realtà sanitarie private accreditate, parrebbe indicare una sostanziale uniformità dell’offerta, da parte del SSN, dei processi sanitari necessari al corretto inquadramento e all’appropriata gestione della BPCO.
Con riferimento alle caratteristiche demografiche dei pazienti, il 16,32% di questi ultimi risulta impegnato in attività produttive remunerate dal mercato o realizzate nel contesto domestico.
Pertanto, come peraltro già sottolineato da una precedente esperienza di ricerca sul tema,
53
lo
Per quanto concerne gli accertamenti laboratoristici, strumentali e per immagini, si conferma, come già riportato da altri autori,55,56 un limitato utilizzo della spirometria, riferita dal 4,43% dei 384 pazienti con riferimento ai tre mesi antecedenti all’arruolamento.
Le terapie farmacologiche attive nel trimestre antecedente l’arruolamento nello studio SAT rappresentano il 27,06% del costo medio totale per paziente. Tale proporzione, guidata essenzialmente dalla terapia di combinazione con ICS/LABA/LAMA, appare coerente con quanto riportato da una pregressa esperienza di ricerca italiana. 6
Preme sottolineare come le raccomandazioni
Alla luce di queste considerazioni, riteniamo che sia necessaria una maggiore attenzione dello pneumologo nell’elezione della terapia più appropriata per il paziente, esclusivamente focalizzata sul grado di malattia piuttosto che sull’eventuale schema terapeutico già in essere al momento del primo contatto con lo specialista.
In conclusione, la descrizione dei costi fondata sui dati raccolti in occasione della prima visita dello studio SAT ha consentito di ottenere alcuni risultati preliminari e, soprattutto, di sperimentare alcuni strumenti di ricerca che saranno utilizzati per indagare, nella fase prospettica di questa esperienza di ricerca, i costi medi annuali di pertinenza del SSN totalizzati dal paziente affetto da BPCO moderata o grave nel nostro Paese.
Supplemental Material
Supplementary_Material – Supplemental material for Cost-description and multiple imputation of missing values: the SATisfaction and adherence to COPD treatment (SAT) study
Supplemental material, Supplementary_Material for Cost-description and multiple imputation of missing values: the SATisfaction and adherence to COPD treatment (SAT) study by Carlo Lazzaro, Fabiano Di Marco, Nicola Scichilone, Fulvio Braido, Marco Contoli, Paola Rogliani, Pierachille Santus, Valentina Acciai, Carla Scognamillo, Irene Olivi and Angelo Guido Corsico in Global & Regional Health Technology Assessment
Footnotes
References
Supplementary Material
Please find the following supplemental material available below.
For Open Access articles published under a Creative Commons License, all supplemental material carries the same license as the article it is associated with.
For non-Open Access articles published, all supplemental material carries a non-exclusive license, and permission requests for re-use of supplemental material or any part of supplemental material shall be sent directly to the copyright owner as specified in the copyright notice associated with the article.
