Abstract
The exploitation of urban habitats by mosquitoes species contributes to the epidemiological risk of transmission of emerging and re-emerging tropical diseases, indicating the need to establish fast and effective procedures than enable the taxonomic identification of species of interest to public health. DNA-barcode methodology uses sequences of mitochondrial cytochrome c oxidase I genes for the identification of a wide range of animal species and is an alternative evaluation tool for important groups of tropical medical importance. In this study, entomological samplings were performed at breeding sites of urban areas in Armenia and Circasia (Quindío-Colombia) in order to identify the morphology of mosquito larvae and to assess DNA-barcodes. Fifty-six (56) DNA-barcode sequences were obtained for immatures of the Aedes (Stegomyia) aegypti, Culex (Culex) quinquefasciatus, Cx. (Phenacomyia) corniger, Cx. (Culex) nigripalpus, and Cx. (Culex) Coronator groups and estimates of genetic diversity, intra/inter-species genetic distances, and neighbor-joining dendrograms were found. The results allowed for the taxonomic identification of mosquitoes and the separation of potentially useful molecular markers within the genetics of these populations: however, for species belonging to the Culex-Coronator group, the molecular markers had insufficient information for the taxonomic separation of species. Epidemiologically, urban mosquitoes identified have been implicated in the past in the transmission of emerging and re-emerging alphavirus and flavivirus of interest to Colombian public health. Thus, the use of DNA-barcoding may be useful in ecological studies in urban areas and in the epidemiological surveillance of emerging pathogens.
Introducción
La familia Culicidae comprende alrededor de 3.490 especies reconocidas en diversos ecosistemas y regiones biogeográfi-cas (Harbach y Howard 2007) de las cuales aproximadamente 150, pertenecientes a los géneros Anopheles (Meigen), Aedes (Meigen) y Culex (Linnaeus), son responsables de la trans-misión vectorial de virus, bacterias, helmintos y protozoos de importancia en salud pública humana y veterinaria (Gubler 2002; Harbach 2007). En Colombia, la presencia de protozo-os y virus transmitidos por insectos, genera un interés en la diversidad de mosquitos presentes en focos activos de trans-misión para patógenos emergentes y re-emergentes, donde la identificación de especies se considera el primer paso en la incriminación, vigilancia y control de estas enfermedades de transmisión vectorial (Krzywinski 2003; Cywinska et al. 2006; Ondrejicka 2014). Sin embargo, la identificación de mosquitos, es principalmente realizada con caracteres morfológicos que frecuentemente sufren daños o alteraciones durante el proceso de colecta, almacenamiento y transporte o, probablemente, no se encuentran en todos los estados del ciclo de vida (Wang et al. 2012). Además durante los muestreos entomológicos, por lo general se capturan pocos machos para la confirmación de especies y una alta cantidad de hembras adultas cuyos carac-teres diagnósticos varían sutilmente y solo pueden ser reco-nocidos por taxónomos experimentados o no se encuentran disponibles atributos para la diferenciación taxonómica. La si-milaridad morfológica dificulta el proceso de identificación de especies, particularmente en grupos que presentan complejos de especies crípticas (Krzywinski 2003; Cywinska et al. 2006; Kumar et al. 2007; Taira et al. 2012; Wang et al. 2012; Versteirt et al. 2014). En este sentido, un acercamiento multidis-ciplinario e integrativo a la taxonomía de mosquitos vectores que incluya caracteres morfológicos, moleculares y ecológi-cos (Schlick-Steiner et al. 2010), es necesario para agilizar la identificación a nivel de especie (Besansky et al. 2003).
El uso de secuencias de ADN ha sido propuesto como base fundamental en la clasificación biológica (Tautz et al. 2003) y como herramienta analitica para el reconocimiento e identificación de especies en grupos particularmente com-plejos (Besansky et al. 2003). Una alternativa metodológica propuesta por Hebert et al. (2003), involucra el análisis de secuencias de un fragmento del gen citocromo c oxidasa I (COI) que sirve para la discriminación de especies de dificil separación morfológica (Besansky et al. 2003; Ondrejicka et al. 2014) y constituye un sistema de bio-identificación por códigos de barras o "DNA barcode" (Valentini 2008). La ini-ciativa ha sido evaluada en diferentes insectos vectores con resultados significativamente exitosos en la separación de es-pecies presentes en zonas activas de transmisión de enferme-dades y en dípteros como Simuliidae (Rivera y Currie 2009), Phlebotominae (Azpurua et al. 2010; Hoyos et al. 2012a; Ku-mar et al. 2012; Contreras et al. 2014), Tabanidae (Cywinska et al. 2010) y Calliphoridae (Solano et al. 2013). En mosqui-tos hay un evidente progreso en la tipificación molecular de especies epidemiológicamente importantes en diversas zonas geográficas de países como Canadá (Cywinska et al. 2006), India (Kumar et al. 2007), Bélgica (Versteirt et al. 2014), Pakistán (Ashfaq et al. 2014), Argentina (Díaz-Nieto et al. 2013), Japón (Taira et al. 2012), Ecuador (Linton et al. 2013) y China (Wang et al. 2012). Este método también ha sido usa-do en la separación de complejos de especies (Rosero et al. 2012; Kumar et al. 2013; Moreno et al. 2013), identificación de potenciales vectores de arbovirus (Golding et al. 2012) y en taxonomía integrativa (Ruiz et al. 2010; Ruiz et al. 2012; Laurito et al. 2013).
Colombia presenta amplias áreas geográficas activas para la transmisión de enfermedades tropicales que involucran mosquitos, entre ellas malaria, dengue, fiebre amarilla, ence-falitis equina venezolana, varios arbovirus de baja circulación (mayaro, Ilheus, Oropouche, bussuquara, guaroa, guama) y recientemente chikungunya (Tinker y Olano 1993; Groot et al. 1996; Rodríguez et al. 1995; Rivas et al. 1995; Ferro et al. 2003; Mattar et al. 2005; Montoya-Lerma et al. 2011; González y Mattar 2015). Algunas de estas patologías tropicales se encuentran presentes en zonas peri-urbanas y urbanas por la adaptación y colonización de mosquitos a hábitats artificia-les en ecosistemas humanos, cambio climático, la actividad antropogénica en la fragmentación de ecosistemas naturales y el consecuente cambio en la estructura y composición de las comunidades de mosquitos (Gubler 2002; Yanoviak et al. 2006; Jones et al. 2008; Keesing et al. 2010; Jinbo et al. 2011; Hoyos et al. 2012).
La identificación taxonómica permite además determinar aspectos como la transmisión trans-ovárica, la identificación de hábitats y criaderos en remanentes urbanos de vegetación nativa y/o artificial favorecen la colonización de mosquitos vectores en zonas residenciales con alta densidad poblacio-nal humana, cobrando alta relevancia en el manejo y control de enfermedades emergentes y re-emergentes, así como en términos de vigilancia entomológica para identificar posibles re-colonizaciones y re-emergencia de micro-organismos pa-tógenos (Parra et al. 2012; Hoyos et al. 2012). En nuestro estudio, evaluamos el fragmento códigos de barras del gen citocromo c oxidasa I en estadios inmaduros de mosquitos colectados en áreas urbanas de los municipios de Armenia y Circasia del departamento de Quindío para evaluar su utili-dad en la vigilancia entomológica y el riesgo epidemiológico en la transmisión de protozoos, bacterias y virus.
Materiales y métodos
Obtención de especímenes.
Los inmaduros de culícidos fueron recolectados en salidas de vigilancia entomológica en compañía con la Secretaría de Salud Departamental en septiembre y octubre de 2013 en áreas urbanas de los mu-nicipios de Armenia (4°32′20″N, 75°40′21″O) y Circasia (4°37′09″N, 75°38′05″O) del departamento de Quindío. Para el muestreo se siguió el método de búsqueda de Belkin et al. (1969) y los inmaduros fueron capturados, con una pi-peta plástica, en criaderos artificiales asociados a viviendas humanas y colocados en recipientes previamente codificados para el transporte de los culícidos al Centro de Investigacio-nes Biomédicas (CIBM) de la Universidad del Quindio para su seguimiento. Larvas en estadío IV (L4) fueron separadas y guardadas en etanol absoluto y enviadas al laboratorio de Medicina Molecular y Translación de la Universidad de An-tioquia. Previo al procesamiento con los protocolos molecu-lares, las larvas L₄ fueron identificadas considerando género y características morfológicas externas con claves dicotómi-cas (Lane 1953; Cova-García et al. 1966; Bram 1967; Forattini 2002; González y Carrejo 2007). Pupas perdidas por mortalidad fueron usadas para verificar la utilidad del código de barras en la identificación taxonómica de especie.
Protocolos moleculares.
Las extracciones de ADN fueron realizadas con el kit DNeasy Blood & Tissue kit (Qiagen, Maryland) y la amplificación del fragmento "DNA barcode" de ~700 pb del gen mitocondrial citocromo oxidasa I fue lo-grada mediante los oligonucleótidos LCO-1490/HCO-2198 y MTNF/MTNR (Folmer et al. 1994; Hebert et al. 2003; Kumar et al. 2007). Cada mix-PCR contenia un amortiguador 1x de NHSO₄, 1 mM de cada DNTP, 5 mM de MgCl₂, 0,5 µM de oligonucleótidos cebadores, 0,4 U de taq polimerasa (Bio-line, Maryland), 4 µL de ADN y volumen final de 50 µL. Los parámetros de amplificación en el termociclador Multigene (Labnet, New Jersey) incluyeron: un ciclo de 94 °C por 10 min, seguido de 35 ciclos de la siguiente forma: 95 °C por 60 s, 50 °C por 60 s y 72 °C por 60 s, una extensión final a 72 °C por 5 min y preservación a 4 °C. Los productos de PCR fueron visualizados en gel de agarosa (1%) con tinción GELSTAR® (Lonza, Rockland) diluido 1/50 y el lector Dark Reader (IMGEN, Alexandria). Los productos de PCR positi-vos fueron secuenciados mediante los cebadores de amplifi-cación previamente usados en Macrogen (Seul, Corea).
Análisis de datos.
Las secuencias fueron editadas manual-mente en el software Bioeditv7.2.0 (Hall 1999) (http://www.mbio.ncsu.edu/BioEdit/bioedit.htm) y los consensos en for-mato fasta fueron alineados en ClustalW (Larkin et al. 2007). Las distancias genéticas fueron estimadas en MEGAv6.0 (Tamura et al. 2013) usando el modelo Kimura 2-parámetros (K2P) (Kimura 1980), y las unidades taxonómicas molecula-res operacionales (MOTUs) fueron identificadas de acuerdo a las distancias genéticas intra e inter-especie calculadas y de acuerdo a agrupaciones dentro de un dendrograma inferido por el algoritmo de "neighbor-joining" (NJ) (Saitou y Nei 1987) (modelo K2P, "bootstrap" = 1.000 réplicas) (Felsenstein 1982). Se estimaron parámetros de diversidad genética como número de sitios polimórficos, número de haplotipos, diversidad haplotípica, diversidad nucleotídica y prueba de neutralidad de Tajima con el software DNAspv5.0 (Librado y Rozas 2009).
Resultados
Cinco especies fueron identificadas: Aedes (Stegomyia) ae-gypti, Culex (Culex) quinquefasciatus, Cx. (Phenacomyia) corniger, Cx. (Culex) nigripalpus y Cx. (Culex) grupo Co-ronator. Este último grupo no fue identificado al nivel de especie por varias razones: la similaridad morfológica de los estadios inmaduros, la dificultad de separar morfológi-camente especies en las hembras adultas que emergen de los mismos criaderos y la ausencia de machos en estos criaderos para realizar disecciones de genitalia y obtener caracteres que permitan una identificación exitosa a nivel de especie. 56 es-pecimenes fueron seleccionados para la extracción de ADN, amplificación por PCR del gen COI - fragmento "DNA bar-code", secuenciación y registro en GenBank (Tabla 1).
Las secuencias obtenidas presentan una longitud de 695 nt, con excepción de las pertenecientes a Cx. nigripalpus (576 pb), y corresponden a las posiciones 1541 a 2201 del gen mitocondrial citocromo oxidasa I (secuencia de referen-cia en GenBank EU352212.1 de COI - Aedes aegypti), región consecuente con la ubicación del fragmento código de barras (posiciones 1498 - 2198) (Hebert et al. 2003); no se eviden-ciaron eventos de inserción-deleción, en las secuencias anali-zadas o la presencia de codones de parada, característica pro-pia de copias nucleares de genes mitocondriales (NUMT's) (Black IV y Bernhardt 2009).
Datos de colecta de las especies de mosquitos identificados y evaluados para el código de barras de ADN. Para cada secuencia caracterizada se da el código de acceso a GenBank.
Un total de 56 secuencias COI - DNA barcode (10 ha-plotipos) pertenecientes a cinco especies de dos géneros de Culicidae fueron obtenidos y las distancias intra-específicas en individuos de la misma especie o MOTU's fueron bajas (0-0,00924) (Tabla 2). Las distancias genéticas inter-especí-ficas fueron consistentes en el rango registrado entre es-pecies del mismo género para Culex spp. con rangos de 5,9-7,9%, y entre especies de géneros diferentes (12,5-13,7%) (Tabla 3). Sin embargo, la diversidad genética de las cinco especies fue baja en haplotipos, diversidad haplotípica y di-versidad nucleotídica (Tabla 2). La prueba de Tajima fue estadísticamente significativa para Cx. corniger evidencian-do evolución no neutral. La caracterización molecular de COI - barcode para Aedes aegypti permitió obtener secuen-cias para dos poblaciones (Circasia y Armenia), y estimar el índice de estructuración genética (F ST = 0,038) y el flujo de genes (Nm = 12,50) (Hudson, Slatkin y Madison 1992), demostrando un alto intercambio de migrantes y escasa di-ferenciación genética.
Diversidad genética del marcador molecular COI - "DNA barcode" para cinco especies de mosquitos colectados en áreas urbanas de Armenia y Circasia (Quindío, Colombia).
Número de secuencias caracterizadas.
Haplotipos.
Sitios polimórficos.
Diversidad nucleotídica.
Diversidad haplotípica.
No significativo estadísticamente.
Estadísticamente significativo.
La separación de especies de mosquitos por distancias ge-néticas fue confirmada por la agrupación de cinco clusters o
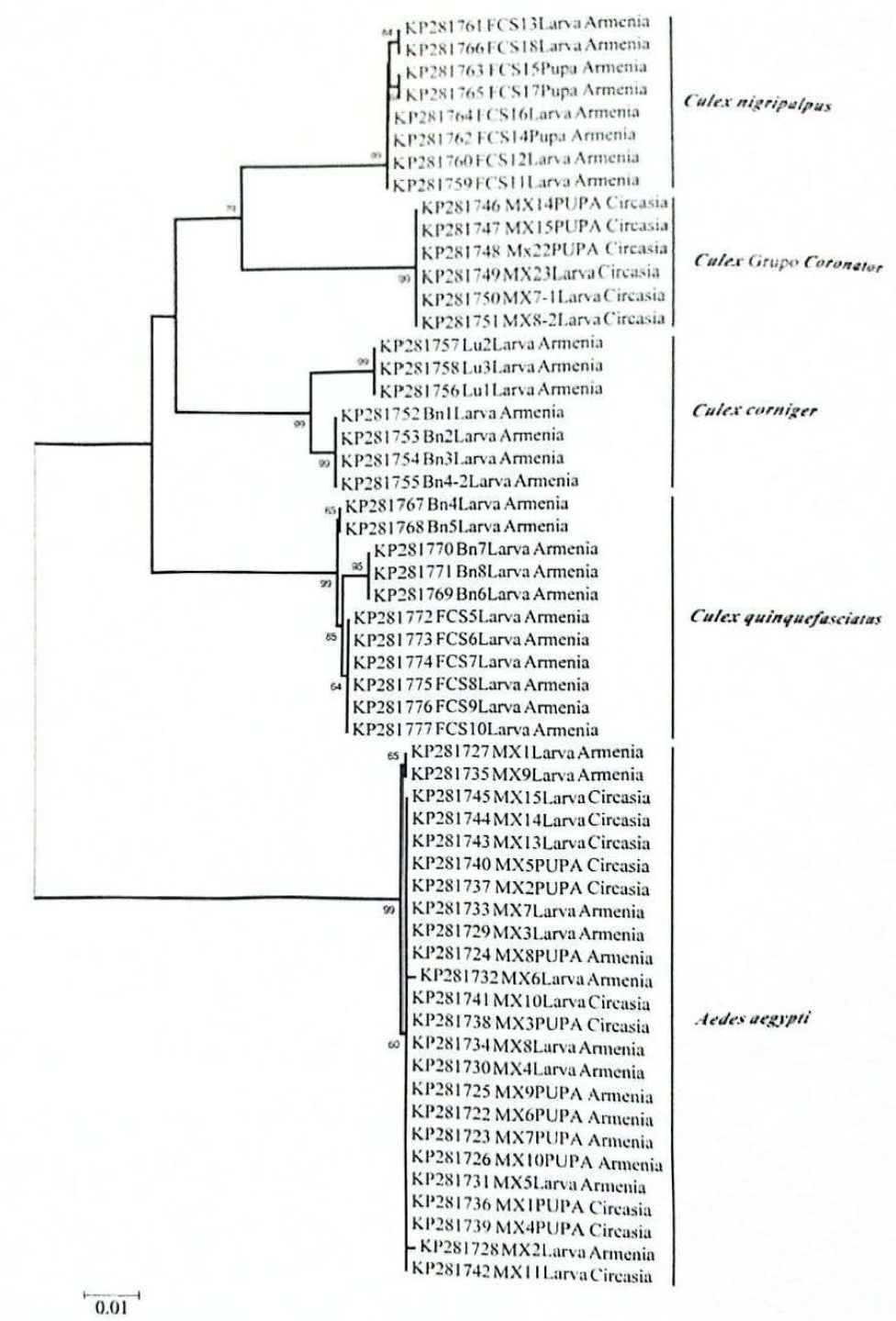
Dendrograma de "neighbor-joining" estimado con secuencias "DNA barcode" (citocromo oxidasa 1) obtenidas a partir de larvas y pupas de cinco especies de mosquitos (Kimura 2-parámetros, "bootstrap" 1.000 réplicas). Los valores en las ramas de los árboles indican el porcentaje de réplicas en que las secuencias se agrupan o constituyen un mismo MOTU por "bootstrap" (valores > 50). El alineamiento final fue de 695 nt con excepción de Cx. nigripalpus (576 nt).
Distancias genéticas entre secuencias "DNA barcode" pertene-cientes a los inmaduros identificados de cinco especies de mosquitos de áreas urbanas de Armenia y Circasia (Quindío, Colombia).
Los números resultados indican distancias genéticas inter-especie y los valores restantes muestran le desviación estándar.
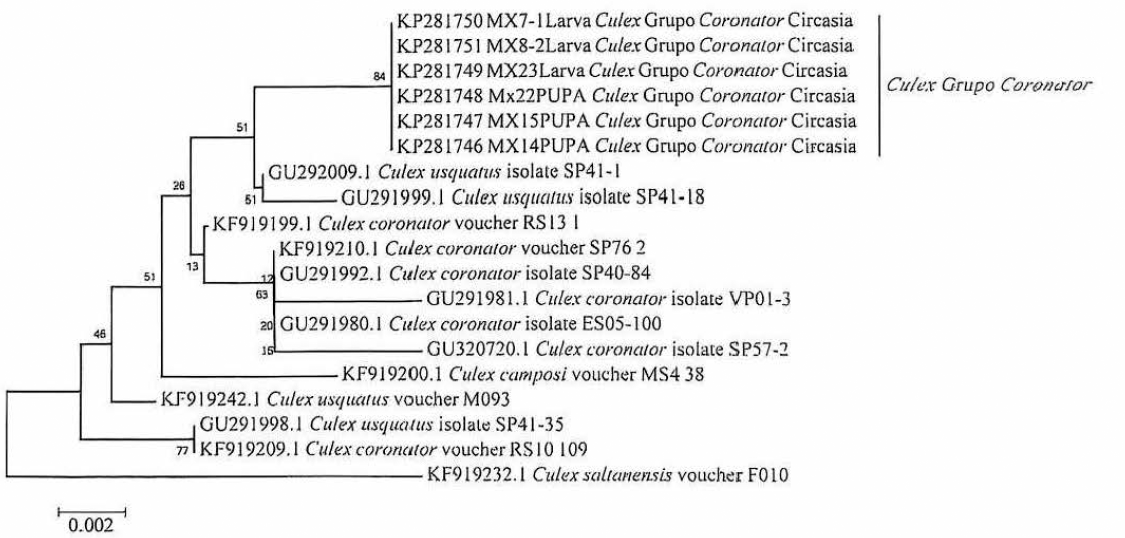
Dendrograma de "neighbor-joining" estimado con secuencias "DNA barcode" (citocromo oxidasa 1) registradas en GenBank para el grupo Coronator (Kimura 2-parámetros, "bootstrap" = 1.000 réplicas). Los valores en las ramas de los árboles indican el número de réplicas en que las secuencias se agrupan o constituyen un mismo MOTU por "bootstrap". El alineamiento final fue de 453 nt. Culex saltanensis del subgrupo Tarsalis (grupo Pipiens) fue tomado como grupo externo según los resultados de Laurito et al. (2013).
Discusión
La colonización de hábitats urbanos por mosquitos de interés médico, constituye una información necesaria para el dise-ño de un esquema de control y prevención de enfermedades infecciosas emergentes y re-emergentes en ecosistemas hu-manos (Hoyos et al. 2012b). No obstante, previamente es ne-cesaria la identificación morfológica de especies de la familia Culicidae, la cual es considerada particularmente problemá-tica por el polimorfismo y solapamiento de caracteres asocia-dos a larvas y hembras adultas (Harbach 2007; Demari-Silva et al. 2011; Laurito et al. 2013); usualmente los caracteres pertenecientes a la genitalia masculina que permiten una identificación más aguda a nivel de especie, están condicio-nados a la colecta de machos, otra dificultad, dado que en los muestreos entomológicos son escasamente colectados. En este sentido. el método "código de barras" o "DNA barcode" fue usado. para evaluar la información genética del fragmen-to de citocromo oxidasa I en la identificación y separación de especics a partir de especímenes inmaduros de mosquitos urbanos, analizar el potencial uso en estudios ecológicos y la relevancia epidemiológica de las especies presentes.
Cinco MOTU's fueron separados por distancias genéticas (K2P) y dendrograma estimado por Neighbor-joining, permi-tiendo diferenciar secuencias pertenecientes a inmaduros co-lectados en zonas urbanas correspondientes a cinco especies identificadas mediante caracteres morfológicos, evidencian-do un patrón de polimorfismos nucleotídicos que posibilita la identificación rápida de mosquitos presentes en hábitats y ecosistemas urbanos. Los resultados del método código de barras en las especies identificadas determinaron un rango intra-especifico de 0 - 0,00316 y 0,059 - 0,137 entre espe-cies; estos valores se encuentran en los rangos intra-especie (0-0,024) e inter-especie (0,022-0,2565) previamente regis-trados para culícidos presentes en diversas áreas geográficas (Cywinska et al. 2006; Kumar et al. 2007; Taira et al. 2012; Wang et al. 2012; Ashfaq et al. 2014).
Aedes aegypti es responsable de la transmisión del virus dengue, el arbovirus más importante en Colombia (Tinker y

Finalmente, la identificación con marcadores moleculares y en especial el método código de barras en mosquitos urbanos, permite establecer posibles riesgos epidemiológicos en la transmisión de enfermedades emergentes y re-emergentes, y en consecuencia establecer los elementos ecológicos que favorecen la presencia de una nueva patologia, teniendo en cuenta la presión antropogénica sobre los ecosistemas naturales, la adaptación de especies resilientes a los cambios del paisaje, los cambios en la estructura y composición de comunidades de insectos hematófagos, el aumento en la frecuencia de contacto humano-vector, los animales domésticos y las poblaciones humanas susceptibles. Además, es clara la necesidad de tipificar molecularmente con códigos de barras a una mayor cantidad de mosquitos en ecosistemas naturales para construir una base de referencia para futuros estudios de biodiversidad, ecología y predicción de nichos que impliquen la transmisión de arbovirus patógenos.
Footnotes
Agradecimientos
A Colciencias por los recursos aprobados para el proyecto 111549326198 “Rastreo de virus emergentes y re-emergentes en mosquitos silvestres de la costa caribe colombiana” y la convocatoria 528 para Becas de Doctorados Nacionales-Colciencias. A los técnicos de vectores de las secretarías de salud de los municipios de Armenia y Circasia por su acompañamiento en las salidas de campo.
