Abstract
Economic evaluation of platelet-rich-plasma versus hyaluronic acid for the treatment of knee osteoarthritis. Scenarios to 1 and 5 years
Purpose
The increasing incidence of total joint arthroplasty reflects the rises of osteoarthritis (OA) prevalence. OA is a degenerative pathology affecting joints with a significant impact on quality of life causing pain, leading to social life limitations and loss of work productivity. According to the World Health Organization, OA is one of the most important causes of people's disability. The burden of the disease is correlated with a huge economic impact on the health care systems. Intra-articular infiltration therapies are used between the pharmacological and the surgical phases, in order to delay surgery. This work aims to carry out an economic evaluation on the use of the Platelet-Rich-Plasma (PRP) therapy in the treatment of knee OA. The comparator is the hyaluronic acid, i.e. the standard therapy for drug-resistant OA that does not benefit or has short term benefits (<1 month) with intra-articular corticosteroids.
Methods
A cost-effectiveness analysis has been performed using a decision-analytic model considering two scenarios: short period and medium period. The effectiveness outcomes are reported in term of quality-adjusted life-years (QALYs), while costs are expressed in euro (€). The adopted perspective is the Italian National Health System (INHS). The results are shown through the incremental cost-effectiveness ratio (ICER) examining the PRP versus the comparator. Moreover, deterministic and probabilistic sensitivity analyses have been performed to test the robustness of the results.
Results
The PRP therapy, for patients with moderate to severe knee OA in the Italian context, is cost-effective versus HA with ICERs of €1,524/QALY in the 1 year and €162/QALY in the 5 year scenarios.
Conclusions
In the short term, it seems that the PRP therapy is cost-effective in the treatment of knee OA versus the HA therapy. However, more research is needed to assess its cost-effectiveness in the long term and to figure out if this treatment may be an efficient resource allocation for the INHS.
Keywords
Introduzione
L'osteoartrosi (OA) è una malattia cronica degenerativa che colpisce le articolazioni ed è correlata a diversi fattori di rischio, tra i quali il genere (le donne sono più predisposte), l'età, il tipo di attività lavorativa, l'obesità (1–3).
Le patologie muscoloscheletriche sono l'ottava causa a livello mondiale, e la quarta nei Paesi occidentali, per anni di vita persi per disabilità (disability-adjusted life-year, DALY). Almeno la metà delle patologie muscoloscheletriche sono attribuibili all'osteoartrosi (4) ed essa risulta essere l'undicesima patologia per peso di contribuzione alla disabilità a livello mondiale su 291 patologie, e trentottesima per DALY (5).
Il carico medico e sociale dell'OA determina un forte impatto economico sui sistemi sanitari (6, 7), in particolare nei Paesi occidentali dove l'incidenza è più elevata. I costi sanitari diretti sono dovuti ai farmaci utilizzati per ridurre il dolore e la limitazione funzionale, esami medici, ricoveri e interventi chirurgici di sostituzione dell'articolazione danneggiata (artroprotesi). I costi indiretti sono rappresentati da perdita di produttività e assenza dal lavoro. Considerando solo i primi costi, o entrambi, è stato stimato che nei Paesi occidentali il costo per la patologia è tra 1% e 2,5% del PIL (prodotto interno lordo) (8). In un recente studio canadese i costi diretti sanitari annuali per persona sono stati stimati in dollari canadesi Can$2.233 all'anno (9), mentre uno studio tedesco, che ha considerato persone inserite in un percorso di cura conservativo, ha stimato il costo medio dovuto alla perdita di produttività in €722 (mediana €217) al mese per persona (10).
Il principale driver dei costi sanitari è l'intervento chirurgico ovvero il punto terminale della storia clinica dell'OA (11). L'incremento dell'incidenza dell'OA, specie a livello di ginocchio e anca, dovuta alla crescita dei fattori di rischio come l'invecchiamento della popolazione e l'obesità, sta comportando un conseguente aumento del numero di interventi di artroprotesi e una crescita continua dei costi legati alla patologia (12, 13).
L'OA in Italia
In Italia l'osteoartrosi risulta essere la settima diagnosi per aggregati clinici di codice (ACC) su 283, per numerosità di dimissioni ospedaliere e degenza media nei ricoveri per acuti in regime ordinario. Le dimissioni ospedaliere per OA sono 127.000 (ICD9CM 2007 - 0203-Osteoartrosi), il 2% del totale con una degenza media di 7,5 giorni (14).
Come in tutti gli altri Paesi occidentali, un fattore di costo particolarmente elevato è il rischio che l'evoluzione della patologia porti all'intervento chirurgico di artroprotesi. In un lavoro sul costo socioeconomico degli interventi di artroprotesi in Italia, Piscitelli et al mostrano la continua crescita negli anni del numero degli interventi e del costo totale (15). Dall'analisi dei dati delle Schede di Dimissione Ospedaliera (SDO), in Italia si effettuano ogni anno circa 170.000 interventi di artroprotesi con una crescita media annua nel periodo 2001-2013 del 4,2%. Per quanto riguarda il solo intervento di artroprotesi al ginocchio (total knee replacement, TKR) gli interventi nel 2013 sono stati circa 65.000, con una crescita media annua del 7,2% negli ultimi 10 anni (nel 2003 erano circa 37.000) (Progetto Registro Italiano Artroprotesi, RIAP) (16). Nel 2005, quando il numero di tali interventi era di circa 40.000 casi, il costo medio per paziente, comprensivo dei costi diretti e perdita di produttività, è stato calcolato in €15.000 (15). Considerando solo i costi diretti dell'intervento, il costo totale stimato è di circa 1 miliardo di euro (15, 17). Questo costo è in continua crescita seguendo il costante incremento degli interventi di artroprotesi.
Il costo dell'intervento chirurgico è sostenuto dal Sistema Sanitario Nazionale (SSN) italiano che fa fatica a gestire e contenere questa crescita di costi. Una delle possibili soluzioni è intervenire sul decorso della patologia in modo da ritardare (o evitare) il ricorso all'intervento chirurgico (18, 19). Come indicato nell'ultimo rapporto ESCEO (European Society for Clinical and Economic Aspects of Osteoporosis and Osteoarthritis), la terapia intra-articolare (i.a.) è consigliata, all'interno del percorso clinico di cura, tra la fase farmacologica e quella chirurgica, proprio con l'intento di ritardare o evitare l'intervento chirurgico (20), così da ridurre il carico della malattia e i relativi costi, incrementando la disponibilità a pagare del sistema sanitario per questo tipo di terapie (21).
Le terapie intra-articolari: PRP e HA
Diversi studi clinici mostrano l'efficacia clinica della terapia i.a. con acido ialuronico (HA) e la maggiore durata nel tempo degli effetti rispetto alle infiltrazioni i.a. di corticosteroidi e l'uso orale di antinfiammatori (FANS) (22–24). Considerando i costi diretti e i costi legati agli effetti collaterali dei FANS è stata inoltre evidenziata la costo-efficacia dell'HA (25). L'HA viene utilizzato da diversi anni ed è considerato uno standard nella cura i.a. dell'OA al ginocchio.
Il plasma arricchito di piastrine (platelet-rich-plasma, PRP) è ottenuto da sangue autologo attraverso un processo specifico che consente di separare la componente piastrinica dalle altre componenti del sangue. Diversi studi confermano l'efficacia clinica del PRP in differenti stadi della patologia OA (26–33).
In alcuni studi comparativi tra HA e PRP, il PRP è risultato maggiormente efficace, nel ridurre la sintomatologia dolorosa e la limitazione funzionale, rispetto all'HA (28, 34–38). I risultati di diverse metanalisi confermano la maggiore efficacia del PRP (39–42).
La valutazione economica oggetto del presente studio sull'OA al ginocchio ha l'obiettivo di comparare le due terapie i.a., il PRP e l'HA, considerato lo standard di cura intra-articolare per i pazienti che non rispondono alla terapia farmacologica tradizionale.
Materiale e metodi
Per valutare la costo-efficacia del trattamento dell'OA al ginocchio con PRP è stato sviluppato un modello decisionale ad albero. L'albero decisionale, insieme al modello markoviano, è uno dei modelli di rappresentazione analitica delle decisioni più usati all'interno delle valutazioni economiche.
Modello decisionale
In questo studio il nodo radice dell'albero rappresenta la scelta tra le due terapie (PRP e HA) per il trattamento dell'OA al ginocchio. Da questa scelta si ramificano i diversi percorsi clinici e di trattamento che i pazienti possono seguire. Per entrambe le terapie il primo nodo divide il percorso circa l'efficacia o la mancata efficacia della terapia. Lo sviluppo dell'albero è riportato nella Figura 1.
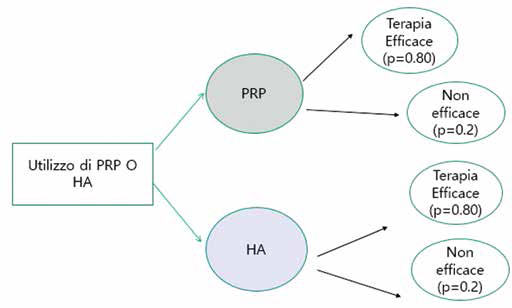
Modello decisionale ad albero con orizzonte temporale a 1 anno. HA = acido ialuronico; PRP = plasma arricchito di piastrine.
Il primo modello è un albero decisionale con orizzonte temporale di 1 anno. Nel nodo radice ci si chiede quale sia la scelta strategica tra l'uso del PRP o dellHA per il trattamento dell'OA al ginocchio. In caso di scelta del PRP si avrà una certa efficacia del trattamento che porterà ai corrispondenti valori di costo ed efficacia. Se il trattamento non è efficace si avranno due diversi valori di costo ed efficacia. Lo sviluppo del ramo per l'HA è analogo, con le stesse probabilità di efficacia del PRP.
È stato inoltre sviluppato un secondo modello con orizzonte temporale a 5 anni (Fig. 2) con le seguenti assunzioni: se la terapia è efficace il paziente può essere trattato solo con le infiltrazioni, oppure nel caso entro alcuni anni (cinque) la terapia non fosse più efficace, il paziente eseguirà un intervento chirurgico di TKR. Nel caso la terapia non risultasse efficace fin dai primi trattamenti, entro 1 anno dal primo ciclo di terapia infiltrativa il paziente sarà sottoposto all'intervento chirurgico, o per una parte dei casi non verrà effettuato alcun intervento chirurgico e si procederà ad altre cure conservative (alcuni pazienti non possono essere operati per motivi legati allo stato di salute, es. diabetici). La struttura dei percorsi delle due terapie è identica, ma sono presenti delle variazioni nei valori dei parametri di probabilità, costo ed efficacia. Non si è tenuto conto della possibilità di un utilizzo del PRP in seguito all'uso dell'HA o viceversa, in quanto ai fini della valutazione avrebbe avuto una scarsa incidenza sul risultato finale. Nel modello con orizzonte temporale a 5 anni, i valori di costo ed efficacia sono stati scontati a un tasso del 3% annuo, come da indicazioni delle linee guida nazionali HTA.
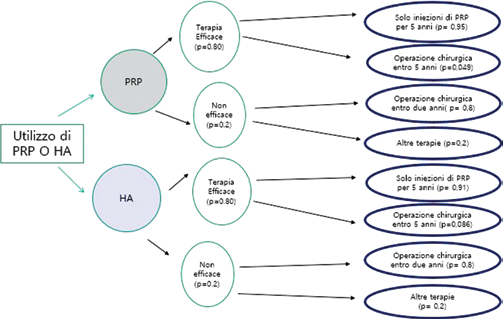
Modello decisionale ad albero con orizzonte temporale a 5 anni. HA = acido ialuronico; PRP = plasma arricchito di piastrine.
Nel valutare la costo-efficacia dei due modelli si è deciso di impiegare sia la soglia utilizzata in letteratura per l'Italia sia un approccio più conservativo. In Italia la soglia rispetto alla disponibilità a pagare (willingness to pay, WTP) varia da €25.000 a €40.000 per QALY guadagnato (43), ma un valore di €30.000 è comunemente accettato (44). Inoltre i risultati sono stati analizzati per diverse soglie di WTP, in particolare è stata utilizzata un'ipotetica soglia di €10.000 adottando la prospettiva di alcuni lavori che evidenziano diverse disponibilità a pagare per ridurre il dolore della patologia OA (45, 46).
Parametri del modello
Costi
Utilizzando la prospettiva del SSN, i costi sono direttamente collegati alle procedure analizzate e al costo dei prodotti e del personale impiegato.
Tramite interviste ai medici e ai direttori dei centri trasfusionali delle ULSS (Unità locale socio sanitaria) del Veneto è stato calcolato il costo al minuto dei professionisti coinvolti nel processo (dirigente medico ematologo e ortopedico).
Esistono diverse tipologie di HA utilizzate che hanno diverse caratteristiche di viscosità, concentrazione, volume e prezzo. Data la vasta gamma di prodotti, sulla base delle informazioni disponibili sul numero di iniezioni i.a. consigliate sulla scheda informativa di ciascuno, è stato calcolato il prezzo medio al pubblico per ciclo terapeutico (47). Nell'ottica del SSN i prezzi al pubblico sono stati scontati del 50% per ottenere un valore analogo a quello presentato dalle aziende private al settore pubblico. Il costo medio per ciclo terapeutico per struttura pubblica è risultato pertanto essere di €82,62, con deviazione standard di €16,4 (IC 95%: €116,2-49).
Il costo del trattamento PRP non dipende dal preparato in sé (sangue autologo), ma è condizionato dal processo di produzione. Rispetto all'HA, il PRP presenta costi di processo e tempi di preparazione più elevati. Oltre ai tempi dell'infiltrazione stimati in 2 minuti e comuni a tutte e due le terapie, la produzione del PRP prevede una fase di preparazione di circa 9 minuti con presenza di un dirigente medico ematologo come da normativa vigente sull'elaborazione di emocomponenti. L'HA richiede solo il tempo di infiltrazione.
Per quanto riguarda il dispositivo medico necessario per produrre il PRP, si è fatto riferimento al RegenKit BCT-1 (Regenlab®), per il quale esiste il prezzo direttamente applicato a un'azienda sanitaria, l'Area Vasta Centro della Regione Toscana (48), pari a €40 per i.a.
Il kit BCT-1, la cui validità e sicurezza è stata dimostrata in uno studio clinico sull'uso del PRP i.a. nel trattamento dell'OA al ginocchio (33), consente la preparazione di un PRP pronto all'uso. La procedura prevede il prelievo dal paziente di circa 8 ml di sangue venoso. Il sangue viene inserito nella provetta, dove è presente dell'anticoagulante e un gel separatore. La provetta viene sottoposta a centrifugazione alla velocità di 1500 g (3400 rpm) per 5 minuti, il che consente di separare i globuli rossi (sotto il gel) dal plasma impoverito di piastrine (PPP) e il PRP (sopra il gel). Capovolgendo dolcemente e più volte la provetta BCT-1 si procede alla risospensione degli elementi cellulari nel surnatante e si ottiene il PRP (circa 4 ml), che può quindi essere prelevato mediante siringa sterile e infiltrato nell'articolazione del paziente (30, 49).
Il numero di iniezioni i.a. di PRP considerato per un ciclo terapeutico è stato di tre come riportato da recenti metanalisi (39, 40, 42).
Per il costo dell'intervento chirurgico si è utilizzato il valore del DRG di riferimento a livello nazionale più il costo della riabilitazione motoria.
Nella Tabella I sono riportati i costi sanitari diretti.
Costi sanitari diretti (€) e dati di efficacia in QALY utilizzati nell'analisi: caso base e input per analisi di sensibilità deterministica e probabilistica
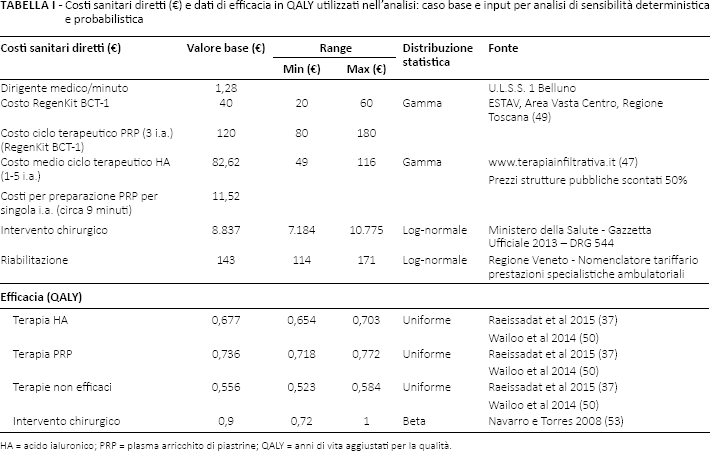
HA = acido ialuronico; PRP = plasma arricchito di piastrine; QALY = anni di vita aggiustati per la qualità.
Dati di efficacia clinica e derivazione della misura di utilità
I lavori presenti in letteratura riportano i dati di efficacia in termini di WOMAC (Mc Master University Arthritis Index).
Le misure di outcome specifiche per una patologia, come la scala WOMAC per l'osteoartrosi, sono scale molto sensibili ai cambiamenti nelle condizioni dei pazienti e misurano accuratamente le variazioni dell'efficacia di diversi trattamenti, ma hanno lo svantaggio di non essere generalizzabili al di fuori del contesto della patologia specifica. Dall'altro lato i profili generali di salute sono meno sensibili, ma permettono l'analisi e il confronto tra diverse patologie. Esistono diversi strumenti utilizzati per misurare i profili generali di salute: l'EuroQol (EQ)-5D, il Short Form 6D (SF-6D) e l’Health Utilities Index (HUI). Essi individuano una serie di stati di salute e a ognuno assegnano un valore che rappresenta la preferenza per quello stato. A ogni stato di salute viene assegnato un peso (health-related quality of life, HRQoL) che può andare da 0 (morte) a 1 (perfetta salute); esistono anche valori negativi nel caso in cui lo stato di salute sia considerato peggiore della morte. È pratica condivisa l'utilizzo dei QALY (misura di outcome di salute) nelle valutazioni economiche. Per ottenere i QALY, i pesi per ogni stato di salute vengono moltiplicati per gli anni vissuti in quel dato stato di salute. In sintesi, i QALY misurano il numero di anni vissuti pesati per la qualità della vita e permettono confronti anche al di fuori del contesto della patologia specifica. Attraverso l'utilizzo di tecniche di mappatura è possibile trasformare i punteggi WOMAC in pesi HRQoL. Nel presente lavoro, per ottenere la trasformazione è stata utilizzata la procedura di conversione proposta da Wailoo et al (50). Il metodo utilizza un modello di regressione multipla derivato da uno studio in cui i pazienti dichiaravano il loro stato di salute sia in WOMAC che in EQ-5D. Il modello stima il peso HRQol utilizzando le variabili demografiche e le sottoscale del punteggio WOMAC, ovvero dolore, rigidità e funzionalità. La presenza di queste sottodimensioni è necessaria per effettuare la trasformazione. In letteratura, e in particolare nei lavori selezionati dalle metanalisi (37–50), soltanto due lavori riportano le informazioni necessarie. Il paper utilizzato per la trasformazione è stato scelto perché meno favorevole al PRP. I dati di QALY ottenuti forniscono così una differenza di efficacia tra le due terapie, in linea con la letteratura internazionale (25, 31–38) (Tab. I). Le analisi di sensibilità deterministica e probabilistica sono state implementate tenendo conto dei dati di tutta la letteratura. In particolare, la scelta della distribuzione uniforme per i valori di efficacia aiuta a modellare la relativa incertezza sull'efficacia delle due terapie, tenendo conto che la maggiore efficacia del PRP rispetto all'HA non è ancora stata sancita in maniera definitiva.
Valori di probabilità
L'efficacia clinica in termini di pazienti responder ai trattamenti i.a. con PRP e HA negli studi clinici ha mostrato una variabilità che va dal 70% al 90% per entrambi i trattamenti (19–29). Nel caso base si è scelto di assegnare le stesse probabilità di efficacia dell’80% alle due terapie, mentre nelle analisi di sensibilità si è fatto variare nel range 70-90%.
Nel modello a 5 anni le probabilità di andare incontro a intervento chirurgico di TKR sono state derivate dall'incidenza annuale di TKR, calcolata stimando la popolazione con OA al ginocchio in Italia nel 2015 (prevalenza 5,39% (51)) e il numero di interventi di artroprotesi al ginocchio rilevato nelle SDO 2013 (65.000). L'incidenza annuale di interventi di artroprotesi al ginocchio, nella popolazione affetta da OA, risulta essere pari all’1,98%. Considerando che l'OA è una patologia degenerativa progressiva, la possibilità di avere una terapia in grado di rallentare la progressione della malattia può di conseguenza ritardare il ricorso finale all'intervento chirurgico. È stato mostrato che lo stesso HA, costo-efficace rispetto ad antinfiammatori e analgesici (22), ritarda l'intervento chirurgico rispetto a chi ha ricevuto una cura convenzionale (18). Essendosi evidenziato negli studi clinici che il PRP risulta più efficace dell'HA (34–42), si è ipotizzato che esso sia in grado di ridurre l'incidenza di TKR (fissando tale valore ipotetico all’1,2%). Questa assunzione è stata oggetto di analisi di sensibilità per capire come potesse influenzare la valutazione economica della terapia.
Per rappresentare la probabilità cumulata che entro un determinato numero di anni ci sia la possibilità che il paziente vada a operazione chirurgica è stata utilizzata la funzione di ripartizione della distribuzione geometrica, del tipo:
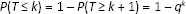
dove P, probabilità che si verifichi l'evento TKR; q = 1 – P, probabilità che non si ricorra a TKR; k, numero di anni; P (T<k), probabilità che si verifichi l'evento T entro k anni.
Ad esempio, nel ramo in cui PRP è efficace, la probabilità annuale di ricorrere a TKR è dell’1,2% e viene trasformata attraverso la funzione per rappresentare la probabilità che entro 5 anni avvenga l'operazione chirurgica (5,8%, e 9,5% per il ramo HA).
Analisi di sensibilità
Per verificare la robustezza dei risultati e tenere in considerazione l'incertezza e la variabilità dei valori in alcuni parametri, sono state eseguite analisi di sensibilità deterministica e probabilistica. Nella prima si sono utilizzati i valori massimi e minimi per ogni parametro. Nella seconda è stata assegnata una distribuzione che modellasse il comportamento reale dei parametri. Per quanto riguarda l'efficacia delle terapie, si è scelta la distribuzione uniforme per modellare la relativa incertezza che abbiamo riscontrato nei vari lavori sull'efficacia delle due terapie. Le distribuzioni beta e gamma sono state modellate per l'efficacia dell'operazione e per i costi delle terapie. Per i costi del TKR si è scelta la distribuzione log-normale per inserire la possibilità di avere alcuni valori massimi distanti dalla media, in modo da modellare l'eventualità di complicanze nella procedura chirurgica (52).
Risultati
Modello con orizzonte temporale a 1 anno
Nessuna delle due terapie domina l'altra. Il costo medio per QALY è rispettivamente €127,1 per HA ed €220,8 per PRP. L'efficacia incrementale del PRP è di 0,0472 QALY con un costo incrementale di €71,94. Il rapporto incrementale di costo efficacia (incremental cost-effectiveness ratio, ICER) tra le due terapie è di €1.524 /QALY.
Nell'analisi tornado (Fig. 3) sono state riassunte le analisi di sensibilità deterministiche a una via, che hanno valutato le variazioni di alcuni parametri del modello. L'analisi effettuata mostra che l'ICER calcolato è maggiormente sensibile rispetto al costo del kit per ottenere il PRP e al numero di iniezioni. Come si può osservare, nessuna variabile sposta in modo significativo il valore dell'ICER. Nella Tabella II sono raccolte le analisi a una via dei parametri principali
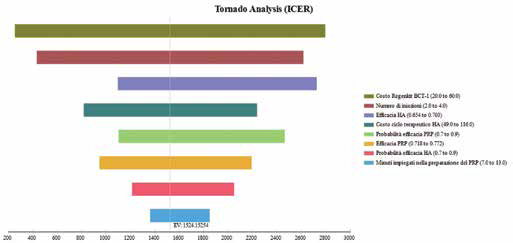
Analisi di sensibilità a una via, analisi Tornado, modello a 1 anno. ICER = incremental cost-effectiveness ratio; HA = acido ialuronico; PRP = plasma arricchito di piastrine.
Modello 1: risultati dell'analisi di sensibilità deterministica a una via
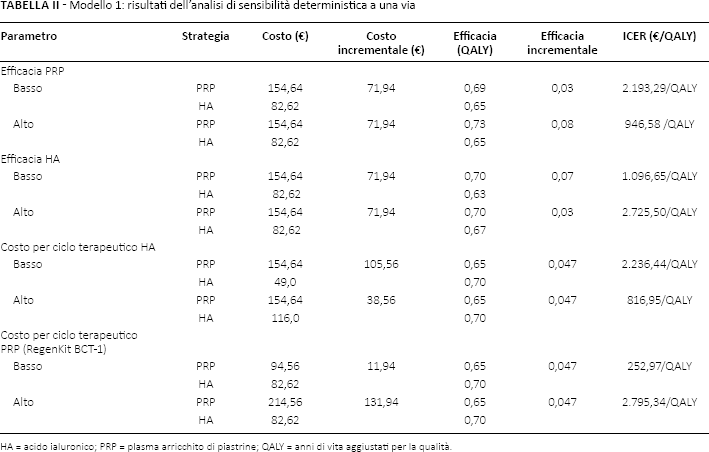
HA = acido ialuronico; PRP = plasma arricchito di piastrine; QALY = anni di vita aggiustati per la qualità.
È stata condotta un'analisi di sensibilità probabilistica mediante una simulazione Monte Carlo (considerando 1000 scenari) facendo variare tutti i parametri e le variabili del modello secondo la distribuzione loro assegnata (Fig. 4). Fissando una WTP di €10.000 per QALY, il PRP è la strategia costo-efficace nel 78,6% degli scenari mentre, considerando un WTP di € 30.000, il PRP supera l’81,1%. Nella Figura 5 è riportata la corrispondente curva di accettabilità.
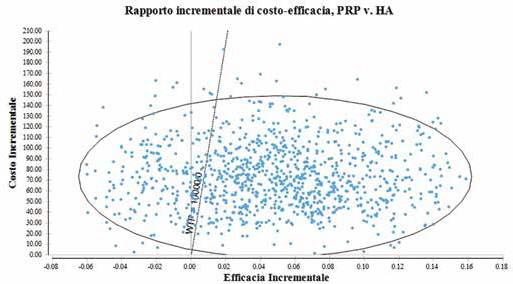
Piano delle distribuzioni congiunte di costo-efficacia. HA = acido ialuronico; PRP = plasma arricchito di piastrine; WTP = willingness to pay.
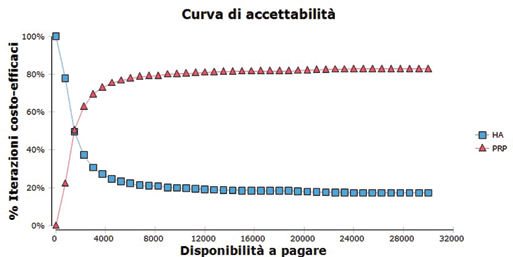
Modello con orizzonte temporale a 1 anno. Curva di accettabilità di costo-efficacia. HA = acido ialuronico; PRP = plasma arricchito di piastrine.
Modello con orizzonte temporale a 5 anni
Nel modello a 5 anni la presenza dell'intervento chirurgico influenza i risultati finali. Il costo medio per QALY è rispettivamente di €729 per l'HA ed €695 per il PRP. L'efficacia incrementale del PRP è di 0,21 QALY con un costo incrementale di €34. L'ICER è di €162/QALY. Anche nell'arco temporale di 5 anni il PRP si dimostra costo-efficace.
Nell'analisi di sensibilità deterministica particolare attenzione è stata posta alla variazione della probabilità di sottoporsi all'intervento chirurgico entro 5 anni, in seguito alla terapia con PRP; i risultati non sono molto sensibili rispetto a questo dato. Non considerando l'ipotetica diminuzione dovuta al trattamento con PRP, e assumendo per entrambe le terapie la stessa probabilità annuale di 1,98% di TKR, l'ICER è di €1.285/QALY, confermando il PRP come costo-efficace rispetto a un WTP di €30.000 o di €10.000. Il PRP, per diventare la terapia cost-saving rispetto all'HA, dovrebbe essere in grado di ridurre la probabilità dell'intervento chirurgico entro 5 anni al 5,3% e quindi l'incidenza annuale all’1,1%. Per quanto riguarda il costo per l'operazione chirurgica (DRG – 544), se dovesse superare gli €10.000 il PRP diventerebbe non solo costo-efficace, ma anche cost-saving. Considerando il limite inferiore (€7.184), l'ICER è di €377/QALY. Questi due dati sono interessanti per studi futuri che dovessero contemplare un arco temporale di più anni. Nella Figura 6 sono raccolte le analisi di sensibilità a una via per tutte le altre variabili. Si nota come, per determinati valori dei parametri, il PRP diventi la strategia dominante (ICER<0). Un parametro sensibile è la probabilità delle due terapie di essere efficaci. In particolare, se la probabilità di risposta al PRP fosse dell’85% (o superiore), oppure quella di risposta all'HA del 75% o minore, il PRP sarebbe la terapia dominante. La forte sensibilità di questo parametro, non mostrata dal modello a 1 anno, ci permette di dire che il modello fotografa bene come l'effettiva capacità di queste terapie di essere efficaci possa incidere fortemente sulla loro costo-efficacia nel medio termine e sul loro ruolo nel percorso di cura dell'OA al ginocchio.
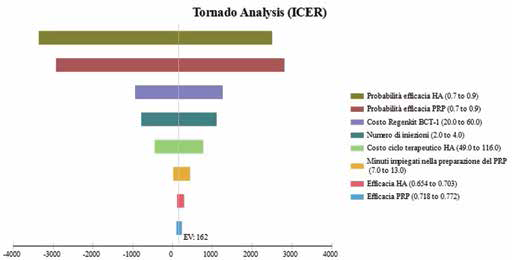
Analisi di sensibilità a una via, analisi Tornado, modello a 5 anni. ICER = incremental cost-effectiveness ratio; HA = acido ialuronico; PRP = plasma arricchito di piastrine.
L'analisi di sensibilità probabilistica (simulazione Monte Carlo con 1000 iterazioni) conferma sostanzialmente la costo-efficacia del PRP rispetto all'HA (Fig. 7). Utilizzando la disponibilità a pagare di €10.000, risultano essere costo-efficaci l’81,6% delle iterazioni (82% con WTP €30.000). Il 35% delle iterazioni totali risulta essere cost-saving. Nella Figura 8 si riporta la curva di accettabilità del modello con orizzonte temporale a 5 anni.
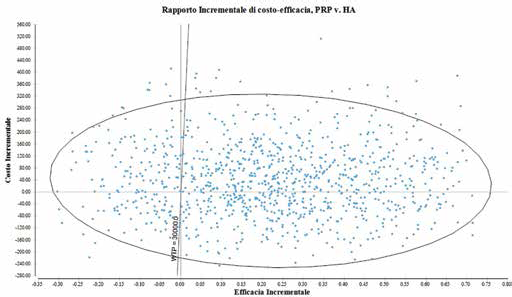
Piano delle distribuzioni congiunte di costo-efficacia, modello a 5 anni. HA = acido ialuronico; PRP = plasma arricchito di piastrine; WTP = willingness to pay.
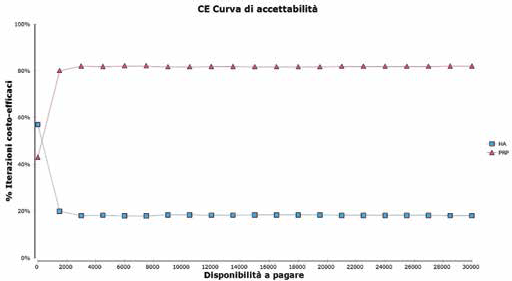
Modello con orizzonte temporale a 5 anni. Curva di accettabilità di costo-efficacia. HA = acido ialuronico; PRP = plasma arricchito di piastrine.
Discussione
PRP e HA sono terapie capaci di dare sollievo ai pazienti affetti da OA, e potenzialmente di ridurre, o per lo meno ritardare, il ricorso all'intervento chirurgico di artroprotesi al ginocchio (22–33). Diversi studi mostrano che il PRP ha un'efficacia superiore all'HA (34–42).
Dall'analisi svolta, il PRP risulta costo-efficace in entrambi i modelli decisionali. Le analisi di sensibilità effettuate indicano una sostanziale robustezza dei risultati. Nel modello a 1 anno la variabile più sensibile è il costo sostenuto per la terapia PRP, in particolare il costo del dispositivo e del processo più lungo necessario per ottenerlo. Il processo più complesso, fotografato nel nostro modello da un aggravio dei costi, sembra essere una delle ragioni per cui la terapia non si è ancora diffusa in modo esteso. La maggiore efficacia del PRP rispetto all'HA, mostrata da diversi studi clinici, può giustificare il maggiore costo per la sua preparazione.
Nelle nostre analisi non abbiamo considerato i costi indiretti dovuti alla perdita di produttività o di interazione sociale derivante dal dolore al ginocchio. Data la relativa maggiore efficacia del PRP, includendo i costi indiretti la terapia con il PRP sarebbe stata ulteriormente favorita.
Seppure ancora da approfondire, il modello a 5 anni ha inserito l'evento intervento chirurgico di artroprotesi nell'analisi. La presenza del TKR è una variabile molto importante dato il suo impatto economico sul SSN. Nel nostro modello si ipotizza che il maggiore costo del PRP nel lungo periodo sia in parte bilanciato dalla sua efficacia e dalla sua capacità di ridurre il tasso di interventi chirurgici. Come mostrato dai risultati, l'ICER nel modello a 5 anni è più basso. Considerando che nel presente studio non si è tenuto conto dei casi di fallimento del TKR e dei costi legati alla revisione della protesi, la direzione sembra essere quella di una terapia che nel lungo periodo potrebbe limitare la crescita dei costi legati al TKR. Futuri studi dovranno approfondire dal punto di vista clinico la capacità del PRP di ritardare l'intervento chirurgico più a lungo rispetto alle terapie standard, e dal punto di vista economico valutare l'impatto sui costi che questa terapia comporterebbe in caso fosse adottata dal SSN, in termini di maggiore costo iniziale a fronte della riduzione del numero di interventi di TKR/anno, principale driver di spesa per la patologia.
Questo studio presenta alcune limitazioni. In primo luogo, i dati oggi disponibili non permettono di avere una stima precisa della popolazione con OA al ginocchio in Italia (la prevalenza utilizzata risale a uno studio del 2004) e della sua incidenza. In particolare, esiste una forte variabilità nell'intervallo di variazione della prevalenza a seconda delle caratteristiche degli individui (età, sesso, zona geografica e tipo di lavoro) che potrebbe portare a risultati diversi. Un altro punto delicato è l'assenza in letteratura di dati sulla durata del beneficio negli anni delle due terapie, così come di evidenze sulla probabilità di ricorrere all'intervento di TKR nel caso si seguano i due percorsi di cura in modo esclusivo; questo riduce l'impatto esplicativo della valutazione economica del modello a 5 anni.
Conclusioni
In conclusione, qualora ulteriori evidenze sull'efficacia comparativa della terapia con PRP confermassero i dati già raccolti, sarebbe possibile affermare che, nel breve periodo, la terapia i.a. a base di PRP è costo-efficace nel trattamento dell'OA al ginocchio rispetto alla terapia i.a. con HA.
La valutazione dell'impatto sul lungo termine della terapia i.a. con PRP, rispetto all'efficacia nel tempo e all'impatto economico, sarebbe utile per comprendere se il PRP possa diventare una terapia da adottare in relazione alle strategie di allocazione efficiente di risorse sanitarie da parte del SSN (21, 54).
Footnotes
Financial support: S.L. receives a research grant from Ca’ Foscari University, Venice. P.L. and S.R. have nothing to declare.
Conflict of interest: The authors declare they have no conflicts of interest related to this article.
