Abstract
The market access of current/future innovative therapies is linked to the capability of payers and industry of negotiating price and reimbursement agreements that reflect drug value for patients and health care systems. Clinical research has provided therapeutic options quite effective, but complex from the perspective of market access management. An example are biological drug combinations, or therapies tailored to the patient, with different therapeutic indications. From this point of view, drugs approved for multiple indications are a great challenge for the definition of an appropriate price; each indication is related to a different value, which in its turn is related to the clinical benefit and to the availability of therapeutic alternatives. If new mechanisms for drug pricing are not implemented, the only possible trade-off is to keep out of the market the indications with lower value, or reduce the price of indications with higher value to the level of indications with lower value. In Italy, the AIFA Register was established in order to guarantee appropriate utilization of costly innovative drugs, i.e. pharmacoutilization patterns able to reduce resources misuse (inappropriate utilization) and to optimize the clinical benefit for patients. In addition to this primary goal, during the last few years innovative price agreements were introduced through the AIFA Register, based on different approaches, such as cost-sharing and payment-by-results. The rationale was to minimize the risk that the Italian National Health Service (NHS) pays for therapeutic failures. Among these examples, it is worth mentioning bevacizumab that, given its seven different indications, negotiated with AIFA a different agreement for each of them. Every agreement reflects bevacizumab value in a different setting; this allows to the drug complete access to the market, though the cost for NHS is differentiated. The challenge/opportunity for the future will be to reassess drugs values taking into account clinical practice data extracted from population registries, that is from populations much larger than those enrolled in pivotal clinical trials.
Introduzione
L'area oncologica
Negli ultimi anni lo scenario epidemiologico e clinico-terapeutico in ambito oncologico è radicalmente mutato (1). Elementi quali il progressivo invecchiamento della popolazione e il maggiore utilizzo degli screening hanno modificato l'andamento dell'incidenza di molte neoplasie. Inoltre i continui progressi scientifici e tecnologici - le chemioterapie, la chirurgia e la radioterapia - hanno offerto trattamenti a tal punto più efficaci da avere determinato una riduzione, a livello generale, della mortalità tumore-specifica (-50%) (1). L'aspettativa di vita dei pazienti è notevolmente aumentata, anche quando la malattia neoplastica si presenta in stadi non più guaribili (tumore metastatico). Ad esempio, i nuovi farmaci chemioterapici introdotti in alcuni ambiti terapeutici hanno consentito di portare a guarigione, o quanto meno di controllare nel lungo periodo, patologie neoplastiche in precedenza a solo esito negativo.
Anche i cambiamenti organizzativi [Percorsi Diagnostici Terapeutici Assistenziali (PDTA), reti regionali ecc.] hanno contribuito a migliorare lo scenario generale (1). In contrasto con questi aspetti che costituiscono un notevole passo in avanti, va purtroppo ricordato come sia aumentato allo stesso tempo il costo associato ai trattamenti innovativi (2), rendendo necessario l'efficientamento delle risorse a disposizione. Nell'ottica quindi di garantire rapidità di accesso e sostenibilità, le principali Agenzie Regolatone si sono orientate verso approcci negoziali finalizzati a rimborsare solo i farmaci in grado di garantire un reale e significativo beneficio clinico rispetto allo standard di trattamento (3, 4).
La terapia del tumore del colon-retto
Ad esempio, nel trattamento del tumore colorettale metastatico, negli ultimi venti anni si è registrato un miglioramento progressivo in termini di capacità di palliazione della malattia, con un incremento progressivo della sopravvivenza globale (overall survival, OS) mediana, passata dai 12-18 mesi, ottenibili con le esclusive fluoropirimidine, agli attuali 30 mesi e oltre ottenibili con le migliori sequenze chemioterapiche in associazione ai farmaci biologici anti-vascolari e anti-EGFR (5, 6). Risulta rilevante osservare come a inizio del secolo attuale la possibilità di sopravvivenza a 5 anni dalla diagnosi di malattia metastatica fosse praticamente nulla, mentre oggi raggiunge circa il 20% (un paziente ogni cinque). È peculiare osservare come questo incremento di sopravvivenza non sia correlato a un analogo incremento della sopravvivenza libera da progressione (progression free survival, PFS), che invece è rimasta sostanzialmente stabile e oscillante tra i 9 e 11 mesi, ma piuttosto all'importanza crescente assunta dalle linee successive alla prima, che oggi costituiscono il continuum terapeutico del paziente metastatico. Per quanto manchino dati completi e puntuali al riguardo, sembrerebbe che questi progressi siano stati ottenuti mantenendo una buona qualità di vita dei pazienti. Va altresì sottolineato come terapie sistemiche progressivamente più efficaci stiano facendo aumentare quella quota, seppure ancora limitata, di pazienti cui possa essere offerto un trattamento integrato medico e chirurgico resettivo della malattia metastatica giudicata non operabile in prima istanza, offrendo così tangibili possibilità di cura in pazienti selezionati (7). Chiaramente la disponibilità di nuove molecole ha comportato un incremento progressivo del costo del trattamento del paziente metastatico, soltanto in parte attenuato dalla perdita del brevetto e dalla conseguente “genericazione” di farmaci quali capecitabina, oxaliplatino e irinotecan. Le molecole biologiche attualmente in uso nella malattia metastatica - bevacizumab, aflibercet, ramucirumab (non ancora registrato in Italia), cetuximab, panitumumab, regorafenib e il chemioterapico TAS-102 (non ancora registrato in Italia) - comportano un esborso importante, pur se “adombrato” dall'incipiente scenario di utilizzo e sostenibilità dell'immunoterapia oncologica. La mancanza di fattori predittivi di efficacia per i farmaci antivascolari e l'ancora subottimale predittività per gli anti-EGFR costituisce oggi la sfida maggiore nell'intento di razionalizzare l'allocazione delle scarse risorse economiche con le quali siamo e saremo destinati a confrontarci.
Valutazione del farmaco e accesso al mercato
La regolazione dell'accesso in Italia
Con la finalità di regolare l'accesso al mercato dei farmaci oncologici, nel 2006 è stato attivato dall'Agenzia Regolatoria Italiana (AIFA) il Registro dei Farmaci Oncologici sottoposti a Monitoraggio (RFOM). La costituzione di questo registro e la contestuale attivazione di specifici accordi di rimborso condizionato nascono dall'esigenza dell'Autorità Regolatoria di garantire un bilanciamento tra innovazione e sostenibilità, soprattutto a fronte dei nuovi farmaci oncologici, degli elevati costi di trattamento a essi associati e della conseguente necessità di garantire un utilizzo appropriato degli stessi. Questa soluzione proposta da AIFA poggia su due elementi: da un lato il costo del nuovo farmaco oncologico deve essere rimborsato solo quando efficace e dall'altro la necessità di attivare delle procedure (scheda di arruolamento – scheda di follow-up – scheda di fine trattamento) per individuare i pazienti responder e attribuire alle aziende farmaceutiche i costi di trattamento in caso di fallimento terapeutico. Così facendo viene riconosciuto alle aziende farmaceutiche l'accesso al mercato dei nuovi farmaci oncologici, ma al contempo viene garantita all'Autorità Regolatoria la possibilità di rimborsare il farmaco solo quando esso è efficace, evitando così che il Servizio Sanitario Nazionale (SSN) si faccia carico del costo per i pazienti non-responder.
Due sono le principali tipologie di accordi bilaterali di rimborso condizionato: Cost Sharing (CS) e Payment-by-Results (PbR). Il primo prevede uno sconto per un certo numero di cicli di trattamento a carico dell'azienda farmaceutica per tutti i pazienti trattati, indipendentemente dal risultato clinico. Il secondo, che costituisce l'accordo ultimamente più utilizzato, rappresenta invece una procedura per cui viene posto a carico dell'azienda farmaceutica il costo totale di trattamento dei pazienti che non hanno tratto beneficio dal trattamento al follow-up (per progressione o tossicità inaccettabile). Quest'ultimo accordo è sicuramente quello che meglio rappresenta la condivisione del rischio tra Agenzia Regolatoria e azienda farmaceutica.
Farmaci con più indicazioni: l'esempio di bevacizumab
In tema di accordi di rimborso condizionato meritano particolare attenzione i farmaci oncologici con più di una indicazione terapeutica approvata. Bevacizumab rappresenta un interessante esempio di value-based pricing differenziato per indicazione. Per questo farmaco oncologico sono state infatti registrate differenti indicazioni in diverse tipologie di tumori, quali carcinoma del colon-retto, carcinoma della mammella, carcinoma renale, carcinoma del polmone e carcinoma ovari-co. Per ognuna di queste indicazioni, sulla base dei rispettivi studi clinici, è stato associato a bevacizumab un differente rapporto valore economico/benefico clinico. Di conseguenza non è stato definito lo stesso prezzo di rimborso per ogni indicazione, che è stato invece differenziato in base al beneficio clinico determinato per quella specifica indicazione. Così facendo, grazie anche alla presenza di un registro di monitoraggio, è stato possibile - partendo sempre dallo stesso prezzo ufficiale di bevacizumab – differenziare, grazie allo specifico accordo di rimborso condizionato, il costo realmente a carico del SSN per ogni specifica indicazione.
L'accordo di rimborso condizionato consente di determinare il prezzo di rimborso in funzione del valore del farmaco nelle pratica clinica (real world evidence, RWE), senza che si debba modificare il prezzo inizialmente riconosciuto. Nella Figura 1, per ogni indicazione rimborsata, viene riportata la differenza tra il prezzo di listino di bevacizumab, posto uguale a 100, e il corrispettivo prezzo di cessione a carico del SSN. I prezzi di cessione di bevacizumab sono stati stimati calcolando l'impatto dell'accordo di rimborso, per le diverse indicazioni, sulla base dei risultati dei rispettivi studi clinici registrativi. L'appropriatezza di utilizzo di bevacizumab per specifica indicazione viene infine assicurata dal RFOM attraverso la scheda di eleggibilità.
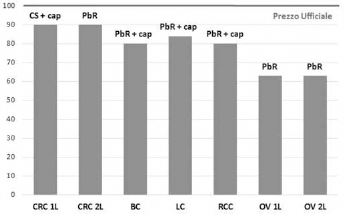
Bevacizumab: prezzo di cessione al SSN in funzione degli accordi differenziati per indicazione (Numero Indice: prezzo ufficiale = 100). CRC = carcinoma del colon-retto; BC = carcinoma mammario; LC = carcinoma polmonare; RCC = carcinoma renale; OV = carcinoma ovarico; CS = cost-sharing; PbR = payment-by-results; 1L = prima linea di trattamento; 2L= seconda linea di trattamento; cap = capping annuo di 11.000 mg.
Complessivamente gli accordi sono sette:
carcinoma del colon-retto (trattamento di prima linea) = cost sharing del 50% per le prime 6 settimane di trattamento con capping annuo di 11.000 mg (con il termine “capping” si indica, come specificato nell'accordo negoziale, la quantità massima di farmaco somministrabile al paziente in un anno che può essere rimborsata dal SSN; se si supera tale soglia, l'eccedenza di farmaco non viene rimborsata);
carcinoma del colon-retto (trattamento di seconda linea, inclusi i pazienti pretrattati con bevacizumab) = payment-by-results con verifica al follow-up a 3 mesi;
carcinoma mammario = payment-by-results con verifica a 3 mesi con un capping annuo di 11.000 mg;
carcinoma polmonare non a piccole cellule = payment-by-results con verifica a 3 mesi con un capping annuo di 11.000 mg;
carcinoma renale = payment-by-results con verifica a 3 mesi con un capping annuo di 11.000 mg;
carcinoma ovarico (trattamento di prima linea) = payment-by-results con verifica a 8 mesi;
carcinoma ovarico (trattamento di seconda linea nelle pazienti platino-sensibili) = payment-by-results con verifica a 6 mesi.
Tra le indicazioni rimborsate, il caso forse più interessante è rappresentato dall'indicazione per il trattamento del carcinoma del colon-retto. Nel trattamento di prima linea, ovvero la prima (in ordine temporale) indicazione di bevacizumab rimborsata dall'Agenzia Regolatoria, è stato posto in essere un accordo a valenza finanziaria (cost-sharing). Successivamente, con l'estensione dell'indicazione di bevacizumab al trattamento di seconda linea, si è passati a un accordo a valenza clinico-economica (payment-by-results). L'utilizzo in sequenza temporale di queste due differenti tipologie di accordo è indicativo di come si sia modificato nel tempo il razionale che sta alla loro base. Il cost-sharing rappresenta infatti, in ordine cronologico, la prima tipologia di accordo di rimborso condizionato negoziato, di tipo essenzialmente finanziario, tra aziende farmaceutiche e Agenzia Regolatoria. In seguito, riconosciuta la maggiore centralità del risultato clinico, quale driver della rimborsabilità, si è passati al payment-by-results. Questo tipo di accordo, a differenza del cost-sharing, pone le proprie fondamenta sull'obiettivo di limitare l'incertezza dei risultati, tra efficacy (studio clinico) ed effectiveness (pratica clinica) del nuovo prodotto, consentendogli un più rapido accesso al mercato.
Conclusioni
L'accesso al mercato delle terapie innovative dipende dalla capacità del Pagatore pubblico e delle aziende farmaceutiche di negoziare accordi di rimborso che riflettano in modo appropriato il rapporto tra il beneficio clinico apportato al paziente dai nuovi farmaci e il costo per il sistema sanitario.
La ricerca clinica sta portando sul mercato opzioni cliniche estremamente efficaci, ma allo stesso tempo complesse dal punto di vista della gestione dell'accesso; si pensi al caso delle combinazioni di biologici o, in particolare, delle terapie personalizzate utilizzate per differenti indicazioni terapeutiche. In uno scenario di questo tipo, farmaci come bevacizumab rappresentano una sfida in termini di appropriata definizione del prezzo, in quanto a ogni indicazione vengono associati differenti benefici clinici. Per questi farmaci, la presenza di un criterio di rimborsabilità che non permetta di differenziare il prezzo di cessione per indicazione potrebbe determinare l'esclusione dall'accesso al mercato (rimborso) delle indicazioni a minore beneficio clinico oppure l'applicazione alle indicazioni a maggiore beneficio clinico dello stesso prezzo di cessione definito per l'indicazione a benefico clinico minore.
Va sottolineato che l'attuale procedura differenziata non sarebbe però applicabile senza i Registri, in quanto strumenti indispensabili per gestire l'efficientamento delle terapie e della relativa spesa farmaceutica. In un prossimo futuro i Registri potrebbero costituire la base-dati per condurre analisi di RWE in riferimento a popolazioni più ampie di quelle arruolate negli studi registrativi.
Rimane infine sempre valida la considerazione generale che la sostenibilità per il SSN dovrebbe essere analizzata nel suo complesso, ovvero considerando tutte le attività che vengono da esso erogate e non esclusivamente quelle legate alla terapia farmacologica.
Footnotes
Financial support: This research was made possible by the financial support of Roche S.p.A.
Conflict of interest: The Authors declare that they have no conflicts of interest.
