Abstract
Avocado Persea americana Mill., is a crop of great economic importance in Mexico and it is affected by pests that cause significant damage. Traditionally, pest control in avocado crops has been based on the use of organosynthetic pesticides; however, their excessive and indiscriminate use has negative effects on the environment, health, and quality of the fruit. In the search for more sustainable alternatives for the control of agricultural pests, the use of entomopathogenic nematodes (EPNs) as biological control agents is one of the most promising options. To explore possible EPNs associated with avocado crops, soil samples were collected from six avocado orchards in the municipality of Atapan, Michoacán, Mexico, and possible entomopathogenic agents were isolated using the bait insect technique with Galleria mellonella larvae. The molecular characterization through partial sequencing of the SSU (Small Subunit) and ITS (Internal Transcribed Spacer) regions of strain ANP003 confirmed that one of the isolates corresponds to the species Pristionchus pacificus, this represents the first report in Mexico of a nematode associated with avocado crop. The genetic distance analysis of SSU-18S allowed us to know the close relationship of this isolate with the entomopathogenic nematode Pristionchus entomophilus.
Introducción
Con una superficie de casi 200.000 ha cosechadas y una producción de millones de toneladas anuales, el aguacate Persea americana Mill. (Laurales: Lauraceae) es uno de los principales cultivos perennes de México (SAGARPA, 2017). En el país, el estado de Michoacán es el principal productor, concentrando el 80% de la producción nacional con una superficie de 134.941 ha y un rendimiento de más de un millón 725 mil toneladas, equivalente a casi 40 mil millones de pesos anuales (SAGARPA, 2017). Sin embargo, el aguacate es uno de los cultivos más demandantes en el manejo fitosanitario, en particular debido a las plagas. Éste se ve afectado por una gran diversidad de artrópodos fitófagos, destacando los trips, ácaros y barrenadores, de estos últimos sobresalen los picudos, e.g., el barrenador pequeño del hueso Conotrachelus aguacatae Barber y C. perseae Barber, el barrenador grande del hueso Heilipus lauri Boheman, el barrenador de ramas Copturus aguacatae Kissinger (Coleoptera: Curculionidae) y la palomilla barrenadora del hueso del aguacate Stenoma catenifer Walsingham (Lepidoptera: Depressariidae) (Rivera-Martínez et al., 2022; Velázquez-Martínez et al., 2022). La limitada oferta de plaguicidas permitidos en la producción de aguacate de exportación, así como la habilidad de los barrenadores de invadir ambientes crípticos reduce en gran medida el éxito en su manejo (González et al., 2000). Una alternativa sostenible para el manejo de plagas es el control biológico, no solo por su eficiencia, sino también por su inocuidad con el ambiente y la salud pública. Entre los agentes de control biológico con mayor potencial para el manejo de barrenadores se incluyen a los basados en nematodos entomopatógenos (NEPs) de las familias Steinernematidae y Heterorhabditidae (Georgis et al., 2006; Kaya & Gaugler, 1993), aunque recientemente se han reportado especies de otros géneros con potencial entomopatogénico como Oscheius y Pristionchus (Tarasco et al., 2023).
Estudios con insectos barrenadores como el picudo negro (Scyphophorus interstitialis Gyllenhal), picudo del nopal (Metamasius (= Cactophagus) spinolae Gyllenhal) y picudo de la raíz (Diaprepes abbreviatus L.) demuestran el potencial de los NEPs en el control de insectos de hábitats crípticos (Aquino-Bolaños et al., 2006; Cortez-Madrigal et al., 2009; Shapiro & McCoy, 2000). Por otra parte, en un estudio realizado por Andaló et al. (2019) con cepas nativas de NEP's en Brasil se aisló Heterorhabditis amazonensis Andaló, Nguyen & Moino (Rhabditida: Heterorhabditidae) y se evaluó para el manejo del barrenador del aguacate S. catenifer, considerada la principal plaga de este cultivo. Los resultados obtenidos revelaron que se registró una reducción en el porcentaje de frutos dañados hasta 90 días posteriores a la aplicación de este NEP. En Sudáfrica en cultivo de aguacate, se evaluó la eficacia de cuatro especies de nematodos para el control de la falsa polilla de la manzana Thaumatotibia leucotreta (Meyrick) (Lepidoptera: Tortricidae) obteniendo mortalidades superiores al 60% (Steyn et al., 2019). Sin embargo, solo dos trabajos han sido documentados en México con el uso de NEPs sobre plagas de aguacate, específicamente C. aguacatae (Huerta de la Peña et al., 1990; Sánchez-Saavedra et al., 2012), ninguno de ellos con cepas nativas. Con respecto a su presencia en suelos cultivados con aguacate se reporta a Steinernema carpocapsae Weiser (Rhabditida: Steinernematidae) en Colombia (Neira-Monsalve et al., 2020), H. amazonensis en Brasil (Andaló et al., 2019), nematodos de vida libre como Mononchida sp., Rhabditides sp. y especies de Dorylaimida (Abanto et al., 2020).
Si se considera que el aguacate es uno de los cultivos de mayor importancia económica para México, pero además que el uso indiscriminado de plaguicidas químicos tiene efectos negativos, es necesario explorar alternativas más amigables con el ambiente y disponibles en el país, por lo que el uso de NEPs nativos como agentes de control biológico para las plagas del aguacate y otros cultivos, conllevará a un manejo sostenible de estos problemas sanitarios, al tiempo que se disminuirá la dependencia a la importación de organismos de control biológico exóticos o foráneos (Hokkanen & Sailer, 1985). El objetivo del presente estudio fue caracterizar una especie de nematodo nativo, potencialmente entomopatógeno, presente en suelos de aguacate mediante secuenciación parcial de la región SSU y la región espaciadora interna (ITS). Así como conocer su proximidad genética con otras especies del mismo género.
Materiales y métodos
Colecta de muestras de suelo
El estudio se realizó en el municipio de Atapan Michoacán, México, (19°40′28″N, 102°24′43″O), donde se seleccionaron seis huertas de aguacate con áreas entre una y tres hectáreas, localizadas a más de 1500 m s.n.m., mayoritariamente con manejo orgánico o con poco o nulo control fitosanitario. Las huertas fueron estratificadas y se establecieron cinco sitios de muestreo aleatorios en cada parcela (Constant et al., 1998).
Seis muestras de suelo fueron colectadas durante los meses de febrero a septiembre de 2023. En cada huerta y de forma aleatoria, se colectaron cinco submuestras de suelo de aproximadamente 1 kg, entre los primeros 10 y 20 cm de profundidad. Las submuestras fueron empacadas en bolsas de plástico de polietileno y mantenidas a 15 °C - 17 °C (Stock, 1995) hasta su llegada al laboratorio de Control Biológico de la Universidad de La Ciénega del Estado de Michoacán de Ocampo (UCEMICH). Las submuestras fueron mezcladas para obtener una muestra compuesta de 500 g (Constant et al., 1998).
Recuperación de nematodos
Los nematodos se recuperaron de las muestras de suelo por la técnica del insecto trampa usando larvas de Galleria mellonella (L.) (Lepidoptera: Pyralidae) (Bedding & Akhurst, 1975). Cuatro larvas de G. mellonella fueron colocadas en contenedores de plástico de 250 mL con 200 g del suelo humedecido (n = 3). Los recipientes fueron tapados, invertidos diariamente y mantenidos en condiciones de laboratorio (25 ± 3 °C, humedad relativa de 65% ± 10% y un fotoperiodo de 16: 8 h luz oscuridad) por un periodo de hasta 20 días. Durante este tiempo todos los insectos muertos con síntomas de parasitismo por nematodos (bacteriemia) fueron colocados individualmente en trampas de White hasta la emergencia de juveniles (White, 1927).
Identificación molecular
El ADN genómico de los nematodos se extrajo a partir de 1 mL de nematodos recién emergidos de la trampa White. Los especímenes fueron recolectados por centrifugación a 14 000 rpm/5 minutos, después se eliminaron 0,9 mL del sobrenadante con micropipeta, se agregaron 0,2 mL de buffer TSNT (2 % Tritón X-100, 1% SDS, 100 mM NaCl, 10 mM Trs-HCl y 1 mM EDTA, pH 8) y se mezcló en vórtex (Genie2®) por 3 minutos (Jaramillo-Pineda, 2014). La extracción continuó conforme al protocolo suplementario de purificación de ADN de lisados crudos usando el kit DNeasy® Blood & Tissue (Qiagen®, cat. 69504).
Las reacciones en cadena de la polimerasa (PCR por sus siglas en inglés), se usaron para amplificar la región parcial SSU-18S del ADN ribosomal, usando los iniciadores SSUF07 (forward): 5′-AAAGATTAAGCCATGCATG-3′ y SSUR26 (reverse): 5′-CATTCTTGGCAAATGCTTTCG-3′ (Islas-López et al., 2021) y para la región ITS1-5.8S-ITS2 usando los iniciadores 18S (forward): 5′- TTGATTACGTCCCTGCCCTTT-3′ y 28S (reverse): 5′-TTTCACTCGCCGTTACTAAGG-3′ (Cimen et al., 2016). Las PCR se realizaron en un volumen de 50 μl que contenía 25 μl de MasterMix 2X (Promega®, cat. M7502), 5 μl de cada iniciador a 10 μM, 5 μl de ADN y 5 μl de agua libre de nucleasas (Promega®, cat. P119A). Las condiciones de PCR incluyeron un ciclo inicial a 95 °C por 2 min seguido de 40 ciclos de 95 °C por 30 seg, 50 °C por 45 seg y 72 °C por 1 min, finalizando con un ciclo a 72 °C por 5 min, usando un termociclador Biorad 1000®. Los productos de amplificación se analizaron por electroforesis en gel de agarosa (Sigma, A9539) al 1 % teñido con SYBR Green I (Sigma-Aldrich®, cat. S9430) y se visualizaron en un fotodocumentador Gel Doc XR+ (Biorad®). Los productos se purificaron con el kit UltraClean® PCR Clean-Up (MO BIO) y fueron enviados para su secuenciación en ambos sentidos por tecnología capilar por el método del dideoxi-terminal de Sanger en LABSERGEN-LANGEBIO, México.
Las secuencias obtenidas fueron editadas eliminando las secuencias de baja calidad de los extremos y ensambladas para obtener la secuencia consenso usando el software BioEdit® v7.0.5.3. Se buscó la homología de las secuencias usando BLASTn considerando una cobertura del 100 % y similitud mayor a 99 % (https://blast.ncbi.nlm.nih.gov/Blast.cgi) y se depositaron en la base de datos GenBank (https://www.ncbi.nlm.nih.gov/WebSub). Las secuencias obtenidas en este trabajo y otras secuencias relacionadas obtenidas del GenBank se alinearon con el software Muscle, los árboles de distancias genéticas óptimos fueron obtenidos por el método Neighbor-Joining (Saitou & Nei, 1987) empleando los parámetros predeterminados del software Mega 7 (v.7.0.26). Se construyeron dos árboles, uno para SSU-18S y otro para ITS1-5.8S ITS2.
Resultados y discusión
Aislamiento de nematodos
Las seis muestras de suelo correspondientes a parcelas cultivadas con aguacate mostraron presencia de larvas con síntomas de parasitismo por nematodos, sin embargo, en solo una de las muestras, perteneciente a una huerta con nulo manejo agronómico, se logró confirmar la emergencia de juveniles y por ende la posible naturaleza entomopatogénica de los nematodos.
Identificación molecular
El amplicón correspondiente a la región parcial SSU-18S fue de aproximadamente de 750 pares de bases (pb), mientras que para la región ITS1-5.8S-ITS2 fue de aproximadamente 1,000 pb (Figura 1). La secuencia consenso obtenida de la región SSU-18S fue de 778 pb, mostró una similitud de 99,87 % con la secuencia de referencia de Pristionchus pacificus (Irán, KY380005.1) con una cobertura del 100 % y valor E de 0.0 después de la búsqueda en BLASTn, mientras que la secuencia consenso de la región ITS1-5.8S-ITS2 fue de 883 pb y mostró una similitud de 100 % con la secuencia de referencia de P. pacificus (Portugal, MG551685.1) con una cobertura del 100 % y valor E de 0,0. Las secuencias consenso de la especie aquí reportada se encuentran disponibles en GenBank con los números de acceso OR591151 y OR594416, respectivamente y se suman a las más de 600 cepas de este género documentadas por todo el mundo (Rae et al., 2008; Sommer & Mcgaughran, 2013).
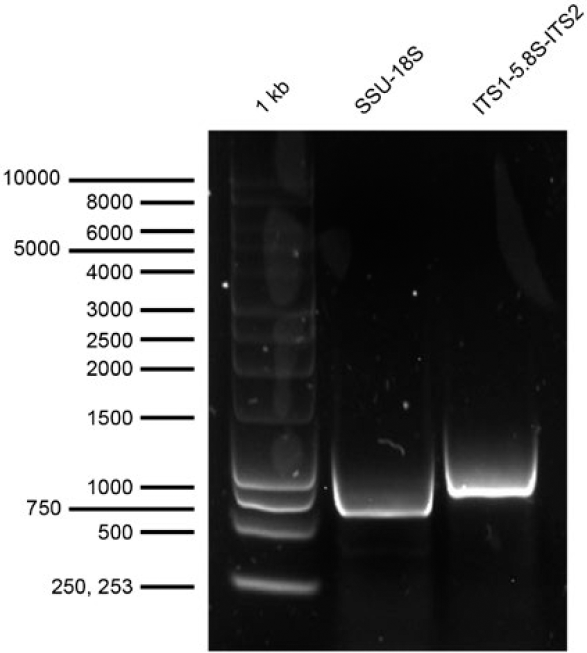
Producto de amplificación parcial del ADNr SSU-18S. Carril 1kb, marcador de peso molecular de 1 kb Promega (cat. G511). Carril SSU-18S, producto amplificado de aproximadamente 750 pb. Carril ITS1-5.8S-ITS2, producto amplificado de aproximadamente 1.000 pb.
El árbol de SUU-18S incluyó un total de 23 secuencias que indican la posición del aislado P. pacificus ANP003 (OR591151) en el mismo nivel con otros especímenes reportados de P. pacificus (KY380005.1 y KX113519.1), además, de la ubicación cercana de Pristionchus entomophilus (KP762794) (Figura 2).
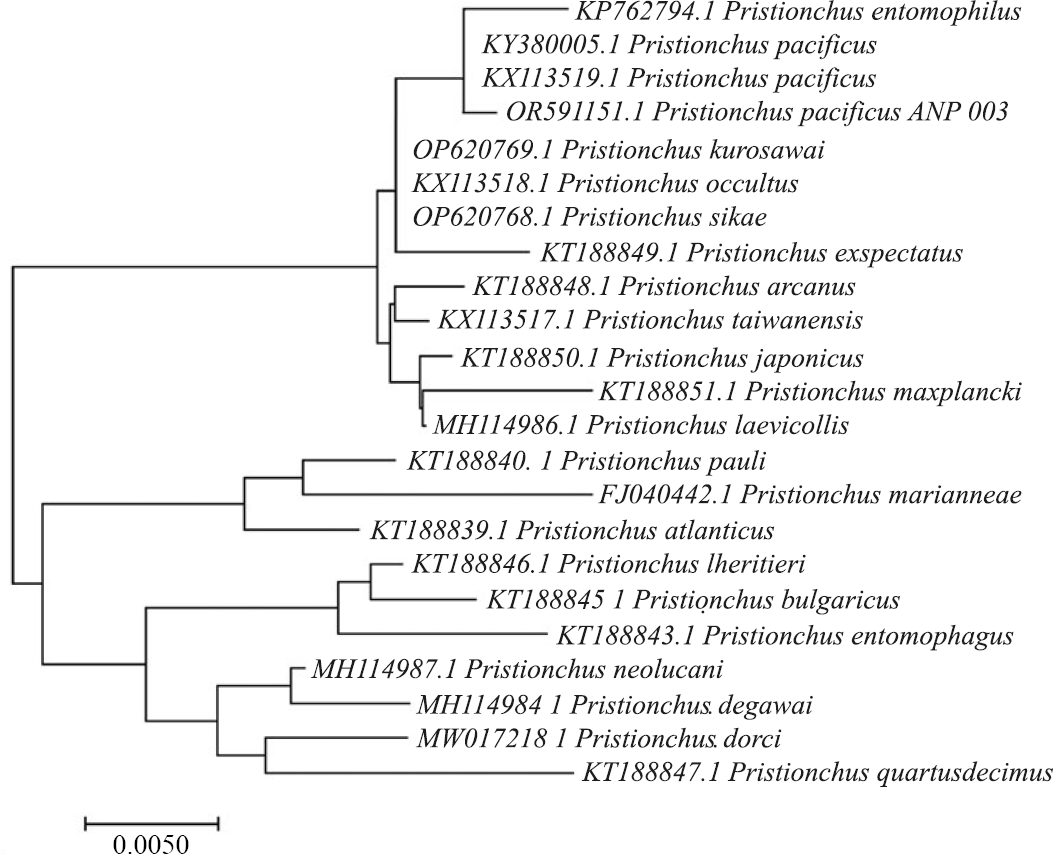
Árbol de las secuencias SSU-18S inferido por el método Neighbor-Joining. Las secuencias KX113519.1 y KY380005.1 de P. pacificus reportadas en la literatura fueron usadas para mostrar la cercanía de P. pacificus ANP003 (OR591151).
El árbol de ITS1-5.8S-ITS2 incluyo un total de 10 secuencias que indican la cercanía filogenética de la secuencia obtenida del aislado P. pacificus ANP003 (OR594416) con otras secuencias reportadas de P. pacificus (MG551685.1 y JQ699288.1) (Figura 3).
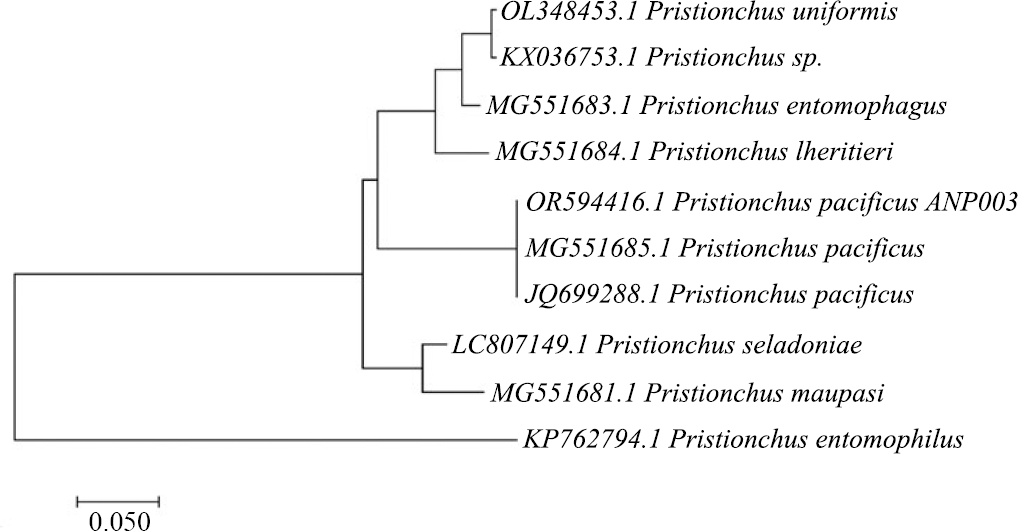
Árbol de las secuencias de la región ITS1-5.8S-ITS2 mediante el método Neighbor-Joining. Las secuencias MG551685.1 y JQ699288.1 de P. pacificus reportadas en la literatura fueron usadas para mostrar la cercanía del aislado P. pacificus ANP003 (OR594416).
Previamente ha sido reportada la dificultad de la identificación morfológica de especies pertenecientes a este género (Herrmann et al., 2006a) por lo que para su identificación precisa se vuelve indispensable la secuenciación de ADN. En este estudio, las regiones del ADN ribosomal SSU-18S e ITS han sido utilizadas para la caracterización molecular de diferentes especies de nematodos (Hominick et al., 1997). Tal es el caso de lo nematodos fitopatógenos Orrina phyllobia Thorne (Tylenchida: Anguinidae) (Medina-Gómez et al., 2016) y Longidorus kheirii Pedram, Niknam, Robbins, Ye y Karegar (Dorylaimida: Longidoridae) (Pedram et al., 2008). También se han identificado molecularmente NEP's del género Steinernema (Lis et al., 2021; Nguyen et al., 2001), del género Pristionchus se reporta a P. aerivorus (Ye et al., 2015) y P. americanus (Islas-López et al., 2021). Mediante el análisis filogenético con base de secuencias de la región SSU-18S, se ha constatado que P. pacificus presenta una estrecha relación con P. entomophilus Li, Dai, Bao, Chen, Gao, Wang, Wang, Wang, Yedid & Zhang (Rhabditida: Neodiplogasteridae) un nematodo que puede infectar larvas vivas de lepidópteros, reproducirse con éxito y asociarse con la bacteria entomopatógena Serratia nematodiphila Zhang (Enterobacterales: Yersiniaceae) (Li et al., 2015).
Si bien la familia Neodiplogasteridae a la cual pertenece el género Pristionchus, es considerada como nematodos saprófitos (Dieterich et al., 2009), otras especies de este género han sido reportadas como entomopatógenos al menos débiles, desde principios del siglo XX (Ye et al., 2015), así como se ha descrito que comparten características genéticas, moleculares y morfológicas encontradas en otros nematodos parásitos de insectos (Brown et al., 2011; D′Anna & Sommer, 2011; Ogawa et al., 2009; Sommer & Mcgaughran, 2013; Srinivasan & Stenberg, 2008; Wilecki et al., 2015).
Aunque en este estudio no se confirmó la patogenicidad de P. pacificus sobre insectos, diferentes investigaciones reportan a este nematodo como necrofílico (Rae et al., 2008; Singh et al., 2022). Sin embargo, existen reportes de la patogenicidad de otras especies del mismo género sobre G. mellonella, como Pristionchus aerivorus Cobb en Merrill y Ford (Rhabditida: Neodiplogasteridae) en Carolina del Norte, EE. UU. (Ye et al., 2015) y Pristionchus americanus Herrmann, Mayer y Sommer (Rhabditida: Neodiplogasteridae) en Querétaro, México (Islas-López et al., 2021). Se ha reportado la posible evolución parasítica de P. pacificus por su conocida asociación a escarabajos (Herrmann et al., 2006b, 2007; Srinivasan & Stenberg, 2008). Sin embargo, Pristionchus pacificus Sommer, Carta, Kim y Sternberg (Rhabditida: Neodiplogastridae) no interfiere con el parasitismo, pero si con la reproducción de otras especies ya que una vez muerto el hospedero éste tiene una mayor tasa de reproducción sobre los entomopatógenos por su capacidad competitiva y nematófaga (Lightfoot et al., 2021; Quach & Chalasin, 2020, 2022; Schroeder, 2021; Wilecki et al., 2015) que le han permitido colonizar diversos hábitats, siendo P. pacificus uno de los más cosmopolitas (Meyer et al., 2017). La capacidad de asociarse con una gran diversidad de bacterias de diferentes hábitats (Rae et al., 2008), así como su adaptación morfológica para no digerir a la bacteria, permitiéndole infectar a insectos a la vez que actúa como vector de bacterias ambientales (Ishaq et al., 2021; Poinar, 1969; von Lieveng et al., 2000). Lo anterior podría ser una ventaja competitiva sobre otros nematodos entomopatógenos, ya que una vez liberados en campo los nematodos del género Pristionchus al aprovechar la diversidad de bacterias entomopatógenas ya adaptadas a las condiciones edafoclimáticas presentes en el cultivo, para ejercer su capacidad de virulencia facultativa sobre las plagas, siendo una alternativa más en el manejo sustentable de plagas agrícolas. Por otra parte, su comportamiento necroménico repercute en la descomposición de cadáveres y su incorporación en la materia orgánica del suelo (Meyer et al., 2017), favoreciendo las propiedades agroecológicas, especialmente para los insectos presentes en el cultivo de aguacate que en su mayoría pertenecen al grupo de los escarabajos barrenadores (Rivera-Martínez et al., 2022; Velázquez-Martínez et al., 2022). En este caso se sugiere realizar un estudio más profundo sobre los análisis filogenéticos de esta especie, el aislamiento de la bacteria asociada para confirmar su patogenicidad, o su posible vínculo con bacterias entomopatógenas (Campos-Herrera et al., 2019; Ishaq et al., 2021; Li et al., 2015; Loulou et al., 2023; Rae et al., 2008) así como determinar su posible evolución parasítica (Brown et al., 2011) en particular sobre plagas del aguacate.
Conclusiones
El nematodo aislado fue identificado como P. pacificus ANP003 y las secuencias consenso se encuentran disponibles en GenBank con los números de acceso OR591151 y OR594416, respectivamente. Este aislado representa el primer reporte de nematodos asociados al cultivo de aguacate en Michoacán, México. Con base en los resultados obtenidos, no se descarta la capacidad patogénica de este aislado, por lo que se sugiere evaluar su rol como entomopatógeno, tanto en condiciones de laboratorio como de campo en diferentes especies de insectos plaga, principalmente en aquellas que limitan la producción nacional como de exportación de aguacate.
Origen y financiamiento
El presente trabajo derivó de la línea de investigación con organismos entomopatógenos que se desarrolla en el grupo de investigación Amigos Naturales de las Plantas (ANP) y fue financiado por los Proyectos UCEMICH 2022,2023 y CONAHCYT-ICTI-PICIR-030- 2022 y PICIR22-030-C-2024 a IZJ.
Contribución de los autores
El primer autor desarrolló la metodología y procedimientos para la identificación molecular y contribuyó en el análisis de los datos y en la escritura del artículo.
La segunda autora desarrolló la fase de experimentación correspondiente a la extracción de los NEPs y contribuyó en el análisis de los datos y en la escritura del artículo.
El tercer autor contribuyó en el análisis de los datos y en la escritura del artículo.
El último autor planteó los objetivos de la investigación, consiguió la financiación, realizó el análisis de los datos y la escritura del artículo en conjunto con el primer autor.
Conflicto de intereses
Los autores declaramos no tener conflicto de intereses.
